专题3 石油化工的基础物质--烃专题检测(A卷)(Word解析版)
文档属性
| 名称 | 专题3 石油化工的基础物质--烃专题检测(A卷)(Word解析版) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-29 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
中小学教育资源及组卷应用平台
专题3 石油化工的基础物质--烃专题检测(A卷)
(时间:75分钟 满分:100分)
一、单选题
1.(2022秋·浙江丽水·高二校考阶段练习)下列对有机化合物的分类结果正确的是
A.乙烯、苯、环己烷属于不饱和烃
B.苯、环戊烷、环己烷同属于芳香烃
C.乙烯、乙炔同属于烯烃
D.、、同属于环烷烃
【答案】D
【解析】A.环己烷属于饱和烃,A不正确;
B.环戊烷、环己烷均不属于芳香烃,B不正确;
C.乙炔属于炔烃,C不正确;
D.选项中提供的物质均属于环烷烃,D正确;
所以选D。
2.(2022春·云南昆明·高二校考期末)在实验室中,下列除去杂质的方法正确的是
A.溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取
B.硝基苯中混有浓硝酸和浓硫酸,加入NaOH溶液,静置,分液
C.用酸性KMnO4溶液除去乙炔中混有的H2S
D.乙烯中混有SO2和CO2,将其先后通入NaOH溶液和KMnO4酸性溶液中洗气
【答案】B
【解析】A.溴苯中混有溴,加入溶液,振荡,再用汽油萃取,此时有机层中会有生成的碘单质,所以除去了溴但引入了碘,A错误;
B.硝基苯中混有浓硝酸和浓硫酸,加入溶液可以反应掉两种酸,静置,分液,B正确;
C.用酸性溶液除去乙炔中混有的时也会和乙炔反应,C错误;
D.乙烯中混有和,将其先通入溶液除去二氧化碳和二氧化硫,再通入酸性溶液时乙烯被除去,D错误;
故选B。
3.(2022春·上海浦东新·高二华师大二附中校考阶段练习)下列表示正确的是
A.氨气的电子式: B.乙炔分子的球棍模型:
C.2—丁烯的键线式: D.结构示意图为:
【答案】B
【解析】A.氨气为共价化合物,电子式为,故A错误;
B.乙炔的结构简式为HC≡CH,球棍模型为,故B正确;
C.2—丁烯的结构简式为CH3CH=CHCH3,键线式为,故C错误;
D.硫离子的核电荷数为16,核外3个电子层,最外层电子数为8,离子的结构示意图为,故D错误;
故选B。
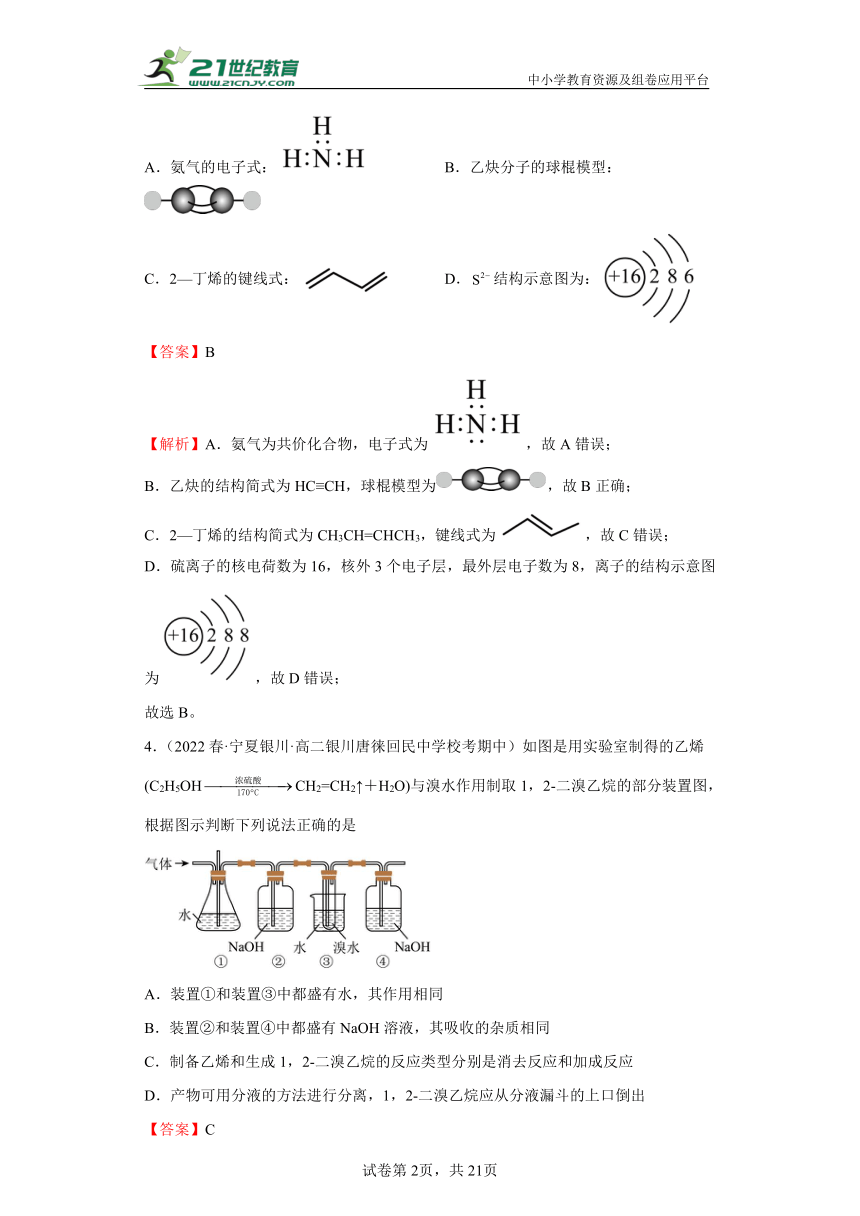
4.(2022春·宁夏银川·高二银川唐徕回民中学校考期中)如图是用实验室制得的乙烯(C2H5OHCH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是
A.装置①和装置③中都盛有水,其作用相同
B.装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C.制备乙烯和生成1,2-二溴乙烷的反应类型分别是消去反应和加成反应
D.产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出
【答案】C
【分析】反应C2H5OHCH2=CH2↑+H2O制得的乙烯中可能混有SO2、CO2,乙烯气体通入装置①中,装置②中的NaOH溶液可以吸收乙烯中混有的SO2、CO2,乙烯和溴水在装置③中反应,装置④是吸收逸出的溴蒸气,防止污染空气。
【解析】A.装置①中气体压力过大时,水就会从玻璃管上端溢出,起到缓冲作用;溴易挥发,装置③水的作用是冷却液溴,可避免溴的大量挥发,故A错误;
B.装置②吸收乙烯中混有的SO2、CO2;装置④是吸收逸出的溴蒸气,防止污染空气,吸收的杂质不相同,故B错误;
C.制备乙烯是乙醇发生消去反应;生成1,2-二溴乙烷是乙烯能与溴水发生加成反应,故C正确;
D.1,2-二溴乙烷与水不溶,密度比水大,在水的下层,应从分液漏斗的下口倒出,故D错误;
故选C。
5.(2022·内蒙古·高二统考学业考试)下图是四种烃分子的球棍模型,下列说法中正确的是
A.甲能使酸性高锰酸钾溶液褪色
B.乙的产量可以用来衡量一个国家的石油化工发展水平
C.丙不存在同分异构体
D.丁分子中含有碳碳单键和碳碳双键
【答案】B
【解析】A.甲是甲烷,甲烷不能与酸性高锰酸钾溶液反应,不能使酸性高锰酸钾溶液褪色,A错误;
B.乙是乙烯,乙烯的产量可以用来衡量一个国家的石油化工发展水平,B正确;
C.丙的分子式为C4H10,结构有CH3CH2CH2CH3和 ,C错误;
D.丁是苯,苯中不存在碳碳单键和碳碳双键,是一种介于单键和双键之间的独特的共价键,D错误;
故选B。
6.(2022春·上海宝山·高二上海交大附中校考期中)在烷烃分子中,、、、中的碳原子分别称为伯、种叔、季碳原子,数目分别用、、、表示。,的烷烃共有
A.2种 B.3种 C.4种 D.5种
【答案】B
【解析】由题干信息可知,符合条件的烷烃共有:(CH3)3CCH(CH3)CH2CH3、(CH3)3CCH2CH(CH3)2、(CH3)2CHC(CH3)2CH2CH3,故答案为:B。
7.(2022春·陕西西安·高二长安一中校考期中)设为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,8g甲烷中含C-H键数目为
B.标准状况下,11.2L苯中含有碳原子数目为
C.溶液中含氧原子数目为
D.与足量完全反应转移电子数目为
【答案】A
【解析】A.8g甲烷的物质的量为0.5mol,而甲烷中含4条C-H 键,故0.5mol甲烷中含2NA条 C-H键,A正确;
B.标况下,苯不是气态,故不能根据气体摩尔体积来计算其物质的量,B错误;
C.硝酸铵溶液中除了硝酸铵外,水也含氧原子,故此溶液中所含的氧原子的个数多于0.3NA个,C错误;
D.7.8g过氧化钠的物质的量为0.1mol,而过氧化钠和二氧化碳反应时,1mol过氧化钠转移1mol电子,故0.1mol过氧化钠转移0.1NA个电子,D错误;
故本题选A。
8.(2022春·宁夏石嘴山·高二石嘴山市第三中学校考期中)下列说法正确的是
A.和互为同系物
B.柠檬烯分子中所有的碳原子不一定在同一平面上
C.CH3CHOHCOOH经加聚反应可生成高分子化合物
D.CH2=CCH3CH=CH2与以物质的量之比加成,产物有两种(不考虑立体异构)
【答案】B
【解析】A.结构相似,相差n个CH2,具有相同官能团的同一类物质是同系物,是苯酚,是苯乙醇,不是同一类别物质,不属于同系物,A项错误;
B.柠檬烯分子中存在苯环模型,连接在苯环上的碳原子同一个平面;乙烯模型中,连在碳碳双键上的碳原子在同一个平面,苯环所处的平面与乙烯模型所处的平面可能不在同一平面上,故所有的碳原子不一定在同一平面上,B项正确;
C.CH3CHOHCOOH中没有碳碳双键或三键,不能发生加聚反应,应是发生缩聚反应,可生成高分子化合物,C项错误;
D.CH2=CCH3CH=CH2与以物质的量之比加成,产物只有一种,D项错误;
故答案选B。
9.(2022春·广东广州·高二校联考期中)X,Y,Z,M,N为原子序数依次增大的五种短周期主族元素,原子序数之和为28。其中Z的一种同位素在考古学中可用于断代,N元素的非金属性在短周期元素中最强。这五种元素组成的一种化合物的结构如图所示。下列说法错误的是
A.简单离子半径:M>N
B.该化合物的阳离子能使溴水褪色
C.M的单质在常温下能与氧气发生化合反应
D.最高价氧化物对应水化物的酸性:M>Z
【答案】C
【分析】根据题目所给信息X,Y,Z,M,N为原子序数依次增大的五种短周期主族元素,原子序数之和为28。其中Z的一种同位素在考古学中可用于断代,N元素的非金属性在短周期元素中最强。推知Z为C,N为F;结合上述物质结构可知X形成1个共价键达到稳定结构,则X为H元素,Y也形成4个共价键,且得到一个电子,则说明Y的最外层有3个电子,结合原子序数的相对大小推知Y为B,五种元素原子序数之和为28,则推知M的原子序数为28-1-5-6-9=7,则M为N元素,综上所述,X,Y,Z,M,N分别是H元素,B元素,C元素,N元素和F元素,据此分析解答。
【解析】A.电子层数相同时,原子序数越小,其元素对应简单离子半径越大,则简单离子半径:M(N3-)>N(F-),A正确;
B.该化合物的阳离子中含有碳碳双键,可与溴单质发生加成反应,从而使溴水褪色,B正确;
C.M的单质为氮气,氮气在常温下较稳定,不能与氧气发生化合反应,C错误;
D.非金属性越强,元素对应最高价氧化物对应水化物的酸性越强,因非金属性:N>C,所以最高价氧化物对应水化物的酸性:HNO3>H2CO3,D正确;
故选C。
10.(2022春·云南昆明·高二昆明一中校考期中)一种实现二氧化碳固定及再利用的反应如下:下列叙述正确的是
A.化合物1分子中的所有原子共平面 B.化合物1与乙醇互为同系物
C.化合物2分子中含有羟基和酯基 D.化合物2可在碱性条件下水解
【答案】D
【解析】A.化合物1分子中还有亚甲基结构,其中心碳原子采用sp3杂化方式,所以所有原子不可能共平面,选项A错误;
B.结构相似,分子上相差n个CH2的有机物互为同系物,上述化合物1为环氧乙烷,属于醚类,乙醇属于醇类,与乙醇结构不相似,不是同系物,选项B错误;
C.根据上述化合物2的分子结构可知,分子中含酯基,不含羟基,选项C错误;
D.化合物2分子中含有酯基,能在碱性条件下发生水解反应,选项D正确;
答案选D。
11.(2022春·江苏无锡·高二校联考期中)关于的说法正确的是
A.分子中的碳原子一定都共平面
B.分子中共平面的原子数目最多为14
C.分子中的苯环由单双键交替组成
D.与Cl2发生取代反应生成两种产物
【答案】A
【解析】A. 根据苯中12个原子共平面,乙炔中四个原子共直线,分子中的碳原子一定都共平面,故A正确;
B. 根据苯中12个原子共平面,乙炔中四个原子共直线,甲烷中最多三个原子共平面,因此分子中共平面的原子数目最多为15个(甲基中碳原子和其中一个氢原子与其他原子共面),故B错误;
C. 苯环中不含碳碳双键,故C错误;
D. 与Cl2发生取代反应,一氯代物有:取代甲基上的氢有一种产物,取代苯环上的氢有四种产物,此外还有二氯代物、三氯代物等,不只两种产物,故D错误;
故选A。
12.(2022春·上海崇明·高二校考阶段练习)0.8mol甲烷完全和氯气发生取代反应,若生成的四种氯代产物的物质的量相同,则反应消耗的氯气的物质的量为
A.0.8mol B.1.6mol C.2.0mol D.3.2mol
【答案】C
【解析】0.8molCH4与Cl2发生取代反应,待反应完成后测得4种取代物物质的量相等,则CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量都是0.2mol,CH4与Cl2发生取代反应时消耗的氢原子和氯气的物质的量之比是1:1,生成0.2molCH3Cl需要Cl2的物质的量为0.2mol,生成0.2molCH2Cl2需要Cl2的物质的量为0.2mol×2=0.4mol,生成0.2molCHCl3需要Cl2的物质的量为0.2mol×3=0.6mol,生成0.2molCCl4需要Cl2的物质的量为0.2mol×4=0.8mol,所以总共消耗的氯气的物质的量=(0.2+0.4+0.6+0.8)mol=2.0mol,故选:C。
13.(2022春·上海崇明·高二校考阶段练习)由乙烯合成聚乙烯,其反应类型是
A.取代反应 B.加成反应 C.加聚反应 D.氧化反应
【答案】C
【解析】乙烯发生加聚反应,生成聚乙烯,故其反应类型为加聚反应,故答案选C。
14.(2022秋·黑龙江佳木斯·高二建三江分局第一中学校考期中)四氯乙烯( )是一种衣物干洗剂,聚四氟乙烯( )是家用不粘锅内侧涂层的主要成分,下列说法正确的是
A.它们都能发生加成反应,都能使酸性高锰酸钾溶液褪色
B.它们的分子中C原子的杂化类型均为sp2杂化
C.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较活泼
D.Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性
【答案】D
【解析】A.四氯乙烯分子中含有不饱和的碳碳双键,能够被酸性高锰酸钾溶液氧化而使溶液褪色,而聚四氯乙烯分子中不含有不饱和的碳碳双键,不能被高锰酸钾溶液氧化,因此不能使含高锰酸钾溶液褪色,A错误;
B.四氯乙烯分子中C原子采用sp2杂化;而聚四氟乙烯分子中C原子都是饱和C原子,采用sp3杂化,B错误;
C.四氯乙烯属于有机物,能溶解油脂;聚四氟乙烯只含饱和碳原子,性质较稳定,所以聚四氟乙烯的化学性质不活泼,C错误;
D.Cl和F为同主族元素,由于元素的非金属性:F>Cl,所以元素的电负性:F>Cl。元素的电负性越大,其与C原子形成的化学键的极性就越强,因此C-F键极性大于C-Cl键极性,D正确;
故合理选项是D。
15.(2022春·湖南邵阳·高二湖南省邵东市第一中学校考阶段练习)科学家提出由催化乙烯和2—丁烯合成丙烯的反应历程如下图(所有碳原子满足最外层8电子稳定结构)。下列说法不正确的是
A.乙烯、丙烯和丁烯互为同系物
B.总反应的化学方程式为:
C.中加入的2—丁烯具有反式结构
D.碳、钨(W)原子间的化学键在的过程中未发生断裂
【答案】D
【解析】A.乙烯、丙烯和2—丁烯结构相似,组成上相差若干个CH2,互为同系物,A正确;
B.由反应历程图可知,总反应的化学方程式为:,B正确;
C.在2—丁烯的结构中两个双键碳所连接的原子或者原子团各不相同,图中结构中两个甲基位于双键的异侧,为反式结构,C正确;
D.由图可知的过程中碳、钨原子间的化学键发生了断裂,D错误;
故选D。
16.(2022春·上海金山·高二华东师范大学第三附属中学校考阶段练习)下列物质不能使酸性溶液褪色的是
A. B. C. D.
【答案】B
【解析】A.A中含碳碳双键,能使酸性高锰酸钾溶液褪色,A不符合题意;
B.B为丙烷,不能使酸性高锰酸钾溶液褪色,B符合题意;
C.C为甲苯,能被酸性高锰酸钾溶液氧化为苯甲酸,酸性高锰酸钾溶液褪色,C不符合题意;
D.D为乙炔,含碳碳三键,能使酸性高锰酸钾溶液褪色,D不符合题意;
故选B。
17.(2022秋·宁夏银川·高二校考阶段练习)工业上可由乙苯生产苯乙烯:+H2 ,下列说法正确的是
A.可用Br2/CCl4鉴别乙苯和苯乙烯
B.乙苯的同分异构体共有三种
C.该反应的类型为加成反应
D.乙苯和苯乙烯分子内共平面的碳原子数均为7
【答案】A
【解析】A.苯乙烯可与溴发生加成反应,溶液褪色,而乙苯不反应,可鉴别,故A正确;
B.乙苯的同分异构体可为二甲苯,有邻、间、对,连同乙苯共4种,如不含苯环,则同分异构体种类更多,故B错误;
C.反应碳碳单键变为碳碳双键,为消去反应,故C错误;
D.苯环和碳碳双键都为平面形,与苯环直接相连的原子在同一个平面上,则乙苯有7个碳原子共平面,苯乙烯有8个碳原子共平面,故D错误;
故选:A。
18.(2022秋·甘肃定西·高二校考期中)2020年我国在新型冠状病毒防控、研究工作中取得重大进展,研究发现含有二苯乙烯结构的孟鲁司特对病毒有抑制作用,二苯乙烯结构简式如图,下列说法正确的是
A.二苯乙烯分子式为C14H14
B.二苯乙烯所有原子不可能共平面
C.1 mol二苯乙烯在一定条件下最多可以加成6 mol H2
D.二苯乙烯能发生取代反应、氧化反应、加成反应、加聚反应
【答案】D
【解析】A.二苯乙烯分子式为C14H12,A错误;
B..苯的12个原子共平面,乙烯的6个原子共平面且单键可以旋转,故二苯乙烯所有原子可能共平面,B错误;
C.1 mol二苯乙烯在一定条件下最多可以加成7 mol H2,C错误;
D.二苯乙烯分子中苯环能发生取代反应、碳碳双键能发生氧化反应、加成反应、加聚反应,D正确;
故选D。
二、多选题
19.(2022春·河北石家庄·高二石家庄二中校考阶段练习)如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
A.逐滴加入饱和食盐水的目的是控制生成乙炔的速率
B.硫酸铜可以除去杂质H2S,PH3;换为NaOH也可以达到除杂的目的
C.若需制备较多乙炔,可用启普发生器
D.CaC2与水反应生成乙炔,则Mg2C3与水反应生成丙炔
【答案】BC
【解析】A.电石与水反应剧烈,则逐滴加入饱和食盐水可控制生成乙炔的速率,A正确;
B.因为H2S+CuSO4=CuS↓+H2SO4(CuS溶解度极小,不溶于稀硫酸)24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4,硫酸铜可以除去杂质H2S、PH3;H2S能与NaOH溶液反应,但PH3性质类似于氨气,难溶于NaOH溶液中,故换为NaOH只可以达到除去H2S杂质的目的,而达不到除去PH3的目的,B错误;
C.由于此反应为放热反应,易使启普发生器炸裂;CaC2能与水蒸气反应,不便于长期放置;且生成的Ca(OH)2是微溶物,易形成糊状附着在CaC2表面,不便于控制,故制备乙炔,不可用启普发生器,C错误;
D.CaC2与水反应生成乙炔,方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,则Mg2C3与水反应的方程式为:Mg2C3+4H2O=2Mg(OH)2↓+C3H4↑生成丙炔,D正确;
故答案为:BC。
20.(2022春·河北石家庄·高二石家庄二中校考阶段练习)已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是
A.该物质所有碳原子不可能共平面
B.该有机物苯环上的一溴代物有3种
C.该物质是苯的同系物,燃烧有浓烟产生
D.分子中最多有6个碳原子处于同一直线上
【答案】BD
【解析】A.该物质含有苯环,苯环中环上的6个碳原子以及与碳原子相连的原子也共面,两个苯环之间为单键相连,可以旋转到同一平面上,故所有碳原子可能共平面,故A错误;
B.该有机物苯环上有3种氢原子,故一溴代物有3种,故B正确;
C.苯的同系物的通式为CnH2n-6,题目中有机物不符合此通式,故C错误;
D.将该有机物的结构简式写成,1、2、3、4、5、6号碳原子一定在同一直线上,故分子中最多有6个碳原子处于同一直线上,故D正确;
故选BD。
第II卷(非选择题)
请点击修改第II卷的文字说明
三、填空题
21.(2022春·江苏无锡·高二校联考期中)按要求回答下列问题:
(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为_______,请预测B的核磁共振氢谱上有_______个峰(序号)。
(2)写出结构简式或名称:
①分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃结构简式_______。
②戊烷(C5H12)的某种同分异构体只有一种一氯代物,写出该戊烷的名称_______。
(3)烯烃中碳碳双键是重要的官能团,在不同条件下能发生多种变化。
①烯烃与高锰酸钾酸性溶液反应的氧化产物有如图的反应关系。
已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸(CH3COOH)和丙酸(CH3CH2COOH),则此烯烃的结构简式是_______;若为二氧化碳和丁酮(),则此烯烃的结构简式是_______。
②双烯合成反应(即 Diels-Alder 反应)是一类二烯烃与单烯烃或炔烃作用生成六元环状化合物的反应,例如,最简单的 1,3-丁二烯和乙烯的作用表示为:。则由1-丁烯和 2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为_______。
【答案】(1) BrCH2-CH2Br 2
(2) 2,2-二甲基丙烷(或新戊烷)
(3) CH3CH=CHCH2CH3
【解析】(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图显示A中只有一种等效氢原子,则A的结构简式为BrCH2-CH2Br,B的结构简式为CH3-CHBr2,B中有两种等效氢原子,故预测B的核磁共振氢谱上有2个峰(序号)。
(2)①分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,则苯环上有两个甲基,且位于对位上,则该芳香烃结构简式。
②戊烷(C5H12)的某种同分异构体只有一种一氯代物,该戊烷的结构简式为,用系统命名法命名为2,2-二甲基丙烷,习惯命名法命名为新戊烷。
(3)已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸(CH3COOH)和丙酸(CH3CH2COOH),根据已知信息可知,双键碳原子上有一个氢原子时,被氧化为羧基,则此烯烃的结构简式是CH3CH=CHCH2CH3;双键碳原子上没有氢原子时,被氧化为羰基,双键碳原子上有两个氢原子时,被氧化为二氧化碳,则若为二氧化碳和丁酮(),则此烯烃的结构简式是。
②已知1,3-丁二烯和乙烯的作用表示为:。则由1-丁烯和 2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为。
22.(2022春·上海崇明·高二校考阶段练习)现代化学工业中,有机原料主要来自石油的裂化、裂解、重整产物。部分反应如图。
(1)请写出反应①由乙烷制备溴乙烷的化学反应方程式_______
(2)请写出反应②由乙烯制备乙醇的化学反应方程式_______。
(3)已知苯制备硝基苯的化学反应方程式是,为则该反应的反应类型为_______。
【答案】(1)
(2)
(3)取代反应
【解析】(1)乙烷和溴蒸气发生取代反应生成溴乙烷和HBr,化学反应方程式为;
(2)反应②由乙烯和水发生加成反应生成乙醇,化学反应方程式为;;
(3)苯上的H原子被硝基发生取代反应制备硝基苯,反应类型是取代反应。
23.(2022秋·河南南阳·高二校考阶段练习)Ⅰ.有下列各组物质:① 和 ;②石墨和足球烯;③正戊烷和异戊烷;④正丁烷和异庚烷;⑤和;⑥CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3。用序号填空:
(1)_______组两者互为同位素。
(2)_______组两者互为同素异形体。
(3)_______组两者属于同系物。
(4)_______组两者互为同分异构体。
II.按要求回答下列问题:
(5)中含有的官能团为(写名称)_______
(6)CH2=CH-CH3加聚产物的结构简式是_______
(7)键线式表示的分子式_______
(8)有机物A的结构简式为CH3CH2CH(CH3)CH(CH3)C(CH3)3
①若A是单烯烃与氢气加成后的产物,则该单烯烃可能有_______种结构(不考虑立体异构);
②若A是炔烃与氢气加成后的产物,则该单炔烃可能有_______种结构;
【答案】(1)①
(2)②
(3)④
(4)③⑥
(5)羟基、羧基
(6)
(7)C8H16
(8) 5 1
【解析】(1)
质子数相同中子数不同的同种元素属于同位素,故① 和互为同位素。
(2)
同种元素组成的不同结构的单质属于同素异形体,②石墨和足球烯属于同素异形体;
(3)
结构相似相差n个CH2的有机物属于同系物,④正丁烷和异庚烷属于同系物;
(4)
分子相同结构不同的分子互为同分异构体,③正戊烷和异戊烷;⑥CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3。这两组属于同分异构体;
(5)
中含有的官能团为羟基、羧基;
(6)
CH2=CH-CH3加聚产物是聚丙烯,结构简式是;
(7)
键线式表示的分子式C8H16;
(8)
①若A是单烯烃与氢气加成后的产物,相邻的两个碳上的氢去掉恢复双键,,双键有可能在12,23,34,35,47,则该单烯烃可能,5种;
②若A是炔烃与氢气加成后的产物,相邻的碳上有两个氢原子,去氢后才能形三键,三键只能在1,2号碳之间,则该单炔烃可能有1种;
24.(2022春·上海黄浦·高二上海市敬业中学校考阶段练习)塑料制品是人类日常生活中使用量最大的合成高分子材料,但也造成了严重的环境问题——白色污染。回答下列问题:
(1)石油裂解气是一种复杂的混合气体,含有乙烯、丙烯、丁二烯等不饱和烃,聚丙烯广泛用于服装、毛毯、医疗器械、汽车、自行车等,请写出工业上利用石油裂解气生产聚丙烯的化学方程式_______。
(2)下列物质与乙烯互为同系物的是_______。
a. b.
c. d.
(3)下列几组物质,可以用分液漏斗分离的是_______。
a.苯与水 b.溴的溶液 c.乙醇与水 d.乙醇与溶液
(4)可以将废旧塑料隔绝空气加强热,使其变成氢气、甲烷、乙烯、苯等有用物质,实验装置如图所示(加热装置略)。
①试管B收集到的产物的结构简式为_______。
②锥形瓶中发生反应的方程式为_______。
【答案】(1)nCH3CH=CH2
(2)c
(3)a
(4) CH2=CH2 + Br2→
【解析】(1)
工业上利用石油裂解气中的丙烯通过加聚反应生产聚丙烯,其方程式为:nCH3CH=CH2;
(2)
同系物必须具有相同的结构且分子组成上相差若干个CH2原子团的有机物,故乙烯的同系物只有c;
(3)
能用分液漏斗分离的的两种液体不能相溶,
a.苯与水不能相溶,可以用分液漏斗分离,a符合题意;
b.溴是有机物可以溶于有机溶剂四氯化碳,不可以用分液漏斗分离,b不符合题意;
c.乙醇和水是相溶的,不可以用分液漏斗分离,c不符合题意;
d.乙醇能溶于水,碳酸钠溶液为无机溶液,两者能相溶,不可以用分液漏斗分离,d不符合题意;
故选a;
(4)
①因为苯在常温下为液体,故废旧塑料加强热之后的产物中只有苯会被冷水冷凝下来,故B中收集到的为物质的结构简式为;
②生成的乙烯使溴水褪色,其方程式为:CH2=CH2 + Br2→ 。
25.(2022秋·山东济南·高二山东师范大学附中校考阶段练习)请回答下列问题。
(1)在下列物质中互为同分异构体的有_______;互为同素异形体的有_______;互为同系物的是_______(填序号)。
①2-甲基丁烷 ②CH3- CH2- CH3③CH3CH2CH2OH ④CH3- Cl ⑤白磷 ⑥CH3- O- CH2CH3⑦红磷 ⑧CH3CH2- Cl
(2)已知有机物:
甲:,乙:,丙:。
①请写出甲中含氧官能团的名称:______、______。
②乙中饱和碳原子有_____个;丙中一定在同一个平面上的碳原子有______个;
③请判别上述哪些化合物互为同分异构体_____。 (填编号)
(3)化合物A、B和C互为同分异构体。它们的元素分析数据为:碳92.3%, 氢7.7%。 1 mol A在氧气中充分燃烧产生179.2 L二氧化碳(标准状况)。A是芳香化合物,分子中所有的原子可能共平面; B是具有两个支链的链状化合物,分子中只有两种不同化学环境的氢原子,B为非极性分子: C中碳原子全是sp3杂化,且化学环境完全相同。
①A、B和C的分子式为_______; B的结构简式为_______; C 的二氯代物有_______种。
②下列关于A分子说法正确的是_______。(填序号)
A.不能使稀高锰酸钾溶液褪色。
B.可以发生加成聚合反应。
C.A属于苯的同系物
D.A可以与4molH2发生加成反应。
【答案】(1) ③和⑥ ⑤和⑦ ①和②、④和⑧
(2) 醛基 (醇)羟基 1 8 甲和丙
(3) C8H8 3 BD
【解析】(1)
分子式相同结构不同的有机物属于同分异构体,③的分子式为C3H8O,⑥的分子式为C3H8O,③和⑥互为同分异构体;同种元素形成的结构不同的单质是同素异形体,⑤白磷和⑦红磷互为同素异形体;结构相似相差n个CH2的有机物互为同系物,①2-甲基丁烷和②CH3- CH2- CH3,④CH3- Cl和⑧CH3CH2- Cl互为同系物;
(2)
①根据结构式可知甲中含氧官能团的名称为醛基和(醇)羟基;
②根据结构式可知只有-CH2OH中的C为饱和碳,故乙中饱和碳原子有1个;苯环上的C处于同一平面,与苯环直接相连的原子与苯环处于同一平面,故丙中一定在同一个平面上的碳原子有8个;
③分子式相同结构不同的有机物属于同分异构体,根据结构可知甲和丙分子式都是C8H8O2,结构不同互为同分异构体,故答案为甲和丙;
(3)
①根据题意,已知碳92.3%, 氢7.7%,化合物的摩尔质量为,,根据计算可知该物质的分子式为C8H8;A是芳香化合物,分子中所有的原子可能共平面,故A为苯乙烯;该分子具有5个不饱和度,B是具有两个支链的链状化合物,分子中只有两种不同化学环境的氢原子,B为非极性分子,故B为;C中碳原子全是sp3杂化,且化学环境完全相同,可知C为立方烷,氯的位置有边上两个顶点,面对角线两个顶点,和体对角线两个顶点,故C 的二氯代物有3中;
②A. A为苯乙烯,有碳碳双键,能使稀高锰酸钾溶液褪色,故A错误。
B. 苯乙烯有碳碳双键,可以发生加成聚合反应,故B正确;
C.A和苯的结构不相似,不属于苯的同系物,故C错误;
D.A为苯乙烯,苯环与氢气加成需要3mol碳碳双键加成需要1mol故,1molA可以与4molH2发生加成反应,故D正确。
故答案为BD
试卷第2页,共2页
试卷第1页,共1页
中小学教育资源及组卷应用平台
专题3 石油化工的基础物质--烃专题检测(A卷)
(时间:75分钟 满分:100分)
一、单选题
1.(2022秋·浙江丽水·高二校考阶段练习)下列对有机化合物的分类结果正确的是
A.乙烯、苯、环己烷属于不饱和烃
B.苯、环戊烷、环己烷同属于芳香烃
C.乙烯、乙炔同属于烯烃
D.、、同属于环烷烃
【答案】D
【解析】A.环己烷属于饱和烃,A不正确;
B.环戊烷、环己烷均不属于芳香烃,B不正确;
C.乙炔属于炔烃,C不正确;
D.选项中提供的物质均属于环烷烃,D正确;
所以选D。
2.(2022春·云南昆明·高二校考期末)在实验室中,下列除去杂质的方法正确的是
A.溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取
B.硝基苯中混有浓硝酸和浓硫酸,加入NaOH溶液,静置,分液
C.用酸性KMnO4溶液除去乙炔中混有的H2S
D.乙烯中混有SO2和CO2,将其先后通入NaOH溶液和KMnO4酸性溶液中洗气
【答案】B
【解析】A.溴苯中混有溴,加入溶液,振荡,再用汽油萃取,此时有机层中会有生成的碘单质,所以除去了溴但引入了碘,A错误;
B.硝基苯中混有浓硝酸和浓硫酸,加入溶液可以反应掉两种酸,静置,分液,B正确;
C.用酸性溶液除去乙炔中混有的时也会和乙炔反应,C错误;
D.乙烯中混有和,将其先通入溶液除去二氧化碳和二氧化硫,再通入酸性溶液时乙烯被除去,D错误;
故选B。
3.(2022春·上海浦东新·高二华师大二附中校考阶段练习)下列表示正确的是
A.氨气的电子式: B.乙炔分子的球棍模型:
C.2—丁烯的键线式: D.结构示意图为:
【答案】B
【解析】A.氨气为共价化合物,电子式为,故A错误;
B.乙炔的结构简式为HC≡CH,球棍模型为,故B正确;
C.2—丁烯的结构简式为CH3CH=CHCH3,键线式为,故C错误;
D.硫离子的核电荷数为16,核外3个电子层,最外层电子数为8,离子的结构示意图为,故D错误;
故选B。
4.(2022春·宁夏银川·高二银川唐徕回民中学校考期中)如图是用实验室制得的乙烯(C2H5OHCH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是
A.装置①和装置③中都盛有水,其作用相同
B.装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C.制备乙烯和生成1,2-二溴乙烷的反应类型分别是消去反应和加成反应
D.产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出
【答案】C
【分析】反应C2H5OHCH2=CH2↑+H2O制得的乙烯中可能混有SO2、CO2,乙烯气体通入装置①中,装置②中的NaOH溶液可以吸收乙烯中混有的SO2、CO2,乙烯和溴水在装置③中反应,装置④是吸收逸出的溴蒸气,防止污染空气。
【解析】A.装置①中气体压力过大时,水就会从玻璃管上端溢出,起到缓冲作用;溴易挥发,装置③水的作用是冷却液溴,可避免溴的大量挥发,故A错误;
B.装置②吸收乙烯中混有的SO2、CO2;装置④是吸收逸出的溴蒸气,防止污染空气,吸收的杂质不相同,故B错误;
C.制备乙烯是乙醇发生消去反应;生成1,2-二溴乙烷是乙烯能与溴水发生加成反应,故C正确;
D.1,2-二溴乙烷与水不溶,密度比水大,在水的下层,应从分液漏斗的下口倒出,故D错误;
故选C。
5.(2022·内蒙古·高二统考学业考试)下图是四种烃分子的球棍模型,下列说法中正确的是
A.甲能使酸性高锰酸钾溶液褪色
B.乙的产量可以用来衡量一个国家的石油化工发展水平
C.丙不存在同分异构体
D.丁分子中含有碳碳单键和碳碳双键
【答案】B
【解析】A.甲是甲烷,甲烷不能与酸性高锰酸钾溶液反应,不能使酸性高锰酸钾溶液褪色,A错误;
B.乙是乙烯,乙烯的产量可以用来衡量一个国家的石油化工发展水平,B正确;
C.丙的分子式为C4H10,结构有CH3CH2CH2CH3和 ,C错误;
D.丁是苯,苯中不存在碳碳单键和碳碳双键,是一种介于单键和双键之间的独特的共价键,D错误;
故选B。
6.(2022春·上海宝山·高二上海交大附中校考期中)在烷烃分子中,、、、中的碳原子分别称为伯、种叔、季碳原子,数目分别用、、、表示。,的烷烃共有
A.2种 B.3种 C.4种 D.5种
【答案】B
【解析】由题干信息可知,符合条件的烷烃共有:(CH3)3CCH(CH3)CH2CH3、(CH3)3CCH2CH(CH3)2、(CH3)2CHC(CH3)2CH2CH3,故答案为:B。
7.(2022春·陕西西安·高二长安一中校考期中)设为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,8g甲烷中含C-H键数目为
B.标准状况下,11.2L苯中含有碳原子数目为
C.溶液中含氧原子数目为
D.与足量完全反应转移电子数目为
【答案】A
【解析】A.8g甲烷的物质的量为0.5mol,而甲烷中含4条C-H 键,故0.5mol甲烷中含2NA条 C-H键,A正确;
B.标况下,苯不是气态,故不能根据气体摩尔体积来计算其物质的量,B错误;
C.硝酸铵溶液中除了硝酸铵外,水也含氧原子,故此溶液中所含的氧原子的个数多于0.3NA个,C错误;
D.7.8g过氧化钠的物质的量为0.1mol,而过氧化钠和二氧化碳反应时,1mol过氧化钠转移1mol电子,故0.1mol过氧化钠转移0.1NA个电子,D错误;
故本题选A。
8.(2022春·宁夏石嘴山·高二石嘴山市第三中学校考期中)下列说法正确的是
A.和互为同系物
B.柠檬烯分子中所有的碳原子不一定在同一平面上
C.CH3CHOHCOOH经加聚反应可生成高分子化合物
D.CH2=CCH3CH=CH2与以物质的量之比加成,产物有两种(不考虑立体异构)
【答案】B
【解析】A.结构相似,相差n个CH2,具有相同官能团的同一类物质是同系物,是苯酚,是苯乙醇,不是同一类别物质,不属于同系物,A项错误;
B.柠檬烯分子中存在苯环模型,连接在苯环上的碳原子同一个平面;乙烯模型中,连在碳碳双键上的碳原子在同一个平面,苯环所处的平面与乙烯模型所处的平面可能不在同一平面上,故所有的碳原子不一定在同一平面上,B项正确;
C.CH3CHOHCOOH中没有碳碳双键或三键,不能发生加聚反应,应是发生缩聚反应,可生成高分子化合物,C项错误;
D.CH2=CCH3CH=CH2与以物质的量之比加成,产物只有一种,D项错误;
故答案选B。
9.(2022春·广东广州·高二校联考期中)X,Y,Z,M,N为原子序数依次增大的五种短周期主族元素,原子序数之和为28。其中Z的一种同位素在考古学中可用于断代,N元素的非金属性在短周期元素中最强。这五种元素组成的一种化合物的结构如图所示。下列说法错误的是
A.简单离子半径:M>N
B.该化合物的阳离子能使溴水褪色
C.M的单质在常温下能与氧气发生化合反应
D.最高价氧化物对应水化物的酸性:M>Z
【答案】C
【分析】根据题目所给信息X,Y,Z,M,N为原子序数依次增大的五种短周期主族元素,原子序数之和为28。其中Z的一种同位素在考古学中可用于断代,N元素的非金属性在短周期元素中最强。推知Z为C,N为F;结合上述物质结构可知X形成1个共价键达到稳定结构,则X为H元素,Y也形成4个共价键,且得到一个电子,则说明Y的最外层有3个电子,结合原子序数的相对大小推知Y为B,五种元素原子序数之和为28,则推知M的原子序数为28-1-5-6-9=7,则M为N元素,综上所述,X,Y,Z,M,N分别是H元素,B元素,C元素,N元素和F元素,据此分析解答。
【解析】A.电子层数相同时,原子序数越小,其元素对应简单离子半径越大,则简单离子半径:M(N3-)>N(F-),A正确;
B.该化合物的阳离子中含有碳碳双键,可与溴单质发生加成反应,从而使溴水褪色,B正确;
C.M的单质为氮气,氮气在常温下较稳定,不能与氧气发生化合反应,C错误;
D.非金属性越强,元素对应最高价氧化物对应水化物的酸性越强,因非金属性:N>C,所以最高价氧化物对应水化物的酸性:HNO3>H2CO3,D正确;
故选C。
10.(2022春·云南昆明·高二昆明一中校考期中)一种实现二氧化碳固定及再利用的反应如下:下列叙述正确的是
A.化合物1分子中的所有原子共平面 B.化合物1与乙醇互为同系物
C.化合物2分子中含有羟基和酯基 D.化合物2可在碱性条件下水解
【答案】D
【解析】A.化合物1分子中还有亚甲基结构,其中心碳原子采用sp3杂化方式,所以所有原子不可能共平面,选项A错误;
B.结构相似,分子上相差n个CH2的有机物互为同系物,上述化合物1为环氧乙烷,属于醚类,乙醇属于醇类,与乙醇结构不相似,不是同系物,选项B错误;
C.根据上述化合物2的分子结构可知,分子中含酯基,不含羟基,选项C错误;
D.化合物2分子中含有酯基,能在碱性条件下发生水解反应,选项D正确;
答案选D。
11.(2022春·江苏无锡·高二校联考期中)关于的说法正确的是
A.分子中的碳原子一定都共平面
B.分子中共平面的原子数目最多为14
C.分子中的苯环由单双键交替组成
D.与Cl2发生取代反应生成两种产物
【答案】A
【解析】A. 根据苯中12个原子共平面,乙炔中四个原子共直线,分子中的碳原子一定都共平面,故A正确;
B. 根据苯中12个原子共平面,乙炔中四个原子共直线,甲烷中最多三个原子共平面,因此分子中共平面的原子数目最多为15个(甲基中碳原子和其中一个氢原子与其他原子共面),故B错误;
C. 苯环中不含碳碳双键,故C错误;
D. 与Cl2发生取代反应,一氯代物有:取代甲基上的氢有一种产物,取代苯环上的氢有四种产物,此外还有二氯代物、三氯代物等,不只两种产物,故D错误;
故选A。
12.(2022春·上海崇明·高二校考阶段练习)0.8mol甲烷完全和氯气发生取代反应,若生成的四种氯代产物的物质的量相同,则反应消耗的氯气的物质的量为
A.0.8mol B.1.6mol C.2.0mol D.3.2mol
【答案】C
【解析】0.8molCH4与Cl2发生取代反应,待反应完成后测得4种取代物物质的量相等,则CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量都是0.2mol,CH4与Cl2发生取代反应时消耗的氢原子和氯气的物质的量之比是1:1,生成0.2molCH3Cl需要Cl2的物质的量为0.2mol,生成0.2molCH2Cl2需要Cl2的物质的量为0.2mol×2=0.4mol,生成0.2molCHCl3需要Cl2的物质的量为0.2mol×3=0.6mol,生成0.2molCCl4需要Cl2的物质的量为0.2mol×4=0.8mol,所以总共消耗的氯气的物质的量=(0.2+0.4+0.6+0.8)mol=2.0mol,故选:C。
13.(2022春·上海崇明·高二校考阶段练习)由乙烯合成聚乙烯,其反应类型是
A.取代反应 B.加成反应 C.加聚反应 D.氧化反应
【答案】C
【解析】乙烯发生加聚反应,生成聚乙烯,故其反应类型为加聚反应,故答案选C。
14.(2022秋·黑龙江佳木斯·高二建三江分局第一中学校考期中)四氯乙烯( )是一种衣物干洗剂,聚四氟乙烯( )是家用不粘锅内侧涂层的主要成分,下列说法正确的是
A.它们都能发生加成反应,都能使酸性高锰酸钾溶液褪色
B.它们的分子中C原子的杂化类型均为sp2杂化
C.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较活泼
D.Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性
【答案】D
【解析】A.四氯乙烯分子中含有不饱和的碳碳双键,能够被酸性高锰酸钾溶液氧化而使溶液褪色,而聚四氯乙烯分子中不含有不饱和的碳碳双键,不能被高锰酸钾溶液氧化,因此不能使含高锰酸钾溶液褪色,A错误;
B.四氯乙烯分子中C原子采用sp2杂化;而聚四氟乙烯分子中C原子都是饱和C原子,采用sp3杂化,B错误;
C.四氯乙烯属于有机物,能溶解油脂;聚四氟乙烯只含饱和碳原子,性质较稳定,所以聚四氟乙烯的化学性质不活泼,C错误;
D.Cl和F为同主族元素,由于元素的非金属性:F>Cl,所以元素的电负性:F>Cl。元素的电负性越大,其与C原子形成的化学键的极性就越强,因此C-F键极性大于C-Cl键极性,D正确;
故合理选项是D。
15.(2022春·湖南邵阳·高二湖南省邵东市第一中学校考阶段练习)科学家提出由催化乙烯和2—丁烯合成丙烯的反应历程如下图(所有碳原子满足最外层8电子稳定结构)。下列说法不正确的是
A.乙烯、丙烯和丁烯互为同系物
B.总反应的化学方程式为:
C.中加入的2—丁烯具有反式结构
D.碳、钨(W)原子间的化学键在的过程中未发生断裂
【答案】D
【解析】A.乙烯、丙烯和2—丁烯结构相似,组成上相差若干个CH2,互为同系物,A正确;
B.由反应历程图可知,总反应的化学方程式为:,B正确;
C.在2—丁烯的结构中两个双键碳所连接的原子或者原子团各不相同,图中结构中两个甲基位于双键的异侧,为反式结构,C正确;
D.由图可知的过程中碳、钨原子间的化学键发生了断裂,D错误;
故选D。
16.(2022春·上海金山·高二华东师范大学第三附属中学校考阶段练习)下列物质不能使酸性溶液褪色的是
A. B. C. D.
【答案】B
【解析】A.A中含碳碳双键,能使酸性高锰酸钾溶液褪色,A不符合题意;
B.B为丙烷,不能使酸性高锰酸钾溶液褪色,B符合题意;
C.C为甲苯,能被酸性高锰酸钾溶液氧化为苯甲酸,酸性高锰酸钾溶液褪色,C不符合题意;
D.D为乙炔,含碳碳三键,能使酸性高锰酸钾溶液褪色,D不符合题意;
故选B。
17.(2022秋·宁夏银川·高二校考阶段练习)工业上可由乙苯生产苯乙烯:+H2 ,下列说法正确的是
A.可用Br2/CCl4鉴别乙苯和苯乙烯
B.乙苯的同分异构体共有三种
C.该反应的类型为加成反应
D.乙苯和苯乙烯分子内共平面的碳原子数均为7
【答案】A
【解析】A.苯乙烯可与溴发生加成反应,溶液褪色,而乙苯不反应,可鉴别,故A正确;
B.乙苯的同分异构体可为二甲苯,有邻、间、对,连同乙苯共4种,如不含苯环,则同分异构体种类更多,故B错误;
C.反应碳碳单键变为碳碳双键,为消去反应,故C错误;
D.苯环和碳碳双键都为平面形,与苯环直接相连的原子在同一个平面上,则乙苯有7个碳原子共平面,苯乙烯有8个碳原子共平面,故D错误;
故选:A。
18.(2022秋·甘肃定西·高二校考期中)2020年我国在新型冠状病毒防控、研究工作中取得重大进展,研究发现含有二苯乙烯结构的孟鲁司特对病毒有抑制作用,二苯乙烯结构简式如图,下列说法正确的是
A.二苯乙烯分子式为C14H14
B.二苯乙烯所有原子不可能共平面
C.1 mol二苯乙烯在一定条件下最多可以加成6 mol H2
D.二苯乙烯能发生取代反应、氧化反应、加成反应、加聚反应
【答案】D
【解析】A.二苯乙烯分子式为C14H12,A错误;
B..苯的12个原子共平面,乙烯的6个原子共平面且单键可以旋转,故二苯乙烯所有原子可能共平面,B错误;
C.1 mol二苯乙烯在一定条件下最多可以加成7 mol H2,C错误;
D.二苯乙烯分子中苯环能发生取代反应、碳碳双键能发生氧化反应、加成反应、加聚反应,D正确;
故选D。
二、多选题
19.(2022春·河北石家庄·高二石家庄二中校考阶段练习)如图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
A.逐滴加入饱和食盐水的目的是控制生成乙炔的速率
B.硫酸铜可以除去杂质H2S,PH3;换为NaOH也可以达到除杂的目的
C.若需制备较多乙炔,可用启普发生器
D.CaC2与水反应生成乙炔,则Mg2C3与水反应生成丙炔
【答案】BC
【解析】A.电石与水反应剧烈,则逐滴加入饱和食盐水可控制生成乙炔的速率,A正确;
B.因为H2S+CuSO4=CuS↓+H2SO4(CuS溶解度极小,不溶于稀硫酸)24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4,硫酸铜可以除去杂质H2S、PH3;H2S能与NaOH溶液反应,但PH3性质类似于氨气,难溶于NaOH溶液中,故换为NaOH只可以达到除去H2S杂质的目的,而达不到除去PH3的目的,B错误;
C.由于此反应为放热反应,易使启普发生器炸裂;CaC2能与水蒸气反应,不便于长期放置;且生成的Ca(OH)2是微溶物,易形成糊状附着在CaC2表面,不便于控制,故制备乙炔,不可用启普发生器,C错误;
D.CaC2与水反应生成乙炔,方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,则Mg2C3与水反应的方程式为:Mg2C3+4H2O=2Mg(OH)2↓+C3H4↑生成丙炔,D正确;
故答案为:BC。
20.(2022春·河北石家庄·高二石家庄二中校考阶段练习)已知碳碳单键可绕键轴自由旋转,某烃的结构简式如图所示,下列说法中正确的是
A.该物质所有碳原子不可能共平面
B.该有机物苯环上的一溴代物有3种
C.该物质是苯的同系物,燃烧有浓烟产生
D.分子中最多有6个碳原子处于同一直线上
【答案】BD
【解析】A.该物质含有苯环,苯环中环上的6个碳原子以及与碳原子相连的原子也共面,两个苯环之间为单键相连,可以旋转到同一平面上,故所有碳原子可能共平面,故A错误;
B.该有机物苯环上有3种氢原子,故一溴代物有3种,故B正确;
C.苯的同系物的通式为CnH2n-6,题目中有机物不符合此通式,故C错误;
D.将该有机物的结构简式写成,1、2、3、4、5、6号碳原子一定在同一直线上,故分子中最多有6个碳原子处于同一直线上,故D正确;
故选BD。
第II卷(非选择题)
请点击修改第II卷的文字说明
三、填空题
21.(2022春·江苏无锡·高二校联考期中)按要求回答下列问题:
(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为_______,请预测B的核磁共振氢谱上有_______个峰(序号)。
(2)写出结构简式或名称:
①分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,写出该芳香烃结构简式_______。
②戊烷(C5H12)的某种同分异构体只有一种一氯代物,写出该戊烷的名称_______。
(3)烯烃中碳碳双键是重要的官能团,在不同条件下能发生多种变化。
①烯烃与高锰酸钾酸性溶液反应的氧化产物有如图的反应关系。
已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸(CH3COOH)和丙酸(CH3CH2COOH),则此烯烃的结构简式是_______;若为二氧化碳和丁酮(),则此烯烃的结构简式是_______。
②双烯合成反应(即 Diels-Alder 反应)是一类二烯烃与单烯烃或炔烃作用生成六元环状化合物的反应,例如,最简单的 1,3-丁二烯和乙烯的作用表示为:。则由1-丁烯和 2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为_______。
【答案】(1) BrCH2-CH2Br 2
(2) 2,2-二甲基丙烷(或新戊烷)
(3) CH3CH=CHCH2CH3
【解析】(1)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图显示A中只有一种等效氢原子,则A的结构简式为BrCH2-CH2Br,B的结构简式为CH3-CHBr2,B中有两种等效氢原子,故预测B的核磁共振氢谱上有2个峰(序号)。
(2)①分子式为C8H10的芳香烃,苯环上的一溴取代物只有一种,则苯环上有两个甲基,且位于对位上,则该芳香烃结构简式。
②戊烷(C5H12)的某种同分异构体只有一种一氯代物,该戊烷的结构简式为,用系统命名法命名为2,2-二甲基丙烷,习惯命名法命名为新戊烷。
(3)已知某烯烃的化学式为C5H10,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸(CH3COOH)和丙酸(CH3CH2COOH),根据已知信息可知,双键碳原子上有一个氢原子时,被氧化为羧基,则此烯烃的结构简式是CH3CH=CHCH2CH3;双键碳原子上没有氢原子时,被氧化为羰基,双键碳原子上有两个氢原子时,被氧化为二氧化碳,则若为二氧化碳和丁酮(),则此烯烃的结构简式是。
②已知1,3-丁二烯和乙烯的作用表示为:。则由1-丁烯和 2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为。
22.(2022春·上海崇明·高二校考阶段练习)现代化学工业中,有机原料主要来自石油的裂化、裂解、重整产物。部分反应如图。
(1)请写出反应①由乙烷制备溴乙烷的化学反应方程式_______
(2)请写出反应②由乙烯制备乙醇的化学反应方程式_______。
(3)已知苯制备硝基苯的化学反应方程式是,为则该反应的反应类型为_______。
【答案】(1)
(2)
(3)取代反应
【解析】(1)乙烷和溴蒸气发生取代反应生成溴乙烷和HBr,化学反应方程式为;
(2)反应②由乙烯和水发生加成反应生成乙醇,化学反应方程式为;;
(3)苯上的H原子被硝基发生取代反应制备硝基苯,反应类型是取代反应。
23.(2022秋·河南南阳·高二校考阶段练习)Ⅰ.有下列各组物质:① 和 ;②石墨和足球烯;③正戊烷和异戊烷;④正丁烷和异庚烷;⑤和;⑥CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3。用序号填空:
(1)_______组两者互为同位素。
(2)_______组两者互为同素异形体。
(3)_______组两者属于同系物。
(4)_______组两者互为同分异构体。
II.按要求回答下列问题:
(5)中含有的官能团为(写名称)_______
(6)CH2=CH-CH3加聚产物的结构简式是_______
(7)键线式表示的分子式_______
(8)有机物A的结构简式为CH3CH2CH(CH3)CH(CH3)C(CH3)3
①若A是单烯烃与氢气加成后的产物,则该单烯烃可能有_______种结构(不考虑立体异构);
②若A是炔烃与氢气加成后的产物,则该单炔烃可能有_______种结构;
【答案】(1)①
(2)②
(3)④
(4)③⑥
(5)羟基、羧基
(6)
(7)C8H16
(8) 5 1
【解析】(1)
质子数相同中子数不同的同种元素属于同位素,故① 和互为同位素。
(2)
同种元素组成的不同结构的单质属于同素异形体,②石墨和足球烯属于同素异形体;
(3)
结构相似相差n个CH2的有机物属于同系物,④正丁烷和异庚烷属于同系物;
(4)
分子相同结构不同的分子互为同分异构体,③正戊烷和异戊烷;⑥CH3-CH2-CH2-CH3和CH3-CH(CH3)CH3。这两组属于同分异构体;
(5)
中含有的官能团为羟基、羧基;
(6)
CH2=CH-CH3加聚产物是聚丙烯,结构简式是;
(7)
键线式表示的分子式C8H16;
(8)
①若A是单烯烃与氢气加成后的产物,相邻的两个碳上的氢去掉恢复双键,,双键有可能在12,23,34,35,47,则该单烯烃可能,5种;
②若A是炔烃与氢气加成后的产物,相邻的碳上有两个氢原子,去氢后才能形三键,三键只能在1,2号碳之间,则该单炔烃可能有1种;
24.(2022春·上海黄浦·高二上海市敬业中学校考阶段练习)塑料制品是人类日常生活中使用量最大的合成高分子材料,但也造成了严重的环境问题——白色污染。回答下列问题:
(1)石油裂解气是一种复杂的混合气体,含有乙烯、丙烯、丁二烯等不饱和烃,聚丙烯广泛用于服装、毛毯、医疗器械、汽车、自行车等,请写出工业上利用石油裂解气生产聚丙烯的化学方程式_______。
(2)下列物质与乙烯互为同系物的是_______。
a. b.
c. d.
(3)下列几组物质,可以用分液漏斗分离的是_______。
a.苯与水 b.溴的溶液 c.乙醇与水 d.乙醇与溶液
(4)可以将废旧塑料隔绝空气加强热,使其变成氢气、甲烷、乙烯、苯等有用物质,实验装置如图所示(加热装置略)。
①试管B收集到的产物的结构简式为_______。
②锥形瓶中发生反应的方程式为_______。
【答案】(1)nCH3CH=CH2
(2)c
(3)a
(4) CH2=CH2 + Br2→
【解析】(1)
工业上利用石油裂解气中的丙烯通过加聚反应生产聚丙烯,其方程式为:nCH3CH=CH2;
(2)
同系物必须具有相同的结构且分子组成上相差若干个CH2原子团的有机物,故乙烯的同系物只有c;
(3)
能用分液漏斗分离的的两种液体不能相溶,
a.苯与水不能相溶,可以用分液漏斗分离,a符合题意;
b.溴是有机物可以溶于有机溶剂四氯化碳,不可以用分液漏斗分离,b不符合题意;
c.乙醇和水是相溶的,不可以用分液漏斗分离,c不符合题意;
d.乙醇能溶于水,碳酸钠溶液为无机溶液,两者能相溶,不可以用分液漏斗分离,d不符合题意;
故选a;
(4)
①因为苯在常温下为液体,故废旧塑料加强热之后的产物中只有苯会被冷水冷凝下来,故B中收集到的为物质的结构简式为;
②生成的乙烯使溴水褪色,其方程式为:CH2=CH2 + Br2→ 。
25.(2022秋·山东济南·高二山东师范大学附中校考阶段练习)请回答下列问题。
(1)在下列物质中互为同分异构体的有_______;互为同素异形体的有_______;互为同系物的是_______(填序号)。
①2-甲基丁烷 ②CH3- CH2- CH3③CH3CH2CH2OH ④CH3- Cl ⑤白磷 ⑥CH3- O- CH2CH3⑦红磷 ⑧CH3CH2- Cl
(2)已知有机物:
甲:,乙:,丙:。
①请写出甲中含氧官能团的名称:______、______。
②乙中饱和碳原子有_____个;丙中一定在同一个平面上的碳原子有______个;
③请判别上述哪些化合物互为同分异构体_____。 (填编号)
(3)化合物A、B和C互为同分异构体。它们的元素分析数据为:碳92.3%, 氢7.7%。 1 mol A在氧气中充分燃烧产生179.2 L二氧化碳(标准状况)。A是芳香化合物,分子中所有的原子可能共平面; B是具有两个支链的链状化合物,分子中只有两种不同化学环境的氢原子,B为非极性分子: C中碳原子全是sp3杂化,且化学环境完全相同。
①A、B和C的分子式为_______; B的结构简式为_______; C 的二氯代物有_______种。
②下列关于A分子说法正确的是_______。(填序号)
A.不能使稀高锰酸钾溶液褪色。
B.可以发生加成聚合反应。
C.A属于苯的同系物
D.A可以与4molH2发生加成反应。
【答案】(1) ③和⑥ ⑤和⑦ ①和②、④和⑧
(2) 醛基 (醇)羟基 1 8 甲和丙
(3) C8H8 3 BD
【解析】(1)
分子式相同结构不同的有机物属于同分异构体,③的分子式为C3H8O,⑥的分子式为C3H8O,③和⑥互为同分异构体;同种元素形成的结构不同的单质是同素异形体,⑤白磷和⑦红磷互为同素异形体;结构相似相差n个CH2的有机物互为同系物,①2-甲基丁烷和②CH3- CH2- CH3,④CH3- Cl和⑧CH3CH2- Cl互为同系物;
(2)
①根据结构式可知甲中含氧官能团的名称为醛基和(醇)羟基;
②根据结构式可知只有-CH2OH中的C为饱和碳,故乙中饱和碳原子有1个;苯环上的C处于同一平面,与苯环直接相连的原子与苯环处于同一平面,故丙中一定在同一个平面上的碳原子有8个;
③分子式相同结构不同的有机物属于同分异构体,根据结构可知甲和丙分子式都是C8H8O2,结构不同互为同分异构体,故答案为甲和丙;
(3)
①根据题意,已知碳92.3%, 氢7.7%,化合物的摩尔质量为,,根据计算可知该物质的分子式为C8H8;A是芳香化合物,分子中所有的原子可能共平面,故A为苯乙烯;该分子具有5个不饱和度,B是具有两个支链的链状化合物,分子中只有两种不同化学环境的氢原子,B为非极性分子,故B为;C中碳原子全是sp3杂化,且化学环境完全相同,可知C为立方烷,氯的位置有边上两个顶点,面对角线两个顶点,和体对角线两个顶点,故C 的二氯代物有3中;
②A. A为苯乙烯,有碳碳双键,能使稀高锰酸钾溶液褪色,故A错误。
B. 苯乙烯有碳碳双键,可以发生加成聚合反应,故B正确;
C.A和苯的结构不相似,不属于苯的同系物,故C错误;
D.A为苯乙烯,苯环与氢气加成需要3mol碳碳双键加成需要1mol故,1molA可以与4molH2发生加成反应,故D正确。
故答案为BD
试卷第2页,共2页
试卷第1页,共1页
