全方位教学辅导教案第九单元 课题1、2上课教案与同步练习
文档属性
| 名称 | 全方位教学辅导教案第九单元 课题1、2上课教案与同步练习 |

|
|
| 格式 | zip | ||
| 文件大小 | 179.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-02-09 00:00:00 | ||
图片预览




文档简介
全方位教学辅导教案
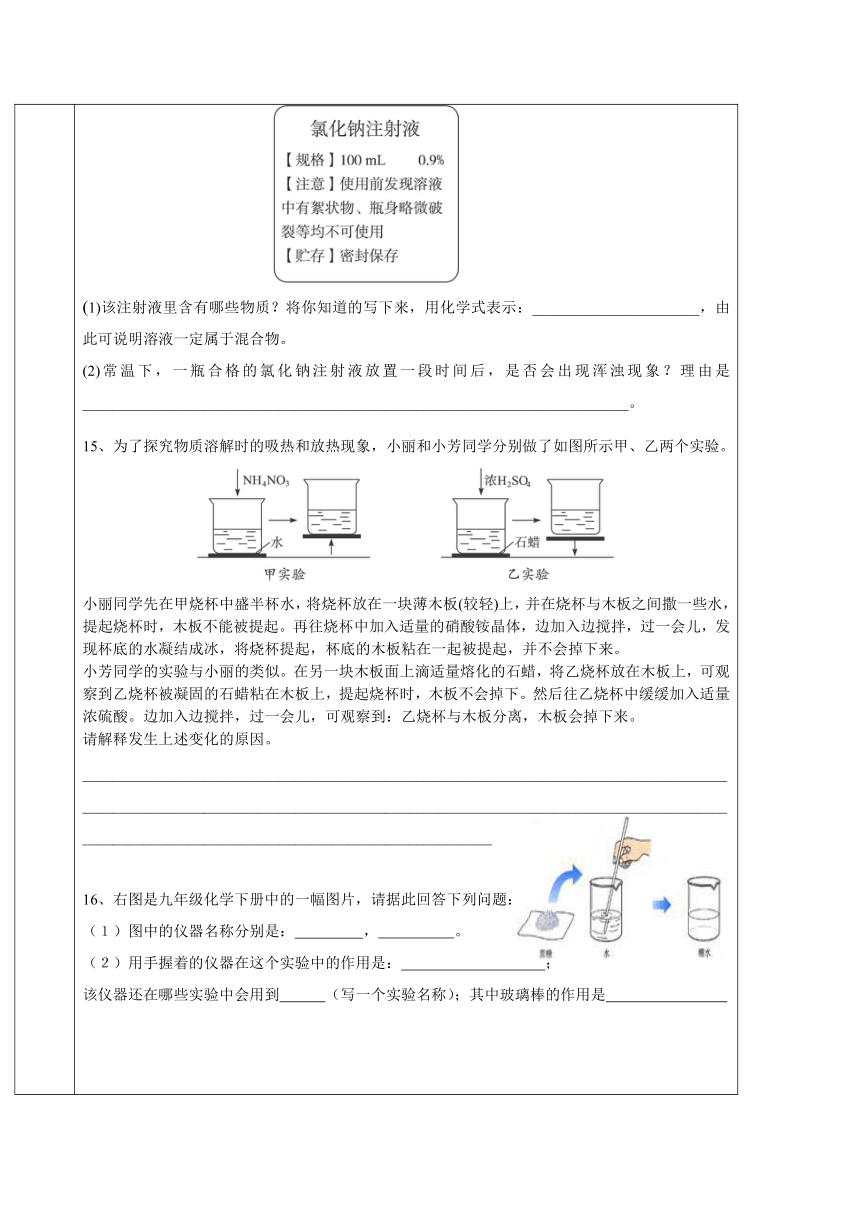
学科:化学 任课教师:黄贵鑫 授课时间: 年 月 日 星期: 档案号 :
姓 名 性 别 年 级 初三 第 次课
教 学内 容 第九单元 溶液的形成和溶解度
重 点难 点 饱和溶液和溶解度的含义; 从溶解度曲线中找到相关信息进行计算溶质质量分数的简单计算;配制一定溶质质量分数的溶液误差分析
教 学目 标 1、能正确描述溶液的组成,理解溶液和溶质、溶剂的概念,明确它们的关系,认识溶液对于化学反应的重要意义。2、正确理解与掌握饱和溶液、不饱和溶液的概念,知道它们在一定的条件下是可以相互转化的。3、记住溶解性和溶解度的概念,明确它们的关系。4、认识固体物质溶解度曲线。5、正确描述温度对固体溶解度的影响规律,并会简单的应用。
教学过程 课前检查与交流 作业完成情况:交流 与 沟通:
课题1 溶液的形成一、溶液的形成1、溶液(1)溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液(2)溶液的基本特征: 性、 性, 物(填“混合”或“纯净”)________:指溶液各部分的性质、组成、浓度完全相同,外观表现为透明、澄清、颜色一致。________:指当外界条件不变时(指溶剂量不变,温度(或压强)不改变)溶液中溶质不论放置多久,溶质与溶剂都不会分层,也不会有溶质析出,即不会发生变化)注意:a、溶液的质量 = 的质量 + 的质量溶质的质量是指溶解在溶剂里的那部分溶质的质量(未溶解的不能计算在内) 溶液的体积 ≠ 溶质的体积 + 溶剂的体积b、溶液不一定无色,CuSO4 色(Cu2+) FeSO4 色(Fe2+) Fe2(SO4)3 色(Fe3+) KMnO4 色(MnO4 ——)c、溶液里溶质可以是一种、两种或多种,而溶剂只能有一种。溶质可以是固体、液体或气体;水是最常用的溶剂 d、溶液的名称:溶质的溶剂溶液(溶质在前,溶剂在后)如:碘酒——碘的酒精溶液2、溶质和溶剂溶剂:能溶解其他物质的物质。常见的溶剂除水外,还有 、 等。溶质:被溶解的物质。固体、气体溶于液体,液体为溶剂溶质和溶剂的判断 有水,水为溶剂 液体溶于液体 无水,量多的为溶剂①结晶水合物溶解于水,其溶质是不含水的化合物,结晶水是溶剂。如:胆矾CuSO4·5H2O溶于水,溶质是CuSO4 ②物质溶于水,如果和水发生反应,溶质就是反应后生成的物质。如:将SO3通入水中,发生反应:SO3 + H2O==H2SO4 ,溶质是H2SO43、物质的溶解性知识回顾:碘几乎不溶于水,却可以溶解在汽油中,高锰酸钾几乎不溶于汽油,却可以溶解在水中水和乙醇可以互溶生活常识:白糖在热水中溶解的量比在等质量的冷水中溶解的量多影响物质溶解能力的因素:溶质的种类(性质)、溶剂的种类、温度影响溶解速率的因素:接触面积(块状、粉末状)、温度(高低)、搅拌(用玻璃棒搅拌,可加快溶解的速率)4、溶解时放热、吸热现象溶解吸热:如NH4Cl、 溶解 溶解放热:如固体NaOH、KOH溶解,浓H2SO4稀释、CaO溶解溶解没有明显热现象(即温度基本不变):如 溶解5、乳浊液和悬浊液(1)乳浊液:小液滴分散到液体里形成的混合物叫乳浊液。(必须是两种互不相溶的液体相混合而成) 例:将植物油滴入水中振荡,由于油是不溶于水的,故在水中悬浮着液体植物油,此混合物称乳浊液。(如往刚炒完菜的锅里放水,水中会出现细小的油滴)特点:不均一、不稳定、静置后液体分层如:牛奶(刚挤出来的牛奶静置后会分层,它是一种乳浊液,我们实际接触到的都是加工过的)(2)生活中常见的乳化剂:肥皂、洗洁精,(乳化剂有乳化功能)乳化功能:洗涤剂有乳化功能,它能使油脂分散成 无数细小的液滴 ,而不聚集成大的油珠这些细小的液滴能随着水流动。乳化是使微溶性的液体以微小液滴分散于溶剂中,形成乳浊液。石油原油、橡胶的乳胶、油漆等都是乳浊液。示例:洗洁精清洗油污利用的是乳化作用,使之形成较稳定的乳浊液,液体不再分层。而汽油清洗油污是将油污溶解于其中,形成溶液。生活中常见的乳化现象:肥皂漂洗衣服、洗洁精洗碗筷、农药等,此外,乳化剂还应用于食品行业:制作冰淇淋,巧克力、口香糖。。。(3)悬浊液:不溶于水的固体小颗粒分散到液体里形成的不稳定混合物。特点:不均匀、不稳定、静置后,其中的固体小颗粒会沉降如:泥水、氢氧化钙的悬浊液、黄河水、豆浆(真正的豆浆是用豆子打碎混在水里的,里面会混有细小的豆渣,固体不溶物,因此属于悬浊液)补充:溶液的特点:均一性、稳定性、静置后不沉淀、不分层 如:糖水、碘酒、食盐水课堂训练1、在①碘酒 ②糖水 ③70%的酒精 ④稀硫酸等几种溶液中,溶剂是同一种物质的是( )A.①③ B.② C.①②③ D.②③④2、下列有关溶液的说法,正确的是( )A.溶液通常是液体,溶质一定是固体 B.凡是溶液一定是混合物 C.一种物质分散到另一种物质中,形成的液体是溶液 D.无色透明的液体是溶液3、下列物质中属于溶液的是( )A.石灰水 B.液氧 C.牛奶 D.冰水4、下列清洗方法中,利用乳化作用的是( )A、用自来水洗手 B、用汽油清洗油污 C、用洗涤剂清洗油腻的餐具 D、用盐酸清除铁锈5、下列物质中,不属于溶液的是 ( )A.泥水 B.硬水 C.矿泉水 D.生理盐水6、下列各种应用中,不属于溶液应用的是( )A.医院里使用消毒酒精对皮肤消毒 B.熟石灰粉配制成喷涂墙壁的涂料C.马拉松运动员运动途中喝葡萄糖水来补充能量 D.如果皮肤上生了疖子,可用碘酒涂抹患处 7、各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂不具有乳化功能的是( )A.用汽油除去衣服上的油污 B.用餐具洗洁精清洗餐具上的油污C.用肥皂液洗衣 D.用沐浴露洗澡8、取A g食盐固体溶于水,得到食盐溶液200 mL。从食盐溶液中取出10 mL,则对于这部分溶液的描述不正确的是( )A.该溶液中含有的食盐的质量为Ag/20 B.该溶液的密度比原溶液的大C.该溶液的密度与原溶液相同 D.该溶液与原溶液一样咸 9、下列物质属于溶液的是( )A.石灰浆 B.生理盐水 C.菜汤 D.牛奶10、夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种化学试剂放入一定量的水中,就可以形成低温的小环境,这种试剂可以是下列物质中的( )A.食盐 B. 熟石灰 C.蔗糖 D. 硝酸铵11、如右图所示,向盛水的试管中加入少量氢氧化钠固体,U形管内有色液面将发生( ) A.无变化 B.A处升高,B处下降C.A、B两处都升高 D.A处降低,B处升高12、在以下空白中填写有关编号。A、溶液 B、悬浊液 C、乳浊液将味精溶于水中得到____________,粉笔末放入水中搅浑得到____________,将水放在油锅里用力涮洗得到____________,粉刷墙壁的石灰搅拌后得到____________,石灰浆静置后上面的澄清透明的液体是____________,其中溶质是____________。13、写出下列溶液中溶剂的名称。 碘酒 白磷的二硫化碳溶液 14、病人在医院接受静脉注射或滴注时,常要用到生理盐水,即氯化钠溶液。右图是某药业公司生产的氯化钠注射液包装标签上的部分文字。请完成下列问题:(1)该注射液里含有哪些物质?将你知道的写下来,用化学式表示:______________________,由此可说明溶液一定属于混合物。(2)常温下,一瓶合格的氯化钠注射液放置一段时间后,是否会出现浑浊现象?理由是________________________________________________________________________。15、为了探究物质溶解时的吸热和放热现象,小丽和小芳同学分别做了如图所示甲、乙两个实验。小丽同学先在甲烧杯中盛半杯水,将烧杯放在一块薄木板(较轻)上,并在烧杯与木板之间撒一些水,提起烧杯时,木板不能被提起。再往烧杯中加入适量的硝酸铵晶体,边加入边搅拌,过一会儿,发现杯底的水凝结成冰,将烧杯提起,杯底的木板粘在一起被提起,并不会掉下来。小芳同学的实验与小丽的类似。在另一块木板面上滴适量熔化的石蜡,将乙烧杯放在木板上,可观察到乙烧杯被凝固的石蜡粘在木板上,提起烧杯时,木板不会掉下。然后往乙烧杯中缓缓加入适量浓硫酸。边加入边搅拌,过一会儿,可观察到:乙烧杯与木板分离,木板会掉下来。请解释发生上述变化的原因。________________________________________________________________________________________________________________________________________________________________________________________________________________________________16、右图是九年级化学下册中的一幅图片,请据此回答下列问题: (1)图中的仪器名称分别是: , 。(2)用手握着的仪器在这个实验中的作用是: ;该仪器还在哪些实验中会用到 (写一个实验名称);其中玻璃棒的作用是 课题2 溶 解 度1、饱和溶液、不饱和溶液 (1)概念:饱和溶液和不饱和溶液饱和溶液: ,向一定量的 里加入某种 溶质 ,当 溶质不能继续溶解 时,所得的溶液叫做这种 溶质 的饱和溶液。(特点:在一定温度、一定量的溶剂中,溶质不能无限溶解的溶液)。不饱和溶液:在一定温度下 ,向一定量的 溶剂 里加入某种 溶 质, 溶质能继续溶解 的溶液,叫做不饱和溶液。(特点:在一定温度、一定量的溶剂中,溶质可以继续溶解的溶液。)明确“某种溶质”的饱和溶液或不饱和溶液的含义:如: 一定条件下,不能再溶解NaCl的溶液,可继续溶解蔗糖,此时的溶液是NaCl的饱和溶液,但对于蔗糖来说,就是不饱和溶液。(2)判断溶液是否饱和的方法:看溶液中是否有不能继续溶解的剩余溶质存在或继续加入该溶质,看能否溶解(3)饱和溶液和不饱和溶液之间的转化 相互转化:不饱和溶液 饱和溶液注:以上转换关系适用于溶解度随温度升高而增大的物质注:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低 ②增加溶质、蒸发溶剂一定能使不饱和溶液变成饱和溶液 ③增加溶剂一定能使饱和溶液变为不饱和溶液示例:对于有剩余KNO3固体的KNO3饱和溶液,要使剩余固体继续溶解,可采用_________或_____________的方法 NaCl溶液由不饱和变为饱和一般可采用:蒸发溶剂至刚好有晶体析出或____________________(4)浓、稀溶液与饱和不饱和溶液之间的关系概念:一定量溶液中,含溶质的质量相对较多的叫浓溶液一定量溶液中,含溶质的质量相对较少的叫稀溶液①饱和溶液不一定是浓溶液,如饱和的石灰水溶液就是稀溶液(澄清石灰水)②不饱和溶液不一定是稀溶液(如20℃时往100克水里加入180克糖,这时糖水的浓度已不算稀了,但是仍未达到饱和状态,实际其溶解度是204克)③在一定温度时,同一种溶质的饱和溶液一定要比它的不饱和溶液浓2、固体的溶解度 (常用符号 S 表示)(1)溶解度定义:在 下,某 物质在 里达到饱和状态时所溶解的 四要素:①条件:一定温度下 ②标准:100g溶剂 ③状态:达到饱和 ④质量:单位:克(2)溶解度的含义: 20℃时NaCl的溶液度为36g含义:在20℃时,在100克水中最多能溶解36克NaCl或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克(3) 溶解性和溶解度的关系:物质的溶解度:<0.01g 该物质叫难溶(常把“难溶”称为“不溶”,绝对不溶的物质是不存在的)物质的溶解度:0.01克~~1g该物质叫微溶物质的溶解度:1g~~10g 该物质叫可溶 物质的溶解度:>10g 该物质叫易溶(4)影响固体溶解度的因素:①溶质、溶剂的性质(种类)20℃时硝酸钾的溶解度是31.6g,氯化钠的溶解度36g,造成此差异的原因是这两种溶质的性质不同,而碘在水和汽油中的溶解度相差很大,这是溶剂的性质不同。 大多数固体物质的溶解度随温度升高而升高;如 ②温度 少数固体物质的溶解度受温度的影响很小;如 极少数物质溶解度随温度升高而降低。如 (5)溶解度曲线 概念:表示物质的 随 的曲线。 曲线上的点:表示物质在该点所示温度下的 。 点 两曲线的交点:表示两物质在该点所示温度下的 。 意义 线:表示同一种物质在不同 下的 或表示 随 而变化的趋势。 面 曲线下面所表示的溶液为 。 曲线上面(包括曲线)所表示的溶液为 。 3、混合物的分离(1)过滤法:分离可溶物 + 难溶物 (2)结晶法:分离几种可溶性物质结晶的概念:热的溶液冷却或溶剂的量减少后,已溶解在溶液中的溶质从溶液中以晶体的形式析出,这一过程叫做结晶。结晶的两种方法 蒸发结晶: 溶剂,如NaCl(海水晒盐)降温结晶:降低温度(冷却热的饱和溶液,如KNO3)蒸发结晶适用于溶解度受温度影响变化不大的溶质,比如NaCl、KCl等。因为溶解度变化小,所以不论冷热都溶解度变化不大,只有通过(加热蒸发)减少溶剂(水)才能使其析出结晶。 降温结晶适用于溶解度受温度影响变化较大而且是随温度降低而降低的溶质(如NaNO3、KNO3)或者是 溶解度受温度影响变化较大而且是随温度升高而升高的溶质降温结晶通常前面还有个过程——蒸发浓缩例:如图,回答相关问题: 例: (1)t3℃时A的溶解度为 (2)P点的的含义 C (3)N点为 ,可通过 加入A物质, , 的方法使它变为饱和。 (4)t1℃时A、B、C、溶解度由大到小的顺序 (5)从A溶液中获取A晶体可用 的方法获取晶体。 (6)从B溶液中获取B晶体可用 的方法获取晶体。(7)t2℃ 时A、B、C的饱和溶液各W克,降温到t1℃会析出晶体的有 和 无晶体析出的有 ,所得溶液中溶质的质量分数由小到大依次为 。 (8)除去A中的泥沙用 法;分离A与B(含量少)的混合物,用 法4、气体的溶解度 (1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。 (2)影响因素: ①气体和水的性质 ②温度(温度越高,气体溶解度越 )③压强(压强越大,气体溶解度越 )课堂训练1.下列说法中,正确的是( )A.任何一种固体物质在水中的溶解度都是一定的,只有一个值B.固体溶质的溶解度随温度的升高而增大,气体溶质的溶解度随温度升高而减小C.某物质的溶解度就是该物质在100 g溶剂中所溶解的克数D.在一定温度下,溶质A的溶解度为SAg,溶质B的溶解度为SBg。已知SA>SB,相同质量的A和B的饱和溶液,A溶液的溶剂量小于B溶液里的溶剂量2. 如果用S表示某物质20 ℃时的溶解度,那么下列式子表示微溶的是( )A.S>10 g B.S>0.01 g C. 0.01 gX>ZC.t℃时,X、Y、Z的饱和溶液中,溶质的质量分数相等D.当X中含有少量Z时,可通过降温结晶来提纯X12、右图是M、N两种物质的溶解度曲线,在t2℃时往盛有100g水的烧杯中先后加入a g M和a g N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌。将混合物的温度降低到t1℃,下列说法正确的是( )A、t2℃时,得到M的饱和溶液 B、t2℃时,得到N的不饱和溶液C、温度降低到t1℃时,M、N的溶质质量分数相等,得到M、N的不饱和溶液D、温度降低到t1℃时,M、N的溶解度相等,得到M、N的饱和溶液13、下图是a,b,c三种固体物质的溶解度曲线。下列说法不正确的是( )A.在℃时,a的溶解度等于b的溶解度B.在℃时,a、c饱和溶液中溶质的质量分数相同C.当a中含有少量b时,可以用降温结晶的方法提纯aD.c的饱和溶液由℃升温至℃时,变成不饱和溶液14、根据下图的溶解度曲线判断,下列说法正确的是( )A. 与B相比,A的溶解度受温度影响不大B. 在时,B的溶解度大于A的溶解度C. 将时,A和B的饱和溶液的温度降低,都没有溶质晶体析出D. 在时,A和B的溶解度相等15、小巍同学通过实验绘制的两种固体物质的溶解度曲线如下图所示: (1)30℃时,甲物质的溶解度是_________(2)从右图中还可获得的信息是(至少答出两条) 16、家庭饲养金鱼,常常向鱼缸里通入空气,目的是 天气闷热时,鱼塘里的鱼会接近水面游动的原因是 。17、10℃时,在两个烧杯中分别盛有相同质量的硝酸钾和氯化钾饱和溶液;保持溶液温度不变,分别向其中加入等质量的相应溶质;再将温度升高到40℃,氯化钾和硝酸钾的溶解情况如图A所示。图B为两种物质的溶解度曲线。请仔细观察、分析图A和图B,回答下列问题: (1)当温度t的取值范围为 时,硝酸钾的溶解度大于氯化钾的溶解度。(2)烧杯甲盛放的是_________溶液。 (3)状态三时,烧杯_______中溶剂水的质量相对较小。(4)当温度由20℃升高至60℃时(不考虑水分蒸发),B烧杯中溶液质量不断增加,则B烧杯溶液中的溶质是 (填“甲”或“乙”)。图1 图2
签字 教研组长: 教学主任: 学生: 教务老师: 家长:
老师课后评价 下节课的计划:
学生的状况、接受情况和配合程度:
给家长的建议:
课题1、2 溶液的形成和溶解度
一1、(2)均一,稳定 混合 均一性,稳定性
蓝,浅绿,黄,紫;溶质,溶剂
2、酒精、汽油 4、NH4NO3 、NaCl溶解
巩固练习 :1-5 DBACA 6—10 BABBD菜汤中含有一定量的油脂11、D 12、A、B、C、B、A 氢氧化钙
13、酒精、二硫化碳 14、(1)NaCl、H2O (2)不会 因为溶液是均一、稳定的
15、甲烧杯中加入硝酸铵晶体,溶于水时吸收热量,使溶液的温度降到0℃以下,木板上的水结冰,从而使烧杯与木块粘在一起;乙烧杯中加入适量浓硫酸,溶于水时放出热量,使粘在木板与烧杯之间的石蜡熔化,使烧杯与木块分离。
16、(1)玻璃棒、烧杯 (2)搅拌,加快溶解;过滤;引流
课题2:
1、(1)在一定温度下,溶剂 (3)降低温度,增加溶质,蒸发溶剂 ;升高温度,增加溶剂
加水、升高温度 加入氯化钠固体至不再溶解
2、(1)一定温度下,固态,100g溶剂,质量
(4)KNO3, NaCl, Ca(OH)2
(5)溶解度,温度的变化;溶解度,溶解度相等;温度,溶解度,溶解度,温度改变;
在相应温度下的不饱和溶液,在相应温度下的饱和溶液
3、蒸发
例:(1)80g,(2)在P点温度 下,A,B的溶解度相同(3)在t30C时,A点的不饱和溶液,降温,蒸发溶剂
(4)C〉B〉A (5)降温结晶 (6)蒸发结晶 (7)A,B,C,A(T3时B的溶解度几乎是A的两倍,虽然由于降温析出晶体,但变化不大)
4、小,大
巩固练习2:1-6 DCDDDC
7(1)等于250C (1)小于250C (3)不饱和 (4)20 g
8. (1)√(2)×(3)×(4)×
9. 氧化钙 浓硫酸 氢氧化钠等
10. 40 g
11-14 DCDD
15(1)30g 甲物质的溶解质受温度的影响比乙大;150C时,甲乙两物质的溶解度相等;
t < 150C 时,乙物质的溶解度大于甲物质的溶解质……
16、(1)增加水中氧气的溶解量,给鱼供给充足的氧气
(2)氧气的溶解度随着温度的升高逐渐减小,天气闷热时,水中溶解的氧气量相对较少,水面与空气接触,溶解的氧气较多,所以鱼会接近水面游动
17、大于220C ;硝酸钾,乙、乙
分析:10摄氏度时,氯化钾的溶解度比硝酸钾高 等质量的饱和溶液 氯化钾溶液的溶质较多 溶剂较少
硝酸钾溶液的溶质较少 溶剂较多 甲是硝酸钾 乙是氯化钾
( )、( )、( )
( )、( )
80g
0
t1
t2
t3
N
t
S
P
·
A
·
B
·
C
学科:化学 任课教师:黄贵鑫 授课时间: 年 月 日 星期: 档案号 :
姓 名 性 别 年 级 初三 第 次课
教 学内 容 第九单元 溶液的形成和溶解度
重 点难 点 饱和溶液和溶解度的含义; 从溶解度曲线中找到相关信息进行计算溶质质量分数的简单计算;配制一定溶质质量分数的溶液误差分析
教 学目 标 1、能正确描述溶液的组成,理解溶液和溶质、溶剂的概念,明确它们的关系,认识溶液对于化学反应的重要意义。2、正确理解与掌握饱和溶液、不饱和溶液的概念,知道它们在一定的条件下是可以相互转化的。3、记住溶解性和溶解度的概念,明确它们的关系。4、认识固体物质溶解度曲线。5、正确描述温度对固体溶解度的影响规律,并会简单的应用。
教学过程 课前检查与交流 作业完成情况:交流 与 沟通:
课题1 溶液的形成一、溶液的形成1、溶液(1)溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液(2)溶液的基本特征: 性、 性, 物(填“混合”或“纯净”)________:指溶液各部分的性质、组成、浓度完全相同,外观表现为透明、澄清、颜色一致。________:指当外界条件不变时(指溶剂量不变,温度(或压强)不改变)溶液中溶质不论放置多久,溶质与溶剂都不会分层,也不会有溶质析出,即不会发生变化)注意:a、溶液的质量 = 的质量 + 的质量溶质的质量是指溶解在溶剂里的那部分溶质的质量(未溶解的不能计算在内) 溶液的体积 ≠ 溶质的体积 + 溶剂的体积b、溶液不一定无色,CuSO4 色(Cu2+) FeSO4 色(Fe2+) Fe2(SO4)3 色(Fe3+) KMnO4 色(MnO4 ——)c、溶液里溶质可以是一种、两种或多种,而溶剂只能有一种。溶质可以是固体、液体或气体;水是最常用的溶剂 d、溶液的名称:溶质的溶剂溶液(溶质在前,溶剂在后)如:碘酒——碘的酒精溶液2、溶质和溶剂溶剂:能溶解其他物质的物质。常见的溶剂除水外,还有 、 等。溶质:被溶解的物质。固体、气体溶于液体,液体为溶剂溶质和溶剂的判断 有水,水为溶剂 液体溶于液体 无水,量多的为溶剂①结晶水合物溶解于水,其溶质是不含水的化合物,结晶水是溶剂。如:胆矾CuSO4·5H2O溶于水,溶质是CuSO4 ②物质溶于水,如果和水发生反应,溶质就是反应后生成的物质。如:将SO3通入水中,发生反应:SO3 + H2O==H2SO4 ,溶质是H2SO43、物质的溶解性知识回顾:碘几乎不溶于水,却可以溶解在汽油中,高锰酸钾几乎不溶于汽油,却可以溶解在水中水和乙醇可以互溶生活常识:白糖在热水中溶解的量比在等质量的冷水中溶解的量多影响物质溶解能力的因素:溶质的种类(性质)、溶剂的种类、温度影响溶解速率的因素:接触面积(块状、粉末状)、温度(高低)、搅拌(用玻璃棒搅拌,可加快溶解的速率)4、溶解时放热、吸热现象溶解吸热:如NH4Cl、 溶解 溶解放热:如固体NaOH、KOH溶解,浓H2SO4稀释、CaO溶解溶解没有明显热现象(即温度基本不变):如 溶解5、乳浊液和悬浊液(1)乳浊液:小液滴分散到液体里形成的混合物叫乳浊液。(必须是两种互不相溶的液体相混合而成) 例:将植物油滴入水中振荡,由于油是不溶于水的,故在水中悬浮着液体植物油,此混合物称乳浊液。(如往刚炒完菜的锅里放水,水中会出现细小的油滴)特点:不均一、不稳定、静置后液体分层如:牛奶(刚挤出来的牛奶静置后会分层,它是一种乳浊液,我们实际接触到的都是加工过的)(2)生活中常见的乳化剂:肥皂、洗洁精,(乳化剂有乳化功能)乳化功能:洗涤剂有乳化功能,它能使油脂分散成 无数细小的液滴 ,而不聚集成大的油珠这些细小的液滴能随着水流动。乳化是使微溶性的液体以微小液滴分散于溶剂中,形成乳浊液。石油原油、橡胶的乳胶、油漆等都是乳浊液。示例:洗洁精清洗油污利用的是乳化作用,使之形成较稳定的乳浊液,液体不再分层。而汽油清洗油污是将油污溶解于其中,形成溶液。生活中常见的乳化现象:肥皂漂洗衣服、洗洁精洗碗筷、农药等,此外,乳化剂还应用于食品行业:制作冰淇淋,巧克力、口香糖。。。(3)悬浊液:不溶于水的固体小颗粒分散到液体里形成的不稳定混合物。特点:不均匀、不稳定、静置后,其中的固体小颗粒会沉降如:泥水、氢氧化钙的悬浊液、黄河水、豆浆(真正的豆浆是用豆子打碎混在水里的,里面会混有细小的豆渣,固体不溶物,因此属于悬浊液)补充:溶液的特点:均一性、稳定性、静置后不沉淀、不分层 如:糖水、碘酒、食盐水课堂训练1、在①碘酒 ②糖水 ③70%的酒精 ④稀硫酸等几种溶液中,溶剂是同一种物质的是( )A.①③ B.② C.①②③ D.②③④2、下列有关溶液的说法,正确的是( )A.溶液通常是液体,溶质一定是固体 B.凡是溶液一定是混合物 C.一种物质分散到另一种物质中,形成的液体是溶液 D.无色透明的液体是溶液3、下列物质中属于溶液的是( )A.石灰水 B.液氧 C.牛奶 D.冰水4、下列清洗方法中,利用乳化作用的是( )A、用自来水洗手 B、用汽油清洗油污 C、用洗涤剂清洗油腻的餐具 D、用盐酸清除铁锈5、下列物质中,不属于溶液的是 ( )A.泥水 B.硬水 C.矿泉水 D.生理盐水6、下列各种应用中,不属于溶液应用的是( )A.医院里使用消毒酒精对皮肤消毒 B.熟石灰粉配制成喷涂墙壁的涂料C.马拉松运动员运动途中喝葡萄糖水来补充能量 D.如果皮肤上生了疖子,可用碘酒涂抹患处 7、各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂不具有乳化功能的是( )A.用汽油除去衣服上的油污 B.用餐具洗洁精清洗餐具上的油污C.用肥皂液洗衣 D.用沐浴露洗澡8、取A g食盐固体溶于水,得到食盐溶液200 mL。从食盐溶液中取出10 mL,则对于这部分溶液的描述不正确的是( )A.该溶液中含有的食盐的质量为Ag/20 B.该溶液的密度比原溶液的大C.该溶液的密度与原溶液相同 D.该溶液与原溶液一样咸 9、下列物质属于溶液的是( )A.石灰浆 B.生理盐水 C.菜汤 D.牛奶10、夏日里想随时喝到凉爽的饮料,可以自制化学“冰箱”,即把一种化学试剂放入一定量的水中,就可以形成低温的小环境,这种试剂可以是下列物质中的( )A.食盐 B. 熟石灰 C.蔗糖 D. 硝酸铵11、如右图所示,向盛水的试管中加入少量氢氧化钠固体,U形管内有色液面将发生( ) A.无变化 B.A处升高,B处下降C.A、B两处都升高 D.A处降低,B处升高12、在以下空白中填写有关编号。A、溶液 B、悬浊液 C、乳浊液将味精溶于水中得到____________,粉笔末放入水中搅浑得到____________,将水放在油锅里用力涮洗得到____________,粉刷墙壁的石灰搅拌后得到____________,石灰浆静置后上面的澄清透明的液体是____________,其中溶质是____________。13、写出下列溶液中溶剂的名称。 碘酒 白磷的二硫化碳溶液 14、病人在医院接受静脉注射或滴注时,常要用到生理盐水,即氯化钠溶液。右图是某药业公司生产的氯化钠注射液包装标签上的部分文字。请完成下列问题:(1)该注射液里含有哪些物质?将你知道的写下来,用化学式表示:______________________,由此可说明溶液一定属于混合物。(2)常温下,一瓶合格的氯化钠注射液放置一段时间后,是否会出现浑浊现象?理由是________________________________________________________________________。15、为了探究物质溶解时的吸热和放热现象,小丽和小芳同学分别做了如图所示甲、乙两个实验。小丽同学先在甲烧杯中盛半杯水,将烧杯放在一块薄木板(较轻)上,并在烧杯与木板之间撒一些水,提起烧杯时,木板不能被提起。再往烧杯中加入适量的硝酸铵晶体,边加入边搅拌,过一会儿,发现杯底的水凝结成冰,将烧杯提起,杯底的木板粘在一起被提起,并不会掉下来。小芳同学的实验与小丽的类似。在另一块木板面上滴适量熔化的石蜡,将乙烧杯放在木板上,可观察到乙烧杯被凝固的石蜡粘在木板上,提起烧杯时,木板不会掉下。然后往乙烧杯中缓缓加入适量浓硫酸。边加入边搅拌,过一会儿,可观察到:乙烧杯与木板分离,木板会掉下来。请解释发生上述变化的原因。________________________________________________________________________________________________________________________________________________________________________________________________________________________________16、右图是九年级化学下册中的一幅图片,请据此回答下列问题: (1)图中的仪器名称分别是: , 。(2)用手握着的仪器在这个实验中的作用是: ;该仪器还在哪些实验中会用到 (写一个实验名称);其中玻璃棒的作用是 课题2 溶 解 度1、饱和溶液、不饱和溶液 (1)概念:饱和溶液和不饱和溶液饱和溶液: ,向一定量的 里加入某种 溶质 ,当 溶质不能继续溶解 时,所得的溶液叫做这种 溶质 的饱和溶液。(特点:在一定温度、一定量的溶剂中,溶质不能无限溶解的溶液)。不饱和溶液:在一定温度下 ,向一定量的 溶剂 里加入某种 溶 质, 溶质能继续溶解 的溶液,叫做不饱和溶液。(特点:在一定温度、一定量的溶剂中,溶质可以继续溶解的溶液。)明确“某种溶质”的饱和溶液或不饱和溶液的含义:如: 一定条件下,不能再溶解NaCl的溶液,可继续溶解蔗糖,此时的溶液是NaCl的饱和溶液,但对于蔗糖来说,就是不饱和溶液。(2)判断溶液是否饱和的方法:看溶液中是否有不能继续溶解的剩余溶质存在或继续加入该溶质,看能否溶解(3)饱和溶液和不饱和溶液之间的转化 相互转化:不饱和溶液 饱和溶液注:以上转换关系适用于溶解度随温度升高而增大的物质注:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低 ②增加溶质、蒸发溶剂一定能使不饱和溶液变成饱和溶液 ③增加溶剂一定能使饱和溶液变为不饱和溶液示例:对于有剩余KNO3固体的KNO3饱和溶液,要使剩余固体继续溶解,可采用_________或_____________的方法 NaCl溶液由不饱和变为饱和一般可采用:蒸发溶剂至刚好有晶体析出或____________________(4)浓、稀溶液与饱和不饱和溶液之间的关系概念:一定量溶液中,含溶质的质量相对较多的叫浓溶液一定量溶液中,含溶质的质量相对较少的叫稀溶液①饱和溶液不一定是浓溶液,如饱和的石灰水溶液就是稀溶液(澄清石灰水)②不饱和溶液不一定是稀溶液(如20℃时往100克水里加入180克糖,这时糖水的浓度已不算稀了,但是仍未达到饱和状态,实际其溶解度是204克)③在一定温度时,同一种溶质的饱和溶液一定要比它的不饱和溶液浓2、固体的溶解度 (常用符号 S 表示)(1)溶解度定义:在 下,某 物质在 里达到饱和状态时所溶解的 四要素:①条件:一定温度下 ②标准:100g溶剂 ③状态:达到饱和 ④质量:单位:克(2)溶解度的含义: 20℃时NaCl的溶液度为36g含义:在20℃时,在100克水中最多能溶解36克NaCl或在20℃时,NaCl在100克水中达到饱和状态时所溶解的质量为36克(3) 溶解性和溶解度的关系:物质的溶解度:<0.01g 该物质叫难溶(常把“难溶”称为“不溶”,绝对不溶的物质是不存在的)物质的溶解度:0.01克~~1g该物质叫微溶物质的溶解度:1g~~10g 该物质叫可溶 物质的溶解度:>10g 该物质叫易溶(4)影响固体溶解度的因素:①溶质、溶剂的性质(种类)20℃时硝酸钾的溶解度是31.6g,氯化钠的溶解度36g,造成此差异的原因是这两种溶质的性质不同,而碘在水和汽油中的溶解度相差很大,这是溶剂的性质不同。 大多数固体物质的溶解度随温度升高而升高;如 ②温度 少数固体物质的溶解度受温度的影响很小;如 极少数物质溶解度随温度升高而降低。如 (5)溶解度曲线 概念:表示物质的 随 的曲线。 曲线上的点:表示物质在该点所示温度下的 。 点 两曲线的交点:表示两物质在该点所示温度下的 。 意义 线:表示同一种物质在不同 下的 或表示 随 而变化的趋势。 面 曲线下面所表示的溶液为 。 曲线上面(包括曲线)所表示的溶液为 。 3、混合物的分离(1)过滤法:分离可溶物 + 难溶物 (2)结晶法:分离几种可溶性物质结晶的概念:热的溶液冷却或溶剂的量减少后,已溶解在溶液中的溶质从溶液中以晶体的形式析出,这一过程叫做结晶。结晶的两种方法 蒸发结晶: 溶剂,如NaCl(海水晒盐)降温结晶:降低温度(冷却热的饱和溶液,如KNO3)蒸发结晶适用于溶解度受温度影响变化不大的溶质,比如NaCl、KCl等。因为溶解度变化小,所以不论冷热都溶解度变化不大,只有通过(加热蒸发)减少溶剂(水)才能使其析出结晶。 降温结晶适用于溶解度受温度影响变化较大而且是随温度降低而降低的溶质(如NaNO3、KNO3)或者是 溶解度受温度影响变化较大而且是随温度升高而升高的溶质降温结晶通常前面还有个过程——蒸发浓缩例:如图,回答相关问题: 例: (1)t3℃时A的溶解度为 (2)P点的的含义 C (3)N点为 ,可通过 加入A物质, , 的方法使它变为饱和。 (4)t1℃时A、B、C、溶解度由大到小的顺序 (5)从A溶液中获取A晶体可用 的方法获取晶体。 (6)从B溶液中获取B晶体可用 的方法获取晶体。(7)t2℃ 时A、B、C的饱和溶液各W克,降温到t1℃会析出晶体的有 和 无晶体析出的有 ,所得溶液中溶质的质量分数由小到大依次为 。 (8)除去A中的泥沙用 法;分离A与B(含量少)的混合物,用 法4、气体的溶解度 (1)气体溶解度的定义:在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。 (2)影响因素: ①气体和水的性质 ②温度(温度越高,气体溶解度越 )③压强(压强越大,气体溶解度越 )课堂训练1.下列说法中,正确的是( )A.任何一种固体物质在水中的溶解度都是一定的,只有一个值B.固体溶质的溶解度随温度的升高而增大,气体溶质的溶解度随温度升高而减小C.某物质的溶解度就是该物质在100 g溶剂中所溶解的克数D.在一定温度下,溶质A的溶解度为SAg,溶质B的溶解度为SBg。已知SA>SB,相同质量的A和B的饱和溶液,A溶液的溶剂量小于B溶液里的溶剂量2. 如果用S表示某物质20 ℃时的溶解度,那么下列式子表示微溶的是( )A.S>10 g B.S>0.01 g C. 0.01 g
签字 教研组长: 教学主任: 学生: 教务老师: 家长:
老师课后评价 下节课的计划:
学生的状况、接受情况和配合程度:
给家长的建议:
课题1、2 溶液的形成和溶解度
一1、(2)均一,稳定 混合 均一性,稳定性
蓝,浅绿,黄,紫;溶质,溶剂
2、酒精、汽油 4、NH4NO3 、NaCl溶解
巩固练习 :1-5 DBACA 6—10 BABBD菜汤中含有一定量的油脂11、D 12、A、B、C、B、A 氢氧化钙
13、酒精、二硫化碳 14、(1)NaCl、H2O (2)不会 因为溶液是均一、稳定的
15、甲烧杯中加入硝酸铵晶体,溶于水时吸收热量,使溶液的温度降到0℃以下,木板上的水结冰,从而使烧杯与木块粘在一起;乙烧杯中加入适量浓硫酸,溶于水时放出热量,使粘在木板与烧杯之间的石蜡熔化,使烧杯与木块分离。
16、(1)玻璃棒、烧杯 (2)搅拌,加快溶解;过滤;引流
课题2:
1、(1)在一定温度下,溶剂 (3)降低温度,增加溶质,蒸发溶剂 ;升高温度,增加溶剂
加水、升高温度 加入氯化钠固体至不再溶解
2、(1)一定温度下,固态,100g溶剂,质量
(4)KNO3, NaCl, Ca(OH)2
(5)溶解度,温度的变化;溶解度,溶解度相等;温度,溶解度,溶解度,温度改变;
在相应温度下的不饱和溶液,在相应温度下的饱和溶液
3、蒸发
例:(1)80g,(2)在P点温度 下,A,B的溶解度相同(3)在t30C时,A点的不饱和溶液,降温,蒸发溶剂
(4)C〉B〉A (5)降温结晶 (6)蒸发结晶 (7)A,B,C,A
4、小,大
巩固练习2:1-6 DCDDDC
7(1)等于250C (1)小于250C (3)不饱和 (4)20 g
8. (1)√(2)×(3)×(4)×
9. 氧化钙 浓硫酸 氢氧化钠等
10. 40 g
11-14 DCDD
15(1)30g 甲物质的溶解质受温度的影响比乙大;150C时,甲乙两物质的溶解度相等;
t < 150C 时,乙物质的溶解度大于甲物质的溶解质……
16、(1)增加水中氧气的溶解量,给鱼供给充足的氧气
(2)氧气的溶解度随着温度的升高逐渐减小,天气闷热时,水中溶解的氧气量相对较少,水面与空气接触,溶解的氧气较多,所以鱼会接近水面游动
17、大于220C ;硝酸钾,乙、乙
分析:10摄氏度时,氯化钾的溶解度比硝酸钾高 等质量的饱和溶液 氯化钾溶液的溶质较多 溶剂较少
硝酸钾溶液的溶质较少 溶剂较多 甲是硝酸钾 乙是氯化钾
( )、( )、( )
( )、( )
80g
0
t1
t2
t3
N
t
S
P
·
A
·
B
·
C
同课章节目录
