课题1 生活中常见的盐第1课时-九年级化学下册系列教学课件(15页)(人教版)
文档属性
| 名称 | 课题1 生活中常见的盐第1课时-九年级化学下册系列教学课件(15页)(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 54.6MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-05 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
课题1.生活中常见的盐
第1课时
第十一单元
01
02
03
了解盐和生活中常见的食盐的区别。
知道氯化钠的性质和用途。
了解粗盐提纯的操作方法和注意事项。
教学目标
引入新课
温故知新:
食盐是盐,盐就是食盐”这句话对吗
日常生活中所说的盐,通常指食盐(主要成分是NaCl);
而化学中的盐不仅仅指食盐(如亚硝酸钠也属于盐,有毒不能食用)。
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
酸→H+ + 酸根离子
碱→金属离子+ OH-
盐→金属离子(或铵根离子)+酸根离子
酸:HCl H2SO4
碱:NaOH Ca(OH)2
盐:CaCO3 Na2CO3
新知探究
指出下列物质中哪些是酸 哪些是碱 哪些是盐
一、盐
新知探究
一、盐
根据盐的组成里所含的阳离子和阴离子,可将盐进行分类并称为“某盐”。
如:含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根
离子的盐称为铵盐。
盐分类:
盐的分类和命名
盐的命名:
根据盐中的酸根离子是否含有氧元素,可以把盐分为含氧酸盐和无氧酸盐。
含氧酸盐称为“某酸某”,如:K2CO3、MgSO4。
无氧酸盐称为“某化某”,如:KCI、NaCI。
新知探究
一、盐
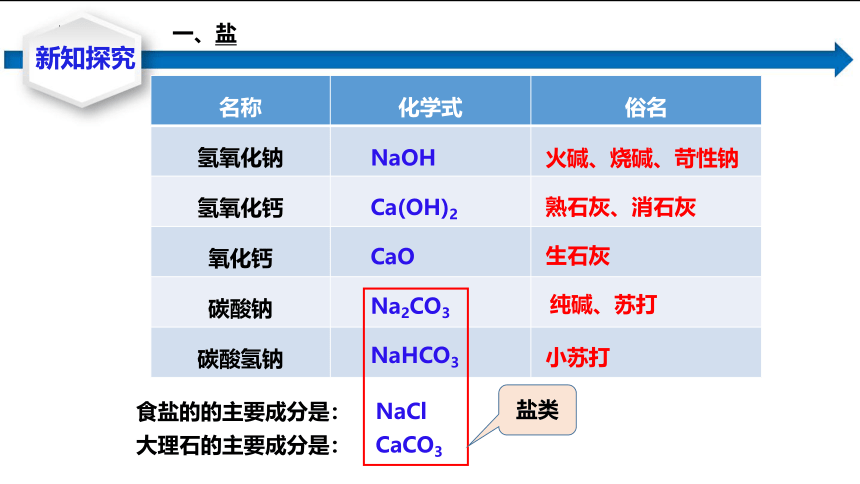
名称 化学式 俗名
氢氧化钠
氢氧化钙
氧化钙
碳酸钠
碳酸氢钠
NaOH
火碱、烧碱、苛性钠
Ca(OH)2
熟石灰、消石灰
CaO
Na2CO3
NaHCO3
生石灰
纯碱、苏打
小苏打
食盐的的主要成分是: NaCl
大理石的主要成分是: CaCO3
盐类
A
B
C
D
盐水消除积雪
腌制
食物
盐水
选种
生理
盐水
新知探究
二、氯化钠
生活重要的调味品
新知探究
二、氯化钠
盐湖、盐井、盐矿、海水中都蕴藏着氯化钠。
盐湖
盐井
盐矿
海水
巩固提升
氯化钠与人体健康
钠离子对维持细胞内外正常的水分分布和促进细胞内外物质交换起主要作用;
氯离子是胃液中的主要成分。
运动过度、出汗太多时,体内的Na+、CI-和K+降低,会导致恶心、呕吐和肌肉痉挛等现象。
因此,运动员在训练或比赛后,需喝运动饮料以补充失去的盐分。
新知探究
二、粗盐提纯
海水
盐井水
盐湖水
粗盐
煮沸
晾晒
溶解
沉淀
过滤
蒸发
结晶
初步提纯的精盐
粗盐制取
粗盐提纯
盐湖
海水
氯化钠的制取
粗盐中含有可溶性杂质(MgCl2,CaCl2等)和不溶性杂质(泥沙等),要将粗盐初步提纯,可以通过什么方法将不溶性杂质——泥沙除去呢?
新知探究
粗盐
精盐
溶解 过滤 蒸发
三、粗盐提纯
新知探究
三、粗盐提纯
溶解粗盐/g 精盐/g 精盐产率/﹪
用托盘天平称取5.0g粗盐,用药匙将粗盐逐渐加入盛有10ml水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,观察所得食盐水是否浑浊。
称量剩下的粗盐。
溶解
称量:
称量氯化钠时注意托盘天平左盘放物体,右盘放砝码 。
量取:
量取液体的体积时视线要与量筒内液体凹液面最低处保持水平。
溶解:
粗盐一次不宜加的太多,以免加多了溶解不了。溶解搅拌时,应控制玻璃棒,尽量不要碰烧杯壁。
新知探究
三、粗盐提纯
溶解操作应该注意什么?
安装好仪器,刚溶解的盐水沿玻璃棒缓缓倒进过滤器进行过滤。过滤完毕后,仔细观察滤纸上的剩余物及滤液的颜色。
查明原因(如过滤时漏斗里的液面高于滤纸边缘、滤纸破损、仪器不洁、操作失误等),再重新过滤。
如果滤液浑浊
新知探究
三、粗盐提纯
过滤
新知探究
一贴:
滤纸紧贴漏斗内壁。
二低:
滤纸低于漏斗边缘。
滤液低于滤纸边缘。
三靠:
盛待滤液的烧杯紧靠玻璃棒。
玻璃棒紧靠三层滤纸。
漏斗末端紧靠烧杯内壁。
三、粗盐提纯
过滤操作应该注意什么?
新知探究
三、粗盐提纯
蒸发
将澄清的滤液全部倒入蒸发皿里,并将蒸发皿放在铁架台的铁圈上,用酒精灯加热,观察蒸发皿中食盐的外观。
溶解粗盐/g 精盐/g 精盐产率/﹪
称量精盐的质量。
新知探究
垫上石棉网:
蒸发皿应放在铁圈上,停止加热时,不要立即把蒸发皿直接放在实验台上,必须垫上石棉网,以免烫坏实验台。
玻璃棒不断搅动:
加热过程中,用玻璃棒不断搅动,防止由于局部温度过高,造成液滴飞溅。
余热使滤液蒸干:
当蒸发皿中出现较多量固体时,即停止加热,利用余热使滤液蒸干。
三、粗盐提纯
蒸发操作应该注意什么?
③蒸发:搅拌防止局部温度过高引起液体飞溅。
④转移时玻璃棒是将固体转移到滤纸上的作用。
①溶解
②过滤
③蒸发
巩固提升
溶解、过滤、蒸发操作都用到了玻璃棒,玻璃棒分别起了什么作用?
①溶解:搅拌加速溶解
②过滤:引流
课堂总结
常见的盐
①盐的定义。
②盐的分类和命名。
盐
氯化钠
氯化钠的分布和用途。
溶解、过滤、蒸发、结晶。
粗盐提纯
1.氯化钠是日常生活中最常见的一种盐,下列有关氯化钠的描述正确
的是( )
A.氯化钠是重要的调味品,可以腌渍蔬菜、鱼、肉、蛋等
B.氯化钠是人体正常生理活动所必需的,所以摄入量越多越好
C.氯化钠可以用来配制农药波尔多液
D.通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到
纯净的氯化钠
课堂练习
A
2.有关粗盐提纯的实验操作合理的是( )
A.溶解时为了加快溶解速率,可以用玻璃棒研碎大颗粒粗盐
B.过滤时为了节省过滤时间,可以将悬浊液直接倒入漏斗
C.蒸发时为了防止物质溅出要不断搅拌,直至实验结束
D.实验结束随即用坩埚钳将热的蒸发皿取下放在实验桌上
课堂练习
C
课堂练习
3.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是___________。
(2)操作⑥中的错误是________________________。
(3)粗盐提纯实验的操作顺序为(填操作序号)_______________,称量精盐并计算产率。
(4)操作④中,当观察到_______________时,停止加热。
①⑤②③⑥④
出现较多固体
未用玻璃棒引流
加速溶解
再见
课题1.生活中常见的盐
第1课时
第十一单元
01
02
03
了解盐和生活中常见的食盐的区别。
知道氯化钠的性质和用途。
了解粗盐提纯的操作方法和注意事项。
教学目标
引入新课
温故知新:
食盐是盐,盐就是食盐”这句话对吗
日常生活中所说的盐,通常指食盐(主要成分是NaCl);
而化学中的盐不仅仅指食盐(如亚硝酸钠也属于盐,有毒不能食用)。
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
酸→H+ + 酸根离子
碱→金属离子+ OH-
盐→金属离子(或铵根离子)+酸根离子
酸:HCl H2SO4
碱:NaOH Ca(OH)2
盐:CaCO3 Na2CO3
新知探究
指出下列物质中哪些是酸 哪些是碱 哪些是盐
一、盐
新知探究
一、盐
根据盐的组成里所含的阳离子和阴离子,可将盐进行分类并称为“某盐”。
如:含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根
离子的盐称为铵盐。
盐分类:
盐的分类和命名
盐的命名:
根据盐中的酸根离子是否含有氧元素,可以把盐分为含氧酸盐和无氧酸盐。
含氧酸盐称为“某酸某”,如:K2CO3、MgSO4。
无氧酸盐称为“某化某”,如:KCI、NaCI。
新知探究
一、盐
名称 化学式 俗名
氢氧化钠
氢氧化钙
氧化钙
碳酸钠
碳酸氢钠
NaOH
火碱、烧碱、苛性钠
Ca(OH)2
熟石灰、消石灰
CaO
Na2CO3
NaHCO3
生石灰
纯碱、苏打
小苏打
食盐的的主要成分是: NaCl
大理石的主要成分是: CaCO3
盐类
A
B
C
D
盐水消除积雪
腌制
食物
盐水
选种
生理
盐水
新知探究
二、氯化钠
生活重要的调味品
新知探究
二、氯化钠
盐湖、盐井、盐矿、海水中都蕴藏着氯化钠。
盐湖
盐井
盐矿
海水
巩固提升
氯化钠与人体健康
钠离子对维持细胞内外正常的水分分布和促进细胞内外物质交换起主要作用;
氯离子是胃液中的主要成分。
运动过度、出汗太多时,体内的Na+、CI-和K+降低,会导致恶心、呕吐和肌肉痉挛等现象。
因此,运动员在训练或比赛后,需喝运动饮料以补充失去的盐分。
新知探究
二、粗盐提纯
海水
盐井水
盐湖水
粗盐
煮沸
晾晒
溶解
沉淀
过滤
蒸发
结晶
初步提纯的精盐
粗盐制取
粗盐提纯
盐湖
海水
氯化钠的制取
粗盐中含有可溶性杂质(MgCl2,CaCl2等)和不溶性杂质(泥沙等),要将粗盐初步提纯,可以通过什么方法将不溶性杂质——泥沙除去呢?
新知探究
粗盐
精盐
溶解 过滤 蒸发
三、粗盐提纯
新知探究
三、粗盐提纯
溶解粗盐/g 精盐/g 精盐产率/﹪
用托盘天平称取5.0g粗盐,用药匙将粗盐逐渐加入盛有10ml水的烧杯中,边加边用玻璃棒搅拌,直到粗盐不再溶解为止,观察所得食盐水是否浑浊。
称量剩下的粗盐。
溶解
称量:
称量氯化钠时注意托盘天平左盘放物体,右盘放砝码 。
量取:
量取液体的体积时视线要与量筒内液体凹液面最低处保持水平。
溶解:
粗盐一次不宜加的太多,以免加多了溶解不了。溶解搅拌时,应控制玻璃棒,尽量不要碰烧杯壁。
新知探究
三、粗盐提纯
溶解操作应该注意什么?
安装好仪器,刚溶解的盐水沿玻璃棒缓缓倒进过滤器进行过滤。过滤完毕后,仔细观察滤纸上的剩余物及滤液的颜色。
查明原因(如过滤时漏斗里的液面高于滤纸边缘、滤纸破损、仪器不洁、操作失误等),再重新过滤。
如果滤液浑浊
新知探究
三、粗盐提纯
过滤
新知探究
一贴:
滤纸紧贴漏斗内壁。
二低:
滤纸低于漏斗边缘。
滤液低于滤纸边缘。
三靠:
盛待滤液的烧杯紧靠玻璃棒。
玻璃棒紧靠三层滤纸。
漏斗末端紧靠烧杯内壁。
三、粗盐提纯
过滤操作应该注意什么?
新知探究
三、粗盐提纯
蒸发
将澄清的滤液全部倒入蒸发皿里,并将蒸发皿放在铁架台的铁圈上,用酒精灯加热,观察蒸发皿中食盐的外观。
溶解粗盐/g 精盐/g 精盐产率/﹪
称量精盐的质量。
新知探究
垫上石棉网:
蒸发皿应放在铁圈上,停止加热时,不要立即把蒸发皿直接放在实验台上,必须垫上石棉网,以免烫坏实验台。
玻璃棒不断搅动:
加热过程中,用玻璃棒不断搅动,防止由于局部温度过高,造成液滴飞溅。
余热使滤液蒸干:
当蒸发皿中出现较多量固体时,即停止加热,利用余热使滤液蒸干。
三、粗盐提纯
蒸发操作应该注意什么?
③蒸发:搅拌防止局部温度过高引起液体飞溅。
④转移时玻璃棒是将固体转移到滤纸上的作用。
①溶解
②过滤
③蒸发
巩固提升
溶解、过滤、蒸发操作都用到了玻璃棒,玻璃棒分别起了什么作用?
①溶解:搅拌加速溶解
②过滤:引流
课堂总结
常见的盐
①盐的定义。
②盐的分类和命名。
盐
氯化钠
氯化钠的分布和用途。
溶解、过滤、蒸发、结晶。
粗盐提纯
1.氯化钠是日常生活中最常见的一种盐,下列有关氯化钠的描述正确
的是( )
A.氯化钠是重要的调味品,可以腌渍蔬菜、鱼、肉、蛋等
B.氯化钠是人体正常生理活动所必需的,所以摄入量越多越好
C.氯化钠可以用来配制农药波尔多液
D.通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到
纯净的氯化钠
课堂练习
A
2.有关粗盐提纯的实验操作合理的是( )
A.溶解时为了加快溶解速率,可以用玻璃棒研碎大颗粒粗盐
B.过滤时为了节省过滤时间,可以将悬浊液直接倒入漏斗
C.蒸发时为了防止物质溅出要不断搅拌,直至实验结束
D.实验结束随即用坩埚钳将热的蒸发皿取下放在实验桌上
课堂练习
C
课堂练习
3.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50 g 5%的氯化钠溶液。
如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是___________。
(2)操作⑥中的错误是________________________。
(3)粗盐提纯实验的操作顺序为(填操作序号)_______________,称量精盐并计算产率。
(4)操作④中,当观察到_______________时,停止加热。
①⑤②③⑥④
出现较多固体
未用玻璃棒引流
加速溶解
再见
同课章节目录
