1.1.3 电子云与原子轨道 课件(16张PPT)2022-2023学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 1.1.3 电子云与原子轨道 课件(16张PPT)2022-2023学年高二化学人教版(2019)选择性必修2 |  | |
| 格式 | zip | ||
| 文件大小 | 38.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 11:01:30 | ||
图片预览




文档简介
(共16张PPT)
电子云与原子轨道
第3课时
01
03
04
核心素养发展目标
1. 能说明微观粒子运动状态与宏观物体运动特点的差异,建立对原子结构的模型认知。2. 知道电子的运动状态可以通过电子云模型来描述。3. 知道s轨道和p轨道的电子云形状及其所表示的含义。
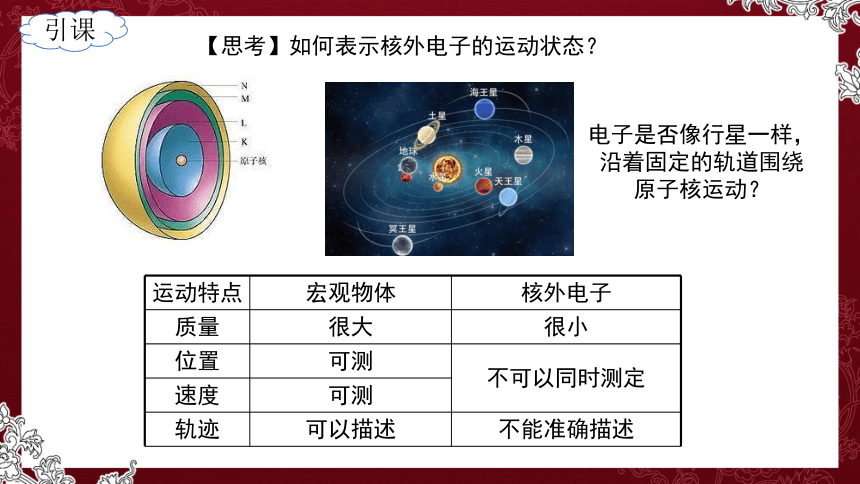
【思考】如何表示核外电子的运动状态?
电子是否像行星一样,沿着固定的轨道围绕原子核运动?
引课
运动特点 宏观物体 核外电子
质量 很大 很小
位置 可测 不可以同时测定
速度 可测 轨迹 可以描述 不能准确描述
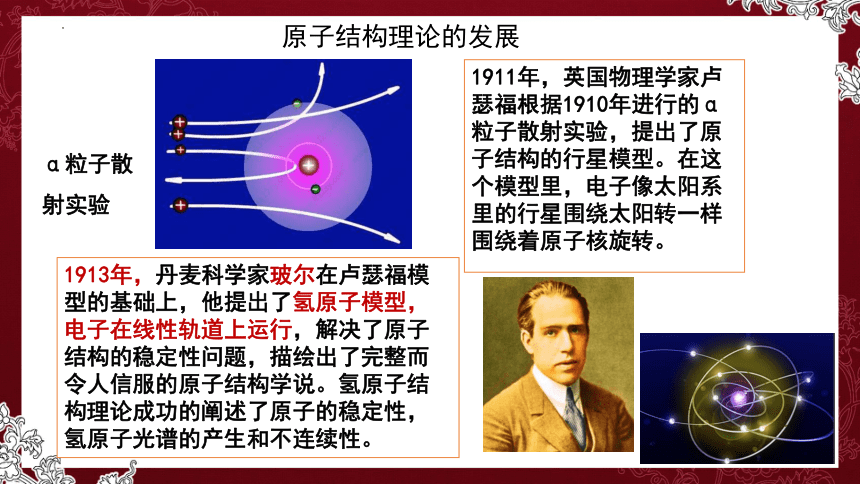
原子结构理论的发展
1911年,英国物理学家卢瑟福根据1910年进行的α粒子散射实验,提出了原子结构的行星模型。在这个模型里,电子像太阳系里的行星围绕太阳转一样围绕着原子核旋转。
α粒子散射实验
1913年,丹麦科学家玻尔在卢瑟福模型的基础上,他提出了氢原子模型,电子在线性轨道上运行,解决了原子结构的稳定性问题,描绘出了完整而令人信服的原子结构学说。氢原子结构理论成功的阐述了原子的稳定性,氢原子光谱的产生和不连续性。
薛定谔方程
薛定谔
1926年奥地利物理学家薛定谔提出:可以用一个数学方程描述核外电子的运动状态,为近代量子力学奠定了理论基础。量子力学推翻了玻尔的氢原子模型。
量子力学指出:一定空间运动状态的电子并不在玻尔假设的线性轨道上运动,而是在核外空间各处都可以出现,只是出现的概率不同。
概率密度分布图与电子云图
氢原子1s电子的概率密度分布图。
概率密度 = (P:电子在某处出现的概率,V:该处的体积)
电子出现的概率密度大
电子出现的概率密度小
小点是1s电子在原子核外出现的概率密度的形象描述。小点越密,表明概率密度越大。由于核外电子的概率密度分布看起来像一片云雾,因而被形象的称作“电子云”。
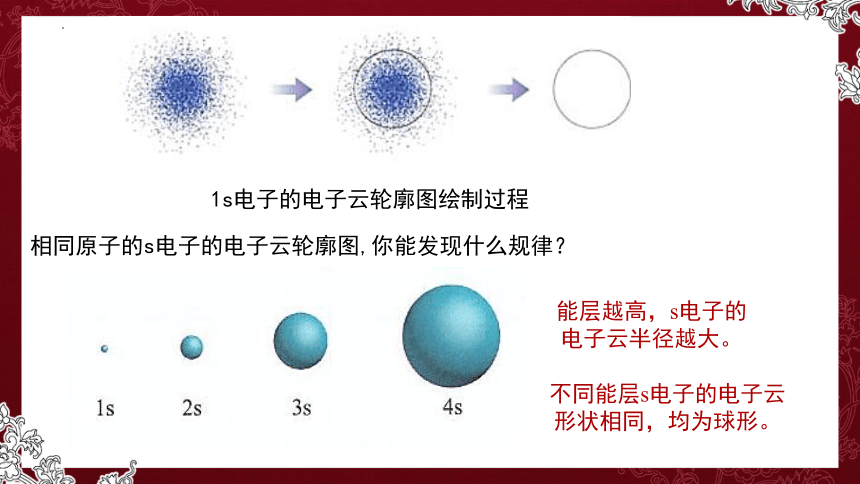
1s电子的电子云轮廓图绘制过程
相同原子的s电子的电子云轮廓图,你能发现什么规律?
不同能层s电子的电子云形状相同,均为球形。
能层越高,s电子的电子云半径越大。
2p 电子云
px、py、pz的电子云轮廓图
p电子云有什么特点?
p电子的电子云形状相同,均为哑铃形,且px、py、pz 的电子云互相垂直。
s 电子有一种空间运动状态,p 电子有三种空间运动状态。
在同一能层中px、py、pz的能量相同。
d能级有5个原子轨道(空间运动状态)
f能级有7个原子轨道
(空间运动状态)
能层序数n越大,原子轨道半径越大
(1)概念:量子力学把电子在原子核外的一个 称为一个原子轨道。
(2)形状
①s电子的原子轨道呈 形,能层序数越大,原子轨道的半径越 。
②p电子的原子轨道呈 形,能层序数越大,原子轨道的半径越大。
原子轨道
空间运动状态
球
大
哑铃
能级 s p d f
最多可容纳电子数 2 6 10 14
原子轨道数
每个轨道容纳电子数
不同能级中的原子轨道数量
请填写下表,并预测d、f能级中的原子轨道数量。
1
3
5
7
2
2
2
2
用身边的常用物品(如橡皮泥、粘土)自制原子轨道模型
【学生活动】
请整理能层、能级和原子轨道之间的关系,并填表。
能层 能级 原子 轨道数 原子轨道符号 电子云轮廓图 形状 取向
K 1s ——
L 2s ——
2p
M 3s ——
3p
3d —— —— ——
小结
能层 能级 原子 轨道数 原子轨道符号 电子云轮廓图 形状 取向
K 1s 1 1s 球形 ——
L 2s 1 2s 球形 ——
2p 3 2px、2py、2pz 哑铃形 相互垂直
M 3s 1 3s 球形 ——
3p 3 3px、3py、3pz 哑铃形 相互垂直
3d 5 —— —— ——
1.符号3px所代表的含义是
A.px轨道上有3个电子 B.第三能层px轨道有3个伸展方向
C.px电子云有3个伸展方向 D.第三能层沿x轴方向伸展的p轨道
解析 p能级有3个轨道,沿x、y、z三个不同的方向延伸,3px所代表的含义是第三能层沿x轴方向伸展的p轨道,最多只容纳2个电子。
训练
√
肆
FOUR
A
解析
B
解析
D
解析
电子云与原子轨道
第3课时
01
03
04
核心素养发展目标
1. 能说明微观粒子运动状态与宏观物体运动特点的差异,建立对原子结构的模型认知。2. 知道电子的运动状态可以通过电子云模型来描述。3. 知道s轨道和p轨道的电子云形状及其所表示的含义。
【思考】如何表示核外电子的运动状态?
电子是否像行星一样,沿着固定的轨道围绕原子核运动?
引课
运动特点 宏观物体 核外电子
质量 很大 很小
位置 可测 不可以同时测定
速度 可测 轨迹 可以描述 不能准确描述
原子结构理论的发展
1911年,英国物理学家卢瑟福根据1910年进行的α粒子散射实验,提出了原子结构的行星模型。在这个模型里,电子像太阳系里的行星围绕太阳转一样围绕着原子核旋转。
α粒子散射实验
1913年,丹麦科学家玻尔在卢瑟福模型的基础上,他提出了氢原子模型,电子在线性轨道上运行,解决了原子结构的稳定性问题,描绘出了完整而令人信服的原子结构学说。氢原子结构理论成功的阐述了原子的稳定性,氢原子光谱的产生和不连续性。
薛定谔方程
薛定谔
1926年奥地利物理学家薛定谔提出:可以用一个数学方程描述核外电子的运动状态,为近代量子力学奠定了理论基础。量子力学推翻了玻尔的氢原子模型。
量子力学指出:一定空间运动状态的电子并不在玻尔假设的线性轨道上运动,而是在核外空间各处都可以出现,只是出现的概率不同。
概率密度分布图与电子云图
氢原子1s电子的概率密度分布图。
概率密度 = (P:电子在某处出现的概率,V:该处的体积)
电子出现的概率密度大
电子出现的概率密度小
小点是1s电子在原子核外出现的概率密度的形象描述。小点越密,表明概率密度越大。由于核外电子的概率密度分布看起来像一片云雾,因而被形象的称作“电子云”。
1s电子的电子云轮廓图绘制过程
相同原子的s电子的电子云轮廓图,你能发现什么规律?
不同能层s电子的电子云形状相同,均为球形。
能层越高,s电子的电子云半径越大。
2p 电子云
px、py、pz的电子云轮廓图
p电子云有什么特点?
p电子的电子云形状相同,均为哑铃形,且px、py、pz 的电子云互相垂直。
s 电子有一种空间运动状态,p 电子有三种空间运动状态。
在同一能层中px、py、pz的能量相同。
d能级有5个原子轨道(空间运动状态)
f能级有7个原子轨道
(空间运动状态)
能层序数n越大,原子轨道半径越大
(1)概念:量子力学把电子在原子核外的一个 称为一个原子轨道。
(2)形状
①s电子的原子轨道呈 形,能层序数越大,原子轨道的半径越 。
②p电子的原子轨道呈 形,能层序数越大,原子轨道的半径越大。
原子轨道
空间运动状态
球
大
哑铃
能级 s p d f
最多可容纳电子数 2 6 10 14
原子轨道数
每个轨道容纳电子数
不同能级中的原子轨道数量
请填写下表,并预测d、f能级中的原子轨道数量。
1
3
5
7
2
2
2
2
用身边的常用物品(如橡皮泥、粘土)自制原子轨道模型
【学生活动】
请整理能层、能级和原子轨道之间的关系,并填表。
能层 能级 原子 轨道数 原子轨道符号 电子云轮廓图 形状 取向
K 1s ——
L 2s ——
2p
M 3s ——
3p
3d —— —— ——
小结
能层 能级 原子 轨道数 原子轨道符号 电子云轮廓图 形状 取向
K 1s 1 1s 球形 ——
L 2s 1 2s 球形 ——
2p 3 2px、2py、2pz 哑铃形 相互垂直
M 3s 1 3s 球形 ——
3p 3 3px、3py、3pz 哑铃形 相互垂直
3d 5 —— —— ——
1.符号3px所代表的含义是
A.px轨道上有3个电子 B.第三能层px轨道有3个伸展方向
C.px电子云有3个伸展方向 D.第三能层沿x轴方向伸展的p轨道
解析 p能级有3个轨道,沿x、y、z三个不同的方向延伸,3px所代表的含义是第三能层沿x轴方向伸展的p轨道,最多只容纳2个电子。
训练
√
肆
FOUR
A
解析
B
解析
D
解析
