化学人教版(2019)必修第二册7.1有机化合物中碳原子的成键特点、烷烃的结构(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.1有机化合物中碳原子的成键特点、烷烃的结构(共23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-08 00:00:00 | ||
图片预览




文档简介
(共23张PPT)
第七章 有机化合物
第一节 认识有机化合物
第1课时
有机化合物中碳原子成键特点 烷烃
【引入】
目前,人们在自然界发现和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物。
有机物的组成元素有哪些?
有机物的组成元素有限却种类繁多,原因是什么呢?
1.甲烷的分子结构
甲烷(CH4)分子中的碳原子以最外层的 个电子与 个氢原子的电子形成 个 共价键,电子式为 ,结构式为 。
4
4
4
C—H
碳原子在元素周期表中位于第 周期 族,最外层有
个电子
二
ⅣA
4
一、有机化合物中碳原子的成键特点
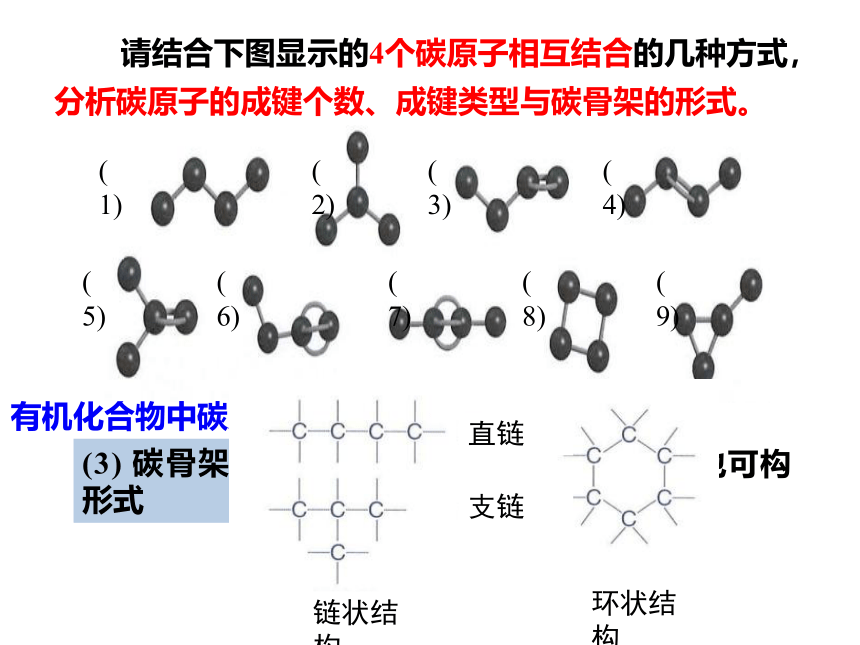
请结合下图显示的4个碳原子相互结合的几种方式,分析碳原子的成键个数、成键类型与碳骨架的形式。
有机化合物中碳原子的成键特点
(1) 键的个数
每个碳原子形成4个共价键
(2) 成键的类型
碳原子与碳原子之间也能形成共价键,可以形成单键、双键或三键。
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
请结合下图显示的4个碳原子相互结合的几种方式,分析碳原子的成键个数、成键类型与碳骨架的形式。
有机化合物中碳原子的成键特点
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(3) 碳骨架形式
碳原子之间可构成链状结构,也可构成环状结构。
链状结构
环状结构
直链
支链
【思考与交流】
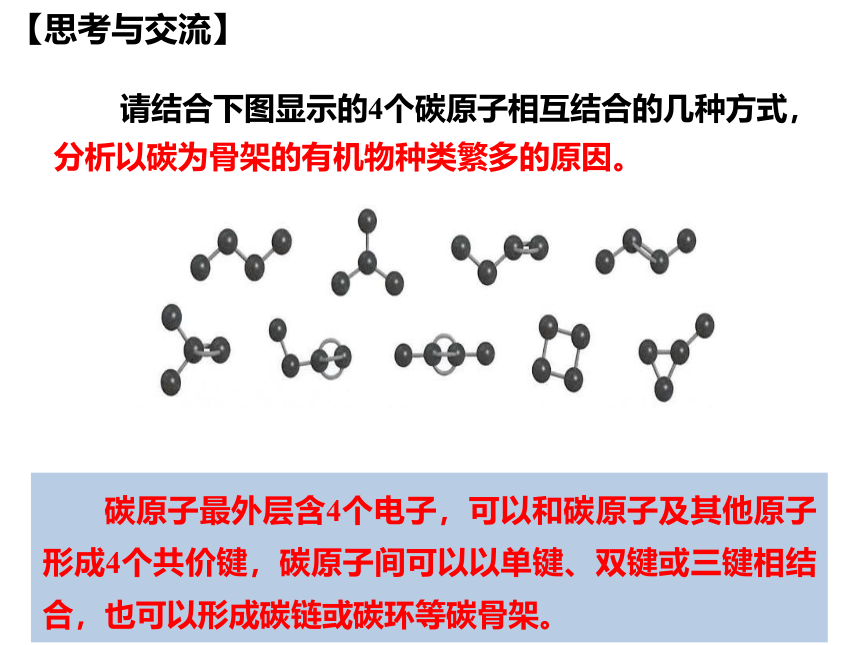
请结合下图显示的4个碳原子相互结合的几种方式,分析以碳为骨架的有机物种类繁多的原因。
碳原子最外层含4个电子,可以和碳原子及其他原子形成4个共价键,碳原子间可以以单键、双键或三键相结合,也可以形成碳链或碳环等碳骨架。
烃:
(碳氢化合物)
只含有碳、氢两种元素的有机物。
+
=
烃
t
īng
q
火
气
àn
t īng
二、烷烃
二、烷烃
1.烷烃的结构
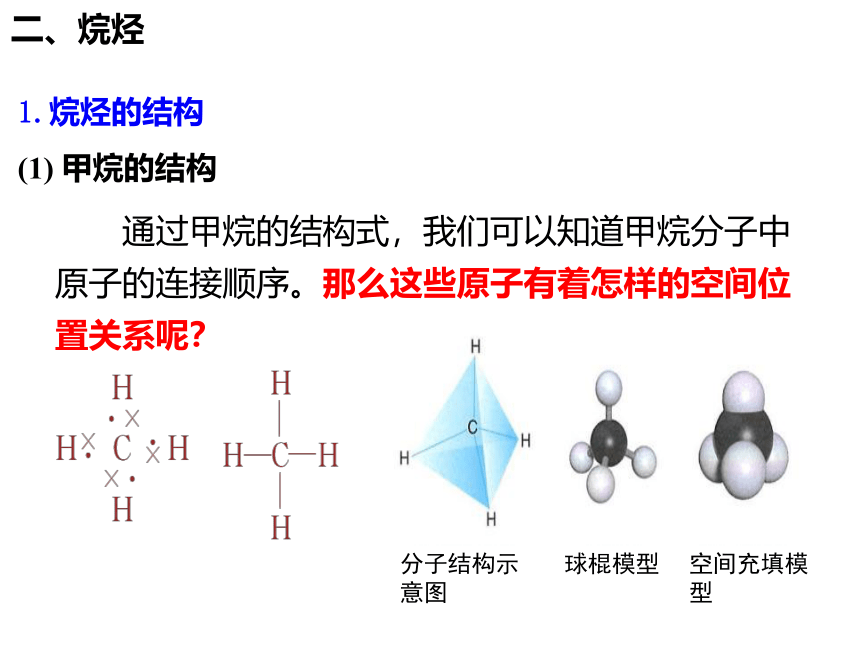
(1) 甲烷的结构
通过甲烷的结构式,我们可以知道甲烷分子中原子的连接顺序。那么这些原子有着怎样的空间位置关系呢?
分子结构示意图
球棍模型
空间充填模型
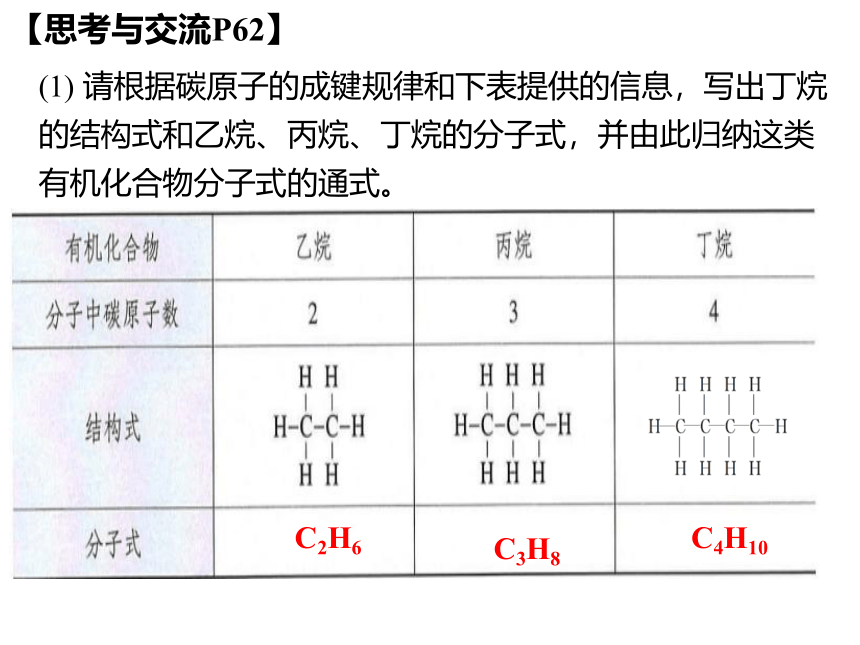
【思考与交流P62】
(1) 请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
结合下图的分子结构模型,总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”,C与C结合成链状,呈锯齿状。
二、烷烃
1.烷烃的结构
链状烷烃的结构特点:
单键 饱和 链状(锯齿状)
烷烃:只含 和 两种元素,分子中的碳原子之间都以 结合,碳原子的剩余价键均与 结合,使碳原子的化合价都达到“ ”,这样的一类有机化合物称为 ,也称为烷烃。链状烷烃的通式:________
(n≥1)。
碳
氢
单键
氢原子
饱和
饱和烃
CnH2n+2
2.同系物
(1)定义:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
(2) 同系物的特点:
通式相同、结构相似、化学性质相似,
分子式不同、组成上相差一个或若干CH2原子团。
[练习]下列物质是否为同系物?
①CH3CH2CH3 和 CH3(CH2)100CH3
②CH3CH2CH3 和 CH3CH(CH3)CH3
③ CH2=CH2 和
④HCl和CH3Cl
CH2
H2C
CH2
是
是
否
否
说明 ①同系物所含元素种类一定相同,除C、H外其他种类元素原子数必须相同。
②同系物一定具有不同的碳、氢原子数和分子式。
③同系物一定具有不同的相对分子质量(相差14n)。
与同学交流,比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
H—C—C—C—C—H
H
H
H
H
H
H
H
H
H—C—C—C—H
H
H
H
H
H
H
C
H— —H
3、同分异构体现象:
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
同分异构体: 具有相同的分子式,但具有不同结构的化合物,互称为同分异构体.
理解
三同
分子式相同、分子组成相同、分子量相同
两不同
结构不同、性质不同
思考1:产生同分异构现象的本质原因是什么
碳原子的连接方式和成键类型不同
思考2:是不是每种分子都有同分异构体
不是。如甲烷、乙烷、丙烷等没有同分异构体
思考3:CH4、C3H8、C4H10、C5H12分子式 只表示一种纯净物吗?
随着碳数的增多同分异构体数目______。
10359
16
8
18
5
6
2
4
1
2
9
3
7
1
1
3
5
同分异构体数
1
碳原子数
烷烃中,碳数___个开始有同分异构体;
4
增大
名称 熔点/0C 沸点/0C 相对密度
正丁烷 -138.4 -0.5 0.5788
异丁烷 -159.6 -11.7 0.557
正丁烷和异丁烷的某些物理性质
(3) 同分异构体性质:
物理性质:
支链越多,熔沸点 密度
化学性质:
不一定相同
同系物、同分异构体、同素异形体、同位素的区别
同系物 同分异构体 同素异形体 同位素
组成
结构
类别
分子相差一个或若干个CH2原子团
分子组成相同
分子组成不同
质子数相同,中子数不同
结构相似
结构不同
结构不同
——
化合物
单质
化合物
同一元素的不同原子
【小结】
二、烷烃
4.烷烃的命名——习惯命名法
(1) 1-10个C原子的直链烷烃:
称为 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 烷
(2) 11个C原子以上的直链烷烃:如:C11H24 称为十一烷
(3) 带支链的烷烃:用正、异、新表示
戊烷
C5H12
C8H18
辛烷
CH3CH2CH2CH2CH3
CH3CHCH2CH3
CH3
CH3
CH3CCH3
CH3
正戊烷
无支链
异戊烷
带一支链
新戊烷
带两支链
CH3CH2CH2CH2CH2CH3
CH3CHCH2CH2CH3
CH3CCH2CH3
CH3
CH3
CH3
正己烷
异己烷
新己烷
CH3-CH2-CH2-CH3
CH3CH2CH2CH3
CH3(CH2)2CH3
CH3CH CH3
5.有机物结构的表示方法:
结构式:
( )2
结构简式:
必省去C-H键
可省去C-C单键
相同可合并
CH3-CH-CH3
CH3
CH3CHCH3
CH3
同位素 同素异形体 同系物 同分异构体
使用范围
相同
不同
化性
物性
相同 相似 相似 相同(或不同)
不同 不同 相似递变 不同
“四同” 有关对照
原子
质子数
中子数
单质
单质内部结构
元素种类
有机物
结构通式
C的个数
化合物
分子式
结构
【资料卡片】
使用模型研究物质结构
将微观的分子结构通过模型呈现出来,便于我们了解分子中原子的结合方式与空间位置关系,获取更多的结构信息。随着现代信息技术的发展,除了实物模型,还可以通过计算机对物质的结构进行模拟和计算。这是人们探索物质结构的重要方法,也是学习化学的直观工具。
同系物的判断标准
说明 ①同系物所含元素种类一定相同,除C、H外其他种类元素原子数必须相同。
②同系物一定具有不同的碳、氢原子数和分子式。
③同系物一定具有不同的相对分子质量(相差14n)。
第七章 有机化合物
第一节 认识有机化合物
第1课时
有机化合物中碳原子成键特点 烷烃
【引入】
目前,人们在自然界发现和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物。
有机物的组成元素有哪些?
有机物的组成元素有限却种类繁多,原因是什么呢?
1.甲烷的分子结构
甲烷(CH4)分子中的碳原子以最外层的 个电子与 个氢原子的电子形成 个 共价键,电子式为 ,结构式为 。
4
4
4
C—H
碳原子在元素周期表中位于第 周期 族,最外层有
个电子
二
ⅣA
4
一、有机化合物中碳原子的成键特点
请结合下图显示的4个碳原子相互结合的几种方式,分析碳原子的成键个数、成键类型与碳骨架的形式。
有机化合物中碳原子的成键特点
(1) 键的个数
每个碳原子形成4个共价键
(2) 成键的类型
碳原子与碳原子之间也能形成共价键,可以形成单键、双键或三键。
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
请结合下图显示的4个碳原子相互结合的几种方式,分析碳原子的成键个数、成键类型与碳骨架的形式。
有机化合物中碳原子的成键特点
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(3) 碳骨架形式
碳原子之间可构成链状结构,也可构成环状结构。
链状结构
环状结构
直链
支链
【思考与交流】
请结合下图显示的4个碳原子相互结合的几种方式,分析以碳为骨架的有机物种类繁多的原因。
碳原子最外层含4个电子,可以和碳原子及其他原子形成4个共价键,碳原子间可以以单键、双键或三键相结合,也可以形成碳链或碳环等碳骨架。
烃:
(碳氢化合物)
只含有碳、氢两种元素的有机物。
+
=
烃
t
īng
q
火
气
àn
t īng
二、烷烃
二、烷烃
1.烷烃的结构
(1) 甲烷的结构
通过甲烷的结构式,我们可以知道甲烷分子中原子的连接顺序。那么这些原子有着怎样的空间位置关系呢?
分子结构示意图
球棍模型
空间充填模型
【思考与交流P62】
(1) 请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式,并由此归纳这类有机化合物分子式的通式。
C2H6
C3H8
C4H10
结合下图的分子结构模型,总结这类有机化合物的组成和分子结构特点。
只含碳和氢两种元素,分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”,C与C结合成链状,呈锯齿状。
二、烷烃
1.烷烃的结构
链状烷烃的结构特点:
单键 饱和 链状(锯齿状)
烷烃:只含 和 两种元素,分子中的碳原子之间都以 结合,碳原子的剩余价键均与 结合,使碳原子的化合价都达到“ ”,这样的一类有机化合物称为 ,也称为烷烃。链状烷烃的通式:________
(n≥1)。
碳
氢
单键
氢原子
饱和
饱和烃
CnH2n+2
2.同系物
(1)定义:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
(2) 同系物的特点:
通式相同、结构相似、化学性质相似,
分子式不同、组成上相差一个或若干CH2原子团。
[练习]下列物质是否为同系物?
①CH3CH2CH3 和 CH3(CH2)100CH3
②CH3CH2CH3 和 CH3CH(CH3)CH3
③ CH2=CH2 和
④HCl和CH3Cl
CH2
H2C
CH2
是
是
否
否
说明 ①同系物所含元素种类一定相同,除C、H外其他种类元素原子数必须相同。
②同系物一定具有不同的碳、氢原子数和分子式。
③同系物一定具有不同的相对分子质量(相差14n)。
与同学交流,比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
H—C—C—C—C—H
H
H
H
H
H
H
H
H
H—C—C—C—H
H
H
H
H
H
H
C
H— —H
3、同分异构体现象:
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
同分异构体: 具有相同的分子式,但具有不同结构的化合物,互称为同分异构体.
理解
三同
分子式相同、分子组成相同、分子量相同
两不同
结构不同、性质不同
思考1:产生同分异构现象的本质原因是什么
碳原子的连接方式和成键类型不同
思考2:是不是每种分子都有同分异构体
不是。如甲烷、乙烷、丙烷等没有同分异构体
思考3:CH4、C3H8、C4H10、C5H12分子式 只表示一种纯净物吗?
随着碳数的增多同分异构体数目______。
10359
16
8
18
5
6
2
4
1
2
9
3
7
1
1
3
5
同分异构体数
1
碳原子数
烷烃中,碳数___个开始有同分异构体;
4
增大
名称 熔点/0C 沸点/0C 相对密度
正丁烷 -138.4 -0.5 0.5788
异丁烷 -159.6 -11.7 0.557
正丁烷和异丁烷的某些物理性质
(3) 同分异构体性质:
物理性质:
支链越多,熔沸点 密度
化学性质:
不一定相同
同系物、同分异构体、同素异形体、同位素的区别
同系物 同分异构体 同素异形体 同位素
组成
结构
类别
分子相差一个或若干个CH2原子团
分子组成相同
分子组成不同
质子数相同,中子数不同
结构相似
结构不同
结构不同
——
化合物
单质
化合物
同一元素的不同原子
【小结】
二、烷烃
4.烷烃的命名——习惯命名法
(1) 1-10个C原子的直链烷烃:
称为 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 烷
(2) 11个C原子以上的直链烷烃:如:C11H24 称为十一烷
(3) 带支链的烷烃:用正、异、新表示
戊烷
C5H12
C8H18
辛烷
CH3CH2CH2CH2CH3
CH3CHCH2CH3
CH3
CH3
CH3CCH3
CH3
正戊烷
无支链
异戊烷
带一支链
新戊烷
带两支链
CH3CH2CH2CH2CH2CH3
CH3CHCH2CH2CH3
CH3CCH2CH3
CH3
CH3
CH3
正己烷
异己烷
新己烷
CH3-CH2-CH2-CH3
CH3CH2CH2CH3
CH3(CH2)2CH3
CH3CH CH3
5.有机物结构的表示方法:
结构式:
( )2
结构简式:
必省去C-H键
可省去C-C单键
相同可合并
CH3-CH-CH3
CH3
CH3CHCH3
CH3
同位素 同素异形体 同系物 同分异构体
使用范围
相同
不同
化性
物性
相同 相似 相似 相同(或不同)
不同 不同 相似递变 不同
“四同” 有关对照
原子
质子数
中子数
单质
单质内部结构
元素种类
有机物
结构通式
C的个数
化合物
分子式
结构
【资料卡片】
使用模型研究物质结构
将微观的分子结构通过模型呈现出来,便于我们了解分子中原子的结合方式与空间位置关系,获取更多的结构信息。随着现代信息技术的发展,除了实物模型,还可以通过计算机对物质的结构进行模拟和计算。这是人们探索物质结构的重要方法,也是学习化学的直观工具。
同系物的判断标准
说明 ①同系物所含元素种类一定相同,除C、H外其他种类元素原子数必须相同。
②同系物一定具有不同的碳、氢原子数和分子式。
③同系物一定具有不同的相对分子质量(相差14n)。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
