11.1生活中常见的盐(第1课时氯化钠)课件(共20张PPT 内嵌视频)—2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 11.1生活中常见的盐(第1课时氯化钠)课件(共20张PPT 内嵌视频)—2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-08 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第十一单元 盐 化肥
11.1 生活中常见的盐
第一课时:氯化钠
学习目标
理解盐的概念。
认识氯化钠的性质和用途。
了解粗盐提纯的操作方法和注意事项。
了解碳酸钠、碳酸氢钠、碳酸钙的性质及其在生活中的主要用途;
掌握碳酸根离子的检验方法。
1.概念:
探究新知
组成里含有金属离子(或铵根离子)和酸根离子的化合物。
2.盐的分类:
例1:食盐是盐,盐就是食盐。
1.盐的概念
×
根据盐的组成里所含的阳离子和阴离子,可将盐进行分类并称为“某盐”。
如:含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根离子的盐称为铵盐。
例2:判断下列物质的类别:
A.CH3COOH B.CaCO3 C.Ca(OH)2 D.MnO2
酸
盐
碱
氧化物
探究新知
3.盐溶液的酸碱性:
盐的水溶液可能显酸性、碱性、中性。
显酸性:CuSO4溶液、NH4Cl溶液等。
显碱性:Na2CO3溶液、NaHCO3溶液、K2CO3溶液等。
显中性:NaCl溶液、Na2SO4等。
例3【P78】:亚硝酸钠NaNO2是一种工业用盐,它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐水溶液呈中性。如果让你来鉴别亚硝酸钠与食盐,你选用什么试剂,如何操作?
无色酚酞溶液;取样,分别滴加2~3滴酚酞溶液。
1.盐的概念
1.物理性质:
探究新知
白色固体、有咸味、易溶于水,其溶解度受温度的变化影响小。
2.用途:
2.氯化钠
医疗上:配制生理盐水(0.9%);
农业上:用16%NaCl溶液选种(密度);
工业上:制取碳酸钠、
氢氧化钠、氯气、盐酸等;
生活上:调味品、腌制蔬菜、鱼、肉、蛋等;
交通上:公路上的积雪用氯化钠来消除。
2NaCl+2H2O === 2NaOH + H2↑+Cl2↑
通电
侯氏制碱法P76
3.分布:
探究新知
氯化钠在自然界中分布很广,海水、盐湖、盐井和盐矿是氯化钠的主要来源。
“
“
茶卡盐湖
底特律盐矿
海水晒盐
自贡盐井
2.氯化钠
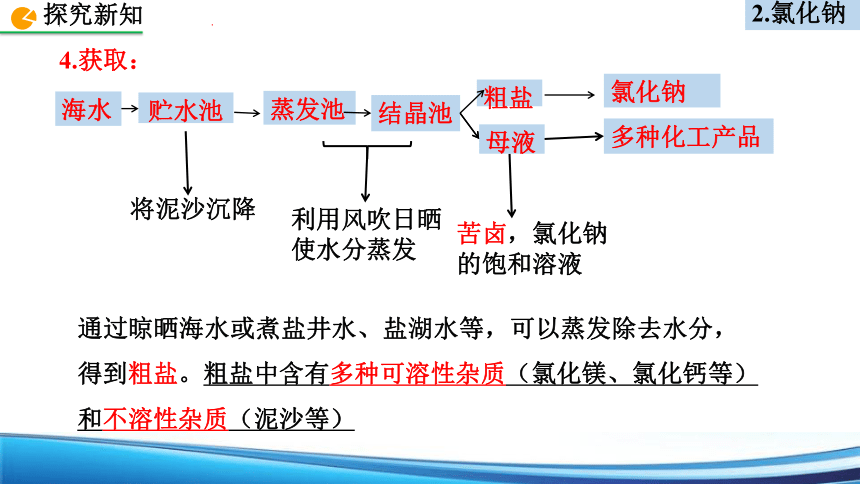
4.获取:
探究新知
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)
2.氯化钠
海水
贮水池
蒸发池
结晶池
多种化工产品
氯化钠
母液
粗盐
将泥沙沉降
利用风吹日晒
使水分蒸发
苦卤,氯化钠的饱和溶液
实验活动8 粗盐中难溶性杂质的去除
3.粗盐提纯
学习目标
掌握粗盐中难溶性杂质去除的实验步骤、误差分析、玻璃棒的作用
学会固体混合物(一种可溶于水且不与水反应;另一种难溶于水)的除杂方法。
掌握实验考试要点。
【实验目的】
探究新知
体验固体混合物初步提纯的实验过程
学习蒸发操作技能,巩固溶解、过滤操作技能
【实验用品】
烧杯(2个)、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒(10mL)、铁架台(带铁圈)、托盘天平、滤纸、火柴。
粗盐(广口瓶)、水(细口瓶)
【实验步骤】
溶解→过滤→蒸发→计算产率
3.粗盐提纯
3.粗盐提纯
3.粗盐提纯
探究新知
1.溶解
a.称量5.0g粗盐
b.将粗盐逐渐加入水中,并用玻璃棒不断搅拌,至不再溶解为止。
c.称量剩下的粗盐。
2.过滤(除去难溶性杂质)
一贴:滤纸紧贴漏斗内壁,中间不要有气泡,否则过滤速度慢。
二低:①滤纸边缘要低于漏斗边缘;
②漏斗里的液面应低于滤纸的边缘。
三靠:①过滤时玻璃棒要靠在有三层滤纸的一边,防止滤纸破损;
②盛有待过滤液的烧杯口要紧靠在玻璃棒上;
③漏斗的下端要紧靠在烧杯内壁,防止液滴飞溅。
若过滤后仍浑浊,应再过滤一次
Q1:玻璃棒的作用?
搅拌,加速溶解。
Q2:玻璃棒的作用?
引流。
探究新知
3.蒸发
a.把所得滤液倒入蒸发皿,用酒精灯加热;
b.加热时用玻璃棒搅拌,目的是防止因局部温度过高,造成液滴飞溅。当有较多固体出现时停止加热,利用余热将其蒸干。
c.停止加热后,不要立即把蒸发皿直接放在实验台上,以免烫坏实验台面。要用坩埚钳取下热的蒸发皿,放在石棉网上,防止烫坏自己和实验台。
3.粗盐提纯
蒸发皿使用时的注意事项
蒸发皿可直接加热,不需要石棉网,要先预热。(类似试管)
液体体积不超过蒸发皿体积的2/3
使用时外壁要干燥,防止受热不均炸裂
冷却后再洗
探究新知
4.计算产率
用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器中。计算产率。
3.粗盐提纯
精盐产率= ×100%
溶解粗盐/g 精盐/g 精盐产率/%
玻璃棒:转移固体
3.7
3.3
89.2
1.粗盐未完全溶解。 2.过滤时液体洒出。
3. 蒸发时有液滴溅出。
4.蒸发后的固体中含有水分。 5.蒸发后,固体未完全转移。
6. 称量精盐时,药品与砝码放反并使用游码。
偏低
偏低
偏低
偏高
偏低
偏低
探究新知
3.粗盐提纯
实验 玻璃棒的作用 目的
固体溶解 搅拌 加速溶解
过滤 引流 防止液体外溅、冲破滤纸
蒸发 搅拌 防止因局部温度过高造成液滴或晶体飞溅
计算产率 转移
探究新知
1. 制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。想一想:能否用降低溶液温度的方法来达到同一目的?
2. 本实验中采用的方法利用了氯化钠的哪些性质?考虑到粗盐的来源,你判断这样提纯的盐是否为纯净物?
不能。氯化钠的溶解度受温度变化影响不大。
过滤利用了氯化钠易溶于水的性质,蒸发利用了氯化钠的溶解度受温度变化影响不大的性质。
不是。还有CaCl2、MgCl2、Na2SO4等可溶性杂质。
3.粗盐提纯
【问题与交流】
课堂小结
定义:组成里含有金属离子(或铵根离子)和酸根离子的化合物
常见的盐:氯化钠(物理性质、用途、制取等)
粗盐提纯:
(1)溶解;(2)过滤;
(3)蒸发;(4)计算产率
盐
巩固练习
B
4. 有关粗盐提纯的实验操作合理的是( )
A. 溶解时为了加快溶解速率,可以用玻璃棒研碎大颗粒粗盐
B. 过滤时为了节省过滤时间,可以将悬浊液直接倒入漏斗
C. 蒸发时为了防止物质溅出要不断搅拌,直至实验结束
D. 实验结束随即用坩埚钳将热的蒸发皿取下放在实验桌上
C
3.下列有关蒸发结晶操作描述正确的是________。
A.当加热至有晶体析出时,即停止加热
B.当蒸发皿中出现较多固体时,即停止加热
C.当水分完全蒸干时,即停止加热
D.蒸发皿应放在石棉网上加热,防止破损
巩固练习
5.【2019·海南】在“粗盐中难溶性杂质的去除”实验中,不需要进行的操作是( )
A.溶解 B.过滤 C.蒸发 D.蒸馏
D
6.【2020·菏泽】在除去粗盐中难溶性杂质的实验中,下列操作正确的是( )
D
7.在“粗盐提纯”实验中,将提纯后的氯化钠与粗盐作比较,以计算精盐的产率。下列可能引起产率偏高的原因是( )
A.粗盐未完全溶解 B.溶解粗盐的烧杯壁上沾有不溶性杂质
C.过滤时液面高于滤纸边缘 D.蒸发时有液滴飞溅出去
C
巩固练习
8.【2019·滨州】结合下图仪器,完成粗盐提纯实验中的有关问题。
(1)仪器②的名称是________。
(2)在过滤粗盐水时,除用到⑤⑥
⑦⑧,还需要用到图中的一种
玻璃仪器是________(填名称)。
(3)蒸发结晶食盐,除用到①②⑧⑨,
还需用到图中的仪器有________(填序号)。
坩埚钳
漏斗
⑥
第十一单元 盐 化肥
11.1 生活中常见的盐
第一课时:氯化钠
学习目标
理解盐的概念。
认识氯化钠的性质和用途。
了解粗盐提纯的操作方法和注意事项。
了解碳酸钠、碳酸氢钠、碳酸钙的性质及其在生活中的主要用途;
掌握碳酸根离子的检验方法。
1.概念:
探究新知
组成里含有金属离子(或铵根离子)和酸根离子的化合物。
2.盐的分类:
例1:食盐是盐,盐就是食盐。
1.盐的概念
×
根据盐的组成里所含的阳离子和阴离子,可将盐进行分类并称为“某盐”。
如:含有碳酸根离子的盐称为碳酸盐,含有钾离子的盐称为钾盐,含有铵根离子的盐称为铵盐。
例2:判断下列物质的类别:
A.CH3COOH B.CaCO3 C.Ca(OH)2 D.MnO2
酸
盐
碱
氧化物
探究新知
3.盐溶液的酸碱性:
盐的水溶液可能显酸性、碱性、中性。
显酸性:CuSO4溶液、NH4Cl溶液等。
显碱性:Na2CO3溶液、NaHCO3溶液、K2CO3溶液等。
显中性:NaCl溶液、Na2SO4等。
例3【P78】:亚硝酸钠NaNO2是一种工业用盐,它有毒、有咸味,外形与食盐相似。人若误食会引起中毒,危害人体健康,甚至致人死亡。亚硝酸钠的水溶液呈碱性,食盐水溶液呈中性。如果让你来鉴别亚硝酸钠与食盐,你选用什么试剂,如何操作?
无色酚酞溶液;取样,分别滴加2~3滴酚酞溶液。
1.盐的概念
1.物理性质:
探究新知
白色固体、有咸味、易溶于水,其溶解度受温度的变化影响小。
2.用途:
2.氯化钠
医疗上:配制生理盐水(0.9%);
农业上:用16%NaCl溶液选种(密度);
工业上:制取碳酸钠、
氢氧化钠、氯气、盐酸等;
生活上:调味品、腌制蔬菜、鱼、肉、蛋等;
交通上:公路上的积雪用氯化钠来消除。
2NaCl+2H2O === 2NaOH + H2↑+Cl2↑
通电
侯氏制碱法P76
3.分布:
探究新知
氯化钠在自然界中分布很广,海水、盐湖、盐井和盐矿是氯化钠的主要来源。
“
“
茶卡盐湖
底特律盐矿
海水晒盐
自贡盐井
2.氯化钠
4.获取:
探究新知
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分,得到粗盐。粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)
2.氯化钠
海水
贮水池
蒸发池
结晶池
多种化工产品
氯化钠
母液
粗盐
将泥沙沉降
利用风吹日晒
使水分蒸发
苦卤,氯化钠的饱和溶液
实验活动8 粗盐中难溶性杂质的去除
3.粗盐提纯
学习目标
掌握粗盐中难溶性杂质去除的实验步骤、误差分析、玻璃棒的作用
学会固体混合物(一种可溶于水且不与水反应;另一种难溶于水)的除杂方法。
掌握实验考试要点。
【实验目的】
探究新知
体验固体混合物初步提纯的实验过程
学习蒸发操作技能,巩固溶解、过滤操作技能
【实验用品】
烧杯(2个)、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒(10mL)、铁架台(带铁圈)、托盘天平、滤纸、火柴。
粗盐(广口瓶)、水(细口瓶)
【实验步骤】
溶解→过滤→蒸发→计算产率
3.粗盐提纯
3.粗盐提纯
3.粗盐提纯
探究新知
1.溶解
a.称量5.0g粗盐
b.将粗盐逐渐加入水中,并用玻璃棒不断搅拌,至不再溶解为止。
c.称量剩下的粗盐。
2.过滤(除去难溶性杂质)
一贴:滤纸紧贴漏斗内壁,中间不要有气泡,否则过滤速度慢。
二低:①滤纸边缘要低于漏斗边缘;
②漏斗里的液面应低于滤纸的边缘。
三靠:①过滤时玻璃棒要靠在有三层滤纸的一边,防止滤纸破损;
②盛有待过滤液的烧杯口要紧靠在玻璃棒上;
③漏斗的下端要紧靠在烧杯内壁,防止液滴飞溅。
若过滤后仍浑浊,应再过滤一次
Q1:玻璃棒的作用?
搅拌,加速溶解。
Q2:玻璃棒的作用?
引流。
探究新知
3.蒸发
a.把所得滤液倒入蒸发皿,用酒精灯加热;
b.加热时用玻璃棒搅拌,目的是防止因局部温度过高,造成液滴飞溅。当有较多固体出现时停止加热,利用余热将其蒸干。
c.停止加热后,不要立即把蒸发皿直接放在实验台上,以免烫坏实验台面。要用坩埚钳取下热的蒸发皿,放在石棉网上,防止烫坏自己和实验台。
3.粗盐提纯
蒸发皿使用时的注意事项
蒸发皿可直接加热,不需要石棉网,要先预热。(类似试管)
液体体积不超过蒸发皿体积的2/3
使用时外壁要干燥,防止受热不均炸裂
冷却后再洗
探究新知
4.计算产率
用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器中。计算产率。
3.粗盐提纯
精盐产率= ×100%
溶解粗盐/g 精盐/g 精盐产率/%
玻璃棒:转移固体
3.7
3.3
89.2
1.粗盐未完全溶解。 2.过滤时液体洒出。
3. 蒸发时有液滴溅出。
4.蒸发后的固体中含有水分。 5.蒸发后,固体未完全转移。
6. 称量精盐时,药品与砝码放反并使用游码。
偏低
偏低
偏低
偏高
偏低
偏低
探究新知
3.粗盐提纯
实验 玻璃棒的作用 目的
固体溶解 搅拌 加速溶解
过滤 引流 防止液体外溅、冲破滤纸
蒸发 搅拌 防止因局部温度过高造成液滴或晶体飞溅
计算产率 转移
探究新知
1. 制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。想一想:能否用降低溶液温度的方法来达到同一目的?
2. 本实验中采用的方法利用了氯化钠的哪些性质?考虑到粗盐的来源,你判断这样提纯的盐是否为纯净物?
不能。氯化钠的溶解度受温度变化影响不大。
过滤利用了氯化钠易溶于水的性质,蒸发利用了氯化钠的溶解度受温度变化影响不大的性质。
不是。还有CaCl2、MgCl2、Na2SO4等可溶性杂质。
3.粗盐提纯
【问题与交流】
课堂小结
定义:组成里含有金属离子(或铵根离子)和酸根离子的化合物
常见的盐:氯化钠(物理性质、用途、制取等)
粗盐提纯:
(1)溶解;(2)过滤;
(3)蒸发;(4)计算产率
盐
巩固练习
B
4. 有关粗盐提纯的实验操作合理的是( )
A. 溶解时为了加快溶解速率,可以用玻璃棒研碎大颗粒粗盐
B. 过滤时为了节省过滤时间,可以将悬浊液直接倒入漏斗
C. 蒸发时为了防止物质溅出要不断搅拌,直至实验结束
D. 实验结束随即用坩埚钳将热的蒸发皿取下放在实验桌上
C
3.下列有关蒸发结晶操作描述正确的是________。
A.当加热至有晶体析出时,即停止加热
B.当蒸发皿中出现较多固体时,即停止加热
C.当水分完全蒸干时,即停止加热
D.蒸发皿应放在石棉网上加热,防止破损
巩固练习
5.【2019·海南】在“粗盐中难溶性杂质的去除”实验中,不需要进行的操作是( )
A.溶解 B.过滤 C.蒸发 D.蒸馏
D
6.【2020·菏泽】在除去粗盐中难溶性杂质的实验中,下列操作正确的是( )
D
7.在“粗盐提纯”实验中,将提纯后的氯化钠与粗盐作比较,以计算精盐的产率。下列可能引起产率偏高的原因是( )
A.粗盐未完全溶解 B.溶解粗盐的烧杯壁上沾有不溶性杂质
C.过滤时液面高于滤纸边缘 D.蒸发时有液滴飞溅出去
C
巩固练习
8.【2019·滨州】结合下图仪器,完成粗盐提纯实验中的有关问题。
(1)仪器②的名称是________。
(2)在过滤粗盐水时,除用到⑤⑥
⑦⑧,还需要用到图中的一种
玻璃仪器是________(填名称)。
(3)蒸发结晶食盐,除用到①②⑧⑨,
还需用到图中的仪器有________(填序号)。
坩埚钳
漏斗
⑥
同课章节目录
