高一化学人教版(2019)必修第一册 第一章第二节 离子反应 第1课时(21张ppt)
文档属性
| 名称 | 高一化学人教版(2019)必修第一册 第一章第二节 离子反应 第1课时(21张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 819.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-12 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第二节 离子反应
2019新教材必修一第一章
第1课时 电解质的电离
学习目标:
1、通过实验、假设、推理等过程,以探究的方式建构电离模型,并以此认识电解质。
2、能用电离方程式表示某些酸、碱、盐的电离过程。
难点:电解质的概念
重点:电解质的概念、电离方程式的书写
导入
生活常识告诉我们,给电器设备通电时,湿手操
作容易发生触电事故。这是为什么呢?
一、电解质
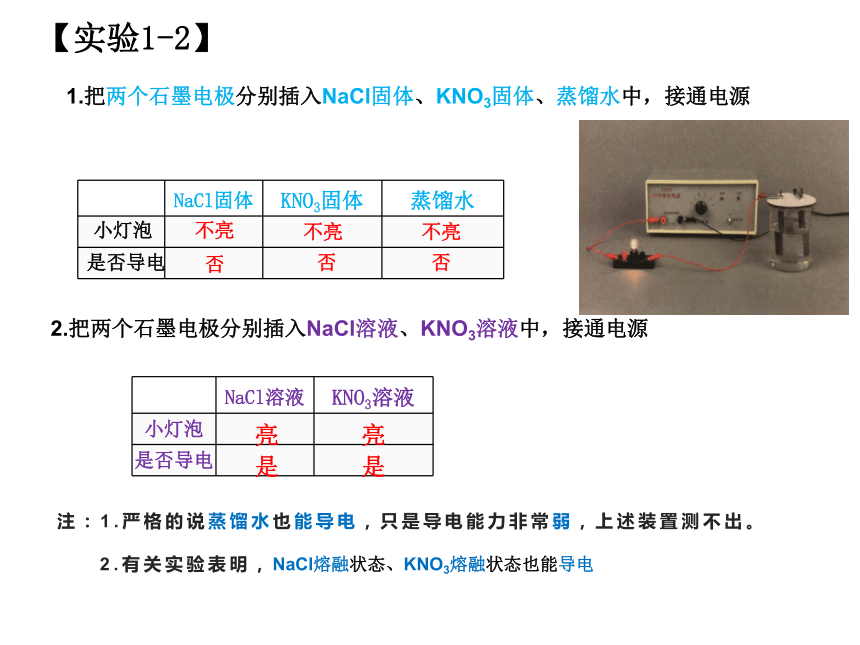
NaCl固体 KNO3固体 蒸馏水
不亮
不亮
不亮
否
否
否
NaCl溶液 KNO3溶液
小灯泡
是否导电
亮
亮
是
是
小灯泡
是否导电
注:1.严格的说蒸馏水也能导电,只是导电能力非常弱,上述装置测不出。
2.有关实验表明,NaCl熔融状态、KNO3熔融状态也能导电
【实验1-2】
1.把两个石墨电极分别插入NaCl固体、KNO3固体、蒸馏水中,接通电源
2.把两个石墨电极分别插入NaCl溶液、KNO3溶液中,接通电源
实验归纳:
1.干燥的NaCl固体、KNO3固体以及蒸馏水都 导电,但是把固体与蒸馏水混合,变成溶液,都能 。
2.初中学过的 、 、 等溶液都能导电。
3. 把固体盐和固体碱加热至 ,也能导电。
不
导电
酸
碱
盐
熔化
电解质的定义:
在水溶液中或熔融状态下能够导电的化合物。
类型:酸、碱、盐、金属氧化物、水
非电解质:在水溶液中和熔融状态下都不导电的化合物。
类型:非金属氧化物(除了H2O)、NH3、大多数有机物
单质和溶液既不是电解质,也不是非电解质
回归生活
1.铁能导电,所以金属是电解质
2.NaCl溶液能导电,NaCl溶液是电解质
3.CO2溶于水能导电,所以CO2是电解质
4.CaCO3难溶于水,所以它是非电解质
5.电解质未必能导电
X
X
X
X
√
随堂测1:
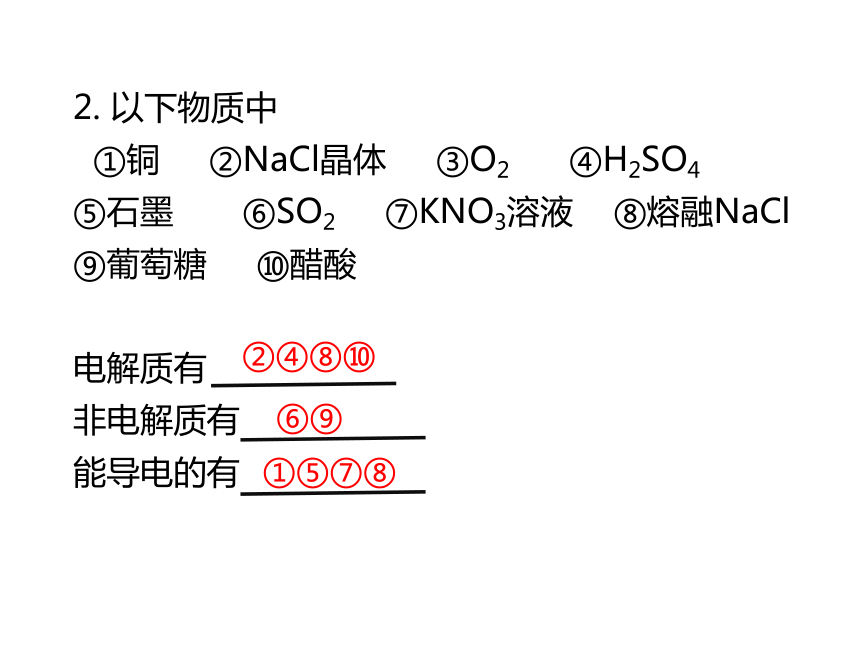
2. 以下物质中
①铜 ②NaCl晶体 ③O2 ④H2SO4 ⑤石墨 ⑥SO2 ⑦KNO3溶液 ⑧熔融NaCl ⑨葡萄糖 ⑩醋酸
电解质有
非电解质有
能导电的有
②④⑧⑩
⑥⑨
①⑤⑦⑧
二、电解质的电离
带电荷的粒子按一定方向移动而形成
能导电的物质必须具有能自由移动的、带电荷的粒子
电流的产生:
物质导电原因分析:
1、石墨、金属单质能导电是因为有自由移动的电子。
2、KNO3溶液、 NaCl溶液、熔融NaCl、熔融KNO3能导电是因为有自由移动的离子
3、固体NaCl、KNO3不导电是因为没有自由移动的离子。
4、自由移动的离子浓度越大,导电能力越强
图1-10 干燥的NaCl固体不导电
Na+和Cl-按一定规则紧密排列,不能自由移动,故而不导电
图析
将NaCl固体加入水中 水分子与NaCl固体作用 NaCl固体溶液
当NaCl溶液中插入电极,接通电源:
Na+向与电源负极相连的电极移动
Cl-向与电源正极相连的电极移动
NaCl固体
熔融NaCl
受热融化
NaCl固体受热熔化时,温度升高,克服了离子间的相互作用,产生自由移动的Na+和Cl-,故而能导电
液态氯化氢HCl、H2SO4、HNO3等不导电,因为是分子型化合物,只有在水中才会电离出离子
1. 电离:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
水溶液中的电离不需要通电,不写条件!
熔融条件下电离要写条件:熔融
2. 电离方程式:用来表示电解质电离的式子
NaCl = Na+ + Cl-
注意:1、要遵守质量守恒、电荷守恒。
2、左边写化学式,右边写离子。
H2SO4 = 2H+ + SO42-
KNO3 = K+ + NO3-
Ca(OH)2= Ca2+ + 2OH-
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
NaOH = Na+ + OH-
Ba(OH)2 = Ba2+ + 2OH-
(NH4)2CO3 = 2NH4+ + CO32-
Al2(SO4)3 == 2Al3+ + 3SO42-
酸:电离出的阳离子全部是H+
碱:电离出的阴离子全部是OH-
盐:电离时产生金属阳离子(或NH4+)和酸根阴离子的化合物
电离
小结
溶于水或
熔融状态
能导电
均不导电
物质
混合物
纯净物
单质
化合物
电解质
非电解质
单质和混合物既不是电解质也不是非电解质
电离方程式
课堂小结:
随堂测2:
1.下列表格中各项分类都正确的一组是( )
纯净物 混合物 电解质 非电解质
A 生理盐水 明矾 液态KNO3 蔗糖
B CaO 海水 铜 乙醇
C 胆矾 铝合金 AgCl CO2
D 氢氧化钠 空气 Na2SO4溶液 食醋
2.下列物质的水溶液能导电,但本身属于非电解质的是( )
A.CH3COOH B.Cl2 C.NH4NO3 D.SO2
C
D
3.下列物质中,既能导电又属于电解质的一组物质是( )A.熔融MgCl2、熔融NaOH B.液氨、石灰水C.石墨、食醋 D.稀硫酸、蔗糖
4.下列物质: ⑴Na⑵ Br2 ⑶Na2O ⑷NO2 ⑸CO2 ⑹ SO3 ⑺NH3 ⑻H2S ⑼HCl ⑽ H2SO4 ⑾Ba(OH)2 ⑿NaCl ⒀蔗糖 ⒁NaCl溶液。属于电解质的是
, 属于非电解质的是 ,能导电的是 。
A
1、14
4、5、6、7、13
3、8、9、10、11、12
6.下列各组物质按单质、电解质、混合物的顺序排列正确的是( )
A.空气,熟石灰,盐酸 B.青铜,纯碱,水玻璃C.石英,二氧化硫,硫酸 D.液氯,烧碱,漂白粉
5.下列物质的分类不正确的是( )
A.水、和干冰都属于氧化物 B.H2SO4、HNO3、H2CO3都属于酸C.烧碱、纯碱(碳酸钠)、熟石灰都属于碱 D.NaHSO4、CuSO4和KMnO4都属于盐
C
D
7.写出HNO3、NaOH、Ba(OH)2、(NH4)2CO3、 Al2(SO4)3的电离方程式
谢谢聆听!~
第二节 离子反应
2019新教材必修一第一章
第1课时 电解质的电离
学习目标:
1、通过实验、假设、推理等过程,以探究的方式建构电离模型,并以此认识电解质。
2、能用电离方程式表示某些酸、碱、盐的电离过程。
难点:电解质的概念
重点:电解质的概念、电离方程式的书写
导入
生活常识告诉我们,给电器设备通电时,湿手操
作容易发生触电事故。这是为什么呢?
一、电解质
NaCl固体 KNO3固体 蒸馏水
不亮
不亮
不亮
否
否
否
NaCl溶液 KNO3溶液
小灯泡
是否导电
亮
亮
是
是
小灯泡
是否导电
注:1.严格的说蒸馏水也能导电,只是导电能力非常弱,上述装置测不出。
2.有关实验表明,NaCl熔融状态、KNO3熔融状态也能导电
【实验1-2】
1.把两个石墨电极分别插入NaCl固体、KNO3固体、蒸馏水中,接通电源
2.把两个石墨电极分别插入NaCl溶液、KNO3溶液中,接通电源
实验归纳:
1.干燥的NaCl固体、KNO3固体以及蒸馏水都 导电,但是把固体与蒸馏水混合,变成溶液,都能 。
2.初中学过的 、 、 等溶液都能导电。
3. 把固体盐和固体碱加热至 ,也能导电。
不
导电
酸
碱
盐
熔化
电解质的定义:
在水溶液中或熔融状态下能够导电的化合物。
类型:酸、碱、盐、金属氧化物、水
非电解质:在水溶液中和熔融状态下都不导电的化合物。
类型:非金属氧化物(除了H2O)、NH3、大多数有机物
单质和溶液既不是电解质,也不是非电解质
回归生活
1.铁能导电,所以金属是电解质
2.NaCl溶液能导电,NaCl溶液是电解质
3.CO2溶于水能导电,所以CO2是电解质
4.CaCO3难溶于水,所以它是非电解质
5.电解质未必能导电
X
X
X
X
√
随堂测1:
2. 以下物质中
①铜 ②NaCl晶体 ③O2 ④H2SO4 ⑤石墨 ⑥SO2 ⑦KNO3溶液 ⑧熔融NaCl ⑨葡萄糖 ⑩醋酸
电解质有
非电解质有
能导电的有
②④⑧⑩
⑥⑨
①⑤⑦⑧
二、电解质的电离
带电荷的粒子按一定方向移动而形成
能导电的物质必须具有能自由移动的、带电荷的粒子
电流的产生:
物质导电原因分析:
1、石墨、金属单质能导电是因为有自由移动的电子。
2、KNO3溶液、 NaCl溶液、熔融NaCl、熔融KNO3能导电是因为有自由移动的离子
3、固体NaCl、KNO3不导电是因为没有自由移动的离子。
4、自由移动的离子浓度越大,导电能力越强
图1-10 干燥的NaCl固体不导电
Na+和Cl-按一定规则紧密排列,不能自由移动,故而不导电
图析
将NaCl固体加入水中 水分子与NaCl固体作用 NaCl固体溶液
当NaCl溶液中插入电极,接通电源:
Na+向与电源负极相连的电极移动
Cl-向与电源正极相连的电极移动
NaCl固体
熔融NaCl
受热融化
NaCl固体受热熔化时,温度升高,克服了离子间的相互作用,产生自由移动的Na+和Cl-,故而能导电
液态氯化氢HCl、H2SO4、HNO3等不导电,因为是分子型化合物,只有在水中才会电离出离子
1. 电离:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
水溶液中的电离不需要通电,不写条件!
熔融条件下电离要写条件:熔融
2. 电离方程式:用来表示电解质电离的式子
NaCl = Na+ + Cl-
注意:1、要遵守质量守恒、电荷守恒。
2、左边写化学式,右边写离子。
H2SO4 = 2H+ + SO42-
KNO3 = K+ + NO3-
Ca(OH)2= Ca2+ + 2OH-
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
NaOH = Na+ + OH-
Ba(OH)2 = Ba2+ + 2OH-
(NH4)2CO3 = 2NH4+ + CO32-
Al2(SO4)3 == 2Al3+ + 3SO42-
酸:电离出的阳离子全部是H+
碱:电离出的阴离子全部是OH-
盐:电离时产生金属阳离子(或NH4+)和酸根阴离子的化合物
电离
小结
溶于水或
熔融状态
能导电
均不导电
物质
混合物
纯净物
单质
化合物
电解质
非电解质
单质和混合物既不是电解质也不是非电解质
电离方程式
课堂小结:
随堂测2:
1.下列表格中各项分类都正确的一组是( )
纯净物 混合物 电解质 非电解质
A 生理盐水 明矾 液态KNO3 蔗糖
B CaO 海水 铜 乙醇
C 胆矾 铝合金 AgCl CO2
D 氢氧化钠 空气 Na2SO4溶液 食醋
2.下列物质的水溶液能导电,但本身属于非电解质的是( )
A.CH3COOH B.Cl2 C.NH4NO3 D.SO2
C
D
3.下列物质中,既能导电又属于电解质的一组物质是( )A.熔融MgCl2、熔融NaOH B.液氨、石灰水C.石墨、食醋 D.稀硫酸、蔗糖
4.下列物质: ⑴Na⑵ Br2 ⑶Na2O ⑷NO2 ⑸CO2 ⑹ SO3 ⑺NH3 ⑻H2S ⑼HCl ⑽ H2SO4 ⑾Ba(OH)2 ⑿NaCl ⒀蔗糖 ⒁NaCl溶液。属于电解质的是
, 属于非电解质的是 ,能导电的是 。
A
1、14
4、5、6、7、13
3、8、9、10、11、12
6.下列各组物质按单质、电解质、混合物的顺序排列正确的是( )
A.空气,熟石灰,盐酸 B.青铜,纯碱,水玻璃C.石英,二氧化硫,硫酸 D.液氯,烧碱,漂白粉
5.下列物质的分类不正确的是( )
A.水、和干冰都属于氧化物 B.H2SO4、HNO3、H2CO3都属于酸C.烧碱、纯碱(碳酸钠)、熟石灰都属于碱 D.NaHSO4、CuSO4和KMnO4都属于盐
C
D
7.写出HNO3、NaOH、Ba(OH)2、(NH4)2CO3、 Al2(SO4)3的电离方程式
谢谢聆听!~
