10.2酸和碱的反应课件(共35张PPT)—2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 10.2酸和碱的反应课件(共35张PPT)—2022-2023学年九年级化学人教版下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-09 00:00:00 | ||
图片预览








文档简介
(共35张PPT)
酸和碱的中和反应
情景引入
蜜蜂与马蜂
蜜蜂
被蜜蜂蛰后,用肥皂水或氨水清洗
马蜂、黄蜂
被马蜂蛰后,用食醋止痛止痒
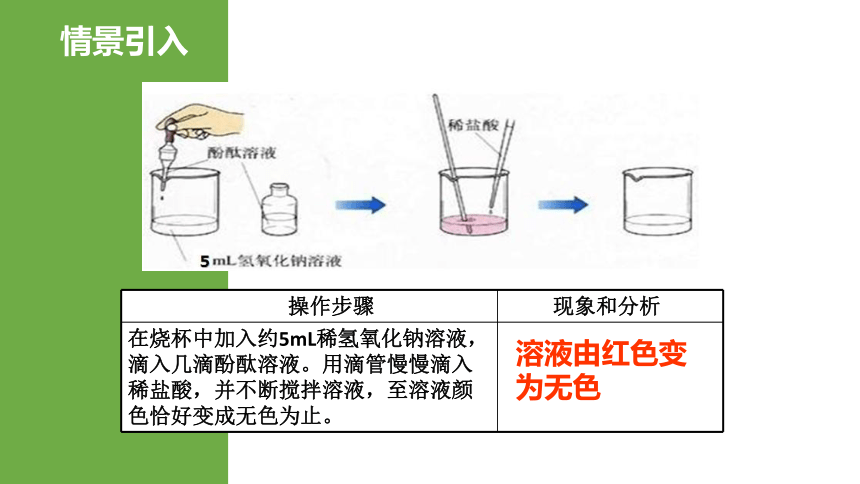
情景引入
操作步骤 现象和分析
在烧杯中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
溶液由红色变为无色
CONTENTS
01
02
酸碱中和反应
pH的测量——pH试纸
01
酸碱中和反应
01
酸碱中和反应
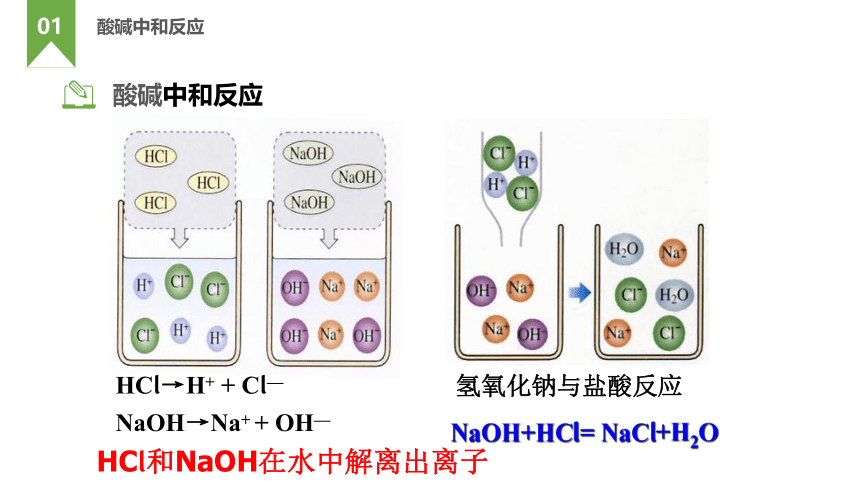
酸碱中和反应
HCl→H+ + Cl—
NaOH→Na+ + OH—
HCl和NaOH在水中解离出离子
氢氧化钠与盐酸反应
NaOH+HCl= NaCl+H2O
01
酸碱中和反应
酸碱中和反应
酸溶液与碱溶液的反应实质是酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。
中和反应实质:H++OH- =H2O
HCl + NaOH = NaCl + H2O
酸 + 碱 → 盐 + 水
中和反应:酸和碱作用生成盐和水的反应
01
酸碱中和反应
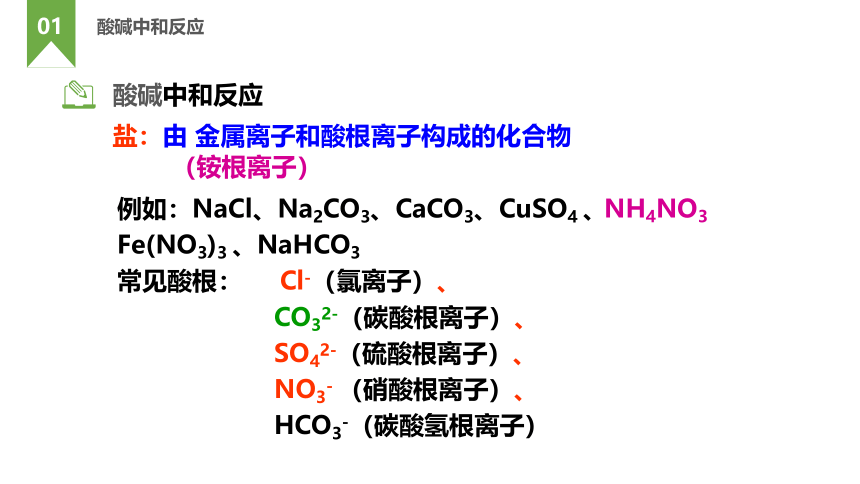
酸碱中和反应
盐:由 金属离子和酸根离子构成的化合物
例如:NaCl、Na2CO3、CaCO3、CuSO4 、Fe(NO3)3 、NaHCO3
常见酸根: Cl-(氯离子)、
CO32-(碳酸根离子)、
SO42-(硫酸根离子)、
NO3- (硝酸根离子)、
HCO3-(碳酸氢根离子)
(铵根离子)
NH4NO3
01
酸碱中和反应
酸碱中和反应
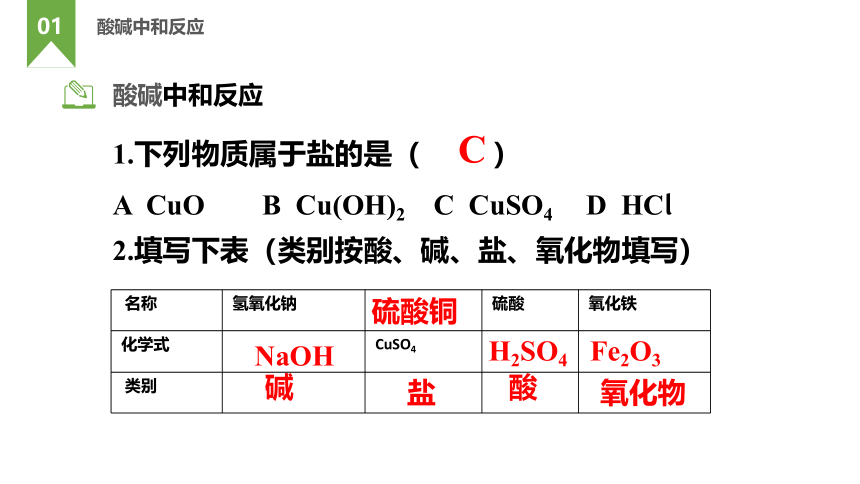
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A CuO B Cu(OH)2 C CuSO4 D HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
C
NaOH
碱
硫酸铜
盐
H2SO4
酸
Fe2O3
氧化物
01
酸碱中和反应
酸碱中和反应
3、下列反应属于中和反应的是
A.CuO+H2SO4=CuSO4+H2O
B.Ca(OH)2+2HCl=CaCl2+2H2O
C.2NaOH+SO2=Na2SO3+H2O
D.2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【解析】选B。酸和碱作用生成盐和水的反应,叫中和反应。A中CuO不是碱;C中SO2不是酸;D中CuSO4是盐。故选项B符合题意。
01
酸碱中和反应
酸碱中和反应在生活中的应用
●改良酸性土壤
●处理工厂废水
●用于医药
中和胃酸
防蚊虫叮咬(止痒)
01
酸碱中和反应
酸碱中和反应在生活中的应用
●改良酸性土壤
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,于是人们将适量的熟石灰(消石灰)加入土壤,以中和酸性
能用生石灰代替熟石灰吗?为什么?
可以:CaO+H2O=Ca(OH)2
如果土壤显碱性?
用熟石灰(消石灰)改良酸性土壤,也可用生石灰代替
01
酸碱中和反应
酸碱中和反应在生活中的应用
●处理工厂废水
硫酸厂排出的废水中含有硫酸等物质
化学方程式:
Ca(OH)2+H2SO4= CaSO4+2H2O
用熟石灰进行中和处理
印染厂的废水呈碱性
可加入硫酸进行中和
01
酸碱中和反应
酸碱中和反应在生活中的应用
●用于医药
盐酸
氢氧化铝
化学方程式: Al(OH)3 + 3HCl = AlCl3 + 3H2O
氢氧化铝能中和胃酸
胃酸的主要成分是
胃乐胶囊的主要成分
也可用Mg(OH)2中和胃酸
Mg(OH)2 +2HCl = MgCl2+ 2H2O
01
酸碱中和反应
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胃 乐
胶
囊
01
酸碱中和反应
酸碱中和反应在生活中的应用
涂一些含有碱性物质减轻痛痒,如被蚊虫叮咬后,由于蚊虫分泌的蚁酸呈酸性,可用一些碱性的物质如稀氨水、肥皂水、牙膏等涂抹患处,它们与蚁酸发生中和反应,将蚁酸反应掉,以减轻痛痒;如不小心被黄蜂刺到,由于黄蜂的刺是碱性的,可在皮肤上涂抹酸性物质如醋酸,以减轻痛痒。
02
pH的测量
02
pH的测量——pH试纸
回顾:如何判断溶液酸碱性?
溶液的酸碱性:表示溶液是酸性还是碱性的。
用酸碱指示剂测出。
溶液的酸碱度:表示溶液酸碱性的强弱程度。
用pH试纸测出。
那么如何表示溶液酸碱性的强弱程度呢?
测定溶液的酸碱性可用指示剂或pH试纸。但测定溶液的酸碱度,只能用pH试纸(或pH计等)。
02
pH的测量——pH试纸
pH
pH试纸
测定pH最简便的方法是使用pH试纸
02
pH的测量——pH试纸
pH
pH和溶液的酸碱性
1. pH的通常范围: 0---14
2. pH值与溶液酸碱性的关系:
酸碱度 酸碱性
pH < 7 溶液呈酸性 pH越小,酸性越强
pH = 7 溶液呈中性
pH > 7 溶液呈碱性 pH越大,碱性越强
02
pH的测量——pH试纸
pH
身边常见物质的pH
02
pH的测量——pH试纸
pH
某溶液pH=0,则该溶液
(A)呈酸性 (B)呈碱性
(C)呈中性 (D)无法判断酸碱性
人体内一些液体的近似pH值如下:血浆
7.35~7.45,胆汁7.1~7.3,胰液7.5~8.0,胃液0.9~1.5,其中一种液体呈酸性,该液体是
(A)血浆 (B)胆汁 (C)胰液 (D)胃液
A
D
02
pH的测量——pH试纸
pH
已知苹果汁的近似pH值为2.9~3.3,在苹果汁中滴入紫色石蕊试液,显示的颜色是 ( )
(A)无色 (B)红色 (C)蓝色 (D)紫色
B
下列各pH值表示溶液酸性最强的是
(A)pH=14 (B)pH=7
(C)pH=1 (D)pH=0
D
02
pH的测量——pH试纸
pH的测定
02
pH的测量——pH试纸
pH的测定
pH值的测定---pH试纸
在玻璃片或白瓷板或表面皿上放一小片试纸,用洁净干燥的玻璃棒蘸取被测溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,颜色最为接近的即为pH值。
02
pH的测量——pH试纸
活动与探究:用pH试纸测定一些溶液的pH
①测定几种酸或碱的稀溶液的pH
pH pH pH pH
稀盐酸 稀硫酸 氢氧化钠溶液 氯化钠溶液
pH 酸碱性 pH 酸碱性
橘汁 汽水
糖水 自来水
牛奶 唾液
番茄汁 草木灰水
肥皂水 洗洁精
②测定生活中的一些物质的pH,说明它们的酸碱性(课外作业)
1
1
13
4
7
6-7
4
6-7
6
8
7-8
8
6-7
弱酸性
弱酸性
弱酸性
弱酸性
弱酸性
弱酸性
接近中性
弱碱性
弱碱性
弱碱性
7
02
pH的测量——pH试纸
pH的测定
下列测定溶液pH值的方法正确的是( )
A、将pH试纸伸入试剂中,用所显示的颜色与标准比色卡对照
B、先将pH试纸湿润,再用玻璃棒蘸取被测溶液滴在试纸上,用所显示的颜色与标准比色卡对照
C、用玻璃棒蘸取被测溶液滴在试纸上,用所显示的颜色与标准比色卡对照
D、以上都可以
C
02
pH的测量——pH试纸
pH的测定
用pH试纸测定稀氨水的pH值,第一次把稀氨水滴在pH试纸上,测得的pH值为12,第二次先将pH试纸用水润湿后,再把稀氨水滴在pH试纸上,则测得的pH值将( )
A、大于12 B、小于12
C、等于12 D、无法确定
B
用pH试纸测定白醋的酸碱度时,如果先将试纸用蒸馏水湿润,再把白醋滴到试纸上,则测得的结果与白醋实际的pH比较
A.偏低 B.偏高 C.相等 D.无法比较
√
02
pH的测量——pH试纸
pH的测定
酸性溶液 (pH<7) 中性溶液 (pH=7) 碱性溶液
(pH>7)
石蕊试液
酚酞试液
红色
紫色
蓝色
红色
无色
无色
02
pH的测量——pH试纸
pH的测定
酸 碱
加水稀释
加酸
加碱
改变溶液pH的方法:
pH增大,但永远小于7
pH减小,但永远大于7
pH由大于7减小到小于7
pH在两种碱之间
pH在两种酸之间
pH由小于7增大到大于7
02
pH的测量——pH试纸
pH的测定
4、测定人体内或排出的液体的pH可以了解人体的健康状况。
1、化工生产中许多反应必须在一定的pH溶液中才能进行
2、在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长
3、测定雨水的pH可以了解空气的污染情况;
了解溶液酸碱度有何重要意义?
正常雨水的pH约为5.6,酸雨的pH小于5.6
胃酸的pH小于7
02
pH的测量——pH试纸
pH的测定
资料
人体内的一些液体和排泄物的正常pH范围:
血浆 7.35-7.45
唾液 6.6-7.1
胃液 0.9-1.5
乳汁 6.6-7.6
胆汁 7.1-7.3
胰液 7.5-8.0
尿液 4.7-8.4
粪便 4.6-8.4
03
常见的酸与碱
练一练
1、下列实验记录合理的是( )
A.用pH试纸测得某碱溶液的pH为12
B.用pH试纸测得某碱溶液的pH为8.1
C.用100ml烧杯量取7.5ml蒸馏水
D.用托盘天平称取10.15g NaCl
A
2、常温时测得鸡蛋清的近似pH为7.6 ~ 8.0,对它酸碱性的判断正确的是( )
A.呈酸性 B.呈碱性
C.呈中性 D.无法判断
B
03
常见的酸与碱
练一练
3、一些食物的近似pH如下:番茄4.0-4.4,苹果是2.9-3.3,牛奶是6.3-6.6,蛋清是7.6-8.0,下列说法不正确的是( )
A.胃酸过多的人应少食苹果 B.番茄汁属酸性食品
C.牛奶和鸡蛋清均属碱性食品 D.苹果汁酸性比牛奶强
4、二氧化碳饱和溶液的pH=5.6,酸性比其强的雨水称为酸雨。一场雨后从A地测得雨水的pH=4,B地测得雨水的pH=6.6,则( )
A.A地是酸雨 B.B地是酸雨
C.均是酸雨 D.都不是酸雨
C
A
感谢您的观看
END
酸和碱的中和反应
情景引入
蜜蜂与马蜂
蜜蜂
被蜜蜂蛰后,用肥皂水或氨水清洗
马蜂、黄蜂
被马蜂蛰后,用食醋止痛止痒
情景引入
操作步骤 现象和分析
在烧杯中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
溶液由红色变为无色
CONTENTS
01
02
酸碱中和反应
pH的测量——pH试纸
01
酸碱中和反应
01
酸碱中和反应
酸碱中和反应
HCl→H+ + Cl—
NaOH→Na+ + OH—
HCl和NaOH在水中解离出离子
氢氧化钠与盐酸反应
NaOH+HCl= NaCl+H2O
01
酸碱中和反应
酸碱中和反应
酸溶液与碱溶液的反应实质是酸溶液中的氢离子与碱中的氢氧根离子结合生成了水。
中和反应实质:H++OH- =H2O
HCl + NaOH = NaCl + H2O
酸 + 碱 → 盐 + 水
中和反应:酸和碱作用生成盐和水的反应
01
酸碱中和反应
酸碱中和反应
盐:由 金属离子和酸根离子构成的化合物
例如:NaCl、Na2CO3、CaCO3、CuSO4 、Fe(NO3)3 、NaHCO3
常见酸根: Cl-(氯离子)、
CO32-(碳酸根离子)、
SO42-(硫酸根离子)、
NO3- (硝酸根离子)、
HCO3-(碳酸氢根离子)
(铵根离子)
NH4NO3
01
酸碱中和反应
酸碱中和反应
名称 氢氧化钠 硫酸 氧化铁
化学式 CuSO4
类别
1.下列物质属于盐的是( )
A CuO B Cu(OH)2 C CuSO4 D HCl
2.填写下表(类别按酸、碱、盐、氧化物填写)
C
NaOH
碱
硫酸铜
盐
H2SO4
酸
Fe2O3
氧化物
01
酸碱中和反应
酸碱中和反应
3、下列反应属于中和反应的是
A.CuO+H2SO4=CuSO4+H2O
B.Ca(OH)2+2HCl=CaCl2+2H2O
C.2NaOH+SO2=Na2SO3+H2O
D.2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【解析】选B。酸和碱作用生成盐和水的反应,叫中和反应。A中CuO不是碱;C中SO2不是酸;D中CuSO4是盐。故选项B符合题意。
01
酸碱中和反应
酸碱中和反应在生活中的应用
●改良酸性土壤
●处理工厂废水
●用于医药
中和胃酸
防蚊虫叮咬(止痒)
01
酸碱中和反应
酸碱中和反应在生活中的应用
●改良酸性土壤
植物需要在一定酸碱性的土壤中生长,但近年来由于不合理使用化肥,或酸雨的形成,破坏土壤的酸碱性,不利于植物的生长,于是人们将适量的熟石灰(消石灰)加入土壤,以中和酸性
能用生石灰代替熟石灰吗?为什么?
可以:CaO+H2O=Ca(OH)2
如果土壤显碱性?
用熟石灰(消石灰)改良酸性土壤,也可用生石灰代替
01
酸碱中和反应
酸碱中和反应在生活中的应用
●处理工厂废水
硫酸厂排出的废水中含有硫酸等物质
化学方程式:
Ca(OH)2+H2SO4= CaSO4+2H2O
用熟石灰进行中和处理
印染厂的废水呈碱性
可加入硫酸进行中和
01
酸碱中和反应
酸碱中和反应在生活中的应用
●用于医药
盐酸
氢氧化铝
化学方程式: Al(OH)3 + 3HCl = AlCl3 + 3H2O
氢氧化铝能中和胃酸
胃酸的主要成分是
胃乐胶囊的主要成分
也可用Mg(OH)2中和胃酸
Mg(OH)2 +2HCl = MgCl2+ 2H2O
01
酸碱中和反应
胃乐说明书
[药品名称] 胃乐胶囊
[性状] 本品为胶囊剂,内容物为灰黄棕色,气味香,味微苦
[主要成分] 氢氧化铝[Al(OH)3]、甘草提取物、白芨、木香等
[药理作用] 中和胃酸过多、抗溃疡、镇痛、抗炎
[功能与主治] 用于慢性胃炎胃酸和多酸胃痛。行气止痛,收敛生肌,促进溃疡愈合。用于胃胀闷疼痛,嗳气泛酸,恶心呕吐,气滞引起的胃腕疼痛。
[用法与用量] 口服,一次2~3粒,一日3次,空腹服用
[规格] 0.4g/粒
[贮藏] 密封,置干燥阴凉处
[包装] 20粒/盒
[有效期] 两年
胃 乐
胶
囊
01
酸碱中和反应
酸碱中和反应在生活中的应用
涂一些含有碱性物质减轻痛痒,如被蚊虫叮咬后,由于蚊虫分泌的蚁酸呈酸性,可用一些碱性的物质如稀氨水、肥皂水、牙膏等涂抹患处,它们与蚁酸发生中和反应,将蚁酸反应掉,以减轻痛痒;如不小心被黄蜂刺到,由于黄蜂的刺是碱性的,可在皮肤上涂抹酸性物质如醋酸,以减轻痛痒。
02
pH的测量
02
pH的测量——pH试纸
回顾:如何判断溶液酸碱性?
溶液的酸碱性:表示溶液是酸性还是碱性的。
用酸碱指示剂测出。
溶液的酸碱度:表示溶液酸碱性的强弱程度。
用pH试纸测出。
那么如何表示溶液酸碱性的强弱程度呢?
测定溶液的酸碱性可用指示剂或pH试纸。但测定溶液的酸碱度,只能用pH试纸(或pH计等)。
02
pH的测量——pH试纸
pH
pH试纸
测定pH最简便的方法是使用pH试纸
02
pH的测量——pH试纸
pH
pH和溶液的酸碱性
1. pH的通常范围: 0---14
2. pH值与溶液酸碱性的关系:
酸碱度 酸碱性
pH < 7 溶液呈酸性 pH越小,酸性越强
pH = 7 溶液呈中性
pH > 7 溶液呈碱性 pH越大,碱性越强
02
pH的测量——pH试纸
pH
身边常见物质的pH
02
pH的测量——pH试纸
pH
某溶液pH=0,则该溶液
(A)呈酸性 (B)呈碱性
(C)呈中性 (D)无法判断酸碱性
人体内一些液体的近似pH值如下:血浆
7.35~7.45,胆汁7.1~7.3,胰液7.5~8.0,胃液0.9~1.5,其中一种液体呈酸性,该液体是
(A)血浆 (B)胆汁 (C)胰液 (D)胃液
A
D
02
pH的测量——pH试纸
pH
已知苹果汁的近似pH值为2.9~3.3,在苹果汁中滴入紫色石蕊试液,显示的颜色是 ( )
(A)无色 (B)红色 (C)蓝色 (D)紫色
B
下列各pH值表示溶液酸性最强的是
(A)pH=14 (B)pH=7
(C)pH=1 (D)pH=0
D
02
pH的测量——pH试纸
pH的测定
02
pH的测量——pH试纸
pH的测定
pH值的测定---pH试纸
在玻璃片或白瓷板或表面皿上放一小片试纸,用洁净干燥的玻璃棒蘸取被测溶液滴在pH试纸上,把试纸显示的颜色与标准比色卡对照,颜色最为接近的即为pH值。
02
pH的测量——pH试纸
活动与探究:用pH试纸测定一些溶液的pH
①测定几种酸或碱的稀溶液的pH
pH pH pH pH
稀盐酸 稀硫酸 氢氧化钠溶液 氯化钠溶液
pH 酸碱性 pH 酸碱性
橘汁 汽水
糖水 自来水
牛奶 唾液
番茄汁 草木灰水
肥皂水 洗洁精
②测定生活中的一些物质的pH,说明它们的酸碱性(课外作业)
1
1
13
4
7
6-7
4
6-7
6
8
7-8
8
6-7
弱酸性
弱酸性
弱酸性
弱酸性
弱酸性
弱酸性
接近中性
弱碱性
弱碱性
弱碱性
7
02
pH的测量——pH试纸
pH的测定
下列测定溶液pH值的方法正确的是( )
A、将pH试纸伸入试剂中,用所显示的颜色与标准比色卡对照
B、先将pH试纸湿润,再用玻璃棒蘸取被测溶液滴在试纸上,用所显示的颜色与标准比色卡对照
C、用玻璃棒蘸取被测溶液滴在试纸上,用所显示的颜色与标准比色卡对照
D、以上都可以
C
02
pH的测量——pH试纸
pH的测定
用pH试纸测定稀氨水的pH值,第一次把稀氨水滴在pH试纸上,测得的pH值为12,第二次先将pH试纸用水润湿后,再把稀氨水滴在pH试纸上,则测得的pH值将( )
A、大于12 B、小于12
C、等于12 D、无法确定
B
用pH试纸测定白醋的酸碱度时,如果先将试纸用蒸馏水湿润,再把白醋滴到试纸上,则测得的结果与白醋实际的pH比较
A.偏低 B.偏高 C.相等 D.无法比较
√
02
pH的测量——pH试纸
pH的测定
酸性溶液 (pH<7) 中性溶液 (pH=7) 碱性溶液
(pH>7)
石蕊试液
酚酞试液
红色
紫色
蓝色
红色
无色
无色
02
pH的测量——pH试纸
pH的测定
酸 碱
加水稀释
加酸
加碱
改变溶液pH的方法:
pH增大,但永远小于7
pH减小,但永远大于7
pH由大于7减小到小于7
pH在两种碱之间
pH在两种酸之间
pH由小于7增大到大于7
02
pH的测量——pH试纸
pH的测定
4、测定人体内或排出的液体的pH可以了解人体的健康状况。
1、化工生产中许多反应必须在一定的pH溶液中才能进行
2、在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长
3、测定雨水的pH可以了解空气的污染情况;
了解溶液酸碱度有何重要意义?
正常雨水的pH约为5.6,酸雨的pH小于5.6
胃酸的pH小于7
02
pH的测量——pH试纸
pH的测定
资料
人体内的一些液体和排泄物的正常pH范围:
血浆 7.35-7.45
唾液 6.6-7.1
胃液 0.9-1.5
乳汁 6.6-7.6
胆汁 7.1-7.3
胰液 7.5-8.0
尿液 4.7-8.4
粪便 4.6-8.4
03
常见的酸与碱
练一练
1、下列实验记录合理的是( )
A.用pH试纸测得某碱溶液的pH为12
B.用pH试纸测得某碱溶液的pH为8.1
C.用100ml烧杯量取7.5ml蒸馏水
D.用托盘天平称取10.15g NaCl
A
2、常温时测得鸡蛋清的近似pH为7.6 ~ 8.0,对它酸碱性的判断正确的是( )
A.呈酸性 B.呈碱性
C.呈中性 D.无法判断
B
03
常见的酸与碱
练一练
3、一些食物的近似pH如下:番茄4.0-4.4,苹果是2.9-3.3,牛奶是6.3-6.6,蛋清是7.6-8.0,下列说法不正确的是( )
A.胃酸过多的人应少食苹果 B.番茄汁属酸性食品
C.牛奶和鸡蛋清均属碱性食品 D.苹果汁酸性比牛奶强
4、二氧化碳饱和溶液的pH=5.6,酸性比其强的雨水称为酸雨。一场雨后从A地测得雨水的pH=4,B地测得雨水的pH=6.6,则( )
A.A地是酸雨 B.B地是酸雨
C.均是酸雨 D.都不是酸雨
C
A
感谢您的观看
END
同课章节目录
