第七章第二节 乙烯与有机高分子材料第1课时 乙烯 课件(共82张PPT)
文档属性
| 名称 | 第七章第二节 乙烯与有机高分子材料第1课时 乙烯 课件(共82张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-12 00:00:00 | ||
图片预览









文档简介
(共82张PPT)
第二节 乙烯与有机高
分子材料
第1课时 乙烯
第7章 有机化合物
【课程标准要求】
1.掌握乙烯的组成及结构特点。
2.掌握乙烯的化学性质,知道氧化、加成、聚合反应等有机反应类型。
3.了解乙烯在生产及生活中的应用。
新知自主预习
课堂互动探究
课时训练
目
录
CONTENTS
///////
///////
///////
课堂小结·即时达标
///////
一、乙烯的组成结构、物理性质
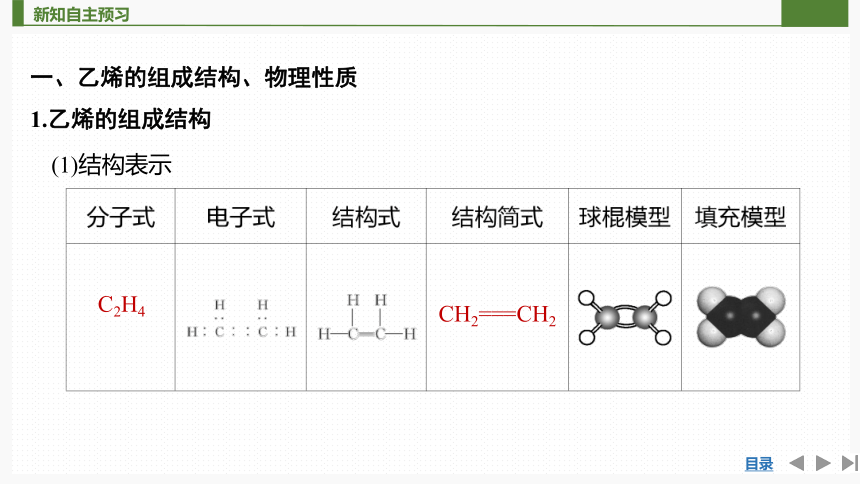
1.乙烯的组成结构
(1)结构表示
C2H4
CH2===CH2
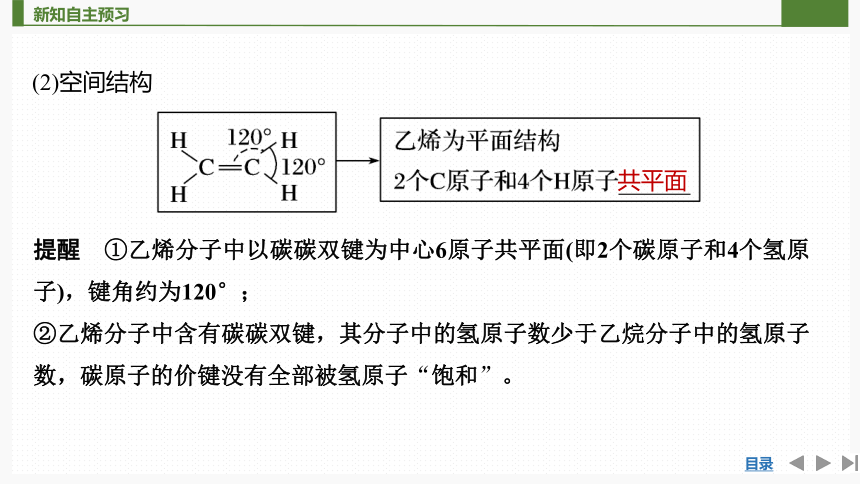
(2)空间结构
提醒 ①乙烯分子中以碳碳双键为中心6原子共平面(即2个碳原子和4个氢原子),键角约为120°;
②乙烯分子中含有碳碳双键,其分子中的氢原子数少于乙烷分子中的氢原子数,碳原子的价键没有全部被氢原子“饱和”。
共平面
2.物理性质
乙烯是一种________,稍有气味,________溶于水,密度比空气________的气体。
无色
难
略小
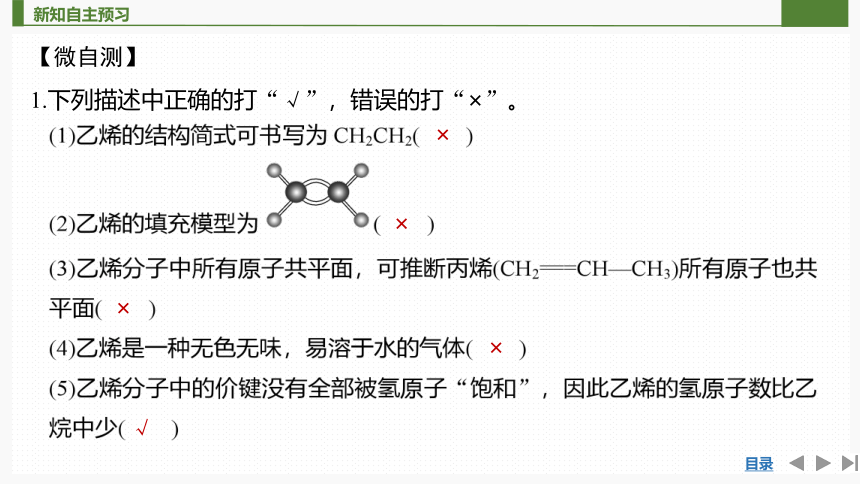
【微自测】
1.下列描述中正确的打“√”,错误的打“×”。
×
×
×
×
√
二、乙烯的化学性质及用途
1.乙烯的化学性质
(1)乙烯的氧化反应
①燃烧:乙烯能在空气中燃烧,火焰________且伴有________,生成二氧化碳和水,同时放出大量的热。化学方程式为____________________________。
②被高锰酸钾等强氧化剂氧化:乙烯能使酸性高锰酸钾溶液________。
明亮
黑烟
褪色
(2)乙烯的加成反应
反应 化学方程式
与Br2加成
与H2加成
与HCl加成
与H2O加成
CH2===CH2+Br2―→CH2BrCH2Br
(3)聚合反应
①乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为:
__________________________________________________________________。
②聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
加聚反应:聚合反应同时也是____________,这样的反应又称为加聚反应。
加成反应
③聚合物 :________反应生成的高分子。
聚合
CH2===CH2
—CH2—CH2—
n
2.乙烯的用途
(1)乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。乙烯的产量可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中可以调节____________。
植物生长
【微自测】
2.①②是两种常见烃的球棍模型,则下列叙述正确的是( )
A.都能在空气中燃烧
B.都能使酸性高锰酸钾溶液褪色
C.都能发生加成反应
D.等质量的①②完全燃烧时,产生CO2的量相同
A
解析 由题图可知,①为乙烷,②为乙烯。乙烷不能使酸性高锰酸钾溶液褪色,而乙烯能,B项错误;乙烷不能发生加成反应,而乙烯能,C项错误;乙烷和乙烯的摩尔质量不同,等质量时二者的物质的量不同,产生CO2的量也不同,D项错误。
二、乙烯加成反应原理探究
一、乙烯氧化反应原理探究
一、乙烯氧化反应原理探究
实验操作:
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
———————【活动探究】———————
实验装置:
乙烯与高锰酸钾反应
1.能用点燃的方法鉴别甲烷和乙烯两种气体吗?
提示:可以。甲烷燃烧火焰是淡蓝色的,乙烯燃烧火焰明亮且伴有黑烟,二者燃烧时的现象不同。
2.为什么甲烷燃烧没有黑烟,而乙烯燃烧有黑烟?
提示:乙烯燃烧时有黑烟是因为乙烯分子里含碳量(约85.7%)比较大,未完全燃烧,产生碳的小颗粒造成的。
3.能用酸性高锰酸钾溶液鉴别甲烷和乙烯吗?能用酸性高锰酸钾溶液除去甲烷中的乙烯吗?
提示:能用酸性高锰酸钾溶液鉴别甲烷和乙烯,甲烷不能使高锰酸钾溶液褪色,乙烯可以使高锰酸钾溶液褪色。但不能用高锰酸钾除去甲烷中的乙烯,因为乙烯被高锰酸钾氧化为CO2,甲烷中又引入新的杂质。
乙烯氧化反应的原理
———————【核心归纳】———————
反应 产物 断裂化学键
燃烧 CO2和H2O 所有碳碳键和碳氢键
与酸性高锰酸钾溶液 乙烯被氧化为CO2,高锰酸钾被还原为Mn2+ 碳碳双键和碳氢键都被破坏
1.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
解析 水果释放出的乙烯是催熟剂,用KMnO4溶液来吸收乙烯,防止水果早熟。
———————【实践应用】———————
C
2.下列关于乙烯的叙述中错误的是( )
A.乙烯使酸性KMnO4溶液褪色,属于氧化反应
B.乙烯燃烧时,火焰明亮且伴有黑烟
C.乙烯可做香蕉等水果的催熟剂
D.被高锰酸钾氧化时,乙烯碳碳双键中的一个键断裂
解析 被高锰酸钾氧化时,乙烯中碳碳双键都断裂。
D
二、乙烯加成反应原理探究
实验素材1
实验步骤:将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
———————【活动探究】———————
实验装置:
乙烯与溴反应
实验素材2
聚乙烯的分子结构模型(局部)
1.乙烯分别通入溴水和溴的四氯化碳中,现象相同吗?
提示:不完全相同,溶液都褪色,但是前者溶液分层,下层是油状液体,而后者溶液不分层。
2.传统乙烯的工业制备是通过丁烷高温裂解进行,产物是乙烷和乙烯的混合物。在合适条件下,可通入H2以除去乙烷中的乙烯吗?
提示:乙烯与氢气反应生成乙烷需要加热和催化剂存在,反应很难进行,且过量的氢气难以除去。
3.如何除去乙烷中的乙烯气体?如何鉴别乙烷和乙烯?
提示:将混合气体通过足量的溴水,乙烯生成液态的1,2-二溴乙烷,从而除去乙烯。
乙烯与乙烷的鉴别方法有以下三种。方法一:将两种气体分别通入溴水(或溴的四氯化碳溶液)中;溶液褪色的为乙烯,溶液不褪色的为乙烷。方法二:将两种气体分别通入酸性KMnO4溶液中;溶液褪色的为乙烯,溶液不褪色的为乙烷。方法三:点燃两种气体,火焰较明亮,有黑烟的为乙烯,另一种为乙烷。
4.用乙烷(CH3CH3)和Cl2反应可以制取氯乙烷(CH3CH2Cl),用乙烯 (CH2===CH2)和HCl反应也能制取氯乙烷,两种方法哪种更好?
提示:用C2H4和HCl反应制取更好。乙烷和Cl2发生的是取代反应,生成物中除CH3CH2Cl外,还有C2H4Cl2、C2H3Cl3、C2H2Cl4、C2HCl5、C2Cl6,生成物不纯,产率低。CH2===CH2和HCl发生的是加成反应,无副反应,生成物只有CH3CH2Cl。
5.丙烯与乙烯互为同系物,由乙烯的结构和性质推测丙烯(CH2===CH—CH3)与HCl在一定条件下能加成的产物有几种?写出结构简式。
1.加成反应原理分析(以CH2===CH2和Br2加成为例)
———————【核心归纳】———————
2.乙烯加聚反应的示意图
3.乙烯与常见物质的加成反应
4.加聚反应
注意 (1)单烯烃的聚合物中碳碳之间是单键,不存在碳碳双键,不具备碳碳双键的性质。
(2)高分子化合物虽被称为“化合物”,但由于高分子化合物中的n不同,所以高分子化合物均为混合物,而不是纯净物。
3.(2021·郑州柘城第二高级中学检测)下列各反应不属于加成反应的是( )
解析 D项中反应为取代反应。
———————【实践应用】———————
D
4.(2021·潍坊高一检测)下列物质不可能是乙烯的加成产物的是( )
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
解析 A项,乙烯与氢气的加成产物是CH3CH3,不符合题意;B项,CH3CHCl2不可能是乙烯的加成产物,符合题意;C项,CH3CH2OH是乙烯与水的加成产物,不符合题意;D项,CH3CH2Br是乙烯与HBr的加成产物,不符合题意。
B
核心体系建构
1.苏轼的《格物粗谈》中有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( )
B
A.氧气 B.乙烯
C.生长素 D.甲烷
解析 乙烯具有催熟作用,因此“气”指的是乙烯。
C
2.下列说法错误的是( )
A.乙烯能使酸性KMnO4溶液褪色
B.将四氯化碳滴入溴水中,振荡后水层接近无色
C.乙烯使溴的四氯化碳溶液褪色是因萃取所致
D.乙烯易发生加成反应
解析 A项,乙烯使酸性KMnO4溶液褪色,是由于乙烯发生了氧化反应,正确;B项,四氯化碳使溴水变成无色,是发生了萃取,是物理变化,由于溴易溶于四氯化碳,从而使水层接近无色,正确;C项,乙烯使溴的四氯化碳溶液褪色是发生了加成反应,是化学变化,错误;D项,乙烯能与多种物质发生加成反应,正确。
A
3. 下列有关乙烯的说法,其中错误的是( )
D
4.(2021·成都高一检测)某课外活动小组设计了以下四种方案除去乙烷中混有的少量乙烯,并得到纯净干燥的乙烷,合理的是( )
A.①②④ B.①②③ C.②③④ D.①②③④
解析 ①和②C2H4与Br2发生加成反应生成液态1,2-二溴乙烷而除去C2H4,①NaOH溶液除去挥发出来的Br2蒸气,浓硫酸除去水蒸气,②碱石灰除去挥发出来的Br2蒸气和水蒸气,①和②均正确;③和④酸性KMnO4溶液将C2H4氧化为CO2,NaOH溶液和碱石灰都能吸收CO2,浓硫酸和碱石灰都能吸收水蒸气,③和④也正确。
5.乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的主要化学性质,实验装置如图所示。
(1)用化学方程式解释B装置中的实验现象:__________________________。
(2)C装置中的现象是_____________________________________________,
其发生反应的类型是____________________________________________。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填字母)中的实验现象可判断该资料是否真实。
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是________(填字母,下同);除去甲烷中乙烯的方法是________。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
答案 (1)CH2===CH2+Br2―→CH2BrCH2Br (2)酸性高锰酸钾溶液褪色 氧化还原反应 (3)D (4)BC B
一、选择题(每小题只有一个选项符合题意)
1.下列关于乙烯结构与性质的叙述中,错误的是( )
B
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应使其褪色
C.乙烯与溴的四氯化碳溶液发生加成反应
D.乙烯分子的一氯代物只有一种结构
解析 B项发生的是氧化反应而不是加成反应。
2.(2021·宾阳中学高一期中)下列有关乙烯燃烧的说法中,正确的是( )
C
A.乙烯燃烧时的现象与氢气燃烧时的现象完全一致
B.乙烯燃烧时的现象与甲烷燃烧时的现象完全一致
C.乙烯燃烧放出大量的热,可作为燃料
D.乙烯燃烧时产生等质量的水和二氧化碳
解析 A.乙烯燃烧火焰明亮,并伴有黑烟,氢气燃烧时产生淡蓝色的火焰,故A错误;B.甲烷含碳量低,燃烧时没有黑烟,乙烯燃烧火焰明亮,并伴有黑烟,故B错误;C.乙烯燃烧放出大量的热,可作为燃料,故C正确;D.乙烯分子中碳与氢的物质的量之比为1∶2,燃烧时产生等物质的量的水和二氧化碳,故D错误。
3.下列有关甲烷和乙烯的说法正确的是( )
C
选项 反应物 反应类型 反应条件
A 甲烷与氯气 取代反应 点燃
B 乙烯与溴水 加成反应 光照
C 甲烷与氧气 氧化反应 点燃
D 乙烯与氧气 氧化反应 光照
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
C
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
解析 分子中的碳氢原子个数比只能说明烃的组成,不能说明其结构特点;燃烧产物的物质的量相等和被酸性KMnO4溶液氧化,不能说明乙烯分子中含有一个碳碳双键;1 mol乙烯只能与1 mol溴单质加成,说明乙烯分子中含有一个碳碳双键。
5.(2021·广东实验中学高一期中)检验乙烷中是否混有少量乙烯的正确方法为( )
D
A.将气体点燃 B.将气体通入浓硫酸
C.将气体通入H2O D.将气体通入酸性KMnO4溶液
解析 A.将气体点燃,乙烷也能燃烧,故A错误;B.将气体通入浓硫酸,两者均不反应,故B错误;C.将气体通入H2O,两者均难溶于水,故C错误;D.将气体通入酸性KMnO4溶液,乙烯能使酸性KMnO4溶液褪色,而乙烷不能,现象不同可检验,故D正确;故选D。
6.(2021·浙江杭州市高一期中)乙烯是一种重要的化工原料。下列物质中,不能通过乙烯的加成反应一步制得的是( )
A
A.CH3COOH B.CH3CH2OH
C.CH3CH2Cl D.BrCH2CH2Br
解析 A.一定条件下,乙烯与水发生加成反应生成乙醇,则乙酸不能通过乙烯的加成反应一步制得,故A符合题意;B.一定条件下,乙烯与水发生加成反应生成乙醇,乙醇能通过乙烯的加成反应一步制得,故B不符合题意;C.一定条件下,乙烯与氯化氢发生加成反应生成氯乙烷,氯乙烷能通过乙烯的加成反应一步制得,故C不符合题意;D.乙烯能与溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷能通过乙烯的加成反应一步制得,故D不符合题意。
7.(2021·四川省蒲江县蒲江中学高一月考)制取CH3CH2Cl最合理的方法是( )
C
A.乙烷与Cl2取代 B.乙烯与Cl2加成
C.乙烯与HCl加成 D.把乙烯通入盐酸中
解析 A.乙烷与Cl2取代的产物有多种,A不符合题意;B.乙烯与Cl2加成得到的是1,2-二氯乙烷,B不符合题意;C.乙烯与HCl加成只生成CH3CH2Cl,C符合题意;D.乙烯与盐酸不反应,D不符合题意;综上所述答案为C。
8.下列说法中错误的是( )
C
A.乙烯与Br2的加成、乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
9.(2020·北京市第九中学月考)1 mol乙烯与HCl完全加成后再被Cl2彻底取代,则消耗氯气的物质的量是( )
D
A.2 mol B.2.5 mol C.4 mol D.5 mol
解析 1 mol CH2===CH2与HCl完全加成生成1 mol CH3CH2Cl,1 mol CH3CH2Cl中含5 mol H,故彻底取代需消耗5 mol Cl2,D项正确。
10.(2020·山东招远第一中学高一检测)将CH4和C2H4的混合气体15 g通入盛有足量溴水的容器中,溴水的质量增加了7 g,则混合气体中CH4和C2H4的体积之比为( )
B
A.1∶2 B.2∶1 C.3∶2 D.2∶3
11.(2021·河北省唐县第一中学高一期中)抗击新冠肺炎的战疫中,N95口罩发挥了重要作用,丙烯是制造N95口罩的原料。下列有关丙烯的说法错误的是( )
B
解析 A.丙烯和乙烯分子中都含有不饱和的碳碳双键,结构相似,在分子组成上相差1个CH2原子团,二者互为同系物,A正确;B.丙烯含有碳碳双键,能使溴的四氯化碳溶液褪色,B错误;C.丙烯分子中含有饱和C原子,具有甲烷的四面体结构,因此不可能所有的原子在同一个平面上,C正确;D.丙烯分子中含有不饱和的碳碳双键,在一定条件下能够与H2发生加成反应产生丙烷,D正确。
12.下列说法正确的是( )
C
二、非选择题
13.请回答下列问题:
(1)根据你所学的有机化学反应类型,对下列反应进行分类。
①用乙烯与氯化氢制氯乙烷
②乙烷在空气中燃烧
③乙烯使溴水褪色
④乙烯使酸性KMnO4溶液褪色
⑤乙烷和氯气在光照条件下反应
其中属于取代反应的是________;属于加成反应的是________;属于氧化反应的是________。
(2)既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯,得到纯净乙烷的方法是________。
a.混合气体通过盛足量的酸性KMnO4溶液的洗气瓶
b.混合气体通过盛足量Br2的水溶液的洗气瓶
c.混合气体在一定条件下通入H2
d.混合气体在一定条件下与适量HCl混合
(3)一瓶无色气体,可能含有CH4和CH2===CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确?________(填“正确”或“不正确”),理由是__________________________
________________________________________________________________。
②上述实验可能涉及的反应类型有_________________________________。
答案 (1)⑤ ①③ ②④ (2)b
(3)①不正确 因为CH2===CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪去,生成的CH2ClCH2Cl也是油状液体 ②取代反应、加成反应
14.乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一、下图是有关乙烯的一些变化:
已知:E是高分子化合物。请回答下列问题:
(1)反应⑤的反应类型是_____________________________________________;
(2)物质C的最简单同系物的空间构型为________;
(3)写出反应④的化学方程式________________________________________;
(4)下列说法正确的是________。
A.反应①和反应②反应类型相同
B.反应②、③可以用于除去乙烷气体中混有的少量乙烯
C.物质E能使酸性高锰酸钾溶液褪色
D.物质D可用作燃料,缓解化石燃料的危机
15.(2021·珠海市第二中学高一期中)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。根据下图回答下列问题:
(3)F是B的一种同系物,其相对分子质量为72,则F的同分异构体有________种,F与氯气光照后得到的一氯代物有________种。
(4)下图显示的是烃中的碳原子相互结合的几种方式:
图中,互为同分异构体的是________,互为同系物的是________。
Thanks!
本课时内容结束
第二节 乙烯与有机高
分子材料
第1课时 乙烯
第7章 有机化合物
【课程标准要求】
1.掌握乙烯的组成及结构特点。
2.掌握乙烯的化学性质,知道氧化、加成、聚合反应等有机反应类型。
3.了解乙烯在生产及生活中的应用。
新知自主预习
课堂互动探究
课时训练
目
录
CONTENTS
///////
///////
///////
课堂小结·即时达标
///////
一、乙烯的组成结构、物理性质
1.乙烯的组成结构
(1)结构表示
C2H4
CH2===CH2
(2)空间结构
提醒 ①乙烯分子中以碳碳双键为中心6原子共平面(即2个碳原子和4个氢原子),键角约为120°;
②乙烯分子中含有碳碳双键,其分子中的氢原子数少于乙烷分子中的氢原子数,碳原子的价键没有全部被氢原子“饱和”。
共平面
2.物理性质
乙烯是一种________,稍有气味,________溶于水,密度比空气________的气体。
无色
难
略小
【微自测】
1.下列描述中正确的打“√”,错误的打“×”。
×
×
×
×
√
二、乙烯的化学性质及用途
1.乙烯的化学性质
(1)乙烯的氧化反应
①燃烧:乙烯能在空气中燃烧,火焰________且伴有________,生成二氧化碳和水,同时放出大量的热。化学方程式为____________________________。
②被高锰酸钾等强氧化剂氧化:乙烯能使酸性高锰酸钾溶液________。
明亮
黑烟
褪色
(2)乙烯的加成反应
反应 化学方程式
与Br2加成
与H2加成
与HCl加成
与H2O加成
CH2===CH2+Br2―→CH2BrCH2Br
(3)聚合反应
①乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为:
__________________________________________________________________。
②聚合反应:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
加聚反应:聚合反应同时也是____________,这样的反应又称为加聚反应。
加成反应
③聚合物 :________反应生成的高分子。
聚合
CH2===CH2
—CH2—CH2—
n
2.乙烯的用途
(1)乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。乙烯的产量可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中可以调节____________。
植物生长
【微自测】
2.①②是两种常见烃的球棍模型,则下列叙述正确的是( )
A.都能在空气中燃烧
B.都能使酸性高锰酸钾溶液褪色
C.都能发生加成反应
D.等质量的①②完全燃烧时,产生CO2的量相同
A
解析 由题图可知,①为乙烷,②为乙烯。乙烷不能使酸性高锰酸钾溶液褪色,而乙烯能,B项错误;乙烷不能发生加成反应,而乙烯能,C项错误;乙烷和乙烯的摩尔质量不同,等质量时二者的物质的量不同,产生CO2的量也不同,D项错误。
二、乙烯加成反应原理探究
一、乙烯氧化反应原理探究
一、乙烯氧化反应原理探究
实验操作:
(1)点燃纯净的乙烯,观察燃烧时的现象。
(2)将乙烯通入盛有酸性高锰酸钾溶液的试管中,观察现象。
———————【活动探究】———————
实验装置:
乙烯与高锰酸钾反应
1.能用点燃的方法鉴别甲烷和乙烯两种气体吗?
提示:可以。甲烷燃烧火焰是淡蓝色的,乙烯燃烧火焰明亮且伴有黑烟,二者燃烧时的现象不同。
2.为什么甲烷燃烧没有黑烟,而乙烯燃烧有黑烟?
提示:乙烯燃烧时有黑烟是因为乙烯分子里含碳量(约85.7%)比较大,未完全燃烧,产生碳的小颗粒造成的。
3.能用酸性高锰酸钾溶液鉴别甲烷和乙烯吗?能用酸性高锰酸钾溶液除去甲烷中的乙烯吗?
提示:能用酸性高锰酸钾溶液鉴别甲烷和乙烯,甲烷不能使高锰酸钾溶液褪色,乙烯可以使高锰酸钾溶液褪色。但不能用高锰酸钾除去甲烷中的乙烯,因为乙烯被高锰酸钾氧化为CO2,甲烷中又引入新的杂质。
乙烯氧化反应的原理
———————【核心归纳】———————
反应 产物 断裂化学键
燃烧 CO2和H2O 所有碳碳键和碳氢键
与酸性高锰酸钾溶液 乙烯被氧化为CO2,高锰酸钾被还原为Mn2+ 碳碳双键和碳氢键都被破坏
1.长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D.利用高锰酸钾溶液的氧化性,催熟水果
解析 水果释放出的乙烯是催熟剂,用KMnO4溶液来吸收乙烯,防止水果早熟。
———————【实践应用】———————
C
2.下列关于乙烯的叙述中错误的是( )
A.乙烯使酸性KMnO4溶液褪色,属于氧化反应
B.乙烯燃烧时,火焰明亮且伴有黑烟
C.乙烯可做香蕉等水果的催熟剂
D.被高锰酸钾氧化时,乙烯碳碳双键中的一个键断裂
解析 被高锰酸钾氧化时,乙烯中碳碳双键都断裂。
D
二、乙烯加成反应原理探究
实验素材1
实验步骤:将乙烯通入盛有溴的四氯化碳溶液的试管中,观察现象。
———————【活动探究】———————
实验装置:
乙烯与溴反应
实验素材2
聚乙烯的分子结构模型(局部)
1.乙烯分别通入溴水和溴的四氯化碳中,现象相同吗?
提示:不完全相同,溶液都褪色,但是前者溶液分层,下层是油状液体,而后者溶液不分层。
2.传统乙烯的工业制备是通过丁烷高温裂解进行,产物是乙烷和乙烯的混合物。在合适条件下,可通入H2以除去乙烷中的乙烯吗?
提示:乙烯与氢气反应生成乙烷需要加热和催化剂存在,反应很难进行,且过量的氢气难以除去。
3.如何除去乙烷中的乙烯气体?如何鉴别乙烷和乙烯?
提示:将混合气体通过足量的溴水,乙烯生成液态的1,2-二溴乙烷,从而除去乙烯。
乙烯与乙烷的鉴别方法有以下三种。方法一:将两种气体分别通入溴水(或溴的四氯化碳溶液)中;溶液褪色的为乙烯,溶液不褪色的为乙烷。方法二:将两种气体分别通入酸性KMnO4溶液中;溶液褪色的为乙烯,溶液不褪色的为乙烷。方法三:点燃两种气体,火焰较明亮,有黑烟的为乙烯,另一种为乙烷。
4.用乙烷(CH3CH3)和Cl2反应可以制取氯乙烷(CH3CH2Cl),用乙烯 (CH2===CH2)和HCl反应也能制取氯乙烷,两种方法哪种更好?
提示:用C2H4和HCl反应制取更好。乙烷和Cl2发生的是取代反应,生成物中除CH3CH2Cl外,还有C2H4Cl2、C2H3Cl3、C2H2Cl4、C2HCl5、C2Cl6,生成物不纯,产率低。CH2===CH2和HCl发生的是加成反应,无副反应,生成物只有CH3CH2Cl。
5.丙烯与乙烯互为同系物,由乙烯的结构和性质推测丙烯(CH2===CH—CH3)与HCl在一定条件下能加成的产物有几种?写出结构简式。
1.加成反应原理分析(以CH2===CH2和Br2加成为例)
———————【核心归纳】———————
2.乙烯加聚反应的示意图
3.乙烯与常见物质的加成反应
4.加聚反应
注意 (1)单烯烃的聚合物中碳碳之间是单键,不存在碳碳双键,不具备碳碳双键的性质。
(2)高分子化合物虽被称为“化合物”,但由于高分子化合物中的n不同,所以高分子化合物均为混合物,而不是纯净物。
3.(2021·郑州柘城第二高级中学检测)下列各反应不属于加成反应的是( )
解析 D项中反应为取代反应。
———————【实践应用】———————
D
4.(2021·潍坊高一检测)下列物质不可能是乙烯的加成产物的是( )
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
解析 A项,乙烯与氢气的加成产物是CH3CH3,不符合题意;B项,CH3CHCl2不可能是乙烯的加成产物,符合题意;C项,CH3CH2OH是乙烯与水的加成产物,不符合题意;D项,CH3CH2Br是乙烯与HBr的加成产物,不符合题意。
B
核心体系建构
1.苏轼的《格物粗谈》中有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( )
B
A.氧气 B.乙烯
C.生长素 D.甲烷
解析 乙烯具有催熟作用,因此“气”指的是乙烯。
C
2.下列说法错误的是( )
A.乙烯能使酸性KMnO4溶液褪色
B.将四氯化碳滴入溴水中,振荡后水层接近无色
C.乙烯使溴的四氯化碳溶液褪色是因萃取所致
D.乙烯易发生加成反应
解析 A项,乙烯使酸性KMnO4溶液褪色,是由于乙烯发生了氧化反应,正确;B项,四氯化碳使溴水变成无色,是发生了萃取,是物理变化,由于溴易溶于四氯化碳,从而使水层接近无色,正确;C项,乙烯使溴的四氯化碳溶液褪色是发生了加成反应,是化学变化,错误;D项,乙烯能与多种物质发生加成反应,正确。
A
3. 下列有关乙烯的说法,其中错误的是( )
D
4.(2021·成都高一检测)某课外活动小组设计了以下四种方案除去乙烷中混有的少量乙烯,并得到纯净干燥的乙烷,合理的是( )
A.①②④ B.①②③ C.②③④ D.①②③④
解析 ①和②C2H4与Br2发生加成反应生成液态1,2-二溴乙烷而除去C2H4,①NaOH溶液除去挥发出来的Br2蒸气,浓硫酸除去水蒸气,②碱石灰除去挥发出来的Br2蒸气和水蒸气,①和②均正确;③和④酸性KMnO4溶液将C2H4氧化为CO2,NaOH溶液和碱石灰都能吸收CO2,浓硫酸和碱石灰都能吸收水蒸气,③和④也正确。
5.乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的主要化学性质,实验装置如图所示。
(1)用化学方程式解释B装置中的实验现象:__________________________。
(2)C装置中的现象是_____________________________________________,
其发生反应的类型是____________________________________________。
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置________(填字母)中的实验现象可判断该资料是否真实。
(4)通过上述实验探究可知,检验甲烷和乙烯的方法是________(填字母,下同);除去甲烷中乙烯的方法是________。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
答案 (1)CH2===CH2+Br2―→CH2BrCH2Br (2)酸性高锰酸钾溶液褪色 氧化还原反应 (3)D (4)BC B
一、选择题(每小题只有一个选项符合题意)
1.下列关于乙烯结构与性质的叙述中,错误的是( )
B
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应使其褪色
C.乙烯与溴的四氯化碳溶液发生加成反应
D.乙烯分子的一氯代物只有一种结构
解析 B项发生的是氧化反应而不是加成反应。
2.(2021·宾阳中学高一期中)下列有关乙烯燃烧的说法中,正确的是( )
C
A.乙烯燃烧时的现象与氢气燃烧时的现象完全一致
B.乙烯燃烧时的现象与甲烷燃烧时的现象完全一致
C.乙烯燃烧放出大量的热,可作为燃料
D.乙烯燃烧时产生等质量的水和二氧化碳
解析 A.乙烯燃烧火焰明亮,并伴有黑烟,氢气燃烧时产生淡蓝色的火焰,故A错误;B.甲烷含碳量低,燃烧时没有黑烟,乙烯燃烧火焰明亮,并伴有黑烟,故B错误;C.乙烯燃烧放出大量的热,可作为燃料,故C正确;D.乙烯分子中碳与氢的物质的量之比为1∶2,燃烧时产生等物质的量的水和二氧化碳,故D错误。
3.下列有关甲烷和乙烯的说法正确的是( )
C
选项 反应物 反应类型 反应条件
A 甲烷与氯气 取代反应 点燃
B 乙烯与溴水 加成反应 光照
C 甲烷与氧气 氧化反应 点燃
D 乙烯与氧气 氧化反应 光照
4.能证明乙烯分子中含有一个碳碳双键的事实是( )
C
A.乙烯分子中碳、氢原子的个数比为1∶2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色
解析 分子中的碳氢原子个数比只能说明烃的组成,不能说明其结构特点;燃烧产物的物质的量相等和被酸性KMnO4溶液氧化,不能说明乙烯分子中含有一个碳碳双键;1 mol乙烯只能与1 mol溴单质加成,说明乙烯分子中含有一个碳碳双键。
5.(2021·广东实验中学高一期中)检验乙烷中是否混有少量乙烯的正确方法为( )
D
A.将气体点燃 B.将气体通入浓硫酸
C.将气体通入H2O D.将气体通入酸性KMnO4溶液
解析 A.将气体点燃,乙烷也能燃烧,故A错误;B.将气体通入浓硫酸,两者均不反应,故B错误;C.将气体通入H2O,两者均难溶于水,故C错误;D.将气体通入酸性KMnO4溶液,乙烯能使酸性KMnO4溶液褪色,而乙烷不能,现象不同可检验,故D正确;故选D。
6.(2021·浙江杭州市高一期中)乙烯是一种重要的化工原料。下列物质中,不能通过乙烯的加成反应一步制得的是( )
A
A.CH3COOH B.CH3CH2OH
C.CH3CH2Cl D.BrCH2CH2Br
解析 A.一定条件下,乙烯与水发生加成反应生成乙醇,则乙酸不能通过乙烯的加成反应一步制得,故A符合题意;B.一定条件下,乙烯与水发生加成反应生成乙醇,乙醇能通过乙烯的加成反应一步制得,故B不符合题意;C.一定条件下,乙烯与氯化氢发生加成反应生成氯乙烷,氯乙烷能通过乙烯的加成反应一步制得,故C不符合题意;D.乙烯能与溴水发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷能通过乙烯的加成反应一步制得,故D不符合题意。
7.(2021·四川省蒲江县蒲江中学高一月考)制取CH3CH2Cl最合理的方法是( )
C
A.乙烷与Cl2取代 B.乙烯与Cl2加成
C.乙烯与HCl加成 D.把乙烯通入盐酸中
解析 A.乙烷与Cl2取代的产物有多种,A不符合题意;B.乙烯与Cl2加成得到的是1,2-二氯乙烷,B不符合题意;C.乙烯与HCl加成只生成CH3CH2Cl,C符合题意;D.乙烯与盐酸不反应,D不符合题意;综上所述答案为C。
8.下列说法中错误的是( )
C
A.乙烯与Br2的加成、乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同物质的量的乙烯和甲烷完全燃烧消耗的氧气的量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷
9.(2020·北京市第九中学月考)1 mol乙烯与HCl完全加成后再被Cl2彻底取代,则消耗氯气的物质的量是( )
D
A.2 mol B.2.5 mol C.4 mol D.5 mol
解析 1 mol CH2===CH2与HCl完全加成生成1 mol CH3CH2Cl,1 mol CH3CH2Cl中含5 mol H,故彻底取代需消耗5 mol Cl2,D项正确。
10.(2020·山东招远第一中学高一检测)将CH4和C2H4的混合气体15 g通入盛有足量溴水的容器中,溴水的质量增加了7 g,则混合气体中CH4和C2H4的体积之比为( )
B
A.1∶2 B.2∶1 C.3∶2 D.2∶3
11.(2021·河北省唐县第一中学高一期中)抗击新冠肺炎的战疫中,N95口罩发挥了重要作用,丙烯是制造N95口罩的原料。下列有关丙烯的说法错误的是( )
B
解析 A.丙烯和乙烯分子中都含有不饱和的碳碳双键,结构相似,在分子组成上相差1个CH2原子团,二者互为同系物,A正确;B.丙烯含有碳碳双键,能使溴的四氯化碳溶液褪色,B错误;C.丙烯分子中含有饱和C原子,具有甲烷的四面体结构,因此不可能所有的原子在同一个平面上,C正确;D.丙烯分子中含有不饱和的碳碳双键,在一定条件下能够与H2发生加成反应产生丙烷,D正确。
12.下列说法正确的是( )
C
二、非选择题
13.请回答下列问题:
(1)根据你所学的有机化学反应类型,对下列反应进行分类。
①用乙烯与氯化氢制氯乙烷
②乙烷在空气中燃烧
③乙烯使溴水褪色
④乙烯使酸性KMnO4溶液褪色
⑤乙烷和氯气在光照条件下反应
其中属于取代反应的是________;属于加成反应的是________;属于氧化反应的是________。
(2)既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯,得到纯净乙烷的方法是________。
a.混合气体通过盛足量的酸性KMnO4溶液的洗气瓶
b.混合气体通过盛足量Br2的水溶液的洗气瓶
c.混合气体在一定条件下通入H2
d.混合气体在一定条件下与适量HCl混合
(3)一瓶无色气体,可能含有CH4和CH2===CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确?________(填“正确”或“不正确”),理由是__________________________
________________________________________________________________。
②上述实验可能涉及的反应类型有_________________________________。
答案 (1)⑤ ①③ ②④ (2)b
(3)①不正确 因为CH2===CH2也可以与Cl2发生加成反应,而使黄绿色逐渐褪去,生成的CH2ClCH2Cl也是油状液体 ②取代反应、加成反应
14.乙烯是世界上产量最大的化学产品之一,世界上已将乙烯产量作为衡量一个国家石油化工发展水平的重要标志之一、下图是有关乙烯的一些变化:
已知:E是高分子化合物。请回答下列问题:
(1)反应⑤的反应类型是_____________________________________________;
(2)物质C的最简单同系物的空间构型为________;
(3)写出反应④的化学方程式________________________________________;
(4)下列说法正确的是________。
A.反应①和反应②反应类型相同
B.反应②、③可以用于除去乙烷气体中混有的少量乙烯
C.物质E能使酸性高锰酸钾溶液褪色
D.物质D可用作燃料,缓解化石燃料的危机
15.(2021·珠海市第二中学高一期中)某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应。根据下图回答下列问题:
(3)F是B的一种同系物,其相对分子质量为72,则F的同分异构体有________种,F与氯气光照后得到的一氯代物有________种。
(4)下图显示的是烃中的碳原子相互结合的几种方式:
图中,互为同分异构体的是________,互为同系物的是________。
Thanks!
本课时内容结束
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
