高一化学人教版(2019)必修第一册 第三章第一节 铁及其化合物 第2课时(21张ppt)
文档属性
| 名称 | 高一化学人教版(2019)必修第一册 第三章第一节 铁及其化合物 第2课时(21张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-13 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
第一节 铁及其化合物
2019新教材必修一第三章
第2课时 铁的重要化合物
学习目标:
1、了解铁的氧化物的性质和应用。
2、知道氢氧化亚铁、氢氧化铁的制备和性质,了解这些物质在生产和生活中的应用
3、知道铁盐和亚铁盐的检验方法
难点:氢氧化亚铁的制取
重点:铁的氢氧化物的制取、铁盐和亚铁盐的检验
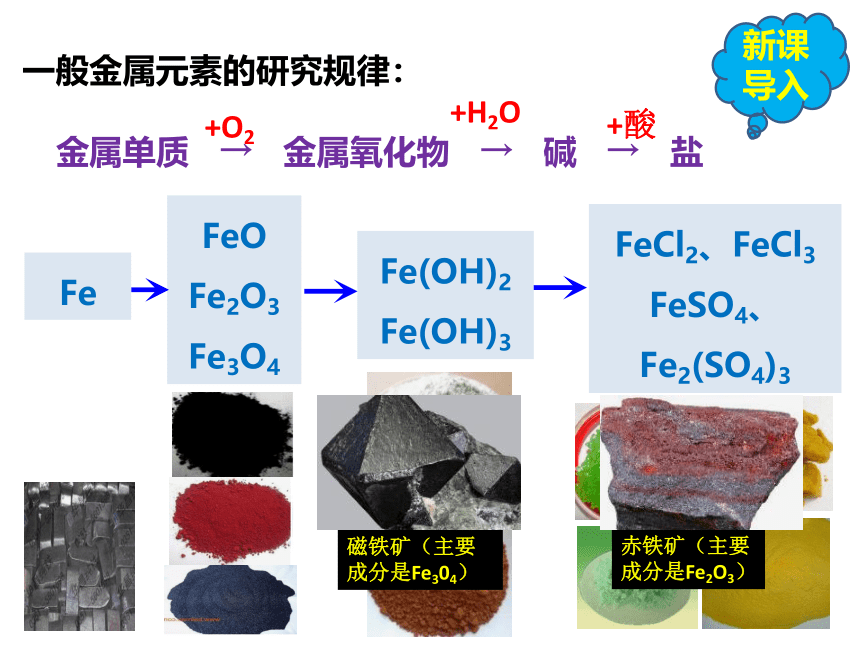
一般金属元素的研究规律:
金属单质 → 金属氧化物 → 碱 → 盐
+O2
+H2O
+酸
Fe
FeO
Fe2O3
Fe3O4
FeCl2、FeCl3
FeSO4、Fe2(SO4)3
Fe(OH)2
Fe(OH)3
新课导入
磁铁矿(主要成分是Fe304)
赤铁矿(主要成分是Fe2O3)
你知道故宫的外墙是用什么颜料粉刷?
你知道补铁剂补的是几价铁?
名称 化学式 铁元素的化合价 俗名 用途
氧化亚铁 无 用作色素、催化剂
氧化铁 铁红、铁丹、赤铁矿、铁锈 油漆、橡胶、建筑等涂料
四氧化三铁 吸铁石、磁铁(磁性氧化铁) 录音磁带、电讯器材
(1)稳定性:FeO不稳定,在空气里受热,迅速被氧化成 。
(2)与酸反应:FeO和Fe2O3属于 氧化物,与盐酸反应的离子方程式分别为 , 。
(3)四氧化三铁(Fe3O4)的化学式可写成FeO·Fe2O3,其溶于盐酸的离子方程式为 Fe3O4 + 8H+ = 2Fe3++Fe2++4H2O 。
一、铁的氧化物
FeO
Fe2O3
Fe3O4
+2
+3
+2、+3
Fe2O3
碱性
Fe2O3+6H+=2Fe3++3H2O
FeO+2H+=Fe2++H2O
二、铁的氢氧化物
1、请根据铁元素的化合价,推测出铁的氢氧化物有哪些?
2、我们怎么制备Fe(OH)2、Fe(OH)3 ?
方案一、能通过铁和水反应得到吗?
方案二、能否通过铁的氧化物和水反应制得?
方案三、分别用可溶性铁盐、亚铁盐与碱溶液反应?
Fe(OH)2白色、难溶
Fe(OH)3红褐色、难溶
铁与水蒸气→Fe3O4
铁与冷水X 铁与热水X
不能
不能
能
铁的氧化物全难溶于水
生成Fe(OH)2 和Fe(OH)3 符合复分解反应的条件
名称 Fe(OH)2 Fe(OH)3
操作
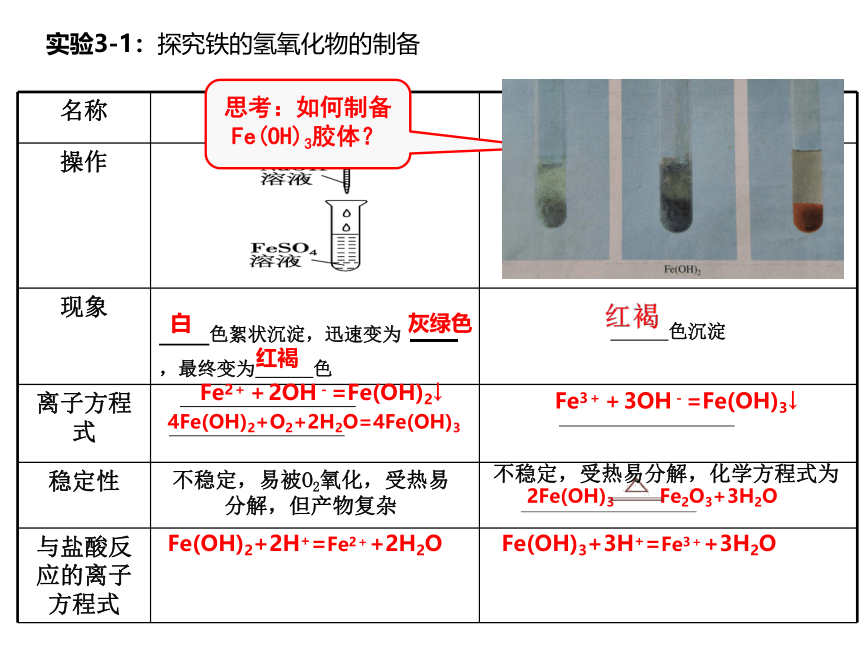
现象 色絮状沉淀,迅速变为 ,最终变为 色
色沉淀
离子方程式
稳定性
与盐酸反应的离子方程式
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
白
灰绿色
红褐
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3 Fe2O3+3H2O
思考:如何制备Fe(OH)3胶体?
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
不稳定,易被O2氧化,受热易分解,但产物复杂
不稳定,受热易分解,化学方程式为
实验3-1:探究铁的氢氧化物的制备
对制备Fe(OH)2你有什么改进措施?----
1. Fe(OH)2最终转化为Fe(OH)3的原因是什么?
内因:
外因:
1)FeSO4(aq)液面加植物油或苯进行液封(加保护层,隔绝空气)
空气中有O2;溶液中可能有溶解氧O2
Fe(OH)2具有很强的还原性,很不稳定,极易被氧化
1) 避免亚铁盐溶液中混进Fe3+
2) 除去试管和溶液中的O2,创造无氧环境
3. 下列措施对成功制备 Fe(OH)2有帮助:
2)胶头滴管的末端伸入FeSO4(aq)液面下,再挤出NaOH溶液(避免接触氧气
3)加热煮沸NaOH溶液或用煮沸过的蒸馏水配置溶液(除去溶解的O2)
4) FeSO4必须是新配制的,并加入Fe粉。(以防Fe2+被氧化成Fe3+)
问题解决:下列四个装置,哪些能较长时间的看到Fe(OH)2白色沉淀?
产生的H2
赶走空气
苯液封作用
阻止空气进入
√
√
√
X
Fe(OH)2和Fe(OH)3都是不溶性碱,与酸反应生成相应的 和水 。常见的铁盐有 Fe(NO3) 3 、Fe2(SO4) 3 、 等;亚铁盐有FeSO4、 等 。
盐
FeCl3
FeCl2
2、铁盐溶液的 色,亚铁盐溶液 色。
棕黄或黄
浅绿
3、如何用化学试剂检验Fe2+和Fe3+呢?
三、铁盐和亚铁盐
铁离子检验:(实验3-2 )
溶液 FeCl3溶液 FeCl2溶液
滴入KSCN溶液现象
应用 无明显现象
溶液变为血红色
可以利用此反应检验Fe3+的存在
总结:Fe2+、Fe3+的检验方法
(1)观察法:浅绿色溶液中含有 ;棕黄色溶液中含有 。
(2)加碱法:若产生的白色沉淀迅速变为灰绿色,最后变为红褐色的为 ;
若直接产生红褐色沉淀的为 。
(3)加KSCN溶液法:无明显现象,再加新制氯水变红色的为 ;
若溶液直接变红色的为 。
Fe2+
Fe3+
Fe2+
Fe3+
Fe3+
不是红色沉淀
Fe2+
硫氰化钾
人体需要的是Fe2+,可溶性亚铁盐易被吸收。
对于缺铁性贫血患者来说,
1、可服用FeSO4、乳酸亚铁,琥珀酸亚铁等补铁剂。
2、食用含铁较多的黑木耳、菠菜、蛋黄、动物内脏等食品。
动物肝脏
瘦肉
鸡蛋黄
黄豆
黑木耳
蘑菇
红枣
桂圆
葡萄
3、也可以通过食用铁强化酱油的方式来补铁。
学习小结
一、铁的氧化物:
二、铁的氢氧化物:
1、制备实验 :可溶性盐和强碱反应
2、化学性质
三、铁盐和亚铁盐:
Fe2+、Fe3+的检验方法
观察法 加碱法 加KSCN溶液法
FeO、Fe2O3、Fe3O4
Fe(OH)2、Fe(OH)3
随堂测:
1、现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能
是( )
A.苹果汁中含有 B.苹果汁中含有
C.苹果汁中含有 D.苹果汁中含有
D
2、下列说法正确的是( )
A.铁的氧化物均为黑色固体,均难溶于水
B.Fe(OH)2在空气中易变质,生成红褐色的
Fe(OH)3
C.铁在氧气中剧烈燃烧,火星四射,生成黑色
的FeO
D.氢氧化亚铁为灰绿色絮状沉淀
B
3、关于Fe2+和Fe3+的叙述,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性
D.Fe3+溶液中滴入含SCN-的溶液,立即
出现红色沉淀
D
4、有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,既有二价铁也有三价铁
C.FeO、Fe2O3、Fe3O4都不溶于水,都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
D
Fe3O4
5、下列说法不正确的是( )
A.铁的氧化物均为黑色固体,均难溶于水
B.Fe(OH)2在空气中易变质,生成红褐色的Fe(OH)3
C.铁在氧气中剧烈燃烧,火星四射,生成黑色的Fe3O4
D.氢氧化亚铁为白色絮状沉淀
A
6、将下列四种化合物溶于稀盐酸,滴加硫氰化钾溶液没有颜色变化的是( )
A.FeS B.Fe2O3 C.FeCl3 D.Fe2(SO4)3
A
7、我国科学家参与研制的阿尔法磁谱仪已随美国发现号航天飞船升入太空,开始探索宇宙中是否存在“反物质”的工作。根据你所学的知识推测用于制造阿尔法磁谱仪的核心部件的材料是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe(OH)3
C
谢谢聆听
第一节 铁及其化合物
2019新教材必修一第三章
第2课时 铁的重要化合物
学习目标:
1、了解铁的氧化物的性质和应用。
2、知道氢氧化亚铁、氢氧化铁的制备和性质,了解这些物质在生产和生活中的应用
3、知道铁盐和亚铁盐的检验方法
难点:氢氧化亚铁的制取
重点:铁的氢氧化物的制取、铁盐和亚铁盐的检验
一般金属元素的研究规律:
金属单质 → 金属氧化物 → 碱 → 盐
+O2
+H2O
+酸
Fe
FeO
Fe2O3
Fe3O4
FeCl2、FeCl3
FeSO4、Fe2(SO4)3
Fe(OH)2
Fe(OH)3
新课导入
磁铁矿(主要成分是Fe304)
赤铁矿(主要成分是Fe2O3)
你知道故宫的外墙是用什么颜料粉刷?
你知道补铁剂补的是几价铁?
名称 化学式 铁元素的化合价 俗名 用途
氧化亚铁 无 用作色素、催化剂
氧化铁 铁红、铁丹、赤铁矿、铁锈 油漆、橡胶、建筑等涂料
四氧化三铁 吸铁石、磁铁(磁性氧化铁) 录音磁带、电讯器材
(1)稳定性:FeO不稳定,在空气里受热,迅速被氧化成 。
(2)与酸反应:FeO和Fe2O3属于 氧化物,与盐酸反应的离子方程式分别为 , 。
(3)四氧化三铁(Fe3O4)的化学式可写成FeO·Fe2O3,其溶于盐酸的离子方程式为 Fe3O4 + 8H+ = 2Fe3++Fe2++4H2O 。
一、铁的氧化物
FeO
Fe2O3
Fe3O4
+2
+3
+2、+3
Fe2O3
碱性
Fe2O3+6H+=2Fe3++3H2O
FeO+2H+=Fe2++H2O
二、铁的氢氧化物
1、请根据铁元素的化合价,推测出铁的氢氧化物有哪些?
2、我们怎么制备Fe(OH)2、Fe(OH)3 ?
方案一、能通过铁和水反应得到吗?
方案二、能否通过铁的氧化物和水反应制得?
方案三、分别用可溶性铁盐、亚铁盐与碱溶液反应?
Fe(OH)2白色、难溶
Fe(OH)3红褐色、难溶
铁与水蒸气→Fe3O4
铁与冷水X 铁与热水X
不能
不能
能
铁的氧化物全难溶于水
生成Fe(OH)2 和Fe(OH)3 符合复分解反应的条件
名称 Fe(OH)2 Fe(OH)3
操作
现象 色絮状沉淀,迅速变为 ,最终变为 色
色沉淀
离子方程式
稳定性
与盐酸反应的离子方程式
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
白
灰绿色
红褐
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3 Fe2O3+3H2O
思考:如何制备Fe(OH)3胶体?
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
不稳定,易被O2氧化,受热易分解,但产物复杂
不稳定,受热易分解,化学方程式为
实验3-1:探究铁的氢氧化物的制备
对制备Fe(OH)2你有什么改进措施?----
1. Fe(OH)2最终转化为Fe(OH)3的原因是什么?
内因:
外因:
1)FeSO4(aq)液面加植物油或苯进行液封(加保护层,隔绝空气)
空气中有O2;溶液中可能有溶解氧O2
Fe(OH)2具有很强的还原性,很不稳定,极易被氧化
1) 避免亚铁盐溶液中混进Fe3+
2) 除去试管和溶液中的O2,创造无氧环境
3. 下列措施对成功制备 Fe(OH)2有帮助:
2)胶头滴管的末端伸入FeSO4(aq)液面下,再挤出NaOH溶液(避免接触氧气
3)加热煮沸NaOH溶液或用煮沸过的蒸馏水配置溶液(除去溶解的O2)
4) FeSO4必须是新配制的,并加入Fe粉。(以防Fe2+被氧化成Fe3+)
问题解决:下列四个装置,哪些能较长时间的看到Fe(OH)2白色沉淀?
产生的H2
赶走空气
苯液封作用
阻止空气进入
√
√
√
X
Fe(OH)2和Fe(OH)3都是不溶性碱,与酸反应生成相应的 和水 。常见的铁盐有 Fe(NO3) 3 、Fe2(SO4) 3 、 等;亚铁盐有FeSO4、 等 。
盐
FeCl3
FeCl2
2、铁盐溶液的 色,亚铁盐溶液 色。
棕黄或黄
浅绿
3、如何用化学试剂检验Fe2+和Fe3+呢?
三、铁盐和亚铁盐
铁离子检验:(实验3-2 )
溶液 FeCl3溶液 FeCl2溶液
滴入KSCN溶液现象
应用 无明显现象
溶液变为血红色
可以利用此反应检验Fe3+的存在
总结:Fe2+、Fe3+的检验方法
(1)观察法:浅绿色溶液中含有 ;棕黄色溶液中含有 。
(2)加碱法:若产生的白色沉淀迅速变为灰绿色,最后变为红褐色的为 ;
若直接产生红褐色沉淀的为 。
(3)加KSCN溶液法:无明显现象,再加新制氯水变红色的为 ;
若溶液直接变红色的为 。
Fe2+
Fe3+
Fe2+
Fe3+
Fe3+
不是红色沉淀
Fe2+
硫氰化钾
人体需要的是Fe2+,可溶性亚铁盐易被吸收。
对于缺铁性贫血患者来说,
1、可服用FeSO4、乳酸亚铁,琥珀酸亚铁等补铁剂。
2、食用含铁较多的黑木耳、菠菜、蛋黄、动物内脏等食品。
动物肝脏
瘦肉
鸡蛋黄
黄豆
黑木耳
蘑菇
红枣
桂圆
葡萄
3、也可以通过食用铁强化酱油的方式来补铁。
学习小结
一、铁的氧化物:
二、铁的氢氧化物:
1、制备实验 :可溶性盐和强碱反应
2、化学性质
三、铁盐和亚铁盐:
Fe2+、Fe3+的检验方法
观察法 加碱法 加KSCN溶液法
FeO、Fe2O3、Fe3O4
Fe(OH)2、Fe(OH)3
随堂测:
1、现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能
是( )
A.苹果汁中含有 B.苹果汁中含有
C.苹果汁中含有 D.苹果汁中含有
D
2、下列说法正确的是( )
A.铁的氧化物均为黑色固体,均难溶于水
B.Fe(OH)2在空气中易变质,生成红褐色的
Fe(OH)3
C.铁在氧气中剧烈燃烧,火星四射,生成黑色
的FeO
D.氢氧化亚铁为灰绿色絮状沉淀
B
3、关于Fe2+和Fe3+的叙述,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性
D.Fe3+溶液中滴入含SCN-的溶液,立即
出现红色沉淀
D
4、有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe2O3,红棕色的,常用作红色油漆和涂料
B.Fe3O4是黑色晶体,既有二价铁也有三价铁
C.FeO、Fe2O3、Fe3O4都不溶于水,都能和盐酸反应生成相应的盐
D.FeO不稳定,在空气中加热迅速被氧化成Fe2O3
D
Fe3O4
5、下列说法不正确的是( )
A.铁的氧化物均为黑色固体,均难溶于水
B.Fe(OH)2在空气中易变质,生成红褐色的Fe(OH)3
C.铁在氧气中剧烈燃烧,火星四射,生成黑色的Fe3O4
D.氢氧化亚铁为白色絮状沉淀
A
6、将下列四种化合物溶于稀盐酸,滴加硫氰化钾溶液没有颜色变化的是( )
A.FeS B.Fe2O3 C.FeCl3 D.Fe2(SO4)3
A
7、我国科学家参与研制的阿尔法磁谱仪已随美国发现号航天飞船升入太空,开始探索宇宙中是否存在“反物质”的工作。根据你所学的知识推测用于制造阿尔法磁谱仪的核心部件的材料是( )
A.FeO B.Fe2O3 C.Fe3O4 D.Fe(OH)3
C
谢谢聆听
