化学人教版(2019)选择性必修3 2.3.2苯的同系物(共50张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.3.2苯的同系物(共50张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 78.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-15 00:00:00 | ||
图片预览





文档简介
(共50张PPT)
第二课时 苯的同系物
第三节 芳香烃
化学家预言第一次世界大战
1912-1913年,德国在国际市场上大量收购石油。由于有利可图,许多国家的石油商都不惜压低价格争着与德国人做生意,但令人不可理解的是,德国人只要婆罗洲的石油,其他的一概不要,并急急忙忙地把收购到婆罗洲的石油运到德国本土去。在石油商人感到百思不得其解时,一位化学家提醒世人说:“德国人在准备发动战争了!”果然不出化学家所料,德国于1914年发动了第一次世界大战。
【情境引入】
这位化学家为何知道德国将发动战争呢?这一奇怪现象引起了一位化学家的注意,他经过化验,发现婆罗洲的石油成分与其他地区的不同,它含有很少的直链烃,它含有大量的苯和甲苯等芳香烃,正是适宜制造“TNT”(三硝基甲苯)烈性炸药的的基础成分。这位化学家们就是在对婆罗洲石油的化学成分进行分析之后才向世人提出历史性预言的。
【情境引入】
那么,“TNT”(三硝基甲苯)是怎么制备的呢?
下面我们来认识以“甲苯”为代表的苯的同系物的性质。
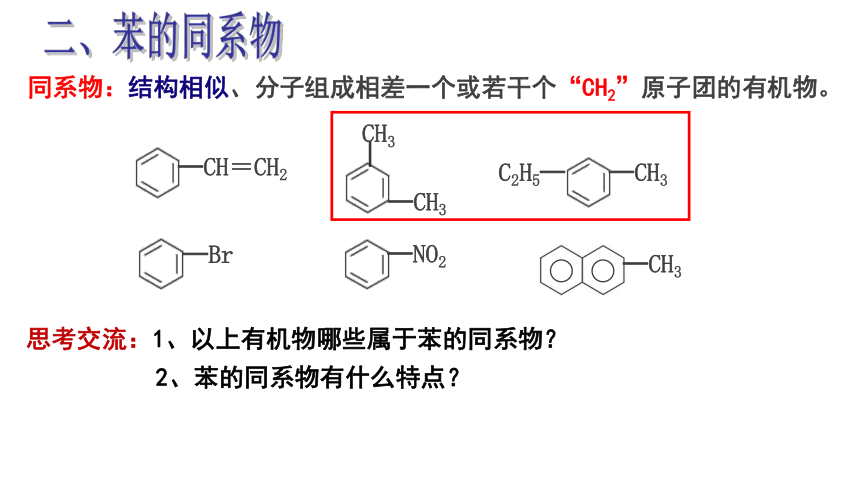
─Br
─CH=CH2
─CH3
─
CH3
─NO2
─CH3
C2H5─
─CH3
思考交流:1、以上有机物哪些属于苯的同系物?
同系物:结构相似、分子组成相差一个或若干个“CH2”原子团的有机物。
2、苯的同系物有什么特点?
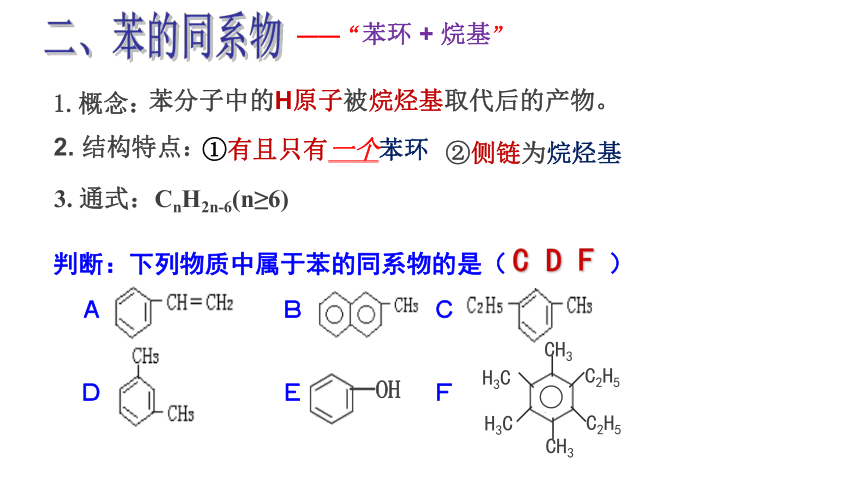
二、苯的同系物
1.概念:
二、苯的同系物
判断:下列物质中属于苯的同系物的是( )
A B C
D E F
C D F
②侧链为烷烃基
3. 通式:CnH2n-6(n≥6)
苯分子中的H原子被烷烃基取代后的产物。
2. 结构特点:
①有且只有一个苯环
——“苯环 + 烷基”
─
CH3
CH3
─
H3C
H3C
C2H5
C2H5
─
─
─
─
─OH
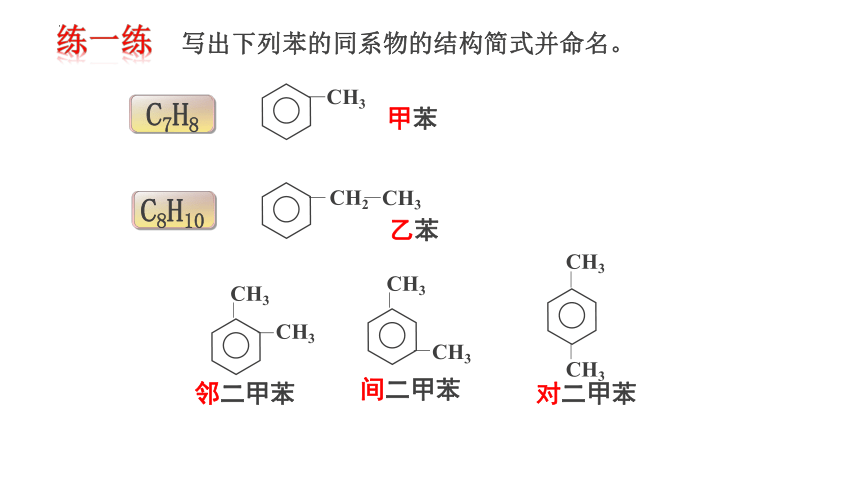
写出下列苯的同系物的结构简式并命名。
甲苯
乙苯
邻二甲苯
间二甲苯
C7H8
C8H10
练一练
CH3
CH3
CH3
CH3
CH2
CH3
CH3
CH3
CH3
对二甲苯
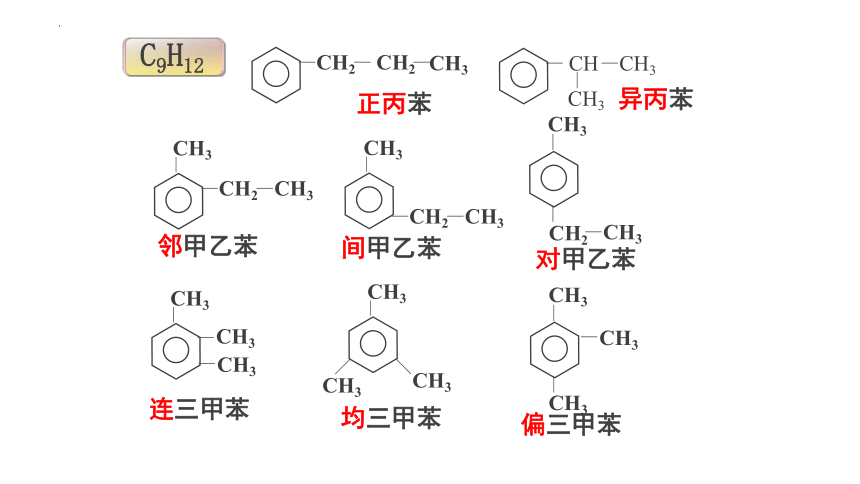
正丙苯
邻甲乙苯
间甲乙苯
C9H12
CH3
CH2 CH2
对甲乙苯
CH3
CH
CH3
CH3
CH3
CH2
CH3
CH3
CH2
CH3
CH3
CH2
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
连三甲苯
均三甲苯
偏三甲苯
异丙苯
间二甲苯
> >
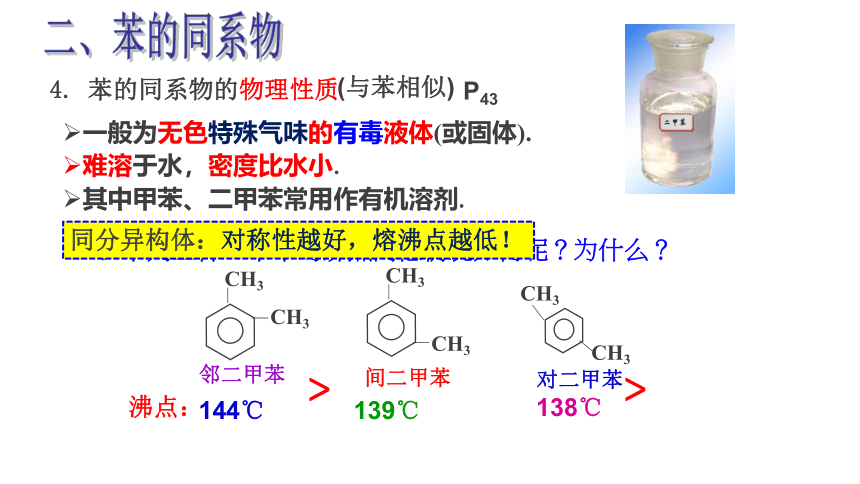
4. 苯的同系物的物理性质
一般为无色特殊气味的有毒液体(或固体).
难溶于水,密度比水小.
其中甲苯、二甲苯常用作有机溶剂.
(与苯相似)
思考:下列三种二甲苯的沸点高低情况如何呢?为什么?
邻二甲苯
对二甲苯
144℃
139℃
138℃
CH3
CH3
CH3
CH3
CH3
CH3
沸点:
同分异构体:对称性越好,熔沸点越低!
二、苯的同系物
P43
P44
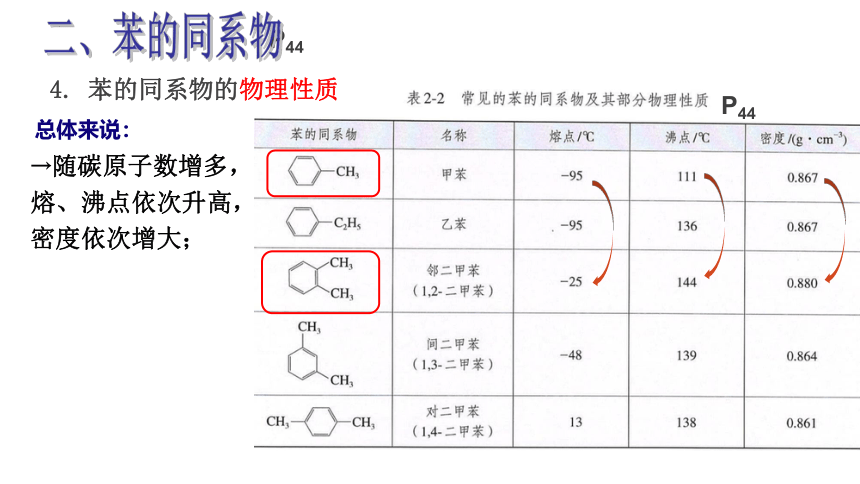
4. 苯的同系物的物理性质
二、苯的同系物
P44
→随碳原子数增多,熔、沸点依次升高,
密度依次增大;
总体来说:
P44
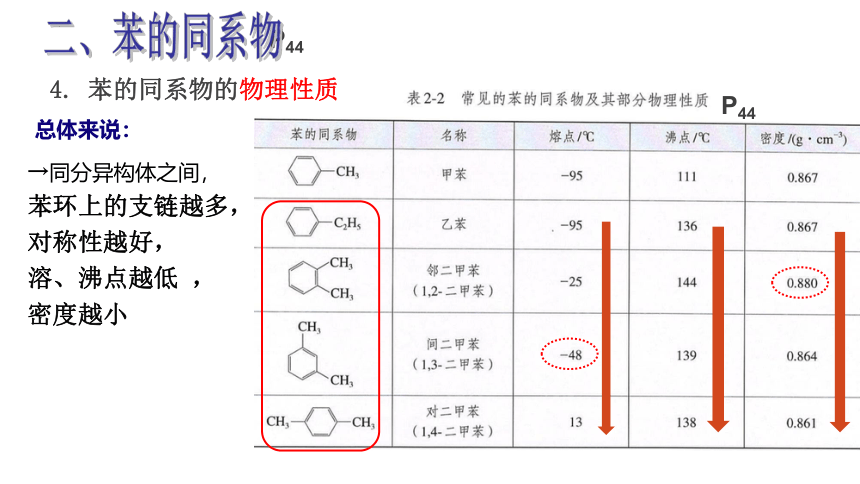
4. 苯的同系物的物理性质
二、苯的同系物
P44
→同分异构体之间,
苯环上的支链越多,
对称性越好,
溶、沸点越低 ,
密度越小
总体来说:
5.化学性质
都含有苯环,性质相似
例如: 可燃烧;易取代(卤代、硝化);能加成等。
—CH3
1)比较苯和甲苯结构的异同点,
推测甲苯的化学性质。
甲苯含有甲基,由于苯环和甲基相互影响,
在化学性质上与苯也有不同之处。
对比思考:
二、苯的同系物
2CnH2n-6 + 3 (n-1)O2
点燃
2nCO2+ 2(n-3)H2O
(1)可燃性
现象:火焰明亮并带有浓烟
5.化学性质
二、苯的同系物
实验2-2
二、苯的同系物
5.化学性质
实验2-2
实验内容 实验现象 解释
溴水沉到液体底部
溴水的密度大于苯和甲苯的密度
两支试管中液体均分层,均是上层为橙红色,下层几乎无色
苯、甲苯与溴水均不能发生化学反应,但能够萃取溴
二、苯的同系物
5.化学性质
(2)将上述试管用力振荡,静置
(1)向两支分别盛有2mL苯和甲苯的试管中各加入几滴溴水,静置
苯环中的碳碳键是介于碳碳单键和碳碳双键之间的特殊共价键。
?
实验内容 实验现象 解释
(3)向两支分别盛有2mL苯和甲苯的试管中各加入几滴酸性高锰酸钾溶液,静置
紫红色酸性KMnO4溶液沉到液体底部
苯未使酸性高锰酸钾溶液褪色,甲苯使酸性高锰酸钾溶液褪色
苯与酸性KMnO4溶液不反应,甲苯与酸性KMnO4溶液反应
酸性KMnO4溶液的密度大于苯和甲苯的密度
实验2-2
二、苯的同系物
5.化学性质
(4)将上述试管用力振荡,
静置
?
KMnO4(H+)
─
CH3
─
COOH
试从结构角度分析甲苯能使酸性高锰酸钾溶液褪色的原因。
KMnO4(H+)溶液
不反应
KMnO4(H+)溶液
不反应
KMnO4(H+)溶液
─
CH3
─
COOH
[性质探究]
(H—CH3)
CH4
苯环取代甲烷上一个H
苯环上的烷烃基比烷烃性质活泼。
【结论】 苯环影响侧链,使侧链甲基能被KMnO4/H+(aq)氧化
苯的同系物都能使酸性高锰酸钾溶液褪色吗?
资料卡片:
①②能使酸性高锰酸钾溶液褪色
③④不能使酸性高锰酸钾溶液褪色
根据以上信息,你能发现什么规律?
CH2
─
CH3
─
CH
─
─
CH3
CH2
─
CH2
─
─
CH3
─
C
CH3
─
─
CH2CH3
─
H3C
─
C
CH3
─
─
CH3
─
H3C
【思考交流】
KMnO4/H+(aq)
COOH
与苯环直接相连的碳原子上必须连有氢原子
KMnO4/H+(aq)
COOH
,并且烷基均被氧化为-COOH。
②
①
④
③
苯的同系物被酸性KMnO4溶液氧化的条件:
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
思考1:产物是什么?
C
|
—C—C
|
C
×
苯环直接相连的碳上无氢原子的侧链不能被氧化
KMnO4/H+
规律:
思考2、如何鉴别苯和甲苯?
可用酸性高锰酸钾溶液鉴别。
思考3:如何除去苯中溶解的少量甲苯
KMnO4/H+(aq)
COOH
分液
NaOH(aq)
COONa
苯
甲苯
苯
苯
(1) 可燃性
(2)使酸性高锰酸钾溶液褪色
[1].氧化反应
思考交流:苯环可以影响烷基,让其易被氧化,烷基是否可以影响苯环呢?
(总结归纳)
二、苯的同系物
5.化学性质
区别苯和苯的同系物
结论:苯环对侧链影响:苯环活化侧链, 使侧链易于氧化。
KMnO4/H+
邻硝基甲苯
对硝基甲苯
CH3
+ HNO3
浓硫酸
300C
CH3
NO2
CH3
NO2
+ H2O
[2].取代反应
①硝化反应
+ H2O
结论:侧链影响了苯环,使苯环上的H(尤其是邻、对位)更活跃,易于取代!
二、苯的同系物
5.化学性质
→温度不同,反应产物不同。硝基取代的位置以甲基的邻、对位为主。
2,4,6-三硝基甲苯
简称三硝基甲苯,又叫TNT
是一种淡黄色针状晶体,不溶于水,是一种烈性炸药
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HNO3
+ 3H2O
浓硫酸
TNT广泛用于国防、开矿、筑路、兴修水利等
[2].取代反应
①硝化反应
注意书写规范
TNT炸药爆炸时的场景
②卤代反应
+ Br2
FeBr3
CH3
CH3
Br
+ HBr
原因:苯环受侧链影响,邻位和对位上的H易被取代
CH3
Br
+ HBr
其他纯的卤素单质(X2)也能发生类似的取代反应
如,甲苯使溴水褪色,是因萃取使水层颜色变浅。
注意:但不能与卤水取代!
[2].取代反应
产物以邻溴甲苯、对溴甲苯为主
比较下列两个反应,指出反应的条件是什么?
+ Br2
CH3
CH3
Br
+ HBr
催化剂(FeBr3)
+ Br2
CH3
CH2Br
+ HBr
思考:
光照
(侧链被取代)
(苯环上H被取代)
规 律:
①光照条件下,苯的同系物取代反应发生在烷基侧链上
②卤化铁做催化剂,苯的同系物取代发生在苯环上烷基的邻位、对位上
特点:有机产物不唯一
产物以邻、对位为主
环己烷
+ 3H2
Ni
Δ
(3)加成反应
1 : 3
1 : 3
(较困难)
一元取代产物有几种?
讨论:
4种
5种
甲基环己烷
CH3
|
CH3
|
+ 3H2
催化剂
△
催化剂
+3H2
─
R
─
R
通式:
①可燃性
1、氧化反应:
苯环与侧链的相互影响将使苯的同系物具有特性!
2、取代反应
3、加成反应(较困难)
侧链对苯环的影响,使邻位和对位上的H易被取代
KMnO4
(H+)
——说明了苯环对侧链的影响,使侧链更易氧化
小结:苯的同系物的化学性质
②可使KMnO4(H+)溶液褪色
多苯代脂烃:苯环通过脂肪烃基连接在一起。
联苯或联多苯:苯环之间通过碳碳单键直接相连。
稠环芳香烃:由两个或两个以上的苯环共用相邻的两个碳原子。
萘C10H8
蒽C14H10
二苯甲烷
联苯
对三联苯
多环芳香烃(了解)
—
—CH2—
稠环芳香烃
(课本P46资料卡片)
稠环芳香烃
【概念】由两个或两个以上的苯环共用相邻的2个碳原子而成的一类芳香烃,称为稠环芳香烃。
C10H8
(课本P46资料卡片)
萘
萘是无色片状晶体,具有特殊的气味,易升华,曾经用来防蛀、驱虫,但因它有一定的毒性,现已禁止使用。
萘是一种重要的化工原料。
苯并芘
C14H10
蒽
蒽是生产染料的主要原料。
蒽也是一种无色的晶体,易升华
菲
C14H10
芳香烃的来源及应用
十九世纪初,由于冶金工业的发展,需要大量焦炭,生产焦炭的主要方法是煤的干馏,即对煤隔绝空气加强热。
煤的干馏除得到焦炭外还能获得有用的煤气,但同时却生成一种黑糊糊、粘乎乎有特殊臭味的油状液体!人们把它称作煤焦油。
当时,煤焦油被当作废物扔掉,污染环境,造成公害。随着炼焦工业的发展,煤焦油的堆积也愈来愈严重,煤焦油的利用就成为当时生产中迫切需要解决的一个重要的环境和社会问题。
(了解)
后来,以法拉第为代表的科学家对煤焦油产生了兴趣,并从煤焦油中分离出了以芳香烃为主的多种重要芳香族化合物,又以这些芳香族化合物为原料合成了多种染料、药品、香料、炸药等有机产品。到十九世纪中叶,形成了以煤焦油为原料的有机合成工业。
自从1845年人们从煤焦油内发现苯及其他芳香烃,很长时间里煤是一切芳香烃的主要来源。但是,从1吨煤中仅可以提取1千克苯和2.5千克其他芳香烃。由于芳香烃的需求在不断增长,仅从煤中提炼芳香烃远不能满足化学工业生产的需要。
芳香烃的来源及应用
(了解)
大约到了1930年,由煤生产苯已经发展成为世界性的大吨位工业。1940年以来,通过石油催化重整生成苯、甲苯、二甲苯等;烃裂解制乙烯时,裂解汽油副产物中含芳香烃达40—48%,因此石油也成为芳香烃的重要来源。
芳香烃的来源
①煤的干馏
②石油的催化重整和裂解
芳香烃的来源及应用
(了解)
1.芳香烃的来源
传统工艺:煤焦油
新工艺:石油产品的催化重整和裂解
简单的芳香烃,如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等。
2.芳香烃的应用
芳香烃的来源及应用
(了解)
芳香烃对人体及环境的危害
烧烤中含有超量的芳香烃,对人体有害。
抽烟呼出的烟气中,含有超
量的芳香烃,对人体有危害!
新装修的居室含有超量的芳香烃,对人体有害。
(1)苯的同系物、芳香烃、芳香族化合物中都含有苯环,所以
是官能团( )
(2)符合CnH2n-6(n≥6)通式的烃一定是苯及其同系物( )
(3)相同物质的量的苯和甲苯与氢气完全加成时消耗的氢气的量相同( )
(4)苯的同系物都能使酸性高锰酸钾溶液褪色( )
(5)甲苯在一定条件下与硝酸反应生成2,4,6-三硝基甲苯,说明苯环对甲基产生了影响( )
×
×
1.正误判断
√
×
×
课堂检测
4、下列关于芳香烃的叙述中不正确的是( )
A.乙烷和甲苯中都含有甲基,甲苯可以被酸性KMnO4溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响。
B.苯和浓硝酸、浓硫酸混合物在100—110℃才能生成二硝基苯,而甲苯在100℃时即可生成三硝基甲苯,说明甲基对苯环产生了影响。
C.苯、甲苯等是重要的有机溶剂,萘(俗称卫生球)是一种重要的绿色杀虫剂。
D.除去苯中混入的少量甲苯可加入适量的酸性KMnO4溶液,充分反应后再加入足量的NaOH溶液,然后分液即可。
C
×
√
√
√
课堂检测
5、要鉴别己烯中是否混有少量甲苯,最恰当的实验方法是( )
A、先加足量酸性高锰酸钾溶液,然后再加入溴水
B、先加适量溴水,然后再加入酸性高锰酸钾溶液
C、点燃这种液体,然后再观察火焰是否有浓烟
D、加入浓硫酸与浓硝酸后加热
B
课堂检测
6.有人设计下图装置吸收氯化氢气体或氨气,能取得良好的效果。由图推测X物质可能是( )
A. 苯 B. 乙醇 C. 四氯化碳 D. 己烷
C
课堂检测
7.某苯的同系物的化学式为C11H16,经测定数据表明:分子中除含苯环外,不再含其他环状结构,分子中还含有两个—CH3,两个—CH2—和一个 ,则该分子由碳链异构所形成的同分异构体有( )
A.3种 B.4种 C.5种 D.6种
B
课堂检测
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
③
①
①
②
②
③
Br
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
1
5
4
2
3
课堂检测
③
①
①
②
②
③
—Br
1
2
3
×
×
2)一个溴定在②号位
3种
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
课堂检测
③
①
①
②
②
③
—Br
×
×
×
×
1
3)一个溴定在③号位
1种
9
由此推断A环上的四溴代物的异构体的数目有 种。
9
2)一个溴定在②号位
3种
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
课堂检测
9.二甲苯苯环上的一溴代物共有6种,可用还原的方法制得3种二甲苯,它们的熔点分别列于下表:
6种溴的二甲苯的熔点(℃) 234 206 213.8 204 214.5 205
对应还原的二甲苯的熔点(℃) 13 -54 -27 -54 -27 -54
CH3
CH3
CH3
CH3
CH3
CH3
一溴代物
2种
3种
1种
由此推断熔点为234℃的分子结构简式为_________
熔点为-54℃的分子结构简式为_________。
10.写出下列稠环芳香烃的分子式,并根据对称性原理推导其一氯代物的种数。
萘:C10H8
蒽:C14H10
菲:C14H10
C13H9
1
2
(2种)
2 3 1
(3种)
1
2
3
(5种)
1
2
(2种)
课堂检测
4
5
有机物 烷烃 烯烃 炔烃 芳香烃
代表物 CH4 C2H4 C2H2 C6H6
结构特点 全部单键 饱和烃 含碳碳双键不饱和 含碳碳叁键不饱和 特殊的键不饱和
空间结构
物理性质
燃烧
与溴水
KMnO4
主要反应类型
烷烃、烯烃、炔烃、芳香烃的比较
正四面体型
平面型
直线型
平面正六边形
无色气体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
不反应
不反应
取代
加成反应
氧化反应
加成、聚合
加成反应
氧化反应
加成、聚合
不反应
可能发生氧化
取代、加成
以下物质:(1)甲烷 (2)苯 (3)聚乙烯 (4)聚乙炔 (5)2 -丁炔 (6)环己烷 (7)邻二甲苯 (8)苯乙烯。 既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
A、(3)(4)(5)(8) B、(4)(5)(7)(8)
C、(4)(5)(8) D、(3)(4)(5)(7)(8)
C
迁移练习
√
√
√
因化学反应使溴水褪色的烃: ;
能使酸性KMnO4溶液褪色的烃: ;
既能使溴水褪色,又能使酸性KMnO4溶液褪色的烃: ;
既不能使溴水褪色,也不能使酸性KMnO4溶液褪色的烃: ;
因为萃取作用使溴水褪色的烃: 。
烯烃、炔烃
烯烃、炔烃、苯的同系物
烯烃、炔烃
烷烃、苯
液态烷烃、苯、苯的同系物
以上各类烃遇溴水、KMnO4溶液的褪色比较
烷烃、烯烃、炔烃、苯及苯的同系物
第二课时 苯的同系物
第三节 芳香烃
化学家预言第一次世界大战
1912-1913年,德国在国际市场上大量收购石油。由于有利可图,许多国家的石油商都不惜压低价格争着与德国人做生意,但令人不可理解的是,德国人只要婆罗洲的石油,其他的一概不要,并急急忙忙地把收购到婆罗洲的石油运到德国本土去。在石油商人感到百思不得其解时,一位化学家提醒世人说:“德国人在准备发动战争了!”果然不出化学家所料,德国于1914年发动了第一次世界大战。
【情境引入】
这位化学家为何知道德国将发动战争呢?这一奇怪现象引起了一位化学家的注意,他经过化验,发现婆罗洲的石油成分与其他地区的不同,它含有很少的直链烃,它含有大量的苯和甲苯等芳香烃,正是适宜制造“TNT”(三硝基甲苯)烈性炸药的的基础成分。这位化学家们就是在对婆罗洲石油的化学成分进行分析之后才向世人提出历史性预言的。
【情境引入】
那么,“TNT”(三硝基甲苯)是怎么制备的呢?
下面我们来认识以“甲苯”为代表的苯的同系物的性质。
─Br
─CH=CH2
─CH3
─
CH3
─NO2
─CH3
C2H5─
─CH3
思考交流:1、以上有机物哪些属于苯的同系物?
同系物:结构相似、分子组成相差一个或若干个“CH2”原子团的有机物。
2、苯的同系物有什么特点?
二、苯的同系物
1.概念:
二、苯的同系物
判断:下列物质中属于苯的同系物的是( )
A B C
D E F
C D F
②侧链为烷烃基
3. 通式:CnH2n-6(n≥6)
苯分子中的H原子被烷烃基取代后的产物。
2. 结构特点:
①有且只有一个苯环
——“苯环 + 烷基”
─
CH3
CH3
─
H3C
H3C
C2H5
C2H5
─
─
─
─
─OH
写出下列苯的同系物的结构简式并命名。
甲苯
乙苯
邻二甲苯
间二甲苯
C7H8
C8H10
练一练
CH3
CH3
CH3
CH3
CH2
CH3
CH3
CH3
CH3
对二甲苯
正丙苯
邻甲乙苯
间甲乙苯
C9H12
CH3
CH2 CH2
对甲乙苯
CH3
CH
CH3
CH3
CH3
CH2
CH3
CH3
CH2
CH3
CH3
CH2
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
连三甲苯
均三甲苯
偏三甲苯
异丙苯
间二甲苯
> >
4. 苯的同系物的物理性质
一般为无色特殊气味的有毒液体(或固体).
难溶于水,密度比水小.
其中甲苯、二甲苯常用作有机溶剂.
(与苯相似)
思考:下列三种二甲苯的沸点高低情况如何呢?为什么?
邻二甲苯
对二甲苯
144℃
139℃
138℃
CH3
CH3
CH3
CH3
CH3
CH3
沸点:
同分异构体:对称性越好,熔沸点越低!
二、苯的同系物
P43
P44
4. 苯的同系物的物理性质
二、苯的同系物
P44
→随碳原子数增多,熔、沸点依次升高,
密度依次增大;
总体来说:
P44
4. 苯的同系物的物理性质
二、苯的同系物
P44
→同分异构体之间,
苯环上的支链越多,
对称性越好,
溶、沸点越低 ,
密度越小
总体来说:
5.化学性质
都含有苯环,性质相似
例如: 可燃烧;易取代(卤代、硝化);能加成等。
—CH3
1)比较苯和甲苯结构的异同点,
推测甲苯的化学性质。
甲苯含有甲基,由于苯环和甲基相互影响,
在化学性质上与苯也有不同之处。
对比思考:
二、苯的同系物
2CnH2n-6 + 3 (n-1)O2
点燃
2nCO2+ 2(n-3)H2O
(1)可燃性
现象:火焰明亮并带有浓烟
5.化学性质
二、苯的同系物
实验2-2
二、苯的同系物
5.化学性质
实验2-2
实验内容 实验现象 解释
溴水沉到液体底部
溴水的密度大于苯和甲苯的密度
两支试管中液体均分层,均是上层为橙红色,下层几乎无色
苯、甲苯与溴水均不能发生化学反应,但能够萃取溴
二、苯的同系物
5.化学性质
(2)将上述试管用力振荡,静置
(1)向两支分别盛有2mL苯和甲苯的试管中各加入几滴溴水,静置
苯环中的碳碳键是介于碳碳单键和碳碳双键之间的特殊共价键。
?
实验内容 实验现象 解释
(3)向两支分别盛有2mL苯和甲苯的试管中各加入几滴酸性高锰酸钾溶液,静置
紫红色酸性KMnO4溶液沉到液体底部
苯未使酸性高锰酸钾溶液褪色,甲苯使酸性高锰酸钾溶液褪色
苯与酸性KMnO4溶液不反应,甲苯与酸性KMnO4溶液反应
酸性KMnO4溶液的密度大于苯和甲苯的密度
实验2-2
二、苯的同系物
5.化学性质
(4)将上述试管用力振荡,
静置
?
KMnO4(H+)
─
CH3
─
COOH
试从结构角度分析甲苯能使酸性高锰酸钾溶液褪色的原因。
KMnO4(H+)溶液
不反应
KMnO4(H+)溶液
不反应
KMnO4(H+)溶液
─
CH3
─
COOH
[性质探究]
(H—CH3)
CH4
苯环取代甲烷上一个H
苯环上的烷烃基比烷烃性质活泼。
【结论】 苯环影响侧链,使侧链甲基能被KMnO4/H+(aq)氧化
苯的同系物都能使酸性高锰酸钾溶液褪色吗?
资料卡片:
①②能使酸性高锰酸钾溶液褪色
③④不能使酸性高锰酸钾溶液褪色
根据以上信息,你能发现什么规律?
CH2
─
CH3
─
CH
─
─
CH3
CH2
─
CH2
─
─
CH3
─
C
CH3
─
─
CH2CH3
─
H3C
─
C
CH3
─
─
CH3
─
H3C
【思考交流】
KMnO4/H+(aq)
COOH
与苯环直接相连的碳原子上必须连有氢原子
KMnO4/H+(aq)
COOH
,并且烷基均被氧化为-COOH。
②
①
④
③
苯的同系物被酸性KMnO4溶液氧化的条件:
CH3
|
—C—CH3
|
CH3
CH3
|
|
CH2—R
CH3
|
CH3—CH—
CH3
|
—C—CH3
|
CH3
HOOC
|
|
COOH
HOOC—
KMnO4/H+
思考1:产物是什么?
C
|
—C—C
|
C
×
苯环直接相连的碳上无氢原子的侧链不能被氧化
KMnO4/H+
规律:
思考2、如何鉴别苯和甲苯?
可用酸性高锰酸钾溶液鉴别。
思考3:如何除去苯中溶解的少量甲苯
KMnO4/H+(aq)
COOH
分液
NaOH(aq)
COONa
苯
甲苯
苯
苯
(1) 可燃性
(2)使酸性高锰酸钾溶液褪色
[1].氧化反应
思考交流:苯环可以影响烷基,让其易被氧化,烷基是否可以影响苯环呢?
(总结归纳)
二、苯的同系物
5.化学性质
区别苯和苯的同系物
结论:苯环对侧链影响:苯环活化侧链, 使侧链易于氧化。
KMnO4/H+
邻硝基甲苯
对硝基甲苯
CH3
+ HNO3
浓硫酸
300C
CH3
NO2
CH3
NO2
+ H2O
[2].取代反应
①硝化反应
+ H2O
结论:侧链影响了苯环,使苯环上的H(尤其是邻、对位)更活跃,易于取代!
二、苯的同系物
5.化学性质
→温度不同,反应产物不同。硝基取代的位置以甲基的邻、对位为主。
2,4,6-三硝基甲苯
简称三硝基甲苯,又叫TNT
是一种淡黄色针状晶体,不溶于水,是一种烈性炸药
CH3
|
|
NO2
CH3
|
NO2
O2N
+ 3HNO3
+ 3H2O
浓硫酸
TNT广泛用于国防、开矿、筑路、兴修水利等
[2].取代反应
①硝化反应
注意书写规范
TNT炸药爆炸时的场景
②卤代反应
+ Br2
FeBr3
CH3
CH3
Br
+ HBr
原因:苯环受侧链影响,邻位和对位上的H易被取代
CH3
Br
+ HBr
其他纯的卤素单质(X2)也能发生类似的取代反应
如,甲苯使溴水褪色,是因萃取使水层颜色变浅。
注意:但不能与卤水取代!
[2].取代反应
产物以邻溴甲苯、对溴甲苯为主
比较下列两个反应,指出反应的条件是什么?
+ Br2
CH3
CH3
Br
+ HBr
催化剂(FeBr3)
+ Br2
CH3
CH2Br
+ HBr
思考:
光照
(侧链被取代)
(苯环上H被取代)
规 律:
①光照条件下,苯的同系物取代反应发生在烷基侧链上
②卤化铁做催化剂,苯的同系物取代发生在苯环上烷基的邻位、对位上
特点:有机产物不唯一
产物以邻、对位为主
环己烷
+ 3H2
Ni
Δ
(3)加成反应
1 : 3
1 : 3
(较困难)
一元取代产物有几种?
讨论:
4种
5种
甲基环己烷
CH3
|
CH3
|
+ 3H2
催化剂
△
催化剂
+3H2
─
R
─
R
通式:
①可燃性
1、氧化反应:
苯环与侧链的相互影响将使苯的同系物具有特性!
2、取代反应
3、加成反应(较困难)
侧链对苯环的影响,使邻位和对位上的H易被取代
KMnO4
(H+)
——说明了苯环对侧链的影响,使侧链更易氧化
小结:苯的同系物的化学性质
②可使KMnO4(H+)溶液褪色
多苯代脂烃:苯环通过脂肪烃基连接在一起。
联苯或联多苯:苯环之间通过碳碳单键直接相连。
稠环芳香烃:由两个或两个以上的苯环共用相邻的两个碳原子。
萘C10H8
蒽C14H10
二苯甲烷
联苯
对三联苯
多环芳香烃(了解)
—
—CH2—
稠环芳香烃
(课本P46资料卡片)
稠环芳香烃
【概念】由两个或两个以上的苯环共用相邻的2个碳原子而成的一类芳香烃,称为稠环芳香烃。
C10H8
(课本P46资料卡片)
萘
萘是无色片状晶体,具有特殊的气味,易升华,曾经用来防蛀、驱虫,但因它有一定的毒性,现已禁止使用。
萘是一种重要的化工原料。
苯并芘
C14H10
蒽
蒽是生产染料的主要原料。
蒽也是一种无色的晶体,易升华
菲
C14H10
芳香烃的来源及应用
十九世纪初,由于冶金工业的发展,需要大量焦炭,生产焦炭的主要方法是煤的干馏,即对煤隔绝空气加强热。
煤的干馏除得到焦炭外还能获得有用的煤气,但同时却生成一种黑糊糊、粘乎乎有特殊臭味的油状液体!人们把它称作煤焦油。
当时,煤焦油被当作废物扔掉,污染环境,造成公害。随着炼焦工业的发展,煤焦油的堆积也愈来愈严重,煤焦油的利用就成为当时生产中迫切需要解决的一个重要的环境和社会问题。
(了解)
后来,以法拉第为代表的科学家对煤焦油产生了兴趣,并从煤焦油中分离出了以芳香烃为主的多种重要芳香族化合物,又以这些芳香族化合物为原料合成了多种染料、药品、香料、炸药等有机产品。到十九世纪中叶,形成了以煤焦油为原料的有机合成工业。
自从1845年人们从煤焦油内发现苯及其他芳香烃,很长时间里煤是一切芳香烃的主要来源。但是,从1吨煤中仅可以提取1千克苯和2.5千克其他芳香烃。由于芳香烃的需求在不断增长,仅从煤中提炼芳香烃远不能满足化学工业生产的需要。
芳香烃的来源及应用
(了解)
大约到了1930年,由煤生产苯已经发展成为世界性的大吨位工业。1940年以来,通过石油催化重整生成苯、甲苯、二甲苯等;烃裂解制乙烯时,裂解汽油副产物中含芳香烃达40—48%,因此石油也成为芳香烃的重要来源。
芳香烃的来源
①煤的干馏
②石油的催化重整和裂解
芳香烃的来源及应用
(了解)
1.芳香烃的来源
传统工艺:煤焦油
新工艺:石油产品的催化重整和裂解
简单的芳香烃,如苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等。
2.芳香烃的应用
芳香烃的来源及应用
(了解)
芳香烃对人体及环境的危害
烧烤中含有超量的芳香烃,对人体有害。
抽烟呼出的烟气中,含有超
量的芳香烃,对人体有危害!
新装修的居室含有超量的芳香烃,对人体有害。
(1)苯的同系物、芳香烃、芳香族化合物中都含有苯环,所以
是官能团( )
(2)符合CnH2n-6(n≥6)通式的烃一定是苯及其同系物( )
(3)相同物质的量的苯和甲苯与氢气完全加成时消耗的氢气的量相同( )
(4)苯的同系物都能使酸性高锰酸钾溶液褪色( )
(5)甲苯在一定条件下与硝酸反应生成2,4,6-三硝基甲苯,说明苯环对甲基产生了影响( )
×
×
1.正误判断
√
×
×
课堂检测
4、下列关于芳香烃的叙述中不正确的是( )
A.乙烷和甲苯中都含有甲基,甲苯可以被酸性KMnO4溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响。
B.苯和浓硝酸、浓硫酸混合物在100—110℃才能生成二硝基苯,而甲苯在100℃时即可生成三硝基甲苯,说明甲基对苯环产生了影响。
C.苯、甲苯等是重要的有机溶剂,萘(俗称卫生球)是一种重要的绿色杀虫剂。
D.除去苯中混入的少量甲苯可加入适量的酸性KMnO4溶液,充分反应后再加入足量的NaOH溶液,然后分液即可。
C
×
√
√
√
课堂检测
5、要鉴别己烯中是否混有少量甲苯,最恰当的实验方法是( )
A、先加足量酸性高锰酸钾溶液,然后再加入溴水
B、先加适量溴水,然后再加入酸性高锰酸钾溶液
C、点燃这种液体,然后再观察火焰是否有浓烟
D、加入浓硫酸与浓硝酸后加热
B
课堂检测
6.有人设计下图装置吸收氯化氢气体或氨气,能取得良好的效果。由图推测X物质可能是( )
A. 苯 B. 乙醇 C. 四氯化碳 D. 己烷
C
课堂检测
7.某苯的同系物的化学式为C11H16,经测定数据表明:分子中除含苯环外,不再含其他环状结构,分子中还含有两个—CH3,两个—CH2—和一个 ,则该分子由碳链异构所形成的同分异构体有( )
A.3种 B.4种 C.5种 D.6种
B
课堂检测
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
③
①
①
②
②
③
Br
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
1
5
4
2
3
课堂检测
③
①
①
②
②
③
—Br
1
2
3
×
×
2)一个溴定在②号位
3种
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
课堂检测
③
①
①
②
②
③
—Br
×
×
×
×
1
3)一个溴定在③号位
1种
9
由此推断A环上的四溴代物的异构体的数目有 种。
9
2)一个溴定在②号位
3种
8.已知分子式为C12H12的物质A结构简式如下,则A环上的一溴代物有 ( )
A、2种 B、3种
C、4种 D、6种
B
5种
1)一个溴定在①号位
A环上的二溴代物有 种同分异构体?
课堂检测
9.二甲苯苯环上的一溴代物共有6种,可用还原的方法制得3种二甲苯,它们的熔点分别列于下表:
6种溴的二甲苯的熔点(℃) 234 206 213.8 204 214.5 205
对应还原的二甲苯的熔点(℃) 13 -54 -27 -54 -27 -54
CH3
CH3
CH3
CH3
CH3
CH3
一溴代物
2种
3种
1种
由此推断熔点为234℃的分子结构简式为_________
熔点为-54℃的分子结构简式为_________。
10.写出下列稠环芳香烃的分子式,并根据对称性原理推导其一氯代物的种数。
萘:C10H8
蒽:C14H10
菲:C14H10
C13H9
1
2
(2种)
2 3 1
(3种)
1
2
3
(5种)
1
2
(2种)
课堂检测
4
5
有机物 烷烃 烯烃 炔烃 芳香烃
代表物 CH4 C2H4 C2H2 C6H6
结构特点 全部单键 饱和烃 含碳碳双键不饱和 含碳碳叁键不饱和 特殊的键不饱和
空间结构
物理性质
燃烧
与溴水
KMnO4
主要反应类型
烷烃、烯烃、炔烃、芳香烃的比较
正四面体型
平面型
直线型
平面正六边形
无色气体,难溶于水
无色液体
易燃,完全燃烧时生成CO2和H2O
不反应
不反应
取代
加成反应
氧化反应
加成、聚合
加成反应
氧化反应
加成、聚合
不反应
可能发生氧化
取代、加成
以下物质:(1)甲烷 (2)苯 (3)聚乙烯 (4)聚乙炔 (5)2 -丁炔 (6)环己烷 (7)邻二甲苯 (8)苯乙烯。 既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
A、(3)(4)(5)(8) B、(4)(5)(7)(8)
C、(4)(5)(8) D、(3)(4)(5)(7)(8)
C
迁移练习
√
√
√
因化学反应使溴水褪色的烃: ;
能使酸性KMnO4溶液褪色的烃: ;
既能使溴水褪色,又能使酸性KMnO4溶液褪色的烃: ;
既不能使溴水褪色,也不能使酸性KMnO4溶液褪色的烃: ;
因为萃取作用使溴水褪色的烃: 。
烯烃、炔烃
烯烃、炔烃、苯的同系物
烯烃、炔烃
烷烃、苯
液态烷烃、苯、苯的同系物
以上各类烃遇溴水、KMnO4溶液的褪色比较
烷烃、烯烃、炔烃、苯及苯的同系物
