山东省枣庄市2022-2023学年高三上学期期末考试(一调)化学试题(含答案)
文档属性
| 名称 | 山东省枣庄市2022-2023学年高三上学期期末考试(一调)化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 939.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-16 00:00:00 | ||
图片预览



文档简介
2022-2023学年第一学期高三质量检测
化学试题
2023.01
注意事项:
1.答卷前,考生先将自己的姓名、考生号、座号填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将草稿纸、本试卷和答题卡一并交回。
可能用到的相对原子质量:
1 12 14 16 23 27 35.5 56 59 65
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.化学与科技、生产、生活密切相关。下列说法正确的是( )
A.航母拦阻索的主要材料特种钢属于合金材料
B.硼硅玻璃中含有的是一种复杂的氧化物
C.用于打印的高聚物光敏树脂是纯净物
D.用于净水的纳米铜粉属于胶体
2.实验室中下列做法正确的是( )
A.使用酒精洗涤附着在试管壁上的硫单质 B.用酸式滴定管准确量取溶液
C.金属钠着火时用湿抹布盖灭 D.用带橡胶塞的广口瓶盛放溶液
3.某汽车安全气囊的产气药剂主要含有、、、等物质。下列说法错误的是( )
A.是气体发生剂,所含阴离子数目为
B.与爆炸时产生的反应,生成还原产物
C.属于离子化合物,含有化学键类型为离子键、共价键
D.是冷却剂,吸收产气过程中释放的热量
4.我国科学家在实验室首次实现以二氧化碳为原料经11步反应合成淀粉,其中第三步反应为
下列说法错误的是( )
A.该反应属于加成反应 B.钛元素()位于周期表的区
C.与葡萄糖互为同系物 D.转化为淀粉的过程包含了氧化还原反应
5.一种新型电池中的电解质(结构如图所示),其中、、为原子序数依次增大的短周期不同主族元素,原子的单电子数是原子的三倍。下列说法中正确的是( )
A.简单离子半径:
B.基态原子电子的空间运动状态有5种
C.第一电离能:
D.该化合物阴离子呈正八面体结构,键角都是
6.部分含铜物质的价类关系如图所示。下列说法正确的是( )
A.能与溶液反应:
B.在酸性环境中可以转化为和
C.经一步反应可转化为
D.若为,则其水溶液中可能大量存在、、
7.工业制备的流程如图:
下列说法错误的是( )
A.次磷酸钠是正盐
B.的还原性强于
C.黄磷和烧碱溶液的反应为
D.若有参加反应,则整个工业流程中理论上能生成
8.苯乙醛可用于生产工业香料,其制备流程如图。下列说法正确的是( )
A.反应①②原子利用率100%
B.环氧乙烷与二甲醚互为同分异构体
C.预测可以发生反应:
D.反应⑤可用酸性高锰酸钾溶液作氧化剂
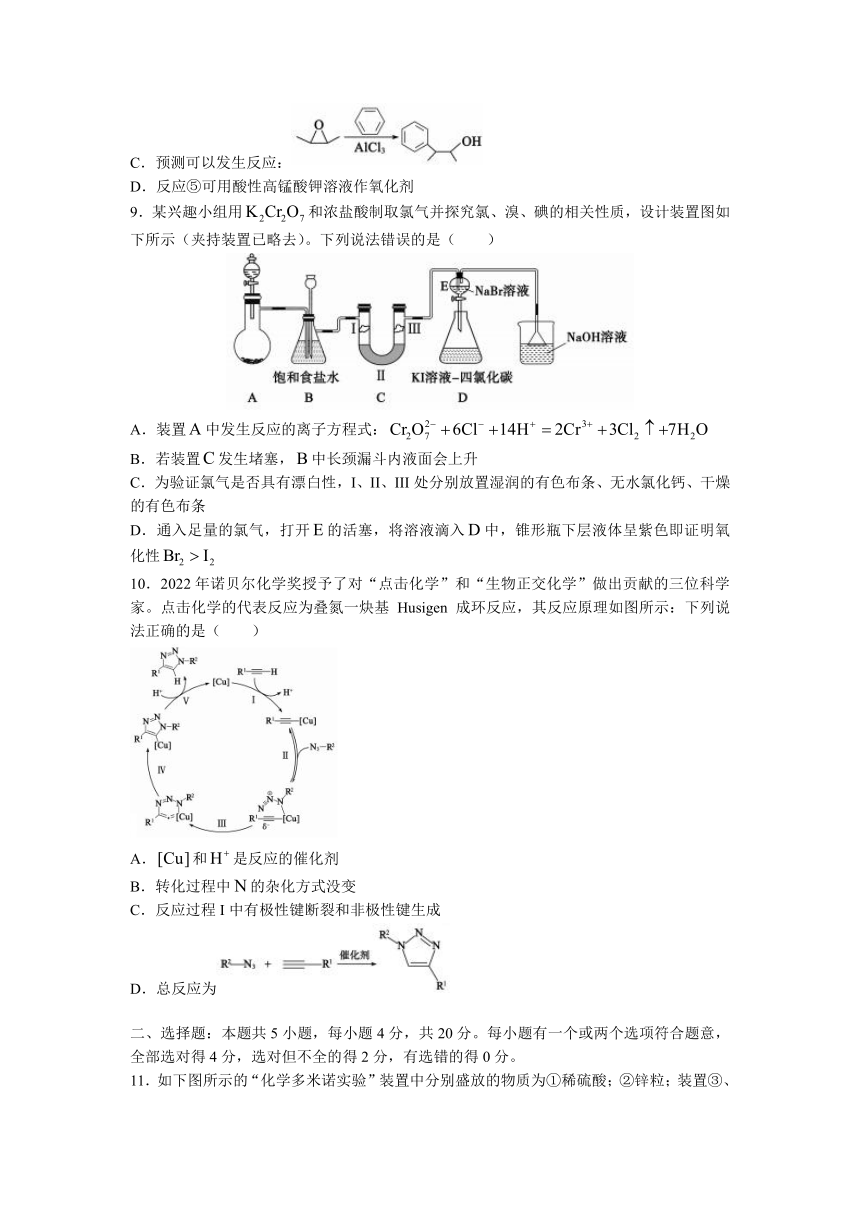
9.某兴趣小组用和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如下所示(夹持装置已略去)。下列说法错误的是( )
A.装置中发生反应的离子方程式:
B.若装置发生堵塞,中长颈漏斗内液面会上升
C.为验证氯气是否具有漂白性,I、II、III处分别放置湿润的有色布条、无水氯化钙、干燥的有色布条
D.通入足量的氯气,打开的活塞,将溶液滴入中,锥形瓶下层液体呈紫色即证明氧化性
10.2022年诺贝尔化学奖授予了对“点击化学”和“生物正交化学”做出贡献的三位科学家。点击化学的代表反应为叠氮一炔基 Husigen 成环反应,其反应原理如图所示:下列说法正确的是( )
A.和是反应的催化剂
B.转化过程中的杂化方式没变
C.反应过程I中有极性键断裂和非极性键生成
D.总反应为
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分。
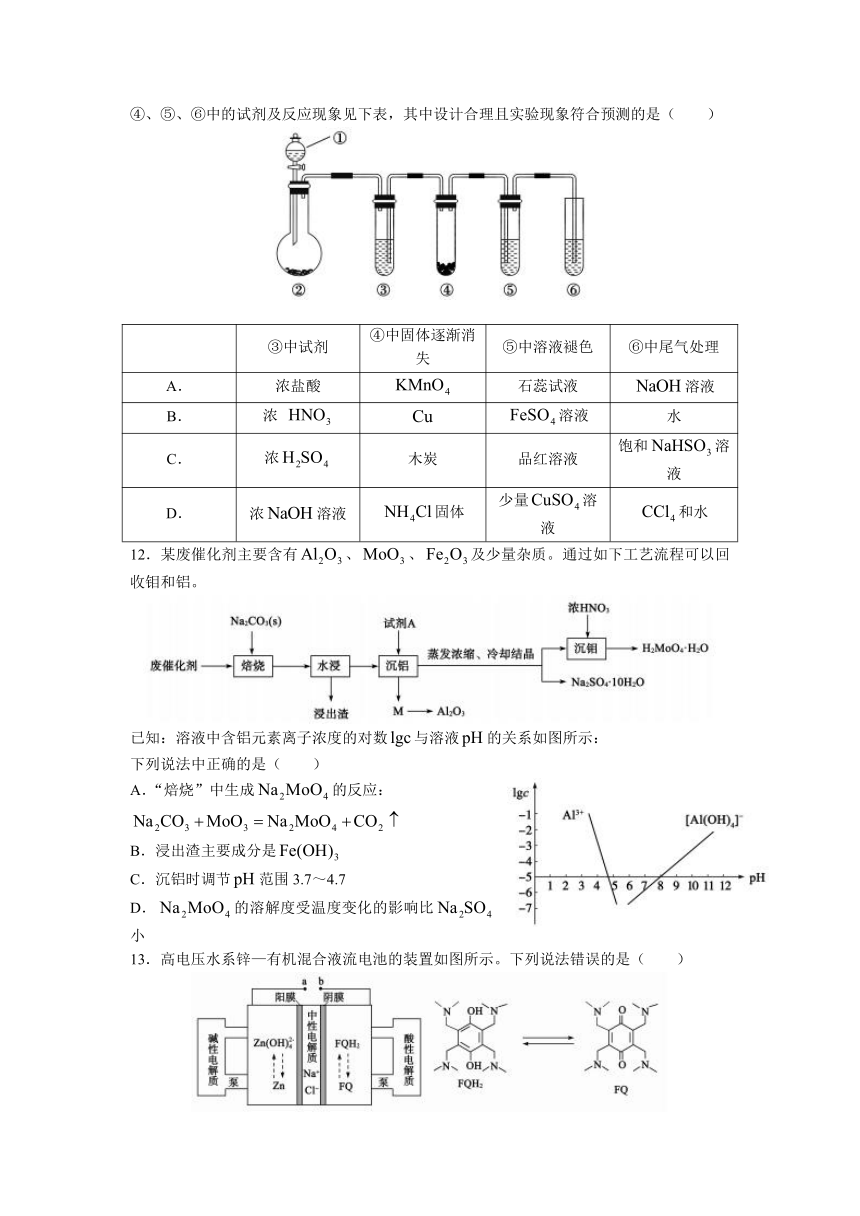
11.如下图所示的“化学多米诺实验”装置中分别盛放的物质为①稀硫酸;②锌粒;装置③、④、⑤、⑥中的试剂及反应现象见下表,其中设计合理且实验现象符合预测的是( )
③中试剂 ④中固体逐渐消失 ⑤中溶液褪色 ⑥中尾气处理
A. 浓盐酸 石蕊试液 溶液
B. 浓 溶液 水
C. 浓 木炭 品红溶液 饱和溶液
D. 浓溶液 固体 少量溶液 和水
12.某废催化剂主要含有、、及少量杂质。通过如下工艺流程可以回收钼和铝。
已知:溶液中含铝元素离子浓度的对数与溶液的关系如图所示:
下列说法中正确的是( )
A.“焙烧”中生成的反应:
B.浸出渣主要成分是
C.沉铝时调节范围3.7~4.7
D.的溶解度受温度变化的影响比小
13.高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是( )
A.放电时,正极区溶液的增大
B.放电时,负极反应式:
C.充电时,电极连接电源负极
D.充电时,负极材料每增重,中性电解质溶液减少
14.时,向的弱碱()溶液中逐滴加入浓度为的盐酸,溶液中
和溶液的随中和率的变化关系如图所示。下列说法错误的是( )
A.该温度下的电离常数
B.该温度下点时,
C.点时,
D.点对应的溶液中,升高温度增大
15.合金的晶胞如图所示,该晶胞可视为、位于形成的立方体体心位置。下列说法正确的是( )
A.原子周围等距且最近的原子有6个
B.合金化学式可表示为
C.若原子的分数坐标为,则原子的为
D.沿晶胞对角面的切面图为
三、非选择题:本题共5小题,共60分。
16.(11分)配合物在工农业生产中有广泛应用。回答下列问题:
(1)铁的一种配合物的化学式为,配体为三氮唑()
①基态与中未成对的电子数之比为___________。
②元素、、、电负性从小到大的顺序为___________。
③阴离子的键角___________的键角(填“等于”、“大于”或“小于”)。
④分子为平面结构,其中共有__________个键;用符号表示大键(代表参与形成大键的原子数,代表参与形成大键的电子数),则分子中的大键可表示为___________。
⑤三氮唑沸点为,与其结构类似的环戊二烯沸点为,三氮唑沸点明显偏高的原因是___________。
(2)钴蓝晶胞结构如下图所示,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___________;为阿伏加德罗常数的值,钴蓝晶体的密度为___________(列计算式)。
17.(13分)铈的氧化物在半导体材料、汽车尾气净化器等方面有广泛应用。以氟碳酸铈(主要成分)为原料制备的工艺流程如下:
已知:①具有较强的氧化性,难溶于一般的酸或碱。
②能与、结合成稳定的、,这有利于酸浸步骤,不利于后续的沉淀步骤。
③溶液中铈的常见离子有、,其中能被萃取剂萃取,而不能被萃取。回答下列问题:
(1)氟碳酸铈矿浮选过程中采用不同捕收剂和(浓度均为)时,对氟碳酸铈矿浮选捕收率的影响如图所示。浮选时应选择的最佳条件为___________。
(2)“氧化焙烧”后的固体产物中含和的物质的量之比为3:1,“酸浸”时溶解,原因是
_________________;有报告认为“酸浸”过程使用盐酸弊端很大,原因是_________________(用化学方程式表示)。
(3)用(有机萃取剂)“萃取”时存在反应,加入氟洗液的目的是
_____________,由题目信息,氟洗液中可加入的物质为______________。
(4)“反萃取”操作过程加入的作用是______________,需要用到的玻璃仪器有______________。
(5)若“沉铈”后,溶液的为6,,此时______________。
已知常温下:
18.(12分)2022年1月1日,曾经的天价抗癌药泊马度胺()被正式纳入国家医保目录,为癌症患者带来了希望。其合成路线如下(部分条件已省略):
已知:①,的结构简式为,
可用代表
②
③,的产物为
回答下列问题:
(1)烃的质谱图如右,其结构简式为___________。
(2)中含氧官能团的名称是___________,有___________个手性碳原子;到的反应类型为___________。
(3)写出等物质的量的化学方程式:___________;由生成至少需要的物质的量为___________。
(4)满足下列要求的的芳香族同分异构体共有___________种;其中核磁共振氢谱中4个峰的分子结构简式为___________
①能发生银镜反应;②与反应有气体产生
(5)如下流程可制备化合物():
则:试剂为___________。
19.(13分)三氯化六氨合钴(III)()是一种重要的含钴配合物,由制备它的流程如下:
已知:在溶液中较稳定,具有较强还原性。
回答下列问题:
(1)原料中加入有利于后续钴离子的络合反应,其原因是_____________。
(2)制备装置如图,向混合液加入溶液与氨水时,应最先打开活塞_____________(填字母代号);加入所有试剂后,水浴的温度控制在左右,反应约30分钟,温度不宜过高的原因是_____________;干燥管中试剂为_____________。
(3)制备的总反应化学方程式为__________________________。
(4)由滤渣获取的步骤:向滤渣中加入左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是_____________(填标号)。
A.甲为浓盐酸 乙为水 B.甲为乙醇 乙为水 C.甲为浓盐酸 乙为乙醇
(5)称取样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,发生反应:
,将生成的氨气通入装有盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用的滴定(杂质不反应)。
①达滴定终点时,共消耗溶液,则样品纯度的为___________。
②下列操作会使纯度测量值偏高的是____________(填标号)。
A.滴定前,碱式滴定管未润洗 B.滴定前尖嘴处无气泡,滴定后有气泡
C.滴定终点时俯视滴定管刻度 D.滴定时选用酚酞为指示剂
20.(11分)丙烷脱氢技术是生产丙烯的主要方法之一,反应过程中伴有生成甲烷、乙烷等物质副反应,涉及反应如下:
主反应:
I.
副反应:
II.
III.
IV.
回答下列问题:
(1)反应II在时能自发进行的理由:________________(用数据说明)。
(2)若仅考虑反应I和II,一定温度下,向恒容密闭容器中通入丙烷,压强为。反应后测得组分的平衡压强(组分的物质的量分数总压):、
①该温度下,反应I用物质的量浓度表示的平衡常数为_____________(保留3位有效数字)。
②平衡时丙烯的选择性为___________()。
(3)对于反应I,下图是某课题组研究设计的一套丙烷连续催化脱氢装置:
①恒温下,将丙烷以恒定的流速依次逐个通过三个相同装置,下图是丙烯的产率随着时间的变化阶段一、二、三的图像,其中阶段二图像是__________(填标号)。
A. B.
②温度对丙烷脱氢反应的影响见下图:
项目
丙烷转化率% 17.67 27.85 32.54 46.35 53.19 57.28
丙烯选择性% 88.64 84.38 71.16 69.65 63.79 48.26
将丙烷以恒定的流速通过不同温度相同反应的装置,主反应适宜的温度范围是_________。
(4)平衡常数与温度的关系曲线如右图所示:下列说法正确的是__________。
A.反应II对应的是图中的曲线③
B.若只发生反应IV,恒温恒容下充入原料
气体,若压强不再改变则反应达到平衡
C.已知高温条件下,键比键更
易断裂,制备丙烯应选择较低温度下的高效催化剂
(5)丙烯与加成制备有机溴代物作为医药合成中间体。反应过程及能量变化如图:
则:升高温度,反应I速率的增大程度____________(填“大于”、“等于”或“小于”)反应II速率的增大程度。
2022-2023学年第一学期高三质量检测
化学试题参考答案
一、选择题
1.A 2.B 3.A 4.C 5.B 6.B 7.D 8.C 9.D 10.D
二、选择题
11.A 12.AD 13.D 14.BC 15.BD
三、非选择题
16.(11分)除注明外,每空1分
(1)①4:5 ②、、、 ③大于 ④8
⑤三氮唑可形成分子间氢键,沸点较高
(2)
17.(13分)除注明外,每空1分
(1)以为捕收剂,(范围内均可)
(2)形成稳定的,促进了的溶解
(或)
(3)去除,提高反萃取效率
(4)将还原为 分液漏斗、烧杯
(5)
18.(12分)除注明外,每空1分
(1)
(2)酰胺基、羧基 1 取代反应
(3) 3
(4)13
(5)
19.(13分)除注明外,每空1分
(1)抑制电离,有利于络合物的形成
(2) 氨水挥发,双氧水分解 或
(3)
或
(4)
(5)①91.67% ②
20.(11分)除注明外,每空1分
(1),,,
,所以反应在时能自发进行
(2)① ②70%
(3)① ②
(4)
(5)小于
化学试题
2023.01
注意事项:
1.答卷前,考生先将自己的姓名、考生号、座号填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将草稿纸、本试卷和答题卡一并交回。
可能用到的相对原子质量:
1 12 14 16 23 27 35.5 56 59 65
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.化学与科技、生产、生活密切相关。下列说法正确的是( )
A.航母拦阻索的主要材料特种钢属于合金材料
B.硼硅玻璃中含有的是一种复杂的氧化物
C.用于打印的高聚物光敏树脂是纯净物
D.用于净水的纳米铜粉属于胶体
2.实验室中下列做法正确的是( )
A.使用酒精洗涤附着在试管壁上的硫单质 B.用酸式滴定管准确量取溶液
C.金属钠着火时用湿抹布盖灭 D.用带橡胶塞的广口瓶盛放溶液
3.某汽车安全气囊的产气药剂主要含有、、、等物质。下列说法错误的是( )
A.是气体发生剂,所含阴离子数目为
B.与爆炸时产生的反应,生成还原产物
C.属于离子化合物,含有化学键类型为离子键、共价键
D.是冷却剂,吸收产气过程中释放的热量
4.我国科学家在实验室首次实现以二氧化碳为原料经11步反应合成淀粉,其中第三步反应为
下列说法错误的是( )
A.该反应属于加成反应 B.钛元素()位于周期表的区
C.与葡萄糖互为同系物 D.转化为淀粉的过程包含了氧化还原反应
5.一种新型电池中的电解质(结构如图所示),其中、、为原子序数依次增大的短周期不同主族元素,原子的单电子数是原子的三倍。下列说法中正确的是( )
A.简单离子半径:
B.基态原子电子的空间运动状态有5种
C.第一电离能:
D.该化合物阴离子呈正八面体结构,键角都是
6.部分含铜物质的价类关系如图所示。下列说法正确的是( )
A.能与溶液反应:
B.在酸性环境中可以转化为和
C.经一步反应可转化为
D.若为,则其水溶液中可能大量存在、、
7.工业制备的流程如图:
下列说法错误的是( )
A.次磷酸钠是正盐
B.的还原性强于
C.黄磷和烧碱溶液的反应为
D.若有参加反应,则整个工业流程中理论上能生成
8.苯乙醛可用于生产工业香料,其制备流程如图。下列说法正确的是( )
A.反应①②原子利用率100%
B.环氧乙烷与二甲醚互为同分异构体
C.预测可以发生反应:
D.反应⑤可用酸性高锰酸钾溶液作氧化剂
9.某兴趣小组用和浓盐酸制取氯气并探究氯、溴、碘的相关性质,设计装置图如下所示(夹持装置已略去)。下列说法错误的是( )
A.装置中发生反应的离子方程式:
B.若装置发生堵塞,中长颈漏斗内液面会上升
C.为验证氯气是否具有漂白性,I、II、III处分别放置湿润的有色布条、无水氯化钙、干燥的有色布条
D.通入足量的氯气,打开的活塞,将溶液滴入中,锥形瓶下层液体呈紫色即证明氧化性
10.2022年诺贝尔化学奖授予了对“点击化学”和“生物正交化学”做出贡献的三位科学家。点击化学的代表反应为叠氮一炔基 Husigen 成环反应,其反应原理如图所示:下列说法正确的是( )
A.和是反应的催化剂
B.转化过程中的杂化方式没变
C.反应过程I中有极性键断裂和非极性键生成
D.总反应为
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.如下图所示的“化学多米诺实验”装置中分别盛放的物质为①稀硫酸;②锌粒;装置③、④、⑤、⑥中的试剂及反应现象见下表,其中设计合理且实验现象符合预测的是( )
③中试剂 ④中固体逐渐消失 ⑤中溶液褪色 ⑥中尾气处理
A. 浓盐酸 石蕊试液 溶液
B. 浓 溶液 水
C. 浓 木炭 品红溶液 饱和溶液
D. 浓溶液 固体 少量溶液 和水
12.某废催化剂主要含有、、及少量杂质。通过如下工艺流程可以回收钼和铝。
已知:溶液中含铝元素离子浓度的对数与溶液的关系如图所示:
下列说法中正确的是( )
A.“焙烧”中生成的反应:
B.浸出渣主要成分是
C.沉铝时调节范围3.7~4.7
D.的溶解度受温度变化的影响比小
13.高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是( )
A.放电时,正极区溶液的增大
B.放电时,负极反应式:
C.充电时,电极连接电源负极
D.充电时,负极材料每增重,中性电解质溶液减少
14.时,向的弱碱()溶液中逐滴加入浓度为的盐酸,溶液中
和溶液的随中和率的变化关系如图所示。下列说法错误的是( )
A.该温度下的电离常数
B.该温度下点时,
C.点时,
D.点对应的溶液中,升高温度增大
15.合金的晶胞如图所示,该晶胞可视为、位于形成的立方体体心位置。下列说法正确的是( )
A.原子周围等距且最近的原子有6个
B.合金化学式可表示为
C.若原子的分数坐标为,则原子的为
D.沿晶胞对角面的切面图为
三、非选择题:本题共5小题,共60分。
16.(11分)配合物在工农业生产中有广泛应用。回答下列问题:
(1)铁的一种配合物的化学式为,配体为三氮唑()
①基态与中未成对的电子数之比为___________。
②元素、、、电负性从小到大的顺序为___________。
③阴离子的键角___________的键角(填“等于”、“大于”或“小于”)。
④分子为平面结构,其中共有__________个键;用符号表示大键(代表参与形成大键的原子数,代表参与形成大键的电子数),则分子中的大键可表示为___________。
⑤三氮唑沸点为,与其结构类似的环戊二烯沸点为,三氮唑沸点明显偏高的原因是___________。
(2)钴蓝晶胞结构如下图所示,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___________;为阿伏加德罗常数的值,钴蓝晶体的密度为___________(列计算式)。
17.(13分)铈的氧化物在半导体材料、汽车尾气净化器等方面有广泛应用。以氟碳酸铈(主要成分)为原料制备的工艺流程如下:
已知:①具有较强的氧化性,难溶于一般的酸或碱。
②能与、结合成稳定的、,这有利于酸浸步骤,不利于后续的沉淀步骤。
③溶液中铈的常见离子有、,其中能被萃取剂萃取,而不能被萃取。回答下列问题:
(1)氟碳酸铈矿浮选过程中采用不同捕收剂和(浓度均为)时,对氟碳酸铈矿浮选捕收率的影响如图所示。浮选时应选择的最佳条件为___________。
(2)“氧化焙烧”后的固体产物中含和的物质的量之比为3:1,“酸浸”时溶解,原因是
_________________;有报告认为“酸浸”过程使用盐酸弊端很大,原因是_________________(用化学方程式表示)。
(3)用(有机萃取剂)“萃取”时存在反应,加入氟洗液的目的是
_____________,由题目信息,氟洗液中可加入的物质为______________。
(4)“反萃取”操作过程加入的作用是______________,需要用到的玻璃仪器有______________。
(5)若“沉铈”后,溶液的为6,,此时______________。
已知常温下:
18.(12分)2022年1月1日,曾经的天价抗癌药泊马度胺()被正式纳入国家医保目录,为癌症患者带来了希望。其合成路线如下(部分条件已省略):
已知:①,的结构简式为,
可用代表
②
③,的产物为
回答下列问题:
(1)烃的质谱图如右,其结构简式为___________。
(2)中含氧官能团的名称是___________,有___________个手性碳原子;到的反应类型为___________。
(3)写出等物质的量的化学方程式:___________;由生成至少需要的物质的量为___________。
(4)满足下列要求的的芳香族同分异构体共有___________种;其中核磁共振氢谱中4个峰的分子结构简式为___________
①能发生银镜反应;②与反应有气体产生
(5)如下流程可制备化合物():
则:试剂为___________。
19.(13分)三氯化六氨合钴(III)()是一种重要的含钴配合物,由制备它的流程如下:
已知:在溶液中较稳定,具有较强还原性。
回答下列问题:
(1)原料中加入有利于后续钴离子的络合反应,其原因是_____________。
(2)制备装置如图,向混合液加入溶液与氨水时,应最先打开活塞_____________(填字母代号);加入所有试剂后,水浴的温度控制在左右,反应约30分钟,温度不宜过高的原因是_____________;干燥管中试剂为_____________。
(3)制备的总反应化学方程式为__________________________。
(4)由滤渣获取的步骤:向滤渣中加入左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是_____________(填标号)。
A.甲为浓盐酸 乙为水 B.甲为乙醇 乙为水 C.甲为浓盐酸 乙为乙醇
(5)称取样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,发生反应:
,将生成的氨气通入装有盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用的滴定(杂质不反应)。
①达滴定终点时,共消耗溶液,则样品纯度的为___________。
②下列操作会使纯度测量值偏高的是____________(填标号)。
A.滴定前,碱式滴定管未润洗 B.滴定前尖嘴处无气泡,滴定后有气泡
C.滴定终点时俯视滴定管刻度 D.滴定时选用酚酞为指示剂
20.(11分)丙烷脱氢技术是生产丙烯的主要方法之一,反应过程中伴有生成甲烷、乙烷等物质副反应,涉及反应如下:
主反应:
I.
副反应:
II.
III.
IV.
回答下列问题:
(1)反应II在时能自发进行的理由:________________(用数据说明)。
(2)若仅考虑反应I和II,一定温度下,向恒容密闭容器中通入丙烷,压强为。反应后测得组分的平衡压强(组分的物质的量分数总压):、
①该温度下,反应I用物质的量浓度表示的平衡常数为_____________(保留3位有效数字)。
②平衡时丙烯的选择性为___________()。
(3)对于反应I,下图是某课题组研究设计的一套丙烷连续催化脱氢装置:
①恒温下,将丙烷以恒定的流速依次逐个通过三个相同装置,下图是丙烯的产率随着时间的变化阶段一、二、三的图像,其中阶段二图像是__________(填标号)。
A. B.
②温度对丙烷脱氢反应的影响见下图:
项目
丙烷转化率% 17.67 27.85 32.54 46.35 53.19 57.28
丙烯选择性% 88.64 84.38 71.16 69.65 63.79 48.26
将丙烷以恒定的流速通过不同温度相同反应的装置,主反应适宜的温度范围是_________。
(4)平衡常数与温度的关系曲线如右图所示:下列说法正确的是__________。
A.反应II对应的是图中的曲线③
B.若只发生反应IV,恒温恒容下充入原料
气体,若压强不再改变则反应达到平衡
C.已知高温条件下,键比键更
易断裂,制备丙烯应选择较低温度下的高效催化剂
(5)丙烯与加成制备有机溴代物作为医药合成中间体。反应过程及能量变化如图:
则:升高温度,反应I速率的增大程度____________(填“大于”、“等于”或“小于”)反应II速率的增大程度。
2022-2023学年第一学期高三质量检测
化学试题参考答案
一、选择题
1.A 2.B 3.A 4.C 5.B 6.B 7.D 8.C 9.D 10.D
二、选择题
11.A 12.AD 13.D 14.BC 15.BD
三、非选择题
16.(11分)除注明外,每空1分
(1)①4:5 ②、、、 ③大于 ④8
⑤三氮唑可形成分子间氢键,沸点较高
(2)
17.(13分)除注明外,每空1分
(1)以为捕收剂,(范围内均可)
(2)形成稳定的,促进了的溶解
(或)
(3)去除,提高反萃取效率
(4)将还原为 分液漏斗、烧杯
(5)
18.(12分)除注明外,每空1分
(1)
(2)酰胺基、羧基 1 取代反应
(3) 3
(4)13
(5)
19.(13分)除注明外,每空1分
(1)抑制电离,有利于络合物的形成
(2) 氨水挥发,双氧水分解 或
(3)
或
(4)
(5)①91.67% ②
20.(11分)除注明外,每空1分
(1),,,
,所以反应在时能自发进行
(2)① ②70%
(3)① ②
(4)
(5)小于
同课章节目录
