人教版(2019)高二化学选择性必修三 3.1卤代烃 课件(45张ppt)
文档属性
| 名称 | 人教版(2019)高二化学选择性必修三 3.1卤代烃 课件(45张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 78.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-16 00:00:00 | ||
图片预览






文档简介
(共45张PPT)
第三章 烃的衍生物
第一节 卤代烃
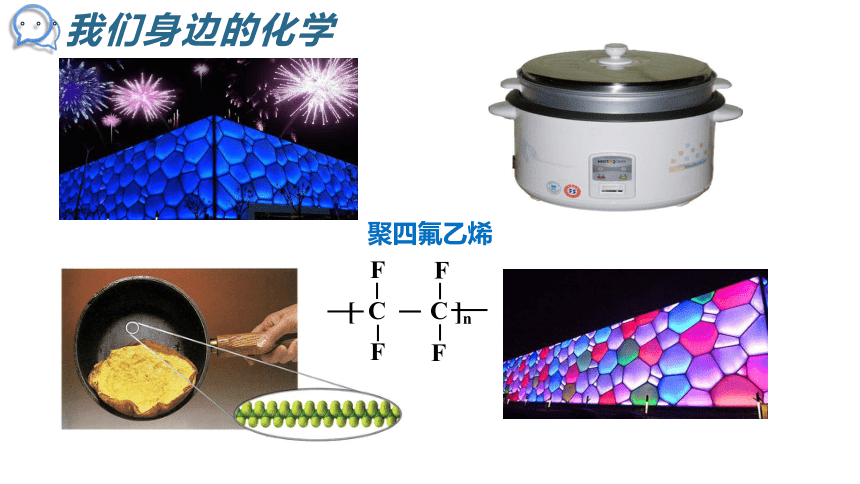
聚四氟乙烯
[ C C ]n
F
F
F
F
我们身边的化学
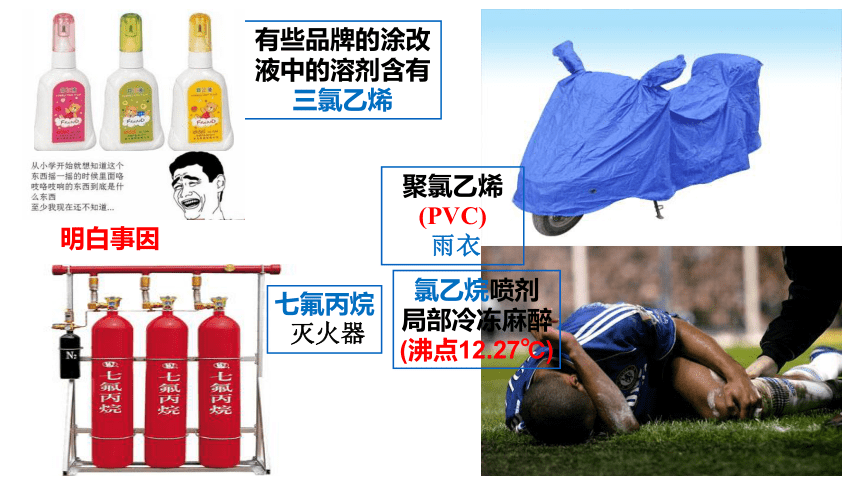
有些品牌的涂改液中的溶剂含有
三氯乙烯
聚氯乙烯(PVC)
雨衣
氯乙烷喷剂
局部冷冻麻醉
(沸点12.27℃)
七氟丙烷
灭火器
明白事因
烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。官能团是 -X(Cl、Br、I、F),可表示为R—X(X=F、Cl、Br、I)。
饱和一卤代烃的通式为:CnH2n+1X
1.卤代烃的定义
一、卤代烃的结构与物理性质
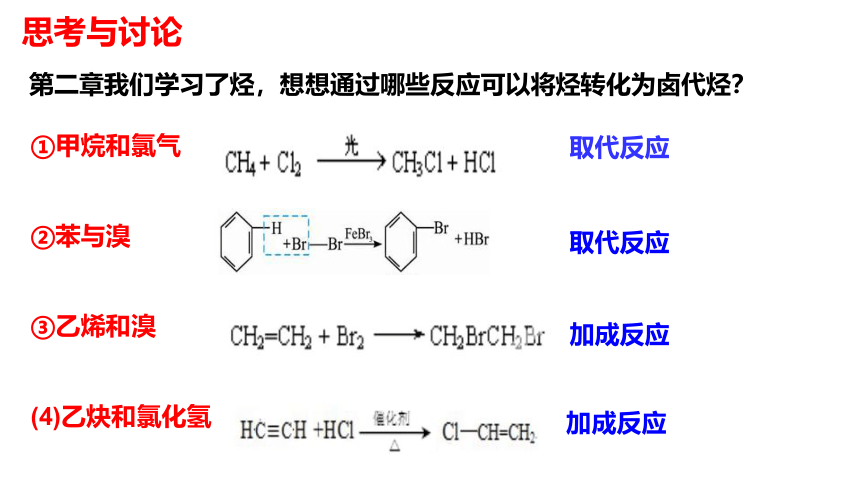
第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
①甲烷和氯气
②苯与溴
③乙烯和溴
(4)乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
思考与讨论
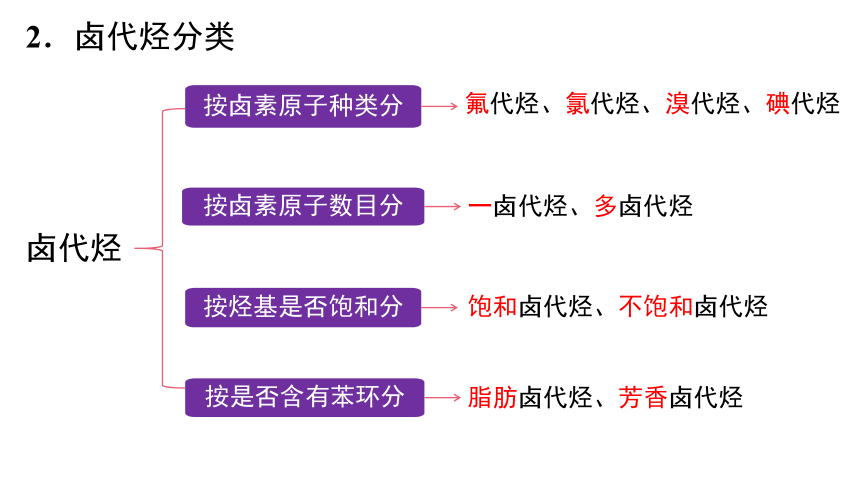
2.卤代烃分类
卤代烃
按卤素原子种类分
氟代烃、氯代烃、溴代烃、碘代烃
按卤素原子数目分
一卤代烃、多卤代烃
按烃基是否饱和分
饱和卤代烃、不饱和卤代烃
按是否含有苯环分
脂肪卤代烃、芳香卤代烃
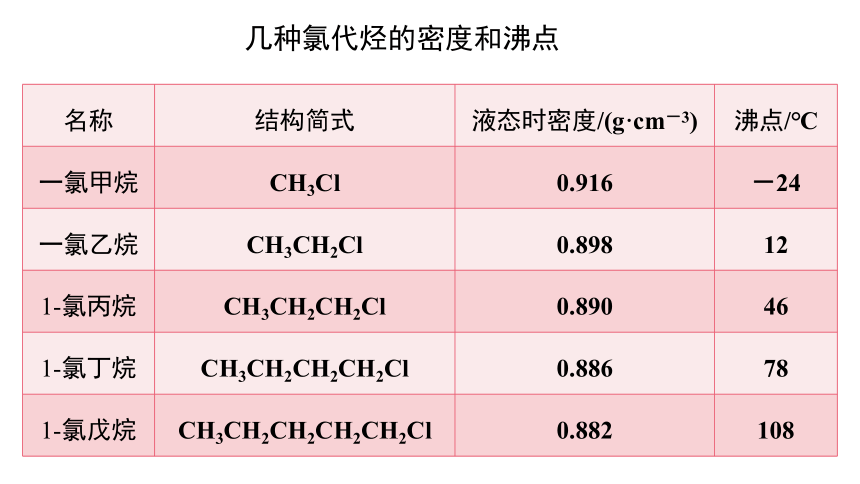
几种氯代烃的密度和沸点
名称 结构简式 液态时密度/(g·cm-3) 沸点/℃
一氯甲烷 CH3Cl 0.916 -24
一氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
3.物理性质
(1)状态:常温下,卤代烃中除一氯甲烷、一溴甲烷、氯乙烯、氯乙烷为气体外,其余均为液体或固体。
(2)溶解性:卤代烃都不溶于水,可溶于有机溶剂,某些卤代烃本身就是很好的有机溶剂,如CCl4、氯仿(CHCl3)等。
(3)密度与沸点:
①卤代烃的密度和沸点都高于相应的烃;
③沸点: 一般随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。如沸点CH3Cl<CH3CH2Cl。
②密度:除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。卤代烃的密度一般随烃基中碳原子数目的增加而减小,
如ρ(CH3Cl)>ρ(CH3CH2Cl);
4.卤代烃的系统命名——类似于烃的命名方法
(1)选择含有卤原子最长的碳链为主链,按主链所含碳原子数目称为“某烷”;
(2)把支链和卤原子看作取代基,主链碳原子的编号从靠近支链一端开始。
(3)命名时把烷基、卤原子的位置和名称依次写在烷烃名称之前。
先考虑碳架异构,即写出同碳数烷烃异构体。
再考虑官能团的位置异构
【思考】说出分子式为 C5H11Cl 的同分异构体有几种?
5.卤代烃的同分异构体
3种等效氢——3种一氯代物
4种等效氢——4种一氯代物
1种等效氢——1种一氯代物
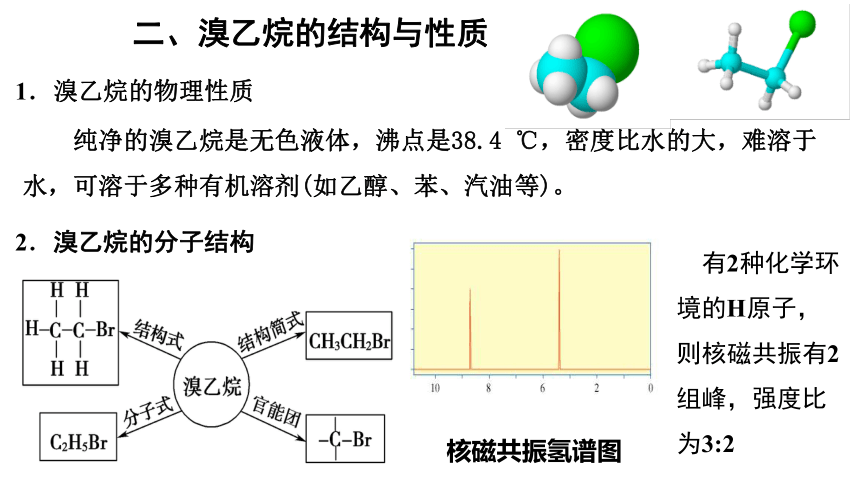
二、溴乙烷的结构与性质
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如乙醇、苯、汽油等)。
1.溴乙烷的物理性质
2.溴乙烷的分子结构
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
核磁共振氢谱图
取一支试管,滴入10~15滴溴乙烷;再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
3.溴乙烷的化学性质
(1)取代反应——又称水解反应
实验 现象 溴乙烷中加入NaOH溶液,振荡后加热,静置后,液体分层,取上层清液滴入过量稀硝酸中,再向其中滴加AgNO3溶液,试管中有浅黄色沉淀生成
有关的 化学方 程式 C2H5Br+NaOH C2H5OH+NaBr,
NaBr+AgNO3===AgBr↓+NaNO3
原理 在卤代烃分子中,卤素原子的电负性比碳原子大,使C—X的电子向卤素原子偏移,进而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性较强的共价键:Cδ+—Xδ。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他原子或原子团所取代,生成负离子而离去。
(1)取代反应——又称水解反应
①条件:NaOH水溶液、加热。
②反应方程式:
C-Br键为极性键,由于溴原子吸引电子能力强, C-Br键易断裂,使溴原子易被取代。因Br的作用,溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
由于卤素原子的引入使卤代烃的反应活性增强。
①CH3CH2Br
② CH3CH2Br
NaOH溶液
AgNO3溶液
取上层清液硝酸酸化
(2)如何判断CH3CH2Br是否完全水解?
(3)如何判断CH3CH2Br已发生水解?
看反应后的溶液是否出现分层,如分层,则没有完全水解。
(1)为什么要加入稀硝酸酸化溶液?
中和过量的NaOH溶液,防止生成Ag2O棕褐色沉淀,影响Br-检验。
【实验注意事项】
待溶液分层后,用滴管吸取少量上层清液,移入另一盛稀硝酸的试管中,然后滴入2~3滴硝酸银溶液,如有淡黄色沉淀出现,则证明含有溴离子。
(2)消去反应——又称为消除反应。
①条件:NaOH的乙醇溶液、加热
③反应方程式:(以溴乙烷为例)
②反应原理:
CH2=CH2 ↑ + NaBr+H2O
△
乙醇
CH2-CH2
Br
H
+ NaOH
④实质:相邻的两个C上脱去HX形成不饱和键!
消去反应(消除反应)
①定义
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键的化合物的反应。
②溴乙烷的消去反应
反应条件 强碱(如NaOH或KOH)的乙醇溶液、加热
断键方式 断裂C—Br和邻位碳原子上的C—H
化学方程式 C2H5Br+NaOH CH2=CH2↑+NaBr+H2O
(1)没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
③卤代烃的消去反应规律
(4)二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
(3)有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 = CH—CH2—CH3。
(2)有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发生消去反应。例如
(1)没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
(2)有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发
③卤代烃的消去反应规律
(4)二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
比较溴乙烷的取代反应和消去反应,体会反应条件对化学反应的影响。
取代反应 消去反应
反应物
反应条件
生成物
断键位置
应用
结论
CH3CH2Br
CH3CH2Br
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
C—Br
C—Br、邻碳的C—H
引入羟基
引入不饱和键
无醇则有醇,有醇则无醇
(3)加成和加聚反应
三、卤代烃的用途与危害
卤代烃破坏臭氧层原理(了解)
氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为:
1.要使卤代烃中的卤素原子转化成离子需要什么条件
提示:氢氧化钠水溶液并加热。
2.在加入NaOH水溶液并加热后,加稀硝酸的作用是什么
提示:NaOH的存在影响卤素离子的检验,所以需要先加入稀硝酸中和NaOH。
四、卤代烃中卤素原子的检验
思考与讨论
1.实验步骤和实验原理
3.注意:
①一般不用卤代烃的消去反应检验卤族元素,因为有的卤代烃不能发生消去反应。
②卤代烃水解完成后,检验卤离子前,应先加硝酸使溶液呈酸性再加AgNO3溶液。
易错警示
(1)卤代烃均属于非电解质,不能电离出X-,不能用AgNO3溶液直接检验卤代烃中卤素的存在。
(2)将卤代烃中的卤素原子X转化为X-也可利用卤代烃的消去反应。
(3)检验卤代烃中的卤素时,常出现的错误是忽略用稀硝酸酸化以中和NaOH。
(1)卤代烃是一类特殊的烃。 ( )
提示:卤代烃含卤族元素,不是烃。
(2)卤代烃中一定含有的元素为C、H和卤素。( )
提示:卤代烃不一定含H元素,如CCl4。
(3)卤代烃不一定是由烃分子和卤素单质发生取代反应得到的。( )
提示:卤代烃可以由烃分子发生加成反应得到,如乙烯与溴水发生加成反应得到1,2-二溴乙烷。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
√
×
×
(4)分子中碳原子数少于4的烃,在常温下为气体,溴乙烷分子中含2个碳原子,所以其在常温下也是气体。( )
提示:溴乙烷不属于烃,常温下是液体。
(5)卤代烃属于有机化合物,都易燃烧。( )
提示:CCl4等卤代烃不能燃烧。
(6)卤代烃都可以发生水解反应和消去反应。( )
提示:卤代烃都可以水解,但不一定能够发生消去反应,如CH3Cl不能发生消去反应。
(7)由溴乙烷生成乙烯和生成乙醇的反应类型及反应条件均相同。( )
提示:前者为消去反应,后者为取代反应,且反应条件不同。
×
×
×
×
(8)卤代烃是一类特殊的烃,可分为单卤代烃和多卤代烃。 ( )
(9)卤代烃不溶于水,均为液态或固体。 ( )
(10)卤代烃发生水解反应时,断裂C—X键。 ( )
(11)任何卤代烃不能发生反应。 ( )
(12)溴乙烷加入HNO3酸化的AgNO3溶液有浅黄色沉淀生成。( )
√
×
×
×
×
2.下列物质中,不属于卤代烃的是( )
A.CH2Cl2 B.CCl2F2
解析:A选项可看作是CH4中两个氢原子被两个氯原子取代的产物,属于卤代烃;B选项可看作是CH4中两个氢原子被两个氯原子取代,另两个氢原子被两个氟原子取代的产物,属于卤代烃;C选项可看作是苯中的一个氢原子被硝基取代的产物,不属于卤代烃;D选项可看作是苯中的一个氢原子被溴原子取代的产物,属于卤代烃。
C
2.溴乙烷中混有杂质乙醇,除去乙醇的方法是( )
A.加热蒸发 B.过滤
C.加水、萃取、分液 D.加苯、萃取、分液
解析:溴乙烷难溶于水,而乙醇可与水以任意比例互溶,故可向混合液中加水进行萃取,然后分液即可除去乙醇。
C
3.下列有关溴乙烷的叙述中,正确的是( )
A.溴乙烷不溶于水,能溶于多种有机溶剂
B.溴乙烷与NaOH的水溶液共热可生成乙烯
C.C与Br之间的共用电子对偏向C原子
D.实验室通常用乙烯与溴的四氯化碳溶液反应来制取溴乙烷
解析:溴乙烷与NaOH的水溶液共热发生水解反应(属取代反应)生成乙醇,溴乙烷与NaOH的乙醇溶液共热发生消去反应生成乙烯,两者反应的条件不同,其反应的类型和产物也不同,不能混淆;由于Br原子吸引电子的能力较强,C、Br之间的共用电子对偏向Br原子;乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷,在实验室中通常用乙烯与溴化氢反应来制取溴乙烷。
A
4.下列有机化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃不存在同分异构体的是( )
B
解析:分析四种物质:A项物质分子中只有一个碳原子,C项物质分子中卤素原子所连碳原子的相邻碳原子上没有氢原子,所以均不能发生消去反应;B、D项物质既可以发生水解反应,又可以发生消去反应,其中B项物质发生消去反应后只能生成一种烯烃CH3CH=CH2,而D项物质发生消去反应可以得到两种烯烃
5.(Ⅰ)1 溴丙烷、2 溴丙烷分别与氢氧化钠醇溶液混合加热;(Ⅱ)1 溴丙烷、2 溴丙烷分别与氢氧化钠水溶液混合加热。关于反应中生成的有机物的说法中正确的是( )
A.(Ⅰ)和(Ⅱ)产物均不同 B.(Ⅰ)和(Ⅱ)产物均相同
C.(Ⅰ)产物相同,(Ⅱ)产物不同 D.(Ⅰ)产物不同,(Ⅱ)产物相同
解析:1 溴丙烷、2 溴丙烷分别与氢氧化钠醇溶液混合加热,均发生消去反应生成丙烯;1 溴丙烷、2 溴丙烷分别与氢氧化钠水溶液混合加热,均发生取代反应,前者生成1 丙醇,后者生成2 丙醇,故选C。
C
6.下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
C
解析:A项,卤代烃的密度比水的大,错;B项,卤代烃的沸点比相应烃的高,错;D项,前者大,错。
7.溴乙烷在某种条件下可生成乙烯或乙醇,下列说法正确的是( )
A.生成乙烯的条件可以是热的氢氧化钾水溶液
B.生成乙醇的条件可以是热的氢氧化钾水溶液
C.生成乙烯的条件是加热
D.生成乙醇的条件可以是热的氢氧化钾醇溶液
解析:溴乙烷与氢氧化钾的醇溶液共热生成乙烯,故A、C项错误;溴乙烷与氢氧化钾的水溶液共热生成乙醇,故B项正确,D项错误。
B
8.为了检验溴乙烷中含有溴元素,有以下操作,顺序合理的是( )
①加AgNO3溶液 ②加NaOH水溶液 ③加热
④加蒸馏水 ⑤加稀硝酸至溶液显酸性
A.②①③⑤ B.②④⑤③ C.②③⑤① D.②①⑤③
解析:溴乙烷中的溴元素不是以离子状态存在的,不能与AgNO3溶液直接反应,因此,必须先使它变为溴离子。由题意可知,应先使溴乙烷在强碱的水溶液中水解得到溴离子,但反应后溶液显碱性,不能直接加入AgNO3溶液检验,否则Ag+与OH-反应生成AgOH,而AgOH不稳定,分解生成Ag2O沉淀,影响溴离子的检验,故需加入足量稀硝酸使溶液呈酸性,再加AgNO3溶液检验。
C
9.Ⅰ.下列卤代烃在NaOH的乙醇溶液中加热得到的烯烃分别有几种
1种
3种
Ⅱ.在实验室里鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加入MnO2固体;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用稀硝酸酸化。
(1)鉴定氯酸钾晶体中氯元素的操作步骤是 (填序号)。
(2)鉴定1-氯丙烷中氯元素的操作步骤是 (填序号)。
④③⑤⑦①
②③⑦①
Ⅱ.要鉴定样品中是否含有氯元素,通常先将样品中的氯元素转化为Cl-,再使Cl-转化为AgCl沉淀,利用沉淀的颜色和不溶于稀硝酸的性质来判断氯元素的存在。
(1)鉴定氯酸钾晶体中的氯元素,可先将其转化成氯化钾,再加入稀硝酸和AgNO3溶液来检验Cl-。
(2)鉴定1-氯丙烷中的氯元素,必须先将1-氯丙烷中的氯原子通过水解或消去反应变为氯离子,再滴入稀硝酸和AgNO3溶液来检验。即先取少量1-氯丙烷加入NaOH的水溶液并加热,使其水解后,再加入足量稀硝酸,然后加入AgNO3溶液,观察沉淀的颜色来判断是否含有氯元素。其实验的关键是在加入AgNO3溶液之前,应加入稀硝酸酸化,以中和过量的NaOH溶液,防止NaOH与AgNO3溶液反应生成的沉淀对实验的观察产生干扰。
第三章 烃的衍生物
第一节 卤代烃
聚四氟乙烯
[ C C ]n
F
F
F
F
我们身边的化学
有些品牌的涂改液中的溶剂含有
三氯乙烯
聚氯乙烯(PVC)
雨衣
氯乙烷喷剂
局部冷冻麻醉
(沸点12.27℃)
七氟丙烷
灭火器
明白事因
烃分子中的氢原子被卤素原子取代后生成的化合物称为卤代烃。官能团是 -X(Cl、Br、I、F),可表示为R—X(X=F、Cl、Br、I)。
饱和一卤代烃的通式为:CnH2n+1X
1.卤代烃的定义
一、卤代烃的结构与物理性质
第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
①甲烷和氯气
②苯与溴
③乙烯和溴
(4)乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
思考与讨论
2.卤代烃分类
卤代烃
按卤素原子种类分
氟代烃、氯代烃、溴代烃、碘代烃
按卤素原子数目分
一卤代烃、多卤代烃
按烃基是否饱和分
饱和卤代烃、不饱和卤代烃
按是否含有苯环分
脂肪卤代烃、芳香卤代烃
几种氯代烃的密度和沸点
名称 结构简式 液态时密度/(g·cm-3) 沸点/℃
一氯甲烷 CH3Cl 0.916 -24
一氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
3.物理性质
(1)状态:常温下,卤代烃中除一氯甲烷、一溴甲烷、氯乙烯、氯乙烷为气体外,其余均为液体或固体。
(2)溶解性:卤代烃都不溶于水,可溶于有机溶剂,某些卤代烃本身就是很好的有机溶剂,如CCl4、氯仿(CHCl3)等。
(3)密度与沸点:
①卤代烃的密度和沸点都高于相应的烃;
③沸点: 一般随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。如沸点CH3Cl<CH3CH2Cl。
②密度:除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。卤代烃的密度一般随烃基中碳原子数目的增加而减小,
如ρ(CH3Cl)>ρ(CH3CH2Cl);
4.卤代烃的系统命名——类似于烃的命名方法
(1)选择含有卤原子最长的碳链为主链,按主链所含碳原子数目称为“某烷”;
(2)把支链和卤原子看作取代基,主链碳原子的编号从靠近支链一端开始。
(3)命名时把烷基、卤原子的位置和名称依次写在烷烃名称之前。
先考虑碳架异构,即写出同碳数烷烃异构体。
再考虑官能团的位置异构
【思考】说出分子式为 C5H11Cl 的同分异构体有几种?
5.卤代烃的同分异构体
3种等效氢——3种一氯代物
4种等效氢——4种一氯代物
1种等效氢——1种一氯代物
二、溴乙烷的结构与性质
纯净的溴乙烷是无色液体,沸点是38.4 ℃,密度比水的大,难溶于水,可溶于多种有机溶剂(如乙醇、苯、汽油等)。
1.溴乙烷的物理性质
2.溴乙烷的分子结构
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
核磁共振氢谱图
取一支试管,滴入10~15滴溴乙烷;再加入1 mL 5% NaOH溶液,振荡后加热,静置。待溶液分层后,用胶头滴管小心吸取少量上层水溶液,移入另一支盛有1 mL稀硝酸的试管中,然后加入2滴AgNO3溶液,观察实验现象。
3.溴乙烷的化学性质
(1)取代反应——又称水解反应
实验 现象 溴乙烷中加入NaOH溶液,振荡后加热,静置后,液体分层,取上层清液滴入过量稀硝酸中,再向其中滴加AgNO3溶液,试管中有浅黄色沉淀生成
有关的 化学方 程式 C2H5Br+NaOH C2H5OH+NaBr,
NaBr+AgNO3===AgBr↓+NaNO3
原理 在卤代烃分子中,卤素原子的电负性比碳原子大,使C—X的电子向卤素原子偏移,进而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性较强的共价键:Cδ+—Xδ。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他原子或原子团所取代,生成负离子而离去。
(1)取代反应——又称水解反应
①条件:NaOH水溶液、加热。
②反应方程式:
C-Br键为极性键,由于溴原子吸引电子能力强, C-Br键易断裂,使溴原子易被取代。因Br的作用,溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
由于卤素原子的引入使卤代烃的反应活性增强。
①CH3CH2Br
② CH3CH2Br
NaOH溶液
AgNO3溶液
取上层清液硝酸酸化
(2)如何判断CH3CH2Br是否完全水解?
(3)如何判断CH3CH2Br已发生水解?
看反应后的溶液是否出现分层,如分层,则没有完全水解。
(1)为什么要加入稀硝酸酸化溶液?
中和过量的NaOH溶液,防止生成Ag2O棕褐色沉淀,影响Br-检验。
【实验注意事项】
待溶液分层后,用滴管吸取少量上层清液,移入另一盛稀硝酸的试管中,然后滴入2~3滴硝酸银溶液,如有淡黄色沉淀出现,则证明含有溴离子。
(2)消去反应——又称为消除反应。
①条件:NaOH的乙醇溶液、加热
③反应方程式:(以溴乙烷为例)
②反应原理:
CH2=CH2 ↑ + NaBr+H2O
△
乙醇
CH2-CH2
Br
H
+ NaOH
④实质:相邻的两个C上脱去HX形成不饱和键!
消去反应(消除反应)
①定义
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键的化合物的反应。
②溴乙烷的消去反应
反应条件 强碱(如NaOH或KOH)的乙醇溶液、加热
断键方式 断裂C—Br和邻位碳原子上的C—H
化学方程式 C2H5Br+NaOH CH2=CH2↑+NaBr+H2O
(1)没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
③卤代烃的消去反应规律
(4)二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
(3)有两个邻位碳原子,且碳原子上均有氢原子时,发生消去反应可能生成不同的产物。例如,
发生消去反应的产物为CH3—CH=CH—CH3、CH2 = CH—CH2—CH3。
(2)有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发生消去反应。例如
(1)没有邻位碳原子的卤代烃不能发生消去反应,例如CH3Br。
(2)有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不能发
③卤代烃的消去反应规律
(4)二卤代烃发生消去反应后可能在有机化合物中引入碳碳三键或两个碳碳双键。例如,
比较溴乙烷的取代反应和消去反应,体会反应条件对化学反应的影响。
取代反应 消去反应
反应物
反应条件
生成物
断键位置
应用
结论
CH3CH2Br
CH3CH2Br
NaOH水溶液,加热
NaOH醇溶液,加热
CH3CH2OH、NaBr
CH2=CH2、NaBr、H2O
溴乙烷在不同的条件下发生不同类型的反应
C—Br
C—Br、邻碳的C—H
引入羟基
引入不饱和键
无醇则有醇,有醇则无醇
(3)加成和加聚反应
三、卤代烃的用途与危害
卤代烃破坏臭氧层原理(了解)
氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为:
1.要使卤代烃中的卤素原子转化成离子需要什么条件
提示:氢氧化钠水溶液并加热。
2.在加入NaOH水溶液并加热后,加稀硝酸的作用是什么
提示:NaOH的存在影响卤素离子的检验,所以需要先加入稀硝酸中和NaOH。
四、卤代烃中卤素原子的检验
思考与讨论
1.实验步骤和实验原理
3.注意:
①一般不用卤代烃的消去反应检验卤族元素,因为有的卤代烃不能发生消去反应。
②卤代烃水解完成后,检验卤离子前,应先加硝酸使溶液呈酸性再加AgNO3溶液。
易错警示
(1)卤代烃均属于非电解质,不能电离出X-,不能用AgNO3溶液直接检验卤代烃中卤素的存在。
(2)将卤代烃中的卤素原子X转化为X-也可利用卤代烃的消去反应。
(3)检验卤代烃中的卤素时,常出现的错误是忽略用稀硝酸酸化以中和NaOH。
(1)卤代烃是一类特殊的烃。 ( )
提示:卤代烃含卤族元素,不是烃。
(2)卤代烃中一定含有的元素为C、H和卤素。( )
提示:卤代烃不一定含H元素,如CCl4。
(3)卤代烃不一定是由烃分子和卤素单质发生取代反应得到的。( )
提示:卤代烃可以由烃分子发生加成反应得到,如乙烯与溴水发生加成反应得到1,2-二溴乙烷。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
√
×
×
(4)分子中碳原子数少于4的烃,在常温下为气体,溴乙烷分子中含2个碳原子,所以其在常温下也是气体。( )
提示:溴乙烷不属于烃,常温下是液体。
(5)卤代烃属于有机化合物,都易燃烧。( )
提示:CCl4等卤代烃不能燃烧。
(6)卤代烃都可以发生水解反应和消去反应。( )
提示:卤代烃都可以水解,但不一定能够发生消去反应,如CH3Cl不能发生消去反应。
(7)由溴乙烷生成乙烯和生成乙醇的反应类型及反应条件均相同。( )
提示:前者为消去反应,后者为取代反应,且反应条件不同。
×
×
×
×
(8)卤代烃是一类特殊的烃,可分为单卤代烃和多卤代烃。 ( )
(9)卤代烃不溶于水,均为液态或固体。 ( )
(10)卤代烃发生水解反应时,断裂C—X键。 ( )
(11)任何卤代烃不能发生反应。 ( )
(12)溴乙烷加入HNO3酸化的AgNO3溶液有浅黄色沉淀生成。( )
√
×
×
×
×
2.下列物质中,不属于卤代烃的是( )
A.CH2Cl2 B.CCl2F2
解析:A选项可看作是CH4中两个氢原子被两个氯原子取代的产物,属于卤代烃;B选项可看作是CH4中两个氢原子被两个氯原子取代,另两个氢原子被两个氟原子取代的产物,属于卤代烃;C选项可看作是苯中的一个氢原子被硝基取代的产物,不属于卤代烃;D选项可看作是苯中的一个氢原子被溴原子取代的产物,属于卤代烃。
C
2.溴乙烷中混有杂质乙醇,除去乙醇的方法是( )
A.加热蒸发 B.过滤
C.加水、萃取、分液 D.加苯、萃取、分液
解析:溴乙烷难溶于水,而乙醇可与水以任意比例互溶,故可向混合液中加水进行萃取,然后分液即可除去乙醇。
C
3.下列有关溴乙烷的叙述中,正确的是( )
A.溴乙烷不溶于水,能溶于多种有机溶剂
B.溴乙烷与NaOH的水溶液共热可生成乙烯
C.C与Br之间的共用电子对偏向C原子
D.实验室通常用乙烯与溴的四氯化碳溶液反应来制取溴乙烷
解析:溴乙烷与NaOH的水溶液共热发生水解反应(属取代反应)生成乙醇,溴乙烷与NaOH的乙醇溶液共热发生消去反应生成乙烯,两者反应的条件不同,其反应的类型和产物也不同,不能混淆;由于Br原子吸引电子的能力较强,C、Br之间的共用电子对偏向Br原子;乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷,在实验室中通常用乙烯与溴化氢反应来制取溴乙烷。
A
4.下列有机化合物中,既能发生水解反应,又能发生消去反应,且消去反应生成的烯烃不存在同分异构体的是( )
B
解析:分析四种物质:A项物质分子中只有一个碳原子,C项物质分子中卤素原子所连碳原子的相邻碳原子上没有氢原子,所以均不能发生消去反应;B、D项物质既可以发生水解反应,又可以发生消去反应,其中B项物质发生消去反应后只能生成一种烯烃CH3CH=CH2,而D项物质发生消去反应可以得到两种烯烃
5.(Ⅰ)1 溴丙烷、2 溴丙烷分别与氢氧化钠醇溶液混合加热;(Ⅱ)1 溴丙烷、2 溴丙烷分别与氢氧化钠水溶液混合加热。关于反应中生成的有机物的说法中正确的是( )
A.(Ⅰ)和(Ⅱ)产物均不同 B.(Ⅰ)和(Ⅱ)产物均相同
C.(Ⅰ)产物相同,(Ⅱ)产物不同 D.(Ⅰ)产物不同,(Ⅱ)产物相同
解析:1 溴丙烷、2 溴丙烷分别与氢氧化钠醇溶液混合加热,均发生消去反应生成丙烯;1 溴丙烷、2 溴丙烷分别与氢氧化钠水溶液混合加热,均发生取代反应,前者生成1 丙醇,后者生成2 丙醇,故选C。
C
6.下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
C
解析:A项,卤代烃的密度比水的大,错;B项,卤代烃的沸点比相应烃的高,错;D项,前者大,错。
7.溴乙烷在某种条件下可生成乙烯或乙醇,下列说法正确的是( )
A.生成乙烯的条件可以是热的氢氧化钾水溶液
B.生成乙醇的条件可以是热的氢氧化钾水溶液
C.生成乙烯的条件是加热
D.生成乙醇的条件可以是热的氢氧化钾醇溶液
解析:溴乙烷与氢氧化钾的醇溶液共热生成乙烯,故A、C项错误;溴乙烷与氢氧化钾的水溶液共热生成乙醇,故B项正确,D项错误。
B
8.为了检验溴乙烷中含有溴元素,有以下操作,顺序合理的是( )
①加AgNO3溶液 ②加NaOH水溶液 ③加热
④加蒸馏水 ⑤加稀硝酸至溶液显酸性
A.②①③⑤ B.②④⑤③ C.②③⑤① D.②①⑤③
解析:溴乙烷中的溴元素不是以离子状态存在的,不能与AgNO3溶液直接反应,因此,必须先使它变为溴离子。由题意可知,应先使溴乙烷在强碱的水溶液中水解得到溴离子,但反应后溶液显碱性,不能直接加入AgNO3溶液检验,否则Ag+与OH-反应生成AgOH,而AgOH不稳定,分解生成Ag2O沉淀,影响溴离子的检验,故需加入足量稀硝酸使溶液呈酸性,再加AgNO3溶液检验。
C
9.Ⅰ.下列卤代烃在NaOH的乙醇溶液中加热得到的烯烃分别有几种
1种
3种
Ⅱ.在实验室里鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加入MnO2固体;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用稀硝酸酸化。
(1)鉴定氯酸钾晶体中氯元素的操作步骤是 (填序号)。
(2)鉴定1-氯丙烷中氯元素的操作步骤是 (填序号)。
④③⑤⑦①
②③⑦①
Ⅱ.要鉴定样品中是否含有氯元素,通常先将样品中的氯元素转化为Cl-,再使Cl-转化为AgCl沉淀,利用沉淀的颜色和不溶于稀硝酸的性质来判断氯元素的存在。
(1)鉴定氯酸钾晶体中的氯元素,可先将其转化成氯化钾,再加入稀硝酸和AgNO3溶液来检验Cl-。
(2)鉴定1-氯丙烷中的氯元素,必须先将1-氯丙烷中的氯原子通过水解或消去反应变为氯离子,再滴入稀硝酸和AgNO3溶液来检验。即先取少量1-氯丙烷加入NaOH的水溶液并加热,使其水解后,再加入足量稀硝酸,然后加入AgNO3溶液,观察沉淀的颜色来判断是否含有氯元素。其实验的关键是在加入AgNO3溶液之前,应加入稀硝酸酸化,以中和过量的NaOH溶液,防止NaOH与AgNO3溶液反应生成的沉淀对实验的观察产生干扰。
