化学人教版九下:11.1 生活中常见的盐(第3课时)课后作业(含答案)
文档属性
| 名称 | 化学人教版九下:11.1 生活中常见的盐(第3课时)课后作业(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 487.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-17 00:00:00 | ||
图片预览



文档简介
11.1 生活中常见的盐(第3课时)
一、单选题
当汽车发生剧烈碰撞时,安全气囊里的物质发生反应使气囊弹出,以保护司乘人员的安全。某汽车安全气囊中的反应之一为:,该反应属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
下列反应属于复分解反应的是( )
A. 3
B.
C.
D.
下列反应中不属于复分解反应的是( )
A.
B.
C.
D.
下列各组物质中,不能发生复分解反应的是( )
A. 和 B. 和
C. 和 D. 和
化学学习者常用化学思维去认识和理解世界。下列关于化学学科核心素养的选项叙述正确的是( )
A. 宏观与微观:稀盐酸和稀硫酸都具有酸的通性,原因是都能在溶液中解离出氢离子
B. 变化与守恒:依据化学方程式,可推测的化学式为
C. 证据与推理:复分解反应有沉淀或气体或水生成,则属于复分解反应
D. 探究与创新:测定空气中氧气的含量实验中,将红磷换成铁丝结论更精确
下列物质能溶于水并形成无色溶液的是( )
A. B. C. D.
下列各组物质中,能发生复分解反应且反应后溶液总质量变大的是( )
A. 铜和硝酸银溶液 B. 稀硫酸和氢氧化钾溶液
C. 稀盐酸和碳酸钙粉末 D. 二氧化碳和澄清石灰水
下列说法正确的是( )
A. 浓硫酸暴露在空气中长期放置,溶质质量分数会增大
B. 为彻底除净铁制品表面的铁锈,可加入过量盐酸
C. 硫酸氢钠中含有氢离子,所以硫酸氢钠属于酸
D. 复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变
用数轴表示某些化学知识直观、简明、易记。下列表示错误的是( )
A.
B.
C.
D.
下列溶液暴露在空气中,因发生化学变化而使溶液质量增大的是( )
A. 氢氧化钠溶液 B. 石灰水 C. 浓硫酸 D. 饱和食盐水
将足量和依次通入饱和食盐水,发生反应:
;
。
下列说法正确的是( )
A. 总的化学方程式为
B. 上述反应过程中观察不到明显现象
C. 反应是有沉淀生成的复分解反应
D. 上述反应中有元素化合价发生变化
下列各组常见的固体物质中,用水不能区分的是 ( )
A. 和 B. 和
C. 和 D. 和
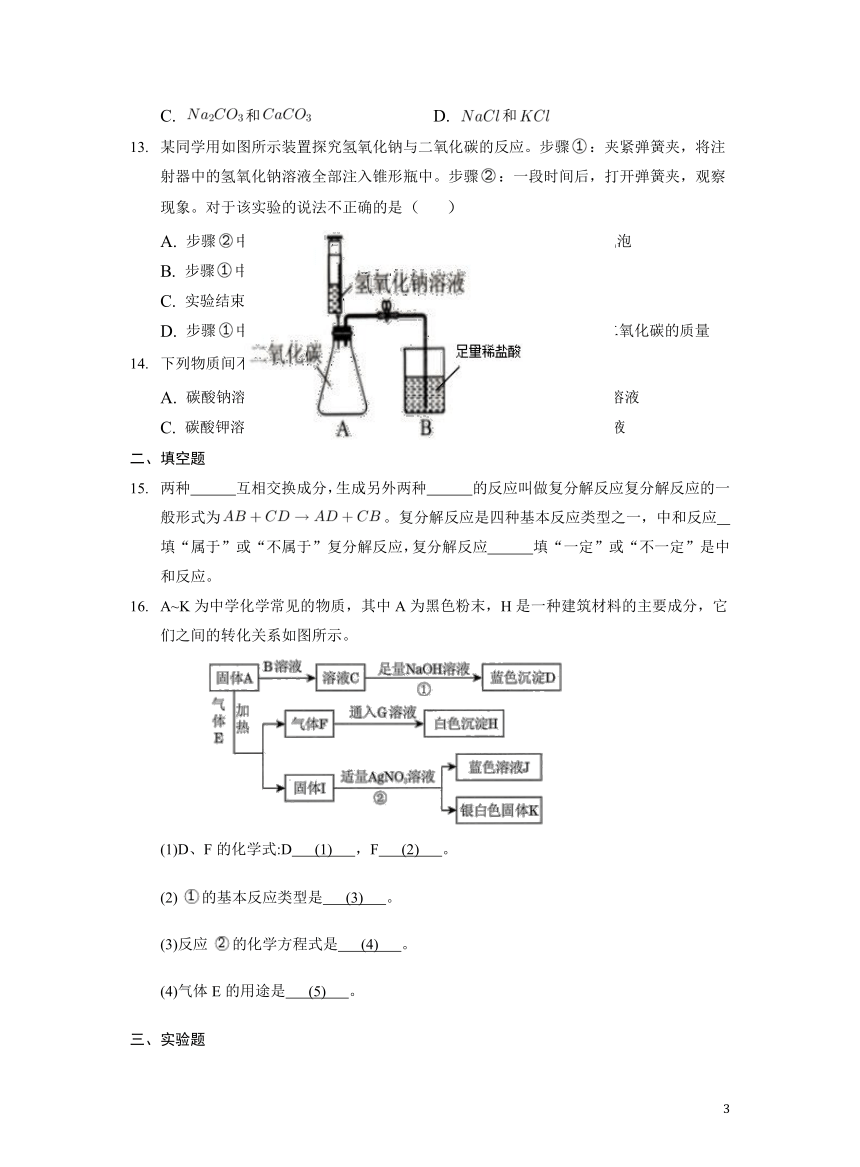
某同学用如图所示装置探究氢氧化钠与二氧化碳的反应。步骤:夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。步骤:一段时间后,打开弹簧夹,观察现象。对于该实验的说法不正确的是( )
A. 步骤中打开弹簧夹后,稀盐酸进入中,锥形瓶内产生大量气泡
B. 步骤中发生的反应属于复分解反应
C. 实验结束后,向锥形瓶内溶液中滴入酚酞试液,溶液为无色
D. 步骤中氢氧化钠吸收的二氧化碳的质量等于步骤中产生的二氧化碳的质量
下列物质间不能发生复分解反应的是( )
A. 碳酸钠溶液和氯化钙溶液 B. 氢氧化钠溶液和氯化钾溶液
C. 碳酸钾溶液和盐酸 D. 硫酸铜溶液和氯化钡溶液
二、填空题
两种 互相交换成分,生成另外两种 的反应叫做复分解反应复分解反应的一般形式为。复分解反应是四种基本反应类型之一,中和反应 填“属于”或“不属于”复分解反应,复分解反应 填“一定”或“不一定”是中和反应。
A~K为中学化学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转化关系如图所示。
(1)D、F的化学式:D (1) ,F (2) 。
(2)的基本反应类型是 (3) 。
(3)反应的化学方程式是 (4) 。
(4)气体E的用途是 (5) 。
三、实验题
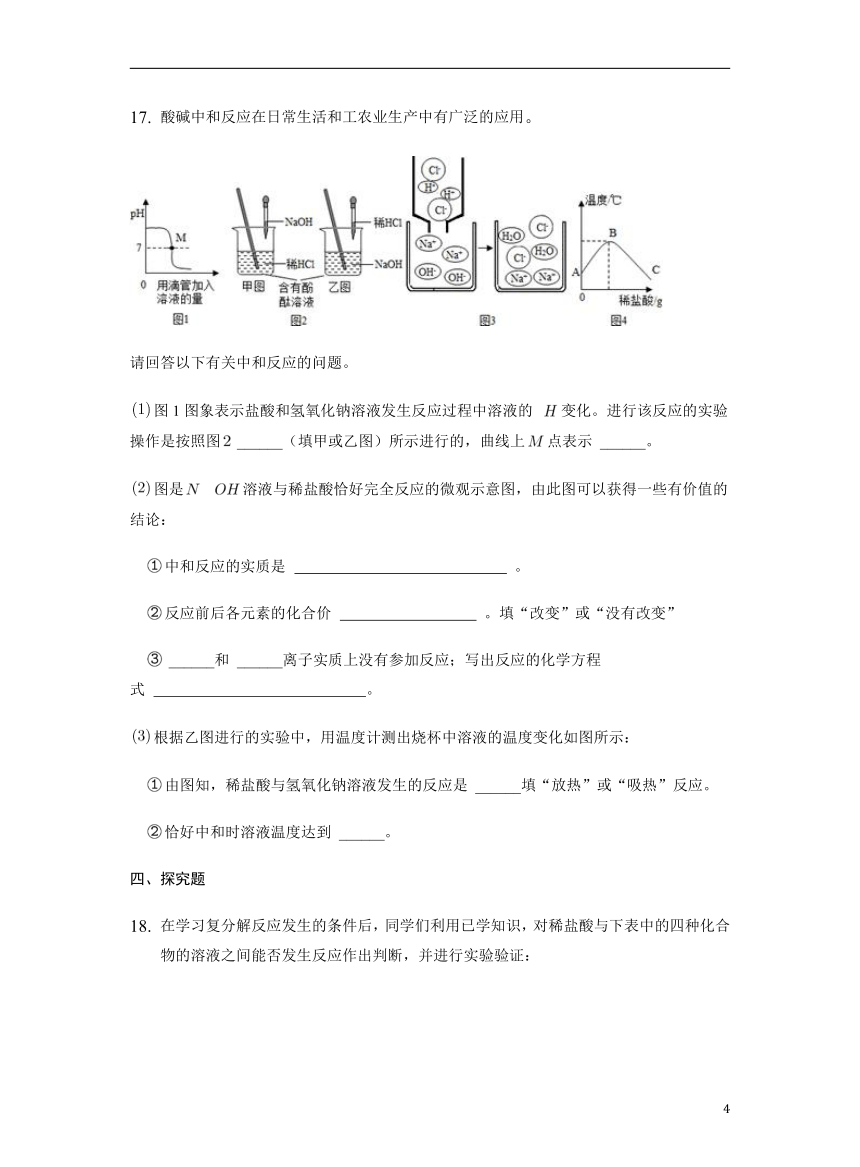
酸碱中和反应在日常生活和工农业生产中有广泛的应用。
请回答以下有关中和反应的问题。
图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的 变化。进行该反应的实验操作是按照图______(填甲或乙图)所示进行的,曲线上点表示 ______。
图是 溶液与稀盐酸恰好完全反应的微观示意图,由此图可以获得一些有价值的结论:
中和反应的实质是 。
反应前后各元素的化合价 。填“改变”或“没有改变”
______和 ______离子实质上没有参加反应;写出反应的化学方程式 。
根据乙图进行的实验中,用温度计测出烧杯中溶液的温度变化如图所示:
由图知,稀盐酸与氢氧化钠溶液发生的反应是 ______填“放热”或“吸热”反应。
恰好中和时溶液温度达到 ______。
四、探究题
在学习复分解反应发生的条件后,同学们利用已学知识,对稀盐酸与下表中的四种化合物的溶液之间能否发生反应作出判断,并进行实验验证:
物质 氢氧化钠溶液 硫酸钠溶液 碳酸钾溶液 硝酸银溶液
实验现象 无明显现象 无明显现象 产生气泡 产生白色沉淀
能否反应 能反应 不能反应 能反应 能反应
【提出问题】对于上述无明显现象的反应,如何设计实验进行验证?
【设计实验】为了验证氢氧化钠溶液与稀盐酸能发生化学反应,小刚设计了如下实验方案并进行实验。
实验步骤 实验现象 实验结论
将氢氧化钠溶液滴入盛有稀盐酸的试管中,振荡 溶液呈无色 稀盐酸与氢氧化钠溶液能发生化学反应
向步骤所得无色溶液中滴加几滴酚酞溶液 溶液呈无色
【分析讨论】小刚设计的实验方案________填“可行”或“不可行”,说明理由:________________。
【总结提升】通过以上实验分析,对于无明显现象的反应,验证思路可以是:
Ⅰ验证生成物是否存在。
Ⅱ验证________是否消失。
【拓展迁移】氢氧化钠溶液与稀盐酸发生反应的微观示意图如图所示,该反应的实质是____________________________________________________________。写出另一个符合上述反应实质的化学方程式__________________________________________________________。
将一定量的氢氧化钠溶液与稀盐酸混合,充分反应后所得溶液中溶质成分可能有________种情况,具体的溶质组合情况分别是________________填化学式。
学习复分解反应发生条件时,小红同学做了下表中的四个实验。
试管编号
试管内试剂 溶液 溶液 溶液 溶液
加入稀硫酸后的现象 无明显现象 无明显现象 产生气泡 白色沉淀生成
根据以上实验,可以判断试管中发生了复分解反应。试管中反应的化学方程式为_________________________________________________________________________。
小明同学向盛有溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管中也发生了反应,这种试剂是__________。
为了验证试管中是否发生复分解反应,小明同学进行了如下探究。
提出猜想猜想:试管中没有发生复分解反应,溶液中有,即和同时存在溶液中。
猜想:试管中发生了复分解反应,溶液中无。
老师提示会对的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。
设计方案
沉淀的化学式是__________。老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为应该将所选的试剂__________改成__________。
小明按照修改后的方案进行了实验,最后得出的结论是猜想正确,则步骤Ⅱ、步骤Ⅲ中必然会观察到的现象是____________________________________________________________。
实验反思小明反思进行步骤Ⅲ时,加溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是________________________________。
某化学兴趣小组同学做了如图甲、乙两个实验。请回答下列问题:
实验的现象为 ______。
把试管中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液。试管中上层清液中的溶质一定含有 ______。写出混合后一定发生反应的化学方程式 ______。
混合后所得溶液中可能含有的溶质为 ______。
【反思拓展】甲、乙两实验能发生复分解反应的原因是 ______。
参考答案
1.【答案】C
2.【答案】D
3.【答案】C
4.【答案】D
5.【答案】A
6.【答案】B
7.【答案】C
8.【答案】D
9.【答案】A
10.【答案】A
11.【答案】C
12.【答案】D
13.【答案】B
14.【答案】B
15.【答案】化合物
化合物 属于 不一定
16.【答案】 复分解反应 ++ 冶炼金属(或作燃料)
17.【答案】乙 盐酸和氢氧化钠恰好反应
氢离子和氢氧根离子反应生成水 不变
放热 点或最高点
18.【答案】【分析讨论】可行;滴加酚酞溶液后溶液仍为无色,说明溶液中氢氧化钠消失了,进而说明氢氧化钠与稀盐酸发生了化学反应 【总结提升】反应物 【拓展迁移】酸中的氢离子与碱中的氢氧根离子结合成水分子; 合理即可 ;、和、和
19.【答案】
酚酞试液或其他合理答案
; ; ;均有白色沉淀;氢氧化钠先与溶液中的酸反应
20.【答案】有白色沉淀生成 氢氧化钠、硫酸钠 氢氧化钠 都生成了沉淀
2
1
一、单选题
当汽车发生剧烈碰撞时,安全气囊里的物质发生反应使气囊弹出,以保护司乘人员的安全。某汽车安全气囊中的反应之一为:,该反应属于( )
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
下列反应属于复分解反应的是( )
A. 3
B.
C.
D.
下列反应中不属于复分解反应的是( )
A.
B.
C.
D.
下列各组物质中,不能发生复分解反应的是( )
A. 和 B. 和
C. 和 D. 和
化学学习者常用化学思维去认识和理解世界。下列关于化学学科核心素养的选项叙述正确的是( )
A. 宏观与微观:稀盐酸和稀硫酸都具有酸的通性,原因是都能在溶液中解离出氢离子
B. 变化与守恒:依据化学方程式,可推测的化学式为
C. 证据与推理:复分解反应有沉淀或气体或水生成,则属于复分解反应
D. 探究与创新:测定空气中氧气的含量实验中,将红磷换成铁丝结论更精确
下列物质能溶于水并形成无色溶液的是( )
A. B. C. D.
下列各组物质中,能发生复分解反应且反应后溶液总质量变大的是( )
A. 铜和硝酸银溶液 B. 稀硫酸和氢氧化钾溶液
C. 稀盐酸和碳酸钙粉末 D. 二氧化碳和澄清石灰水
下列说法正确的是( )
A. 浓硫酸暴露在空气中长期放置,溶质质量分数会增大
B. 为彻底除净铁制品表面的铁锈,可加入过量盐酸
C. 硫酸氢钠中含有氢离子,所以硫酸氢钠属于酸
D. 复分解反应只是两种化合物相互交换成分,则复分解反应一定没有元素化合价的改变
用数轴表示某些化学知识直观、简明、易记。下列表示错误的是( )
A.
B.
C.
D.
下列溶液暴露在空气中,因发生化学变化而使溶液质量增大的是( )
A. 氢氧化钠溶液 B. 石灰水 C. 浓硫酸 D. 饱和食盐水
将足量和依次通入饱和食盐水,发生反应:
;
。
下列说法正确的是( )
A. 总的化学方程式为
B. 上述反应过程中观察不到明显现象
C. 反应是有沉淀生成的复分解反应
D. 上述反应中有元素化合价发生变化
下列各组常见的固体物质中,用水不能区分的是 ( )
A. 和 B. 和
C. 和 D. 和
某同学用如图所示装置探究氢氧化钠与二氧化碳的反应。步骤:夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。步骤:一段时间后,打开弹簧夹,观察现象。对于该实验的说法不正确的是( )
A. 步骤中打开弹簧夹后,稀盐酸进入中,锥形瓶内产生大量气泡
B. 步骤中发生的反应属于复分解反应
C. 实验结束后,向锥形瓶内溶液中滴入酚酞试液,溶液为无色
D. 步骤中氢氧化钠吸收的二氧化碳的质量等于步骤中产生的二氧化碳的质量
下列物质间不能发生复分解反应的是( )
A. 碳酸钠溶液和氯化钙溶液 B. 氢氧化钠溶液和氯化钾溶液
C. 碳酸钾溶液和盐酸 D. 硫酸铜溶液和氯化钡溶液
二、填空题
两种 互相交换成分,生成另外两种 的反应叫做复分解反应复分解反应的一般形式为。复分解反应是四种基本反应类型之一,中和反应 填“属于”或“不属于”复分解反应,复分解反应 填“一定”或“不一定”是中和反应。
A~K为中学化学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转化关系如图所示。
(1)D、F的化学式:D (1) ,F (2) 。
(2)的基本反应类型是 (3) 。
(3)反应的化学方程式是 (4) 。
(4)气体E的用途是 (5) 。
三、实验题
酸碱中和反应在日常生活和工农业生产中有广泛的应用。
请回答以下有关中和反应的问题。
图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的 变化。进行该反应的实验操作是按照图______(填甲或乙图)所示进行的,曲线上点表示 ______。
图是 溶液与稀盐酸恰好完全反应的微观示意图,由此图可以获得一些有价值的结论:
中和反应的实质是 。
反应前后各元素的化合价 。填“改变”或“没有改变”
______和 ______离子实质上没有参加反应;写出反应的化学方程式 。
根据乙图进行的实验中,用温度计测出烧杯中溶液的温度变化如图所示:
由图知,稀盐酸与氢氧化钠溶液发生的反应是 ______填“放热”或“吸热”反应。
恰好中和时溶液温度达到 ______。
四、探究题
在学习复分解反应发生的条件后,同学们利用已学知识,对稀盐酸与下表中的四种化合物的溶液之间能否发生反应作出判断,并进行实验验证:
物质 氢氧化钠溶液 硫酸钠溶液 碳酸钾溶液 硝酸银溶液
实验现象 无明显现象 无明显现象 产生气泡 产生白色沉淀
能否反应 能反应 不能反应 能反应 能反应
【提出问题】对于上述无明显现象的反应,如何设计实验进行验证?
【设计实验】为了验证氢氧化钠溶液与稀盐酸能发生化学反应,小刚设计了如下实验方案并进行实验。
实验步骤 实验现象 实验结论
将氢氧化钠溶液滴入盛有稀盐酸的试管中,振荡 溶液呈无色 稀盐酸与氢氧化钠溶液能发生化学反应
向步骤所得无色溶液中滴加几滴酚酞溶液 溶液呈无色
【分析讨论】小刚设计的实验方案________填“可行”或“不可行”,说明理由:________________。
【总结提升】通过以上实验分析,对于无明显现象的反应,验证思路可以是:
Ⅰ验证生成物是否存在。
Ⅱ验证________是否消失。
【拓展迁移】氢氧化钠溶液与稀盐酸发生反应的微观示意图如图所示,该反应的实质是____________________________________________________________。写出另一个符合上述反应实质的化学方程式__________________________________________________________。
将一定量的氢氧化钠溶液与稀盐酸混合,充分反应后所得溶液中溶质成分可能有________种情况,具体的溶质组合情况分别是________________填化学式。
学习复分解反应发生条件时,小红同学做了下表中的四个实验。
试管编号
试管内试剂 溶液 溶液 溶液 溶液
加入稀硫酸后的现象 无明显现象 无明显现象 产生气泡 白色沉淀生成
根据以上实验,可以判断试管中发生了复分解反应。试管中反应的化学方程式为_________________________________________________________________________。
小明同学向盛有溶液的试管中先加了一种试剂,再加稀硫酸,从而能说明试管中也发生了反应,这种试剂是__________。
为了验证试管中是否发生复分解反应,小明同学进行了如下探究。
提出猜想猜想:试管中没有发生复分解反应,溶液中有,即和同时存在溶液中。
猜想:试管中发生了复分解反应,溶液中无。
老师提示会对的检验有干扰,需要先除去,小明根据老师的提示和自己的猜想提出了以下实验方案。
设计方案
沉淀的化学式是__________。老师评价该方案时指出:设计思路正确,但试剂选择有误,你认为应该将所选的试剂__________改成__________。
小明按照修改后的方案进行了实验,最后得出的结论是猜想正确,则步骤Ⅱ、步骤Ⅲ中必然会观察到的现象是____________________________________________________________。
实验反思小明反思进行步骤Ⅲ时,加溶液采用了滴加的方式,但没有立即观察到任何现象,你认为其中的原因是________________________________。
某化学兴趣小组同学做了如图甲、乙两个实验。请回答下列问题:
实验的现象为 ______。
把试管中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液。试管中上层清液中的溶质一定含有 ______。写出混合后一定发生反应的化学方程式 ______。
混合后所得溶液中可能含有的溶质为 ______。
【反思拓展】甲、乙两实验能发生复分解反应的原因是 ______。
参考答案
1.【答案】C
2.【答案】D
3.【答案】C
4.【答案】D
5.【答案】A
6.【答案】B
7.【答案】C
8.【答案】D
9.【答案】A
10.【答案】A
11.【答案】C
12.【答案】D
13.【答案】B
14.【答案】B
15.【答案】化合物
化合物 属于 不一定
16.【答案】 复分解反应 ++ 冶炼金属(或作燃料)
17.【答案】乙 盐酸和氢氧化钠恰好反应
氢离子和氢氧根离子反应生成水 不变
放热 点或最高点
18.【答案】【分析讨论】可行;滴加酚酞溶液后溶液仍为无色,说明溶液中氢氧化钠消失了,进而说明氢氧化钠与稀盐酸发生了化学反应 【总结提升】反应物 【拓展迁移】酸中的氢离子与碱中的氢氧根离子结合成水分子; 合理即可 ;、和、和
19.【答案】
酚酞试液或其他合理答案
; ; ;均有白色沉淀;氢氧化钠先与溶液中的酸反应
20.【答案】有白色沉淀生成 氢氧化钠、硫酸钠 氢氧化钠 都生成了沉淀
2
1
同课章节目录
