人教版化学九下学案:8.3 金属资源的利用和保护(第1课时)(教师用)(含答案)
文档属性
| 名称 | 人教版化学九下学案:8.3 金属资源的利用和保护(第1课时)(教师用)(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 121.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-17 00:00:00 | ||
图片预览



文档简介
课题3 金属资源的利用和保护
第1课时 金属资源及其利用
一、学习目标
1.知道一些含常见的金属如铁、铝、铜等的矿物,了解我国矿藏资源;
2.了解从铁矿石中将铁还原出来的原理和方法;
3.能根据化学方程式对含有某些杂质的反应物或生成物进行简单的计算。
二、学习重难点
重点:从常见铁矿石中提炼铁的原理和方法。
难点:1.冶炼铁的原理;2.有关杂质问题的计算。
三、学习过程
【知识回顾】
1.金属之最:
(1)地壳中含量最多的金属元素_________;
(2)人体中含量最多的金属元素_________;
(3)海水中含量最高的金属元素_________;
(4)目前世界年产量最多的金属_________。
2.还原反应:
(1)概念:_______________________________________________。
(2)_______和_________都有还原性,可用于冶金工业。请写出下列还原反应的化学方程式:①碳还原氧化铁:__________________________;
②一氧化碳还原氧化铜:________________________________。
【答案】1.铝、钙、钠、铁;2.含氧化合物里的氧被夺去的反应、C、CO、2Fe2O3+3C4Fe+3CO2↑、CO+CuOCu+CO2。
【课堂探究】
一、金属元素在自然界中的存在形式(自主学习)
1.地球上的金属资源广泛的存在于地壳和海洋中,除少数很不活泼的金属如_____、_____等以_____形式存在外,其余都以_____形式存在。
2.自然界含量最多的元素是 ,其次是 。(填化学符号)
自然界含量最多的金属元素是 ,其次是 。(填化学符号)
3.写出下列金属矿石的主要成分
矿石名称 主要成分的化学式
赤铁矿
磁铁矿
黄铁矿
菱铁矿
铝土矿
黄铜矿
辉铜矿
【答案】1.金、银、单质、化合物;2.O、Si、Al、Fe; 3. Fe2O3、Fe3O4、FeS2、FeCO3、Al2O3、CuFeS2、Cu2S。
【练一练】下列金属在自然界中主要以单质的形式存在的是( )
A.Fe B.Al C.Zn D.Au
【答案】D
二、铁的冶炼
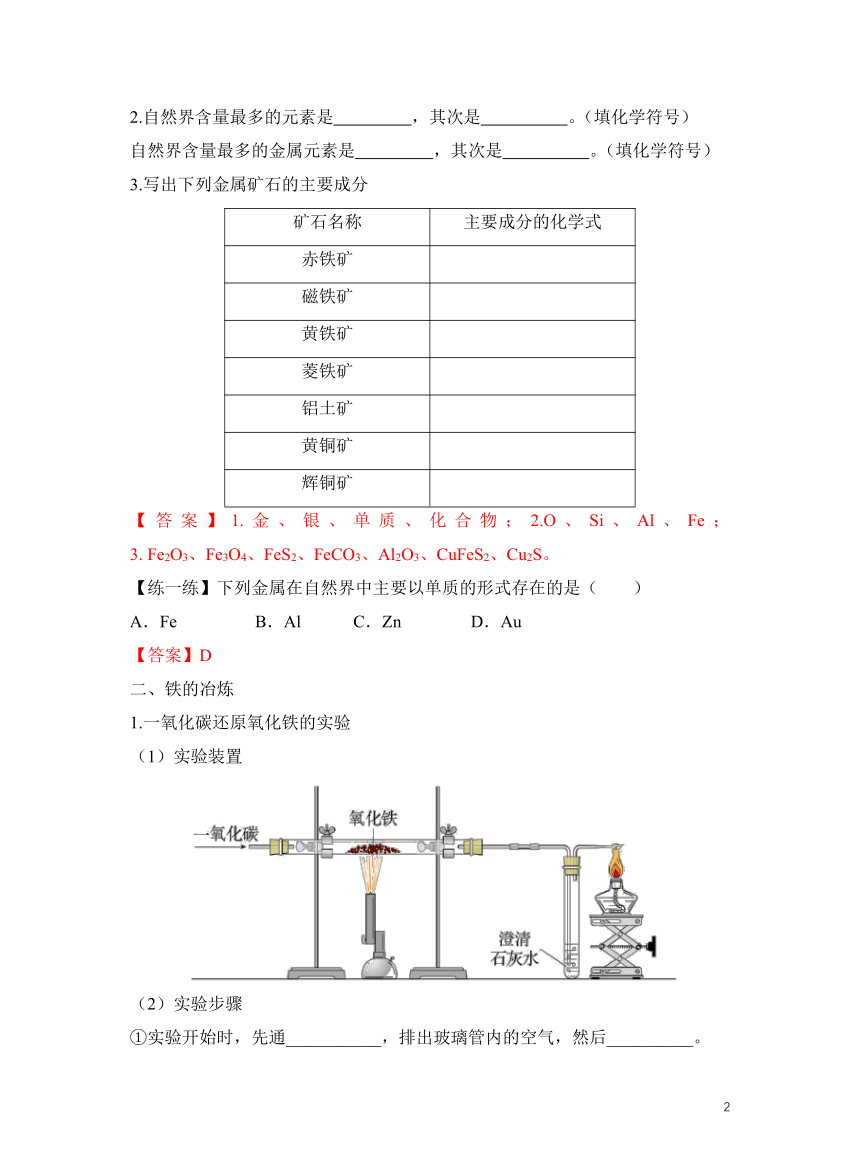
1.一氧化碳还原氧化铁的实验
(1)实验装置
(2)实验步骤
①实验开始时,先通___________,排出玻璃管内的空气,然后__________。
②实验结束时,要先______________,继续______________,直到______________。
(3)实验现象:_____色的氧化铁变为_____色,澄清石灰水_____,导管口有_____色火焰。
(4)CO还原氧化铁的反应原理(用化学方程式表示):_________________。
【总结】可简单记忆为:CO是早来晚走,酒精灯是迟到早退。
(5)交流讨论:
①实验开始时,为什么要先通入CO再点燃酒精灯?
②导气管中的气体为何要接一个燃着的酒精灯?还可以如何处理?
【答案】(2)CO、加热氧化铁、停止加热、通入CO、室温;(3)红、黑、变浑浊、蓝;(4)3CO+Fe2O32Fe+3CO2;(5)①由于CO气体与空气混合加热时可能出现爆炸,因此在进行加热前要把玻璃管中空气全部排出;②用酒精灯点燃尾气是防止未反应的一氧化碳逸散到空气中污染空气、用密封的塑料袋收集。
【练一练】(2021·肥东模拟)用型玻璃管进行微型实验,如图所示,下列错误的是( )
A.a处的反应方程式为
B.a处红棕色粉末变为黑色
C.b处澄清石灰水变浑浊证明有CO2生成
D.可利用点燃的方法进行尾气处理
【答案】 A
2.工业炼铁
(1)主要设备:高炉。
(2)原料:铁矿石、焦炭、石灰石、空气等。
(3)原理:在_____条件下,利用_____与_____反应生成的一氧化碳把铁从 中还原出来。
(4)产品:__________。
(5)交流讨论:高炉炼铁和实验室炼铁有什么区别?其产物是纯铁吗?
【总结】工业炼铁使用了焦炭,虽然焦炭也具有还原性,但高炉炼铁中用一氧化碳还原氧化铁。
【答案】(3)高温、C、CO2;(4)生铁;(5)实验室中氧化铁与一氧化碳反应产生的铁是纯铁,而工业炼出的生铁是铁碳合金。
【练一练】下列物质中不是炼铁高炉中投放的基本原料的是( )
A.铁矿石 B.石灰石 C.焦炭 D.生铁
【答案】D
3.含杂质物质的化学方程式的计算
(1)化学方程式所表达的是纯净的物质间的质量关系,因此当反应物或生成物物质所含杂质时,应首先换算成纯净物质的质量,再进行计算。
(2)不纯物质、纯物质和纯度之间的关系:
①纯物质的质量=不纯物质的质量×纯度
②不纯物质的质量= ____________________
③纯度 =____________________
【答案】纯物质的质量÷纯度、。
【练一练】某钢铁厂每天需消耗5000 t含氧化铁76%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是多少?
【答案】解:设理论上可以炼出含铁98%的生铁的质量为x。
Fe2O3+3CO 2Fe+3CO2
160 112
5000 t×76% x·98%
x≈2714.3 t
答:理论上可日产含Fe98%的生铁的质量是2714.3 t。
【学后反思】通过本节课的学习,你收获了什么?
【测评反馈】
1.“金、银、铜、铁、锡”俗称五金,在这五种金属里,有单质形式存在于自然界中的银白色固体是( )
A. 铁 B. 铜 C. 金 D. 银
【答案】 D
【解析】由金属在自然界的存在形式可知:自然界中的金属除极少数不活泼的金属(金、银)以单质形式存在外,都以化合物的形式存在。属于银白色固体是银。
故答案为:D。
2.(2021·岳池模拟)下列有关模拟工业炼铁的叙述错误的是( )
A. 炼铁用赤铁矿的主要成分是Fe3O4
B. 用燃着的酒精灯可防止CO污染空气
C. 硬质玻璃管中红色固体变为黑色
D. 实验过程中澄清石灰水变浑浊
【答案】 A
【解析】A. 炼铁用赤铁矿的主要成分是Fe2O3, 故错误,符合题意;
B. 一氧化碳有毒,直接排放会污染空气,用燃着的酒精灯可防止CO污染空气,故正确,不符合题意;
C. 一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,硬质玻璃管中可观察到红色固体变为黑色,故正确,不符合题意;
D. 反应有二氧化碳生成,二氧化碳能使澄清的石灰水变浑浊,所以实验过程中澄清石灰水变浑浊,故正确,不符合题意。
故答案为:A。
3.如图为CO还原Fe2O3的微型实验装置(夹持仪器已略去),甲酸在热的浓硫酸作用下分解生成CO,利用CO还原Fe2O3。(已知: )下列有关该实验的说法错误的是( )
A. 此装置内空间较小,空气易排尽,实验危险系数小
B. 此实验装置的主要优点是尾气处理有效节能
C. 该实验中CO既表现出还原性,又表现出可燃性
D. 该实验中观察到的现象是红色固体变成了银白色,澄清石灰水变浑浊
【答案】 D
【解析】A.此装置内空间较小,空气容易排尽,实验危险系数小,不符合题意;
B.此实验装置尾气中的一氧化碳燃烧产生的热量对氧化铁进行加热,充分利用了能源,此实验装置的主要优点是尾气处理有效节能,不符合题意;
C.一氧化碳与氧化铁反应生成铁和二氧化碳,尾气中的一氧化碳燃烧生成二氧化碳,该实验中CO既表现出还原性,又表现出可燃性,不符合题意;
D.一氧化碳具有还原性,高温下能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管A中出现的现象是红棕色粉末逐渐变黑,符合题意。
故答案为:D。
4.(2021·本溪模拟)在用一氧化碳还原氧化铁的实验中,下列说法错误的是( )
A. A 处玻璃管中固体颜色改变
B. 该装置未进行尾气处理
C. 实验中先通一氧化碳,然后再加热氧化铁
D. B 处试管可以防止因液体倒吸,使玻璃管炸裂
【答案】 B
【解析】A.氧化铁为红色,反应后生成的铁粉为黑色,A不合题意;
B.该装置中的C瓶,即可以检验反应的产物,也可收集过量的CO,因此该装置进行了尾气处理,B符合题意;
C.因一氧化碳为可燃性气体,为防止爆炸,应先通一氧化碳排尽装置内的空气,然后再加热氧化铁,C不合题意;
D.B处试管为安全试管,可防止液体倒吸,D不合题意;
故答案为:B。
5.工业炼铁可利用一氧化碳与氧化铁反应。若要生产含铁97%的生铁231 t,需含氧化铁80%的赤铁矿石的质量最接近( )
A. 224 t B. 280 t C. 320 t D. 400 t
【答案】 D
【解析】生铁231 t中含铁的质量是:231 t×97%≈224 t,设该厂至少应储备含氧化铁80%的赤铁矿质量为x,
x=400 t。
故答案为:D。
6.(2021·东城模拟)用下图装置进行实验(夹持仪器略去)。
(1)玻璃管中的现象是________,反应的化学方程式为________。
(2)澄清石灰水的作用是________。
(3)尾气中主要含有 CO2和________,应处理后再排放。
【答案】 (1)红色固体变黑色;
(2)检验生成的二氧化碳气体
(3)CO
【解析】(1)一氧化碳在高温下和氧化铁反应生成二氧化碳和铁粉, ;故玻璃管中的现象是红色固体变黑色。
(2)二氧化碳能使澄清石灰水变浑浊,故澄清石灰水的作用是检验生成的二氧化碳气体。
(3)一氧化碳有剧毒,尾气中主要含有反应生成 CO2和没有参加反应的CO,应处理后再排放。
1
第1课时 金属资源及其利用
一、学习目标
1.知道一些含常见的金属如铁、铝、铜等的矿物,了解我国矿藏资源;
2.了解从铁矿石中将铁还原出来的原理和方法;
3.能根据化学方程式对含有某些杂质的反应物或生成物进行简单的计算。
二、学习重难点
重点:从常见铁矿石中提炼铁的原理和方法。
难点:1.冶炼铁的原理;2.有关杂质问题的计算。
三、学习过程
【知识回顾】
1.金属之最:
(1)地壳中含量最多的金属元素_________;
(2)人体中含量最多的金属元素_________;
(3)海水中含量最高的金属元素_________;
(4)目前世界年产量最多的金属_________。
2.还原反应:
(1)概念:_______________________________________________。
(2)_______和_________都有还原性,可用于冶金工业。请写出下列还原反应的化学方程式:①碳还原氧化铁:__________________________;
②一氧化碳还原氧化铜:________________________________。
【答案】1.铝、钙、钠、铁;2.含氧化合物里的氧被夺去的反应、C、CO、2Fe2O3+3C4Fe+3CO2↑、CO+CuOCu+CO2。
【课堂探究】
一、金属元素在自然界中的存在形式(自主学习)
1.地球上的金属资源广泛的存在于地壳和海洋中,除少数很不活泼的金属如_____、_____等以_____形式存在外,其余都以_____形式存在。
2.自然界含量最多的元素是 ,其次是 。(填化学符号)
自然界含量最多的金属元素是 ,其次是 。(填化学符号)
3.写出下列金属矿石的主要成分
矿石名称 主要成分的化学式
赤铁矿
磁铁矿
黄铁矿
菱铁矿
铝土矿
黄铜矿
辉铜矿
【答案】1.金、银、单质、化合物;2.O、Si、Al、Fe; 3. Fe2O3、Fe3O4、FeS2、FeCO3、Al2O3、CuFeS2、Cu2S。
【练一练】下列金属在自然界中主要以单质的形式存在的是( )
A.Fe B.Al C.Zn D.Au
【答案】D
二、铁的冶炼
1.一氧化碳还原氧化铁的实验
(1)实验装置
(2)实验步骤
①实验开始时,先通___________,排出玻璃管内的空气,然后__________。
②实验结束时,要先______________,继续______________,直到______________。
(3)实验现象:_____色的氧化铁变为_____色,澄清石灰水_____,导管口有_____色火焰。
(4)CO还原氧化铁的反应原理(用化学方程式表示):_________________。
【总结】可简单记忆为:CO是早来晚走,酒精灯是迟到早退。
(5)交流讨论:
①实验开始时,为什么要先通入CO再点燃酒精灯?
②导气管中的气体为何要接一个燃着的酒精灯?还可以如何处理?
【答案】(2)CO、加热氧化铁、停止加热、通入CO、室温;(3)红、黑、变浑浊、蓝;(4)3CO+Fe2O32Fe+3CO2;(5)①由于CO气体与空气混合加热时可能出现爆炸,因此在进行加热前要把玻璃管中空气全部排出;②用酒精灯点燃尾气是防止未反应的一氧化碳逸散到空气中污染空气、用密封的塑料袋收集。
【练一练】(2021·肥东模拟)用型玻璃管进行微型实验,如图所示,下列错误的是( )
A.a处的反应方程式为
B.a处红棕色粉末变为黑色
C.b处澄清石灰水变浑浊证明有CO2生成
D.可利用点燃的方法进行尾气处理
【答案】 A
2.工业炼铁
(1)主要设备:高炉。
(2)原料:铁矿石、焦炭、石灰石、空气等。
(3)原理:在_____条件下,利用_____与_____反应生成的一氧化碳把铁从 中还原出来。
(4)产品:__________。
(5)交流讨论:高炉炼铁和实验室炼铁有什么区别?其产物是纯铁吗?
【总结】工业炼铁使用了焦炭,虽然焦炭也具有还原性,但高炉炼铁中用一氧化碳还原氧化铁。
【答案】(3)高温、C、CO2;(4)生铁;(5)实验室中氧化铁与一氧化碳反应产生的铁是纯铁,而工业炼出的生铁是铁碳合金。
【练一练】下列物质中不是炼铁高炉中投放的基本原料的是( )
A.铁矿石 B.石灰石 C.焦炭 D.生铁
【答案】D
3.含杂质物质的化学方程式的计算
(1)化学方程式所表达的是纯净的物质间的质量关系,因此当反应物或生成物物质所含杂质时,应首先换算成纯净物质的质量,再进行计算。
(2)不纯物质、纯物质和纯度之间的关系:
①纯物质的质量=不纯物质的质量×纯度
②不纯物质的质量= ____________________
③纯度 =____________________
【答案】纯物质的质量÷纯度、。
【练一练】某钢铁厂每天需消耗5000 t含氧化铁76%的赤铁矿石,该厂理论上可日产含Fe98%的生铁的质量是多少?
【答案】解:设理论上可以炼出含铁98%的生铁的质量为x。
Fe2O3+3CO 2Fe+3CO2
160 112
5000 t×76% x·98%
x≈2714.3 t
答:理论上可日产含Fe98%的生铁的质量是2714.3 t。
【学后反思】通过本节课的学习,你收获了什么?
【测评反馈】
1.“金、银、铜、铁、锡”俗称五金,在这五种金属里,有单质形式存在于自然界中的银白色固体是( )
A. 铁 B. 铜 C. 金 D. 银
【答案】 D
【解析】由金属在自然界的存在形式可知:自然界中的金属除极少数不活泼的金属(金、银)以单质形式存在外,都以化合物的形式存在。属于银白色固体是银。
故答案为:D。
2.(2021·岳池模拟)下列有关模拟工业炼铁的叙述错误的是( )
A. 炼铁用赤铁矿的主要成分是Fe3O4
B. 用燃着的酒精灯可防止CO污染空气
C. 硬质玻璃管中红色固体变为黑色
D. 实验过程中澄清石灰水变浑浊
【答案】 A
【解析】A. 炼铁用赤铁矿的主要成分是Fe2O3, 故错误,符合题意;
B. 一氧化碳有毒,直接排放会污染空气,用燃着的酒精灯可防止CO污染空气,故正确,不符合题意;
C. 一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,硬质玻璃管中可观察到红色固体变为黑色,故正确,不符合题意;
D. 反应有二氧化碳生成,二氧化碳能使澄清的石灰水变浑浊,所以实验过程中澄清石灰水变浑浊,故正确,不符合题意。
故答案为:A。
3.如图为CO还原Fe2O3的微型实验装置(夹持仪器已略去),甲酸在热的浓硫酸作用下分解生成CO,利用CO还原Fe2O3。(已知: )下列有关该实验的说法错误的是( )
A. 此装置内空间较小,空气易排尽,实验危险系数小
B. 此实验装置的主要优点是尾气处理有效节能
C. 该实验中CO既表现出还原性,又表现出可燃性
D. 该实验中观察到的现象是红色固体变成了银白色,澄清石灰水变浑浊
【答案】 D
【解析】A.此装置内空间较小,空气容易排尽,实验危险系数小,不符合题意;
B.此实验装置尾气中的一氧化碳燃烧产生的热量对氧化铁进行加热,充分利用了能源,此实验装置的主要优点是尾气处理有效节能,不符合题意;
C.一氧化碳与氧化铁反应生成铁和二氧化碳,尾气中的一氧化碳燃烧生成二氧化碳,该实验中CO既表现出还原性,又表现出可燃性,不符合题意;
D.一氧化碳具有还原性,高温下能与氧化铁反应生成铁和二氧化碳,实验进行一段时间后,玻璃管A中出现的现象是红棕色粉末逐渐变黑,符合题意。
故答案为:D。
4.(2021·本溪模拟)在用一氧化碳还原氧化铁的实验中,下列说法错误的是( )
A. A 处玻璃管中固体颜色改变
B. 该装置未进行尾气处理
C. 实验中先通一氧化碳,然后再加热氧化铁
D. B 处试管可以防止因液体倒吸,使玻璃管炸裂
【答案】 B
【解析】A.氧化铁为红色,反应后生成的铁粉为黑色,A不合题意;
B.该装置中的C瓶,即可以检验反应的产物,也可收集过量的CO,因此该装置进行了尾气处理,B符合题意;
C.因一氧化碳为可燃性气体,为防止爆炸,应先通一氧化碳排尽装置内的空气,然后再加热氧化铁,C不合题意;
D.B处试管为安全试管,可防止液体倒吸,D不合题意;
故答案为:B。
5.工业炼铁可利用一氧化碳与氧化铁反应。若要生产含铁97%的生铁231 t,需含氧化铁80%的赤铁矿石的质量最接近( )
A. 224 t B. 280 t C. 320 t D. 400 t
【答案】 D
【解析】生铁231 t中含铁的质量是:231 t×97%≈224 t,设该厂至少应储备含氧化铁80%的赤铁矿质量为x,
x=400 t。
故答案为:D。
6.(2021·东城模拟)用下图装置进行实验(夹持仪器略去)。
(1)玻璃管中的现象是________,反应的化学方程式为________。
(2)澄清石灰水的作用是________。
(3)尾气中主要含有 CO2和________,应处理后再排放。
【答案】 (1)红色固体变黑色;
(2)检验生成的二氧化碳气体
(3)CO
【解析】(1)一氧化碳在高温下和氧化铁反应生成二氧化碳和铁粉, ;故玻璃管中的现象是红色固体变黑色。
(2)二氧化碳能使澄清石灰水变浑浊,故澄清石灰水的作用是检验生成的二氧化碳气体。
(3)一氧化碳有剧毒,尾气中主要含有反应生成 CO2和没有参加反应的CO,应处理后再排放。
1
同课章节目录
