2023浙江中考科学一轮复习(基础版)第30讲 物质的分类和常见的有机物(课件 32张ppt)
文档属性
| 名称 | 2023浙江中考科学一轮复习(基础版)第30讲 物质的分类和常见的有机物(课件 32张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 683.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-01-18 09:11:50 | ||
图片预览










文档简介
(共32张PPT)
2023浙江中考科学一轮复习(基础版)
第30讲 物质的分类和常见的有机物
物质的分类(九上教材P57)
1.混合物:由_______物质混合而成,如空气、矿泉水等。
2.纯净物:
(1)单质(由_______元素组成)
①金属:铁、铜、银等。
②非金属(包括稀有气体):氧气、氦气、碘等。
(2)化合物(由不同种元素组成)
①无机物
a.氧化物
概念:由两种元素组成,其中一种是____元素的化合物
多种
同种
氧
b.酸:电离时阳离子全部是_________的化合物,如:盐酸、硫酸、硝酸等。
c.碱:电离时阴离子全部是____________的化合物,如:氢氧化钠、氨水等。
d.盐:由金属阳离子(或铵根离子)和酸根离子组成的化合物,如NH4Cl、CuSO4。
②有机物:含碳的化合物(碳的氧化物、碳酸、碳酸盐等除外),大多含有C、H、O、N等元素。
氢离子
氢氧根离子
1.下列物质分类正确的是( )
A.单质:氧气 水
B.氧化物:二氧化锰 氯化钾
C.碱:氢氧化钠 氢氧化钙
D.混合物:五氧化二磷 空气
2.(2022,舟山)钻石素有“宝石之王”的称谓,因其优越的特性和漂亮的外表而受到大众喜爱。天然钻石产量极其稀少,在很多领域会用性质相近的氧化锆(ZrO2)替代。前者属于单质,后者属于化合物,分类的依据是_______________________。
C
是否由同种元素组成
常见的有机物(九上教材P47)
1.有机物的定义和特点
(1)定义:含碳的化合物(碳的氧化物、碳酸、碳酸盐等除外),大多含有C、H、O、N等元素。
(2)性质:大部分有机物____溶于水,熔点____、易______、易______。
2.常见的有机物
(1)简单的有机物
①甲烷(CH4):最简单的有机物,甲烷是沼气、天然气的主要成分,燃烧的化学方程式为____________________________,
与空气混合点燃易发生爆炸,故点燃前应验纯。
难
低
燃烧
挥发
②丁烷(C4H10):打火机内液体及家用液化气的主要成分,燃烧的化学方程式为__________________________________。
③乙炔(C2H2):在氧气中燃烧可产生3000 ℃以上的高温,可用于金属焊接和切割,燃烧的化学反应方程式为_____________________________。
④乙醇(C2H5OH):俗名酒精,易燃烧,燃烧的化学反应方程式为_____________________________。可用于饮料、溶剂、消毒、燃料等。工业酒精中含甲醇,不能饮用。
⑤乙酸(CH3COOH):俗称醋酸,酸性比H2CO3强,具有酸的
通性。
(2)生命体中的有机物
①糖类:生命活动所需能量的主要来源,面包、面条、米饭等食物主要含有糖类。
②蛋白质:构成生命体的基本物质,鸡肉、大豆、鱼肉等食物富含蛋白质。
③脂肪:生命体重要的营养物质,贮存能量的主要物质。
(3)有机材料可分为天然有机材料和合成有机材料。天然有机高分子材料,如:棉花、羊毛、天然橡胶。合成有机高分子材料(合成材料),如:合成塑料、合成纤维、合成橡胶。
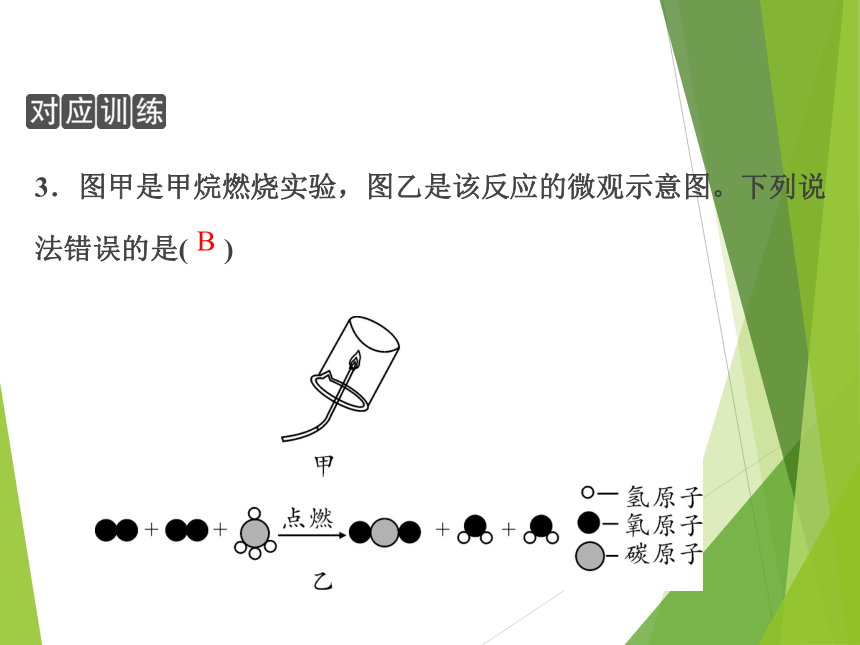
3.图甲是甲烷燃烧实验,图乙是该反应的微观示意图。下列说法错误的是( )
B
A.从实验操作角度分析,点燃甲烷前需要检验甲烷的纯度
B.从物质检验角度分析,可在烧杯内壁涂澄清石灰水来检验甲烷燃烧的两种产物
C.从物质分类角度分析,甲烷属于有机物,甲烷燃烧的两种产物均属于氧化物
D.从能量变化角度分析,甲烷燃烧反应的能量变化是化学能转化为内能
4.随着经济的发展,能源与环境成为人们日益关注的问题。
(1)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体。为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷。该反应的化学方程式____________________________。
(2)“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例反应,生成一种产物——甲酸(CH2O2),就能实现“零排放”。在物质分类上,甲酸属于
_________(填“有机物”或“无机物”)。
有机物
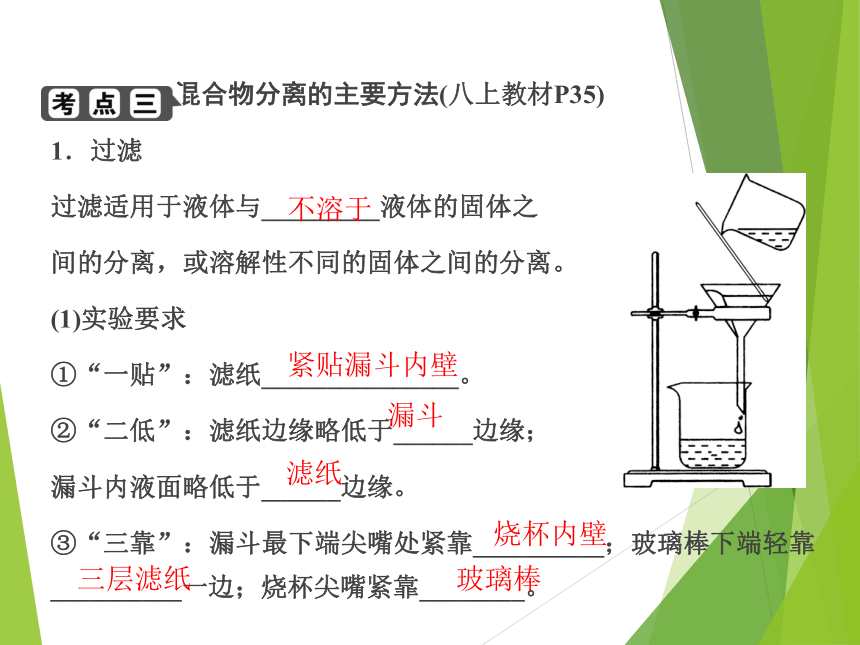
混合物分离的主要方法(八上教材P35)
1.过滤
过滤适用于液体与_________液体的固体之
间的分离,或溶解性不同的固体之间的分离。
(1)实验要求
①“一贴”:滤纸_______________。
②“二低”:滤纸边缘略低于______边缘;
漏斗内液面略低于______边缘。
③“三靠”:漏斗最下端尖嘴处紧靠__________;玻璃棒下端轻靠__________一边;烧杯尖嘴紧靠________。
不溶于
紧贴漏斗内壁
漏斗
滤纸
烧杯内壁
三层滤纸
玻璃棒
(2)异常现象分析
气泡
异常现象 可能原因
滤液仍然浑浊 a.滤纸破损;b.液面高于滤纸边缘
过滤速度很慢 a.杂质太多;b.滤纸与漏斗之间有_______
2.蒸发法
蒸发法的实验器材及操作要点:
①用玻璃棒不断搅拌,以防止液滴飞溅。
②当_________________________时停止加热,不停搅拌,靠_______蒸干。
③移开蒸发皿时要用坩埚钳,以免烫伤。
蒸发皿
酒精灯
玻璃棒
蒸发皿中出现大量固体
余热
5.(2020,台州)台州甘蔗制糖有着悠久的历史。甘蔗制糖的部分环节为:清洗甘蔗→压榨甘蔗→分离渣汁→蒸发浓缩→……
(1)甘蔗在压榨过程中发生的
变化属于____________。
(2)渣汁的分离与图中的____
(填“A”“B”或“C”)实验原
理相同。
(3)糖汁在蒸发浓缩过程中,溶液的溶质质量分数将怎么变化?_______。
物理变化
B
变大
粗盐提纯(八上教材P37)
1.实验用品
(1)实验仪器:烧杯、玻璃棒、铁架台(带铁圈)、漏斗、蒸发
皿、酒精灯、药匙、量筒、托盘天平、砝码、坩埚钳、剪刀。
(2)实验药品:粗盐(含有不溶性杂质及氯化钙、硫酸钠、硫酸镁等可溶性杂质)、蒸馏水。
2.实验装置及顺序
3.实验中玻璃棒的作用
(1)溶解时,用玻璃棒搅拌,____________。
(2)过滤时,用玻璃棒引流,________________________。
(3)蒸发时,用玻璃棒搅拌,____________________________。
(4)蒸发结束,用玻璃棒转移固体。
加速溶解
防止液体外溅或冲破滤纸
防止因局部温度过高造成液滴飞溅
6.(2021,北京)如图是去除粗盐中难溶性杂质实验的三步操作。
(1)三步操作的正确顺序是________(填序号)。
(2)B中,用玻璃棒不断搅拌的目的是__________________________________。
ACB
防止局部温度过高,造成液滴飞溅
【误差分析】
误差 分析
产率偏低 ①溶解粗盐时未用玻璃棒充分搅拌
②过滤时漏斗内残留液体
③蒸发时液体或固体溅出
④转移固体时固体撒落
产率偏高 ①过滤时液面高于滤纸边缘
②蒸发时未充分蒸干
物质的分类
【例1】 如图中不同的圆圈表示不同的原子。下列物质的分
类,错误的是( )
A.混合物 B.单质 C.化合物 D.氧化物
D
1.分类是研究物质及其变化的重要思想和方法,如图可表示纯净物、单质、化合物、氧化物之间的关系,若整个大圆圈表示纯净物,则下列物质中属于Z范围的是( )
A.臭氧
B.小苏打
C.生石灰
D.酒精
C
混合物的分离
方法物 适用范围或原理 举例
物理方法 过滤法 ①固体与液体混合物的分离②可溶性固体与不溶性固体混合物的分离 粗盐的提纯
结晶法 蒸发 ①分离溶质与溶剂
②除去易挥发的杂质 从含有HCl的NaCl溶液中分离出固体NaCl
降温结晶 可溶性固体溶质溶解度受温度影响变化大小不同 分离NaCl与KNO3的混合物
【例2】 下列分离或提纯物质的方法,所依据的原理正
确的是( )
A.用活性炭吸附污水中的悬浮杂质——悬浮杂质易溶于
活性炭
B.蒸馏法分离水和酒精——水和酒精的密度不同
C.用结晶法提纯纯碱——纯碱的溶解度受温度影响大
D.分离液态空气制取氧气——利用氮气和氧气的熔点不同
C
2.(2022,海南)我省是海洋大省,海水淡化一直是重要研究
课题,膜技术的引入使研究有了突破性进展。如图对醋酸纤
维膜右侧的海水加压,水分子可透过膜进入左侧淡水池,而
海水中各种离子不能通过膜,从而得到淡水。下列有关说法
正确的是( )
D
A.在未加压的情况下,也可使淡水量增加
B.持续增大压强更有利于得到更多的淡水
C.a口排出液通过蒸发结晶得到精制食盐
D.加压后a口排出液中离子的种类不变
粗盐的提纯
粗盐中除了含有泥沙等不溶性杂质外,还含有可溶性的杂质MgCl2、CaCl2、Na2SO4等。
注意:无论顺序如何互换,但Na2CO3必须加在BaCl2之后,否则过量的BaCl2无法除去。
【例3】 (2021,凉山州)通过海水晒盐可得到粗盐。化学兴趣小组为了除去粗盐中难溶性杂质,进行了如图操作:
(1)上述操作的正确顺序是____________(填序号)。
②⑤①④③
(2)下列情况可能导致精盐产率偏低的是_____(填字母代号)。
A.溶解时加入的水过少导致粗盐未溶完
B.过滤时漏斗内液面超过滤纸边缘
C.蒸发时有液体飞溅
D.所得精盐中含有少量水分
AC
3.某研究性学习小组的同学欲分离氯化钠和氯化钙的混合物,设计了如下实验操作:
(1)②中发生反应的化学方程式为
__________________________________。
Na2CO3+CaCl2===2NaCl+CaCO3↓
(2)②中需要进行的操作是______,操作⑤的名称是________,两个操作中都需用到的玻璃仪器是________。
(3)小组内的乙同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需对实验进行改进,他的做法是________________________。
过滤
蒸发结晶
玻璃棒
在④中加入过量的稀盐酸
【例】 (2022,丽水)思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小科建构了“混合物提纯”的思维模型:
【初步理解】根据混合物组分的性质差异,获得混合物中目标组份。
(1)海水淡化是将海水中的盐与水分开,常压加热蒸馏法是其中的一种:常压下将海水加热形成水蒸气,再液化得到淡水的过程。从建模角度分析,海水加热形成水蒸气属于上述模型中的_________(填“分离转移”或“反应转化”)。
【探究本质】根据组分的性质差异,选择合适方法,实现物质提纯。
(2)从含少量氯化钠的硝酸钾固体中提纯硝酸钾,是通过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥实现的。其中过滤操作将硝酸钾晶体与溶液分离是根据_________不同。
分离转移
颗粒大小
【实践应用】根据混合物中某组分发生化学反应,提高混合物中目标组分纯度。
(3)小科取10克混有少量硫酸的盐酸溶液,滴入氯化钡溶液至不再产生沉淀,经过滤、洗涤和干燥得到沉淀0.233克,则原混合溶液中硫酸的溶质质量分数为______。
【融合创新】依据科学原理,融合技术与工程,形成新颖而有价值的解决实际问题的方案。
(4)常压加热蒸馏法,能耗大、成本高。小科查阅资料获知,现在世界上的许多大型海水淡化工厂,都已经采用低压加热蒸馏法,请解释其蕴含的科学道理:___________________________________________________。
0.98%
液体的沸点随气压的降低而
降低,从而节约能量消耗
2023浙江中考科学一轮复习(基础版)
第30讲 物质的分类和常见的有机物
物质的分类(九上教材P57)
1.混合物:由_______物质混合而成,如空气、矿泉水等。
2.纯净物:
(1)单质(由_______元素组成)
①金属:铁、铜、银等。
②非金属(包括稀有气体):氧气、氦气、碘等。
(2)化合物(由不同种元素组成)
①无机物
a.氧化物
概念:由两种元素组成,其中一种是____元素的化合物
多种
同种
氧
b.酸:电离时阳离子全部是_________的化合物,如:盐酸、硫酸、硝酸等。
c.碱:电离时阴离子全部是____________的化合物,如:氢氧化钠、氨水等。
d.盐:由金属阳离子(或铵根离子)和酸根离子组成的化合物,如NH4Cl、CuSO4。
②有机物:含碳的化合物(碳的氧化物、碳酸、碳酸盐等除外),大多含有C、H、O、N等元素。
氢离子
氢氧根离子
1.下列物质分类正确的是( )
A.单质:氧气 水
B.氧化物:二氧化锰 氯化钾
C.碱:氢氧化钠 氢氧化钙
D.混合物:五氧化二磷 空气
2.(2022,舟山)钻石素有“宝石之王”的称谓,因其优越的特性和漂亮的外表而受到大众喜爱。天然钻石产量极其稀少,在很多领域会用性质相近的氧化锆(ZrO2)替代。前者属于单质,后者属于化合物,分类的依据是_______________________。
C
是否由同种元素组成
常见的有机物(九上教材P47)
1.有机物的定义和特点
(1)定义:含碳的化合物(碳的氧化物、碳酸、碳酸盐等除外),大多含有C、H、O、N等元素。
(2)性质:大部分有机物____溶于水,熔点____、易______、易______。
2.常见的有机物
(1)简单的有机物
①甲烷(CH4):最简单的有机物,甲烷是沼气、天然气的主要成分,燃烧的化学方程式为____________________________,
与空气混合点燃易发生爆炸,故点燃前应验纯。
难
低
燃烧
挥发
②丁烷(C4H10):打火机内液体及家用液化气的主要成分,燃烧的化学方程式为__________________________________。
③乙炔(C2H2):在氧气中燃烧可产生3000 ℃以上的高温,可用于金属焊接和切割,燃烧的化学反应方程式为_____________________________。
④乙醇(C2H5OH):俗名酒精,易燃烧,燃烧的化学反应方程式为_____________________________。可用于饮料、溶剂、消毒、燃料等。工业酒精中含甲醇,不能饮用。
⑤乙酸(CH3COOH):俗称醋酸,酸性比H2CO3强,具有酸的
通性。
(2)生命体中的有机物
①糖类:生命活动所需能量的主要来源,面包、面条、米饭等食物主要含有糖类。
②蛋白质:构成生命体的基本物质,鸡肉、大豆、鱼肉等食物富含蛋白质。
③脂肪:生命体重要的营养物质,贮存能量的主要物质。
(3)有机材料可分为天然有机材料和合成有机材料。天然有机高分子材料,如:棉花、羊毛、天然橡胶。合成有机高分子材料(合成材料),如:合成塑料、合成纤维、合成橡胶。
3.图甲是甲烷燃烧实验,图乙是该反应的微观示意图。下列说法错误的是( )
B
A.从实验操作角度分析,点燃甲烷前需要检验甲烷的纯度
B.从物质检验角度分析,可在烧杯内壁涂澄清石灰水来检验甲烷燃烧的两种产物
C.从物质分类角度分析,甲烷属于有机物,甲烷燃烧的两种产物均属于氧化物
D.从能量变化角度分析,甲烷燃烧反应的能量变化是化学能转化为内能
4.随着经济的发展,能源与环境成为人们日益关注的问题。
(1)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体。为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷。该反应的化学方程式____________________________。
(2)“绿色化学”的特点之一是“零排放”。一定条件下,二氧化碳和氢气可以按照不同比例反应,生成一种产物——甲酸(CH2O2),就能实现“零排放”。在物质分类上,甲酸属于
_________(填“有机物”或“无机物”)。
有机物
混合物分离的主要方法(八上教材P35)
1.过滤
过滤适用于液体与_________液体的固体之
间的分离,或溶解性不同的固体之间的分离。
(1)实验要求
①“一贴”:滤纸_______________。
②“二低”:滤纸边缘略低于______边缘;
漏斗内液面略低于______边缘。
③“三靠”:漏斗最下端尖嘴处紧靠__________;玻璃棒下端轻靠__________一边;烧杯尖嘴紧靠________。
不溶于
紧贴漏斗内壁
漏斗
滤纸
烧杯内壁
三层滤纸
玻璃棒
(2)异常现象分析
气泡
异常现象 可能原因
滤液仍然浑浊 a.滤纸破损;b.液面高于滤纸边缘
过滤速度很慢 a.杂质太多;b.滤纸与漏斗之间有_______
2.蒸发法
蒸发法的实验器材及操作要点:
①用玻璃棒不断搅拌,以防止液滴飞溅。
②当_________________________时停止加热,不停搅拌,靠_______蒸干。
③移开蒸发皿时要用坩埚钳,以免烫伤。
蒸发皿
酒精灯
玻璃棒
蒸发皿中出现大量固体
余热
5.(2020,台州)台州甘蔗制糖有着悠久的历史。甘蔗制糖的部分环节为:清洗甘蔗→压榨甘蔗→分离渣汁→蒸发浓缩→……
(1)甘蔗在压榨过程中发生的
变化属于____________。
(2)渣汁的分离与图中的____
(填“A”“B”或“C”)实验原
理相同。
(3)糖汁在蒸发浓缩过程中,溶液的溶质质量分数将怎么变化?_______。
物理变化
B
变大
粗盐提纯(八上教材P37)
1.实验用品
(1)实验仪器:烧杯、玻璃棒、铁架台(带铁圈)、漏斗、蒸发
皿、酒精灯、药匙、量筒、托盘天平、砝码、坩埚钳、剪刀。
(2)实验药品:粗盐(含有不溶性杂质及氯化钙、硫酸钠、硫酸镁等可溶性杂质)、蒸馏水。
2.实验装置及顺序
3.实验中玻璃棒的作用
(1)溶解时,用玻璃棒搅拌,____________。
(2)过滤时,用玻璃棒引流,________________________。
(3)蒸发时,用玻璃棒搅拌,____________________________。
(4)蒸发结束,用玻璃棒转移固体。
加速溶解
防止液体外溅或冲破滤纸
防止因局部温度过高造成液滴飞溅
6.(2021,北京)如图是去除粗盐中难溶性杂质实验的三步操作。
(1)三步操作的正确顺序是________(填序号)。
(2)B中,用玻璃棒不断搅拌的目的是__________________________________。
ACB
防止局部温度过高,造成液滴飞溅
【误差分析】
误差 分析
产率偏低 ①溶解粗盐时未用玻璃棒充分搅拌
②过滤时漏斗内残留液体
③蒸发时液体或固体溅出
④转移固体时固体撒落
产率偏高 ①过滤时液面高于滤纸边缘
②蒸发时未充分蒸干
物质的分类
【例1】 如图中不同的圆圈表示不同的原子。下列物质的分
类,错误的是( )
A.混合物 B.单质 C.化合物 D.氧化物
D
1.分类是研究物质及其变化的重要思想和方法,如图可表示纯净物、单质、化合物、氧化物之间的关系,若整个大圆圈表示纯净物,则下列物质中属于Z范围的是( )
A.臭氧
B.小苏打
C.生石灰
D.酒精
C
混合物的分离
方法物 适用范围或原理 举例
物理方法 过滤法 ①固体与液体混合物的分离②可溶性固体与不溶性固体混合物的分离 粗盐的提纯
结晶法 蒸发 ①分离溶质与溶剂
②除去易挥发的杂质 从含有HCl的NaCl溶液中分离出固体NaCl
降温结晶 可溶性固体溶质溶解度受温度影响变化大小不同 分离NaCl与KNO3的混合物
【例2】 下列分离或提纯物质的方法,所依据的原理正
确的是( )
A.用活性炭吸附污水中的悬浮杂质——悬浮杂质易溶于
活性炭
B.蒸馏法分离水和酒精——水和酒精的密度不同
C.用结晶法提纯纯碱——纯碱的溶解度受温度影响大
D.分离液态空气制取氧气——利用氮气和氧气的熔点不同
C
2.(2022,海南)我省是海洋大省,海水淡化一直是重要研究
课题,膜技术的引入使研究有了突破性进展。如图对醋酸纤
维膜右侧的海水加压,水分子可透过膜进入左侧淡水池,而
海水中各种离子不能通过膜,从而得到淡水。下列有关说法
正确的是( )
D
A.在未加压的情况下,也可使淡水量增加
B.持续增大压强更有利于得到更多的淡水
C.a口排出液通过蒸发结晶得到精制食盐
D.加压后a口排出液中离子的种类不变
粗盐的提纯
粗盐中除了含有泥沙等不溶性杂质外,还含有可溶性的杂质MgCl2、CaCl2、Na2SO4等。
注意:无论顺序如何互换,但Na2CO3必须加在BaCl2之后,否则过量的BaCl2无法除去。
【例3】 (2021,凉山州)通过海水晒盐可得到粗盐。化学兴趣小组为了除去粗盐中难溶性杂质,进行了如图操作:
(1)上述操作的正确顺序是____________(填序号)。
②⑤①④③
(2)下列情况可能导致精盐产率偏低的是_____(填字母代号)。
A.溶解时加入的水过少导致粗盐未溶完
B.过滤时漏斗内液面超过滤纸边缘
C.蒸发时有液体飞溅
D.所得精盐中含有少量水分
AC
3.某研究性学习小组的同学欲分离氯化钠和氯化钙的混合物,设计了如下实验操作:
(1)②中发生反应的化学方程式为
__________________________________。
Na2CO3+CaCl2===2NaCl+CaCO3↓
(2)②中需要进行的操作是______,操作⑤的名称是________,两个操作中都需用到的玻璃仪器是________。
(3)小组内的乙同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需对实验进行改进,他的做法是________________________。
过滤
蒸发结晶
玻璃棒
在④中加入过量的稀盐酸
【例】 (2022,丽水)思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小科建构了“混合物提纯”的思维模型:
【初步理解】根据混合物组分的性质差异,获得混合物中目标组份。
(1)海水淡化是将海水中的盐与水分开,常压加热蒸馏法是其中的一种:常压下将海水加热形成水蒸气,再液化得到淡水的过程。从建模角度分析,海水加热形成水蒸气属于上述模型中的_________(填“分离转移”或“反应转化”)。
【探究本质】根据组分的性质差异,选择合适方法,实现物质提纯。
(2)从含少量氯化钠的硝酸钾固体中提纯硝酸钾,是通过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥实现的。其中过滤操作将硝酸钾晶体与溶液分离是根据_________不同。
分离转移
颗粒大小
【实践应用】根据混合物中某组分发生化学反应,提高混合物中目标组分纯度。
(3)小科取10克混有少量硫酸的盐酸溶液,滴入氯化钡溶液至不再产生沉淀,经过滤、洗涤和干燥得到沉淀0.233克,则原混合溶液中硫酸的溶质质量分数为______。
【融合创新】依据科学原理,融合技术与工程,形成新颖而有价值的解决实际问题的方案。
(4)常压加热蒸馏法,能耗大、成本高。小科查阅资料获知,现在世界上的许多大型海水淡化工厂,都已经采用低压加热蒸馏法,请解释其蕴含的科学道理:___________________________________________________。
0.98%
液体的沸点随气压的降低而
降低,从而节约能量消耗
同课章节目录
