化学人教版(2019)必修第一册3.2.3铁的重要化合物(共26张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册3.2.3铁的重要化合物(共26张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 9.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-19 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
铁的重要化合物
人教版 高中化学 必修一 第三章 第二节 第三课时
赤铁矿( )
磁铁矿( )
红色的油漆( )
课程导入
磁铁( )
Fe2O3
Fe2O3
Fe3O4
Fe3O4
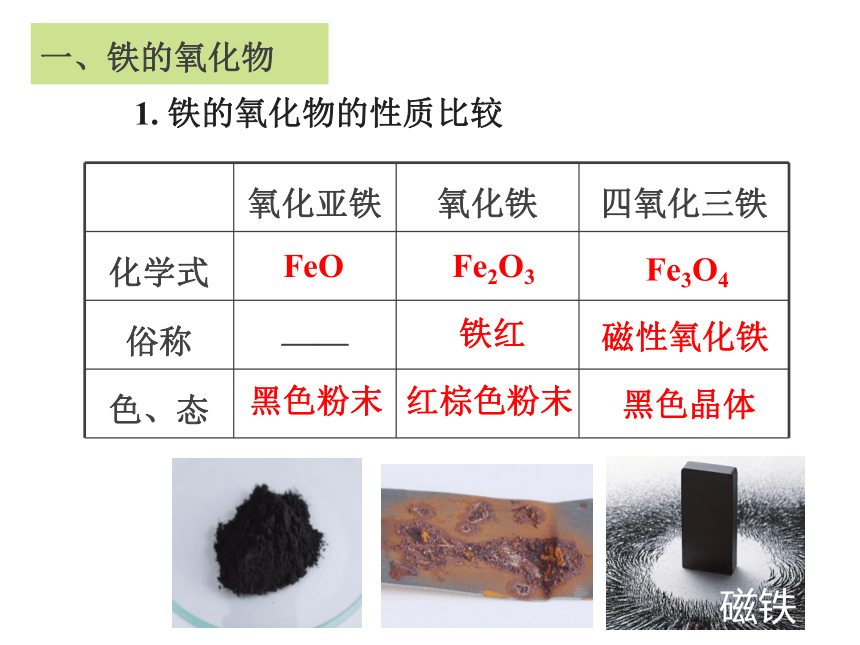
1. 铁的氧化物的性质比较
氧化亚铁 氧化铁 四氧化三铁
化学式
俗称 ——
色、态
磁性氧化铁
黑色晶体
一、铁的氧化物
FeO
Fe2O3
Fe3O4
铁红
黑色粉末
红棕色粉末
磁铁
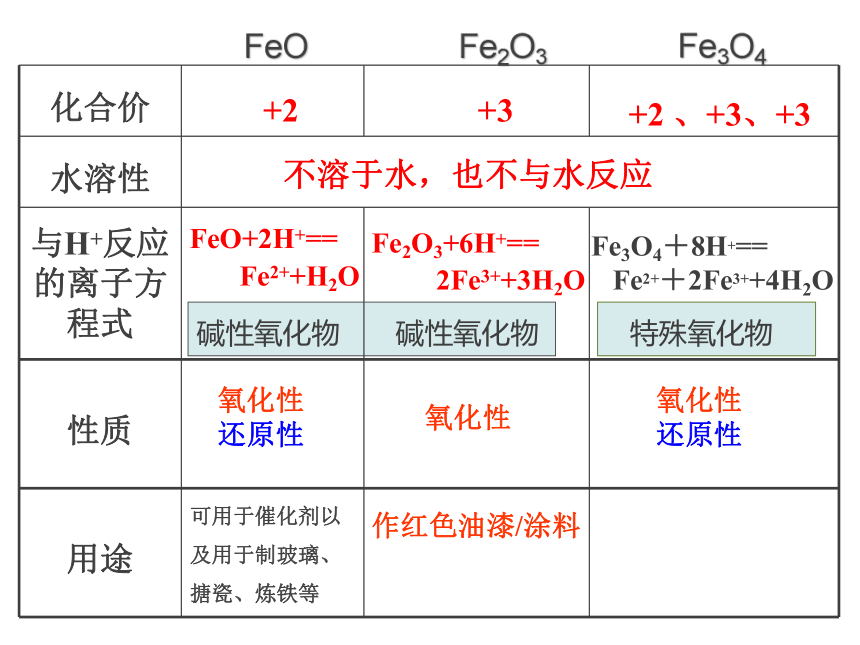
碱性氧化物 碱性氧化物
化合价
水溶性
与H+反应的离子方程式
性质
用途 可用于催化剂以及用于制玻璃、搪瓷、炼铁等
Fe2O3+6H+==
2Fe3++3H2O
FeO+2H+==
Fe2++H2O
+2 、+3、+3
+2
+3
特殊氧化物
不溶于水,也不与水反应
Fe3O4+8H+==
Fe2++2Fe3++4H2O
作红色油漆/涂料
氧化性
还原性
氧化性
氧化性
还原性
FeO Fe2O3 Fe3O4
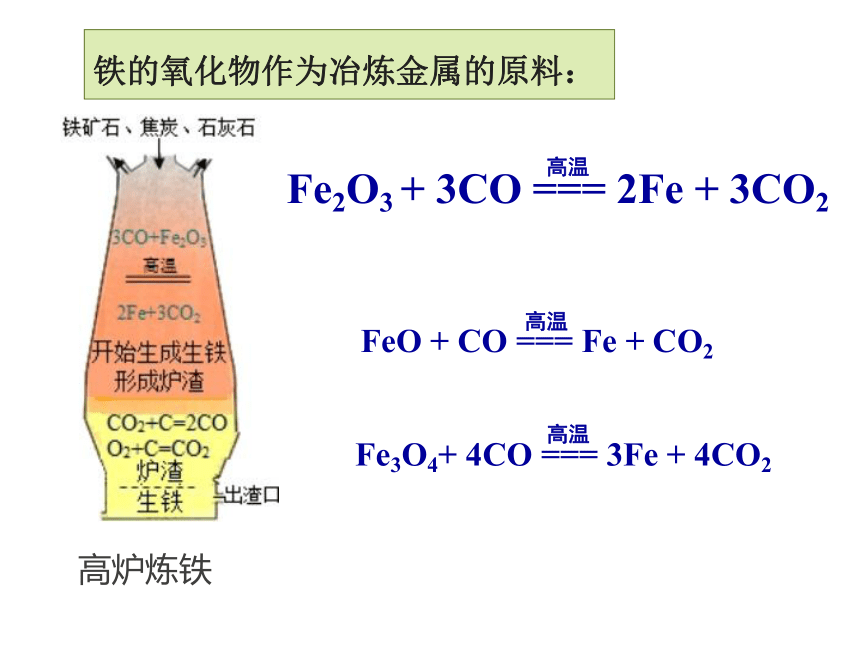
铁的氧化物作为冶炼金属的原料:
Fe2O3 + 3CO === 2Fe + 3CO2
高温
FeO + CO === Fe + CO2
高温
Fe3O4+ 4CO === 3Fe + 4CO2
高温
高炉炼铁
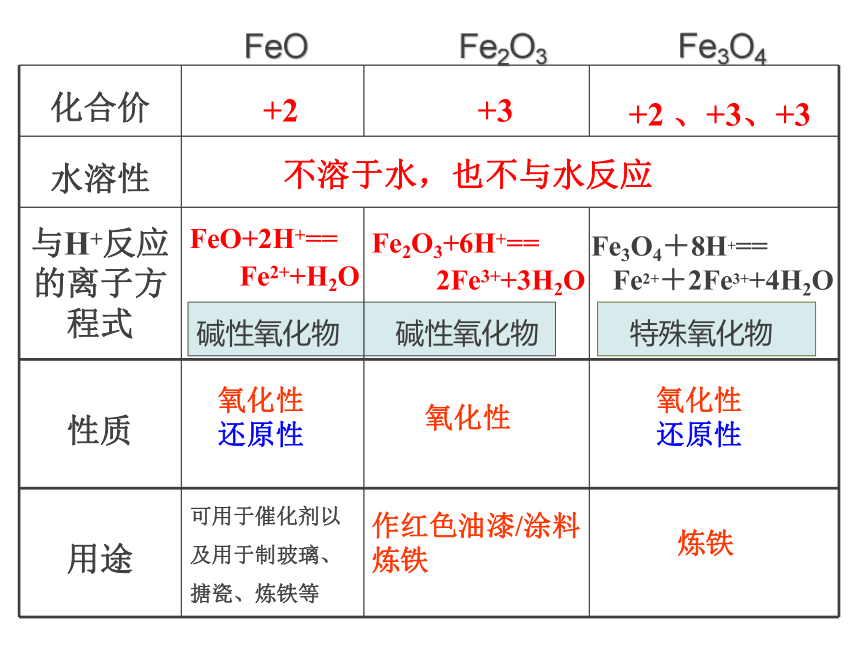
碱性氧化物 碱性氧化物
化合价
水溶性
与H+反应的离子方程式
性质
用途 可用于催化剂以及用于制玻璃、搪瓷、炼铁等
Fe2O3+6H+==
2Fe3++3H2O
FeO+2H+==
Fe2++H2O
+2 、+3、+3
+2
+3
特殊氧化物
不溶于水,也不与水反应
Fe3O4+8H+==
Fe2++2Fe3++4H2O
作红色油漆/涂料
炼铁
炼铁
氧化性
还原性
氧化性
氧化性
还原性
FeO Fe2O3 Fe3O4
二、铁的氢氧化物
在FeCl2、FeCl3溶液中分别加入NaOH溶液
实验3-9
Fe(OH)2转变过程
FeCl3 FeCl2
加入NaOH 溶液的现象
离子方程式
产生红褐色沉淀
先产生白色沉淀,
迅速变成灰绿色,
最后变成红褐色
Fe3++3OH-
==Fe(OH)3 ↓
①Fe2++2OH-==Fe(OH)2 ↓
②4Fe(OH)2+O2+2H2O
==4Fe(OH)3
浅绿色
黄色
www.themegallery.com
【改进实验】
由于Fe(OH)2易被空气中、溶液中的氧气氧化,因此在制备过程中要注意隔绝氧气:
1、煮沸NaOH溶液赶尽溶液的空气
4、采用铁粉和稀H2SO4制备新FeSO4溶液(现配现用)
2、滴加NaOH溶液时使用长胶头滴管并插入液面以下再将NaOH溶液挤出
5、制造还原性气氛(如H2),避免Fe(OH)2被氧化
3、向盛有 FeSO4 溶液的试管里加入植物油/苯
下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是?
A. B. C.
BC
当堂检测
【小结】氢氧化亚铁和氢氧化铁的性质
铁的氢氧化物 氢氧化亚铁 氢氧化铁
化学式
颜色、状态
水溶性
制备(离子方程式)
与盐酸反应 化学方程式
离子方程式
稳定性
转化关系
Fe(OH)2
Fe(OH)3
白色固体
红褐色固体
难溶于水
难溶于水
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
Fe(OH)3+3HCl==
FeCl3+3H2O
Fe(OH)2+2HCl==
FeCl2+2H2O
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)2+2H+=Fe2++2H2O
在空气中易被氧化成Fe(OH)3
白色沉淀迅速变为灰绿色,最终变为红褐色
阅读P62:资料卡片——铜盐
古代铜制品上往往覆盖着一层铜绿
Cu2(OH)2CO3
Cu单质不活泼
使用铜器皿比较安全
铜盐溶液有毒—— Cu2+有毒
Cu2+能与蛋白质作用,使蛋白质失去生理功能
铜盐
铜
用途广泛的金属材料
P64
金属材料:
纯金属
合金(※)
铝合金锅
钛合金羽毛球拍
镍合金门锁
金属材料:
纯金属
合金(※)
初中曾学过有关合金的知识,你还记得什么是合金吗?
想一想
△注意:
①合金一定是混合物
合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
②合金中至少含有一种金属元素,合金中也可能含有非金属元素
合金具有许多优良的物理、化学或机械性能:
(1)合金的熔点一般低于它的各成分金属。
(2)合金的硬度、抗腐蚀性能强于它的各成分金属。
为什么我们使用的金属材料主要是合金,而不是纯金属?
铜合金
青铜
黄铜
白铜
(铜、锡及少量的铅)
(铜、锌及少量的锡、铅、铝等)
(铜、镍、锌及少量的锰)
青铜是最早发现的合金
常见的合金
1、铜合金
铁合金
生铁
钢
碳素钢
合金钢
不锈钢
锰钢
含碳0.03%~2%
用锰钢制成的钢轨
含碳2%~4.3%
用量最大,
用途最广的合金
常见的合金
2、铁合金
“21世纪最有发展前景的金属材料”
常应用于航天、汽车、医疗方面
常见的合金
3、钛合金
稀土金属
稀土金属有着广泛的用途,它既可以单独使用,
也可用于生产合金。在合金中加入适量稀土金属,
能大大改善合金的性能。它被
广泛应用在冶金、石油化工、
材料工业、医药及农业等领域。
含稀土元素的汽车尾气净化器
冶金工业的维生素
科学视野P67
随堂练习
关于铁及其化合物的叙述正确的是
A 铁是一种较活泼的金属
B Fe2O3在常温下可以导电
C Fe2O3溶于水生成Fe(OH)3
D 在常温下铁丝容易与水反应放出H2
A
随堂练习
下列有关氢氧化亚铁及其制备方法的叙述中,不正确的是( )
A氢氧化亚铁易被空气氧化
B氢氧化亚铁为灰绿色絮状沉淀
C可利用如图所示装置,制备氢氧化亚铁
D实验制备中,氢氧化钠溶液应预先煮沸
B
随堂练习
下列物质中,不属于合金的是
A.硬铝 B.黄铜
C. 钢铁 D. 水银
D
随堂练习
某物质由铁和氧两种元素组成实验测得铁元素与氧元素的质量比为21:8,下列说法不正确的是( )
A铁元素与氧元素物质的量之比为3:4
B该物质一定为四氧化三铁
C该物质可能为四氧化三铁
D该物质可能为混合物
B
铁的重要化合物
人教版 高中化学 必修一 第三章 第二节 第三课时
赤铁矿( )
磁铁矿( )
红色的油漆( )
课程导入
磁铁( )
Fe2O3
Fe2O3
Fe3O4
Fe3O4
1. 铁的氧化物的性质比较
氧化亚铁 氧化铁 四氧化三铁
化学式
俗称 ——
色、态
磁性氧化铁
黑色晶体
一、铁的氧化物
FeO
Fe2O3
Fe3O4
铁红
黑色粉末
红棕色粉末
磁铁
碱性氧化物 碱性氧化物
化合价
水溶性
与H+反应的离子方程式
性质
用途 可用于催化剂以及用于制玻璃、搪瓷、炼铁等
Fe2O3+6H+==
2Fe3++3H2O
FeO+2H+==
Fe2++H2O
+2 、+3、+3
+2
+3
特殊氧化物
不溶于水,也不与水反应
Fe3O4+8H+==
Fe2++2Fe3++4H2O
作红色油漆/涂料
氧化性
还原性
氧化性
氧化性
还原性
FeO Fe2O3 Fe3O4
铁的氧化物作为冶炼金属的原料:
Fe2O3 + 3CO === 2Fe + 3CO2
高温
FeO + CO === Fe + CO2
高温
Fe3O4+ 4CO === 3Fe + 4CO2
高温
高炉炼铁
碱性氧化物 碱性氧化物
化合价
水溶性
与H+反应的离子方程式
性质
用途 可用于催化剂以及用于制玻璃、搪瓷、炼铁等
Fe2O3+6H+==
2Fe3++3H2O
FeO+2H+==
Fe2++H2O
+2 、+3、+3
+2
+3
特殊氧化物
不溶于水,也不与水反应
Fe3O4+8H+==
Fe2++2Fe3++4H2O
作红色油漆/涂料
炼铁
炼铁
氧化性
还原性
氧化性
氧化性
还原性
FeO Fe2O3 Fe3O4
二、铁的氢氧化物
在FeCl2、FeCl3溶液中分别加入NaOH溶液
实验3-9
Fe(OH)2转变过程
FeCl3 FeCl2
加入NaOH 溶液的现象
离子方程式
产生红褐色沉淀
先产生白色沉淀,
迅速变成灰绿色,
最后变成红褐色
Fe3++3OH-
==Fe(OH)3 ↓
①Fe2++2OH-==Fe(OH)2 ↓
②4Fe(OH)2+O2+2H2O
==4Fe(OH)3
浅绿色
黄色
www.themegallery.com
【改进实验】
由于Fe(OH)2易被空气中、溶液中的氧气氧化,因此在制备过程中要注意隔绝氧气:
1、煮沸NaOH溶液赶尽溶液的空气
4、采用铁粉和稀H2SO4制备新FeSO4溶液(现配现用)
2、滴加NaOH溶液时使用长胶头滴管并插入液面以下再将NaOH溶液挤出
5、制造还原性气氛(如H2),避免Fe(OH)2被氧化
3、向盛有 FeSO4 溶液的试管里加入植物油/苯
下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是?
A. B. C.
BC
当堂检测
【小结】氢氧化亚铁和氢氧化铁的性质
铁的氢氧化物 氢氧化亚铁 氢氧化铁
化学式
颜色、状态
水溶性
制备(离子方程式)
与盐酸反应 化学方程式
离子方程式
稳定性
转化关系
Fe(OH)2
Fe(OH)3
白色固体
红褐色固体
难溶于水
难溶于水
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
Fe(OH)3+3HCl==
FeCl3+3H2O
Fe(OH)2+2HCl==
FeCl2+2H2O
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)2+2H+=Fe2++2H2O
在空气中易被氧化成Fe(OH)3
白色沉淀迅速变为灰绿色,最终变为红褐色
阅读P62:资料卡片——铜盐
古代铜制品上往往覆盖着一层铜绿
Cu2(OH)2CO3
Cu单质不活泼
使用铜器皿比较安全
铜盐溶液有毒—— Cu2+有毒
Cu2+能与蛋白质作用,使蛋白质失去生理功能
铜盐
铜
用途广泛的金属材料
P64
金属材料:
纯金属
合金(※)
铝合金锅
钛合金羽毛球拍
镍合金门锁
金属材料:
纯金属
合金(※)
初中曾学过有关合金的知识,你还记得什么是合金吗?
想一想
△注意:
①合金一定是混合物
合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
②合金中至少含有一种金属元素,合金中也可能含有非金属元素
合金具有许多优良的物理、化学或机械性能:
(1)合金的熔点一般低于它的各成分金属。
(2)合金的硬度、抗腐蚀性能强于它的各成分金属。
为什么我们使用的金属材料主要是合金,而不是纯金属?
铜合金
青铜
黄铜
白铜
(铜、锡及少量的铅)
(铜、锌及少量的锡、铅、铝等)
(铜、镍、锌及少量的锰)
青铜是最早发现的合金
常见的合金
1、铜合金
铁合金
生铁
钢
碳素钢
合金钢
不锈钢
锰钢
含碳0.03%~2%
用锰钢制成的钢轨
含碳2%~4.3%
用量最大,
用途最广的合金
常见的合金
2、铁合金
“21世纪最有发展前景的金属材料”
常应用于航天、汽车、医疗方面
常见的合金
3、钛合金
稀土金属
稀土金属有着广泛的用途,它既可以单独使用,
也可用于生产合金。在合金中加入适量稀土金属,
能大大改善合金的性能。它被
广泛应用在冶金、石油化工、
材料工业、医药及农业等领域。
含稀土元素的汽车尾气净化器
冶金工业的维生素
科学视野P67
随堂练习
关于铁及其化合物的叙述正确的是
A 铁是一种较活泼的金属
B Fe2O3在常温下可以导电
C Fe2O3溶于水生成Fe(OH)3
D 在常温下铁丝容易与水反应放出H2
A
随堂练习
下列有关氢氧化亚铁及其制备方法的叙述中,不正确的是( )
A氢氧化亚铁易被空气氧化
B氢氧化亚铁为灰绿色絮状沉淀
C可利用如图所示装置,制备氢氧化亚铁
D实验制备中,氢氧化钠溶液应预先煮沸
B
随堂练习
下列物质中,不属于合金的是
A.硬铝 B.黄铜
C. 钢铁 D. 水银
D
随堂练习
某物质由铁和氧两种元素组成实验测得铁元素与氧元素的质量比为21:8,下列说法不正确的是( )
A铁元素与氧元素物质的量之比为3:4
B该物质一定为四氧化三铁
C该物质可能为四氧化三铁
D该物质可能为混合物
B
