2022-2023学年高二化学人教版(2019)选择性必修31.2.1 有机化合物的分离、提纯 课件(32张PPT)
文档属性
| 名称 | 2022-2023学年高二化学人教版(2019)选择性必修31.2.1 有机化合物的分离、提纯 课件(32张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 47.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-20 00:00:00 | ||
图片预览






文档简介
(共32张PPT)
有机化合物的分离、提纯
第一章 第二节
第1课时
情境导入
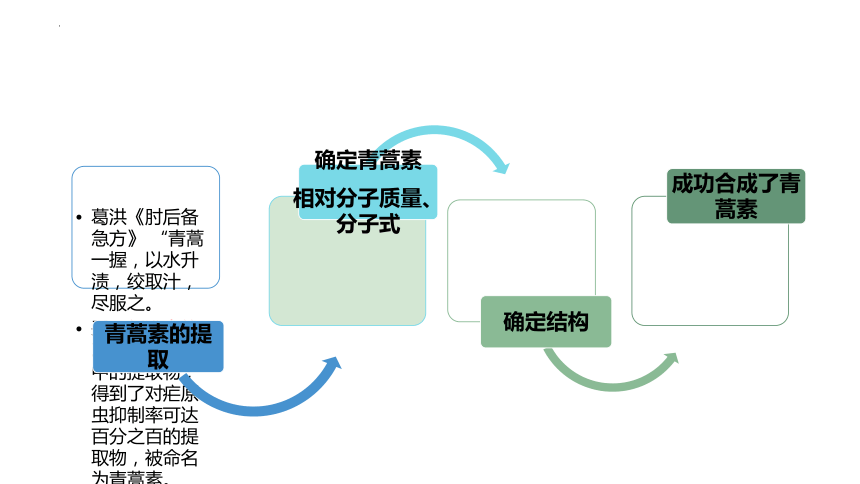
中国药学家屠呦呦发现了青蒿素,开创了疟疾治疗新方法,全球数亿人因这种“中国神药”而受益,她因此荣获2015年诺贝尔生理学或医学奖。
目标一 有机化合物的分离、提纯
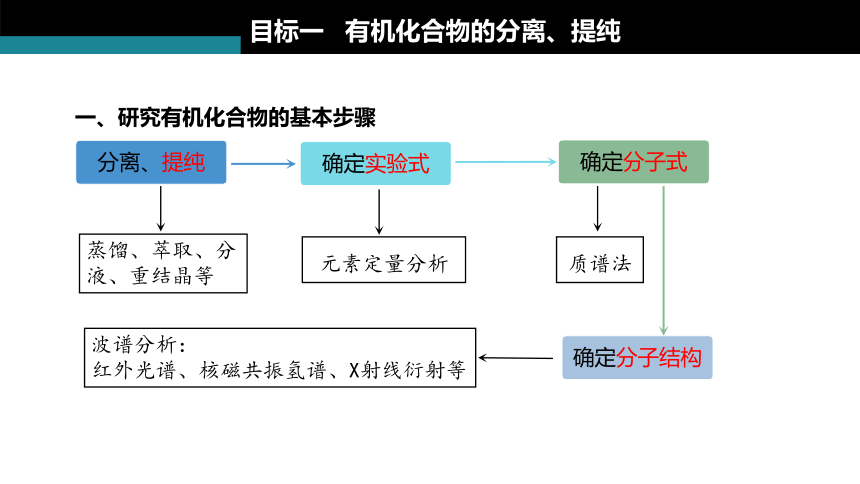
一、研究有机化合物的基本步骤
蒸馏、萃取、分液、重结晶等
元素定量分析
质谱法
波谱分析:
红外光谱、核磁共振氢谱、X射线衍射等
分离、提纯
确定实验式
确定分子式
确定分子结构
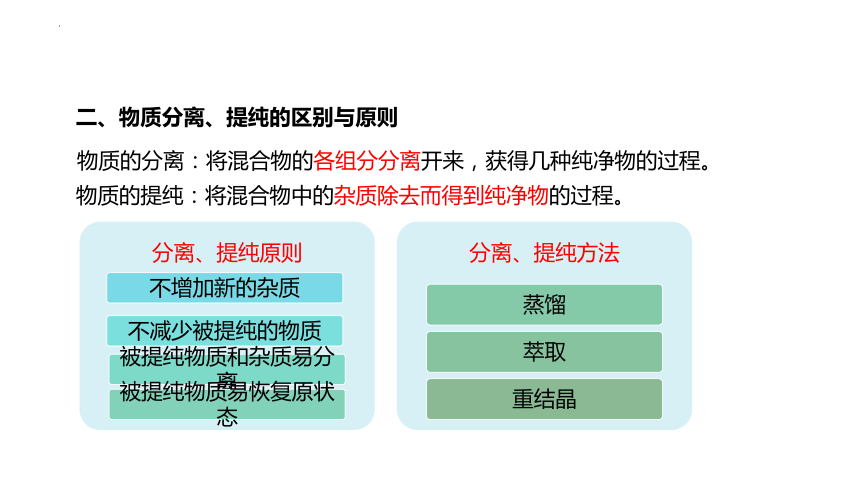
二、物质分离、提纯的区别与原则
物质的分离:将混合物的各组分分离开来,获得几种纯净物的过程。
物质的提纯:将混合物中的杂质除去而得到纯净物的过程。
三、物质分离、提纯的物理方法
1. 蒸馏
(2)适用条件:
(1)原理:利用沸点差异分离液体混合物。
①液态有机物中含有少量杂质;
②有机物热稳定性较高;
③有机物与杂质的沸点相差较大(一般约大于30 ℃)。
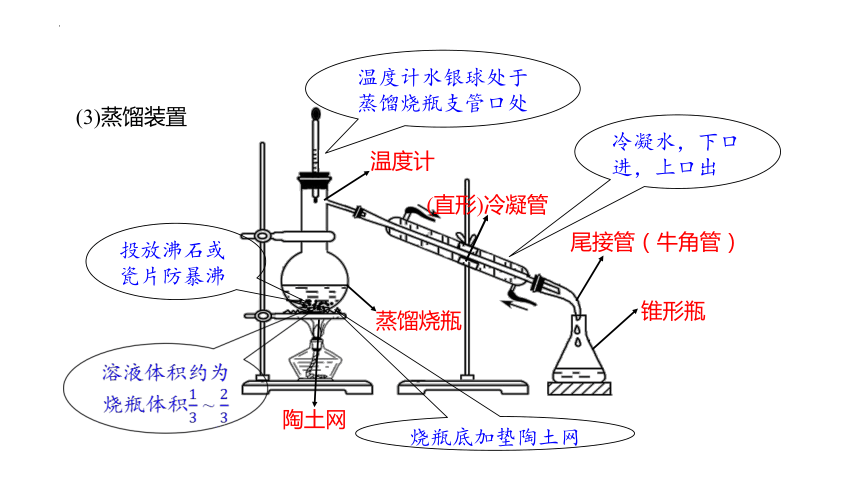
(3)蒸馏装置
(直形)冷凝管
蒸馏烧瓶
尾接管(牛角管)
锥形瓶
温度计
温度计水银球处于蒸馏烧瓶支管口处
冷凝水,下口进,上口出
投放沸石或瓷片防暴沸
烧瓶底加垫陶土网
溶液体积约为烧瓶体积 ~
陶土网
2. 萃取
(1)类型
固-液萃取:用溶剂从固体物质中溶解出待分离组分的过程。
液-液萃取:利用待分离组分在两种不互溶的溶剂中的溶解度不同,将其从一种溶剂转移到另一种溶剂的过程。
(2)对萃取剂的要求
萃取剂与原溶剂互不相溶
溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度
萃取剂与原溶液中的成分不反应
(3)常用萃取剂:乙醚、乙酸乙酯、二氯甲烷等。
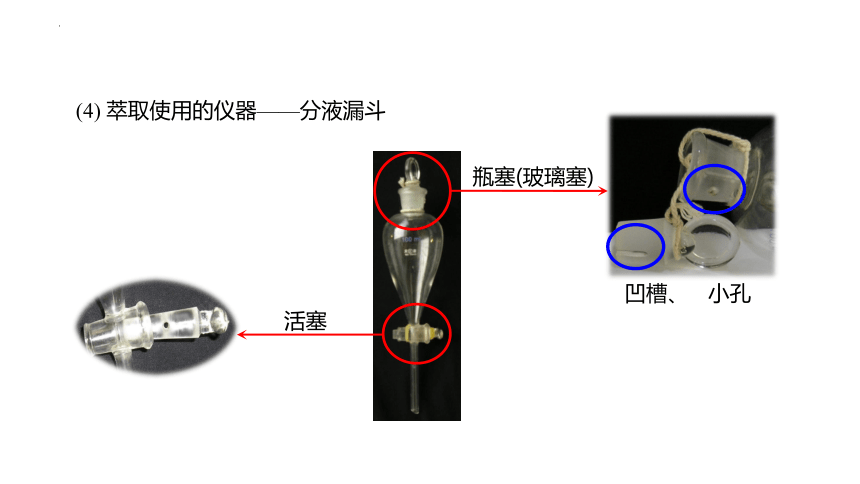
(4) 萃取使用的仪器——分液漏斗
活塞
瓶塞(玻璃塞)
凹槽、 小孔
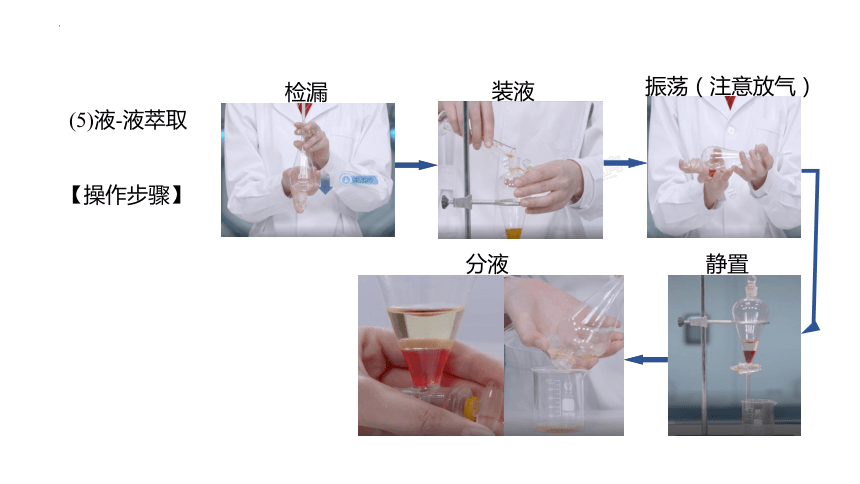
(5)液-液萃取
【操作步骤】
检漏
装液
振荡(注意放气)
静置
分液
3. 分液
含义:将萃取后的两层液体分开的操作。
①分液时,将漏斗上口的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔。
②分液时,漏斗下端管口尖嘴部分紧靠烧杯内壁。
③分液时,下层液体从下口流出,上层液体从上口倒出。
注意事项
4. 重结晶
(1)原理:利用被提纯物质与杂质在同一溶剂中的溶解度不同而将杂质除去。
关键:选择适当的溶剂
①杂质在溶剂中的溶解度很小或很大;
②被提纯的有机物在此溶剂中的溶解度受温度的影响较大,能够进行冷却结晶。
冷却结晶
(2)操作步骤:
加热溶解
趁热过滤
重结晶法提纯苯甲酸
实验探究
提示 原理是苯甲酸在不同温度的蒸馏水中溶解度不同。主要操作步骤有加热溶解、趁热过滤、冷却结晶、过滤洗涤、干燥称量。
问题讨论:
(1)重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
(2)溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
提示 加热是为了提高苯甲酸的溶解速率、增大苯甲酸的溶解度,使苯甲酸充分溶解。趁热过滤是为了防止苯甲酸提前结晶析出。
(3)实验操作中多次用到了玻璃棒,分别起到了哪些作用?
提示 ①溶解时搅拌,加快溶解速率;②过滤、洗涤时引流。
(4)如何检验提纯后的苯甲酸中氯化钠已被除净?
提示 用适量蒸馏水洗涤过滤器中的苯甲酸晶体,取少量最后一次的洗涤液,向其中滴加几滴硝酸银溶液,观察是否有沉淀产生。若无沉淀产生,则氯化钠已被除净。
用胶头滴管往晶体上加蒸馏水直至晶体被浸没,待水完全流出后,重复操作两至三次,直至晶体被洗净。
不纯固体物质
残渣(不溶性杂质)
滤液
母液(可溶性杂质和部分被提纯物)
晶体(产品)
溶于溶剂,制成饱和溶液,趁热过滤
冷却,结晶,过滤,洗涤
如何洗涤结晶或沉淀?
(3)重结晶的基本流程:
导思
1.冷凝管是蒸馏操作中的重要仪器。为了使冷凝效果最佳,在实验操作中冷水的通入、停止与加热的先后关系是什么?冷凝管中冷却水为什么采取进水口在下,出水口在上的方式?
提示:实验开始时,应先通冷却水,后点燃酒精灯。
实验结束时应先熄灭酒精灯(注意不能蒸干,应在蒸馏烧瓶内还有少量液体时停止),等蒸馏烧瓶恢复至室温时停止通入冷却水。
冷却水的流动方向与需要冷却的蒸气的方向相反,冷却效果好
导思
2.当互溶的两种液态有机物中各组分的沸点相差较小时如何处理?
提示 最好将混合物“预处理”,一般先将其中的一种物质转化为不挥发的盐类化合物,再进行蒸馏。比如乙醇中混有乙酸,可先加生石灰,将乙酸转化为乙酸钙再蒸馏。
导思
3.重结晶实验中,温度越低,苯甲酸的溶解度越小,为了得到更多的苯甲酸晶体,是不是结晶时的温度越低越好?
提示 不是。温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的。
导练
1.正误判断
(1)能用分液的方法分离植物油和水的混合物( )
(2)Br2、I2在水中的溶解度较小,但易溶于有机溶剂,故可用酒精萃取溴水中的Br2或碘水中的I2( )
(3)利用蒸馏法分离液态有机物时,温度计可以插入液面以下( )
(4)在蒸馏实验中,发现忘记加沸石,应立即停止实验,马上加入( )
(5)重结晶要求杂质的溶解度比被提纯的物质小才能进行分离( )
√
×
×
×
×
2.现有3组混合物:
①乙酸乙酯和乙酸钠溶液、
②乙醇和丁醇、
③溴化钠和单质溴的水溶液,
分离以上各组混合物的正确方法依次是( )
A.分液法、萃取法、蒸馏法 B.萃取法、蒸馏法、分液法
C.分液法、蒸馏法、萃取法 D.蒸馏法、萃取法、分液法
导练
C
不互溶
互溶,沸点不同
单质溴易溶于有机溶剂,溴化钠不溶于有机溶剂
思维聚焦
获取晶体的两种方法
将溶剂蒸发获取晶体,此法适用于溶解度随温度变化不大的溶液,如粗盐的提纯
蒸发结晶
将热的饱和溶液慢慢冷却后析出晶体,此法适用于溶解度随温度变化较大的溶液,如氯化钠和硝酸钾的分离。
降温结晶
目标二 常见有机混合物的分离与提纯
1. 气体有机混合物的分离与提纯
下表中括号内的物质为杂质,请你在下面对应的空格中填上除杂试剂。
有机混合物 (1)甲烷(水蒸气) (2)乙烷(乙烯) (3)乙烯(二氧化硫)
除杂试剂
浓硫酸(或碱石灰或五氧化二磷或氯化钙)
溴水
氢氧化钠溶液
2. 液体有机混合物的分离与提纯
例1 请你根据要求,在下面对应的空格中填上不同的分离和提纯方法。
有机混合物 (1)苯、高锰酸钾溶液 (2)工业酒精 (3)含酚工业废水
实验要求 分离苯、高锰酸钾溶液 除去甲醇、水 回收酚
操作名称
分液
蒸馏
萃取、分液
例2 探究用环己烯粗品精制环己烯的方法。
已知实验室制取环己烯的化学原理:
+H2O
密度/(g·cm-3) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25 161 可溶
环己烯 0.81 -103 83 难溶
(1)除去环己烯粗品中的杂质,需先加入饱和碳酸钠溶液,其主要目的是什么?
提示 除去环己烯中的酸性杂质和部分环己醇。
(2)加入饱和碳酸钠溶液后,振荡、静置,环己烯在上层还是下层?
提示 环己烯在上层。
例2 探究用环己烯粗品精制环己烯的方法。
已知实验室制取环己烯的化学原理:
+H2O
密度/(g·cm-3) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25 161 可溶
环己烯 0.81 -103 83 难溶
(3)静置后如何操作?该操作用到的主要仪器是什么?
提示 静置后应进行分液操作:将下层液体从分液漏斗下口放出,环己烯从分液漏斗上口倒出。用到的主要仪器是分液漏斗、烧杯。
3.固体有机混合物的分离与提纯
例3 目前从大豆油提取油脂主要采用的是浸出法,先用“扎坯机”进行加工,然后将加工过的大豆投入浸出器,浸出溶剂一般有两种,一是“6号”抽提油,二是“正己烷”,它们统称“溶剂油”,“溶剂油”的作用实际就是“洗涤剂”,它把油脂从大豆中“带走”,然后经过加热处理回收溶剂,容器中剩下的就是豆油。
提示 萃取、蒸馏。
(1)上述豆油提取过程中,涉及的实验操作方法有哪些?
(2)讨论并回忆学过哪些与水互不相溶的溶剂?它们的密度比水大还是比水小?
提示 密度比水小的有:苯、汽油、乙醚等,密度比水大的有:四氯化碳、氯仿等。
导练
采用浸取方法可从花生中得到食用花生油,应选用的浸取剂为( )
A.正己烷 B.苯
C.蒸馏水 D.甲醇
A
有毒
有毒且与水互溶
易溶于有机溶剂而难溶于水
1.在一定条件下,萘可与浓硝酸、浓硫酸两种混酸反应生成二硝基化合物,它是1,5-二硝基萘和1,8-二硝基萘的混合物:后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可以将这两种物质分离。在上述硝化产物中加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8-二硝基萘,应采用的方法是( )
A.对所得的滤液蒸发浓缩、冷却结晶
B.向滤液中缓缓加入水后过滤
C.将滤液缓缓加入水中后过滤
D.向滤液中缓缓加入Na2CO3溶液后过滤
自我检测
1
2
1,5-二硝基萘
1,8-二硝基萘
C
2.绿原酸(C16H18O9)具有较广泛的抗菌、抗病毒、抗氧化作用。利用乙醚、60%乙醇浸泡杜仲干叶,得到提取液,进一步获得绿原酸粗产品的一种工艺流程如图,下列说法错误的是( )
A.得到有机层的实验操作为萃取、分液
B.减压蒸馏的目的是防止温度过高,绿原酸变质
C.绿原酸在温水中溶解度小于在冷水中的溶解度
D.绿原酸粗产品可以通过重结晶法进一步提纯
自我检测
1
2
C
有机化合物的分离、提纯
第一章 第二节
第1课时
情境导入
中国药学家屠呦呦发现了青蒿素,开创了疟疾治疗新方法,全球数亿人因这种“中国神药”而受益,她因此荣获2015年诺贝尔生理学或医学奖。
目标一 有机化合物的分离、提纯
一、研究有机化合物的基本步骤
蒸馏、萃取、分液、重结晶等
元素定量分析
质谱法
波谱分析:
红外光谱、核磁共振氢谱、X射线衍射等
分离、提纯
确定实验式
确定分子式
确定分子结构
二、物质分离、提纯的区别与原则
物质的分离:将混合物的各组分分离开来,获得几种纯净物的过程。
物质的提纯:将混合物中的杂质除去而得到纯净物的过程。
三、物质分离、提纯的物理方法
1. 蒸馏
(2)适用条件:
(1)原理:利用沸点差异分离液体混合物。
①液态有机物中含有少量杂质;
②有机物热稳定性较高;
③有机物与杂质的沸点相差较大(一般约大于30 ℃)。
(3)蒸馏装置
(直形)冷凝管
蒸馏烧瓶
尾接管(牛角管)
锥形瓶
温度计
温度计水银球处于蒸馏烧瓶支管口处
冷凝水,下口进,上口出
投放沸石或瓷片防暴沸
烧瓶底加垫陶土网
溶液体积约为烧瓶体积 ~
陶土网
2. 萃取
(1)类型
固-液萃取:用溶剂从固体物质中溶解出待分离组分的过程。
液-液萃取:利用待分离组分在两种不互溶的溶剂中的溶解度不同,将其从一种溶剂转移到另一种溶剂的过程。
(2)对萃取剂的要求
萃取剂与原溶剂互不相溶
溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度
萃取剂与原溶液中的成分不反应
(3)常用萃取剂:乙醚、乙酸乙酯、二氯甲烷等。
(4) 萃取使用的仪器——分液漏斗
活塞
瓶塞(玻璃塞)
凹槽、 小孔
(5)液-液萃取
【操作步骤】
检漏
装液
振荡(注意放气)
静置
分液
3. 分液
含义:将萃取后的两层液体分开的操作。
①分液时,将漏斗上口的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔。
②分液时,漏斗下端管口尖嘴部分紧靠烧杯内壁。
③分液时,下层液体从下口流出,上层液体从上口倒出。
注意事项
4. 重结晶
(1)原理:利用被提纯物质与杂质在同一溶剂中的溶解度不同而将杂质除去。
关键:选择适当的溶剂
①杂质在溶剂中的溶解度很小或很大;
②被提纯的有机物在此溶剂中的溶解度受温度的影响较大,能够进行冷却结晶。
冷却结晶
(2)操作步骤:
加热溶解
趁热过滤
重结晶法提纯苯甲酸
实验探究
提示 原理是苯甲酸在不同温度的蒸馏水中溶解度不同。主要操作步骤有加热溶解、趁热过滤、冷却结晶、过滤洗涤、干燥称量。
问题讨论:
(1)重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
(2)溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
提示 加热是为了提高苯甲酸的溶解速率、增大苯甲酸的溶解度,使苯甲酸充分溶解。趁热过滤是为了防止苯甲酸提前结晶析出。
(3)实验操作中多次用到了玻璃棒,分别起到了哪些作用?
提示 ①溶解时搅拌,加快溶解速率;②过滤、洗涤时引流。
(4)如何检验提纯后的苯甲酸中氯化钠已被除净?
提示 用适量蒸馏水洗涤过滤器中的苯甲酸晶体,取少量最后一次的洗涤液,向其中滴加几滴硝酸银溶液,观察是否有沉淀产生。若无沉淀产生,则氯化钠已被除净。
用胶头滴管往晶体上加蒸馏水直至晶体被浸没,待水完全流出后,重复操作两至三次,直至晶体被洗净。
不纯固体物质
残渣(不溶性杂质)
滤液
母液(可溶性杂质和部分被提纯物)
晶体(产品)
溶于溶剂,制成饱和溶液,趁热过滤
冷却,结晶,过滤,洗涤
如何洗涤结晶或沉淀?
(3)重结晶的基本流程:
导思
1.冷凝管是蒸馏操作中的重要仪器。为了使冷凝效果最佳,在实验操作中冷水的通入、停止与加热的先后关系是什么?冷凝管中冷却水为什么采取进水口在下,出水口在上的方式?
提示:实验开始时,应先通冷却水,后点燃酒精灯。
实验结束时应先熄灭酒精灯(注意不能蒸干,应在蒸馏烧瓶内还有少量液体时停止),等蒸馏烧瓶恢复至室温时停止通入冷却水。
冷却水的流动方向与需要冷却的蒸气的方向相反,冷却效果好
导思
2.当互溶的两种液态有机物中各组分的沸点相差较小时如何处理?
提示 最好将混合物“预处理”,一般先将其中的一种物质转化为不挥发的盐类化合物,再进行蒸馏。比如乙醇中混有乙酸,可先加生石灰,将乙酸转化为乙酸钙再蒸馏。
导思
3.重结晶实验中,温度越低,苯甲酸的溶解度越小,为了得到更多的苯甲酸晶体,是不是结晶时的温度越低越好?
提示 不是。温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的。
导练
1.正误判断
(1)能用分液的方法分离植物油和水的混合物( )
(2)Br2、I2在水中的溶解度较小,但易溶于有机溶剂,故可用酒精萃取溴水中的Br2或碘水中的I2( )
(3)利用蒸馏法分离液态有机物时,温度计可以插入液面以下( )
(4)在蒸馏实验中,发现忘记加沸石,应立即停止实验,马上加入( )
(5)重结晶要求杂质的溶解度比被提纯的物质小才能进行分离( )
√
×
×
×
×
2.现有3组混合物:
①乙酸乙酯和乙酸钠溶液、
②乙醇和丁醇、
③溴化钠和单质溴的水溶液,
分离以上各组混合物的正确方法依次是( )
A.分液法、萃取法、蒸馏法 B.萃取法、蒸馏法、分液法
C.分液法、蒸馏法、萃取法 D.蒸馏法、萃取法、分液法
导练
C
不互溶
互溶,沸点不同
单质溴易溶于有机溶剂,溴化钠不溶于有机溶剂
思维聚焦
获取晶体的两种方法
将溶剂蒸发获取晶体,此法适用于溶解度随温度变化不大的溶液,如粗盐的提纯
蒸发结晶
将热的饱和溶液慢慢冷却后析出晶体,此法适用于溶解度随温度变化较大的溶液,如氯化钠和硝酸钾的分离。
降温结晶
目标二 常见有机混合物的分离与提纯
1. 气体有机混合物的分离与提纯
下表中括号内的物质为杂质,请你在下面对应的空格中填上除杂试剂。
有机混合物 (1)甲烷(水蒸气) (2)乙烷(乙烯) (3)乙烯(二氧化硫)
除杂试剂
浓硫酸(或碱石灰或五氧化二磷或氯化钙)
溴水
氢氧化钠溶液
2. 液体有机混合物的分离与提纯
例1 请你根据要求,在下面对应的空格中填上不同的分离和提纯方法。
有机混合物 (1)苯、高锰酸钾溶液 (2)工业酒精 (3)含酚工业废水
实验要求 分离苯、高锰酸钾溶液 除去甲醇、水 回收酚
操作名称
分液
蒸馏
萃取、分液
例2 探究用环己烯粗品精制环己烯的方法。
已知实验室制取环己烯的化学原理:
+H2O
密度/(g·cm-3) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25 161 可溶
环己烯 0.81 -103 83 难溶
(1)除去环己烯粗品中的杂质,需先加入饱和碳酸钠溶液,其主要目的是什么?
提示 除去环己烯中的酸性杂质和部分环己醇。
(2)加入饱和碳酸钠溶液后,振荡、静置,环己烯在上层还是下层?
提示 环己烯在上层。
例2 探究用环己烯粗品精制环己烯的方法。
已知实验室制取环己烯的化学原理:
+H2O
密度/(g·cm-3) 熔点/℃ 沸点/℃ 溶解性
环己醇 0.96 25 161 可溶
环己烯 0.81 -103 83 难溶
(3)静置后如何操作?该操作用到的主要仪器是什么?
提示 静置后应进行分液操作:将下层液体从分液漏斗下口放出,环己烯从分液漏斗上口倒出。用到的主要仪器是分液漏斗、烧杯。
3.固体有机混合物的分离与提纯
例3 目前从大豆油提取油脂主要采用的是浸出法,先用“扎坯机”进行加工,然后将加工过的大豆投入浸出器,浸出溶剂一般有两种,一是“6号”抽提油,二是“正己烷”,它们统称“溶剂油”,“溶剂油”的作用实际就是“洗涤剂”,它把油脂从大豆中“带走”,然后经过加热处理回收溶剂,容器中剩下的就是豆油。
提示 萃取、蒸馏。
(1)上述豆油提取过程中,涉及的实验操作方法有哪些?
(2)讨论并回忆学过哪些与水互不相溶的溶剂?它们的密度比水大还是比水小?
提示 密度比水小的有:苯、汽油、乙醚等,密度比水大的有:四氯化碳、氯仿等。
导练
采用浸取方法可从花生中得到食用花生油,应选用的浸取剂为( )
A.正己烷 B.苯
C.蒸馏水 D.甲醇
A
有毒
有毒且与水互溶
易溶于有机溶剂而难溶于水
1.在一定条件下,萘可与浓硝酸、浓硫酸两种混酸反应生成二硝基化合物,它是1,5-二硝基萘和1,8-二硝基萘的混合物:后者可溶于质量分数大于98%的硫酸,而前者不能。利用这一性质可以将这两种物质分离。在上述硝化产物中加入适量的98.3%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1,8-二硝基萘,应采用的方法是( )
A.对所得的滤液蒸发浓缩、冷却结晶
B.向滤液中缓缓加入水后过滤
C.将滤液缓缓加入水中后过滤
D.向滤液中缓缓加入Na2CO3溶液后过滤
自我检测
1
2
1,5-二硝基萘
1,8-二硝基萘
C
2.绿原酸(C16H18O9)具有较广泛的抗菌、抗病毒、抗氧化作用。利用乙醚、60%乙醇浸泡杜仲干叶,得到提取液,进一步获得绿原酸粗产品的一种工艺流程如图,下列说法错误的是( )
A.得到有机层的实验操作为萃取、分液
B.减压蒸馏的目的是防止温度过高,绿原酸变质
C.绿原酸在温水中溶解度小于在冷水中的溶解度
D.绿原酸粗产品可以通过重结晶法进一步提纯
自我检测
1
2
C
