人教版选修二 1.1.2 构造原理与电子排布式 课件(19张ppt)
文档属性
| 名称 | 人教版选修二 1.1.2 构造原理与电子排布式 课件(19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 477.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-20 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第一节 原子结构(第2课时)
构造原理与电子排布式
《物质结构与性质》
学习目标:
1.了解原子核外电子排布的构造原理。
2.能根据思维模型熟练书写1~36号元素的电子排布式。
《物质结构与性质》
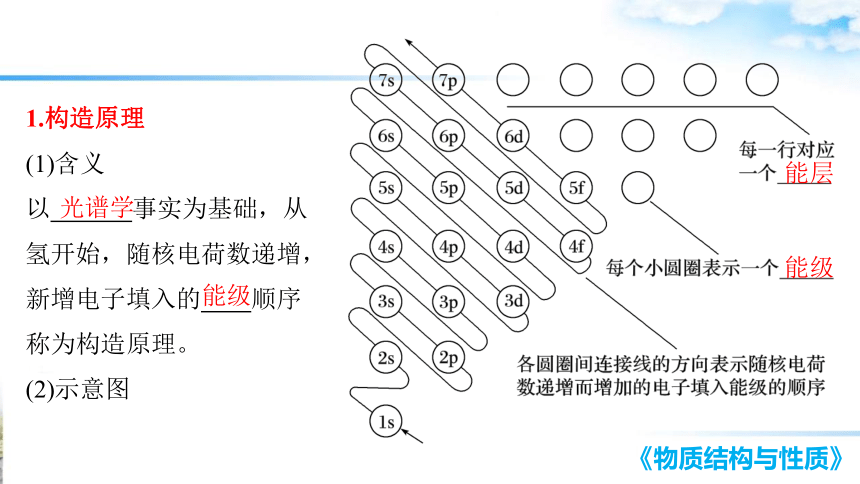
1.构造原理
(1)含义
以 事实为基础,从氢开始,随核电荷数递增,新增电子填入的 顺序
称为构造原理。
(2)示意图
光谱学
能级
能层
能级
《物质结构与性质》
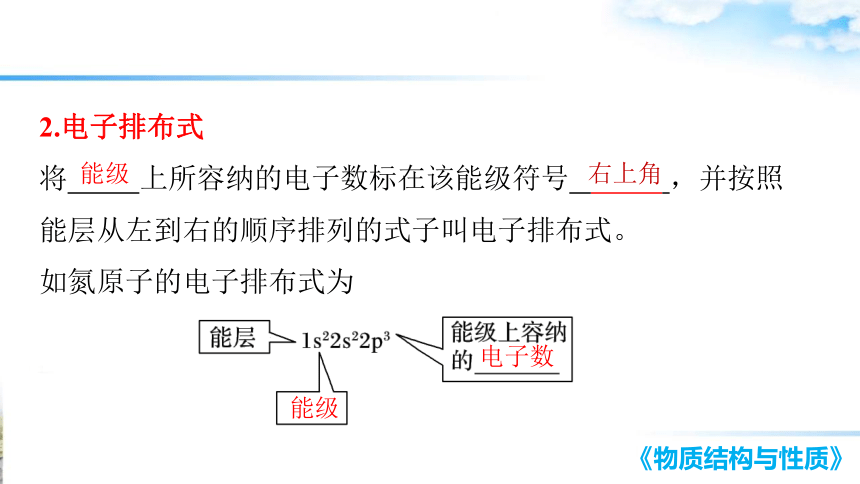
2.电子排布式
将 上所容纳的电子数标在该能级符号 ,并按照能层从左到右的顺序排列的式子叫电子排布式。
如氮原子的电子排布式为
能级
右上角
能级
电子数
《物质结构与性质》
例题:书写下列元素基态原子的电子排布式
H O Si K Ca Fe
《物质结构与性质》
《物质结构与性质》
8O
1s22s22p63s23p2
1s1
按构造原理填充电子,但要按能层顺序书写。
1H
14Si
基态原子
电子填充顺序
电子排布式
1s1
1s22s22p4
1s22s22p4
1s22s22p63s23p2
《物质结构与性质》
基态原子
电子填充顺序
电子排布式
19K
20Ca
26Fe
1s22s22p63s23p64s1
1s22s22p63s23p64s1
1s22s22p63s23p64s2
1s22s22p63s23p64s2
1s22s22p63s23p64s23d6
1s22s22p63s23p63d64s2
《物质结构与性质》
书写原则
按照构造原理将电子依次填充到能量逐渐升高的能级中
(1)相同能层的不同能级的能量高低顺序 :
(2)英文字母相同的不同能级的能量高低顺序:
(3) 不同层不同能级可由下面的公式得出:
各能级的能量高低顺序
ns<np<nd<nf
1s<2s<3s<4s;2p<3p<4p;3d<4d
ns<(n-2)f<(n-1)d<np (n为能层序数) 称为能级交错现象
《物质结构与性质》
能级交错
从第三能层开始出现能级交错现象,能级交错排列的顺序即电子能量由低到高的顺序,即Ens<E(n-2)f<E(n-1)d<Enp
随着电荷数递增,电子并不总是填满一个能层后再开始填入下一个能层的,电子是按能量由低到高的顺序填充的,这种现象被称为能级交错。
源于光谱学事实
《物质结构与性质》
按照构造原理将电子依次填充到能量逐渐升高的能级中
一般情况下,能层低的能级要写在左边,而不是按照构造原理顺序写
如:26Fe 1s22s22p63s23p63d64s2
基态铬、铜的核外电子排布不符合构造原理
Cr基态原子的电子排布式:
Cu基态原子的电子排布式:
1s22s22p63s23p63d54s1
1s22s22p63s23p63d104s1
半充满
全充满
练习1.根据构造原理,试比较下列能级的能量高低(填“>”或“<”)。
①2p____3p____4p
②4s____4p____4d____4f
③4s____3d
④6s____4f____5d
<
<
<
<
<
<
<
<
《物质结构与性质》
《物质结构与性质》
练习2:按构造原理写出稀有气体氦、氖、氩、氪、氙、氡的基态原子的最外层电子排布; 除氦外它们的通式是什么?
He 1s2
Ne 2s22p6
Ar 3s23p6
Kr 4s 24p6
Xe 5s 25p6
Rn 6s 26p6
通式:ns2np6
3.简化电子排布式
Na的电子排布式为1s22s22p63s1,可简化为[Ne]3s1,Na的内层电子排布与稀有气体元素Ne的核外电子排布相同。
《物质结构与性质》
练习3:根据构造原理,写出下列基态原子的核外电子排布式和简化电子排布式。
(1)8O:____________________;
(2)14Si:_________________________;
(3)18Ar:_________________________;
(4)19K:________________________;
(5)21Sc:______________________________;
(6)26Fe:______________________________。
1s22s22p4 [He]2s22p4
1s22s22p63s23p2 [Ne]3s23p2
1s22s22p63s23p6 [Ne]3s23p6
1s22s22p63s23p64s1 [Ar]4s1
1s22s22p63s23p63d14s2 [Ar]3d14s2
1s22s22p63s23p63d64s2 [Ar]3d64s2
《物质结构与性质》
4.价层电子排布式
为突出化合价与电子排布的关系,将在化学反应中可能发生电子变动的能级称为价电子层(简称价层)。
如:Ni的简化电子排布式为_______,价层电子排布为 _______。
练习4:试写出下列原子的价层电子排布:
①13Al:_______;②32Ge:_______;③34Se:_______。
[Ar]3d84s2
3d84s2
3s23p1
4s24p2
4s24p4
《物质结构与性质》
《物质结构与性质》
先写原子的电子排布式,然后再考虑得失得失电子的情况。
如O2-的电子排布式,先写O原子的电子排布式为1s22s22p4,再得2个电子知O2-的电子排布式为1s22s22p6。
5、简单离子电子排布式:
《物质结构与性质》
课堂小结:原子核外电子排布的表示方法
电子排布式
简化电子排布式
价电子排布式
轨道表示式
课堂巩固:
1.下列各原子或离子的电子排布式错误的是
A.Mg2+ 1s22s22p6
B.Br 1s22s22p63s23p63d104s24p5
C.O2- 1s22s22p6
D.Cr 1s22s22p63s23p63d44s2
√
《物质结构与性质》
2.某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法不正确的是
A.该元素原子中共有25个电子
B.该元素原子核外有4个能层
C.该元素原子最外层共有2个电子
D.该元素原子M能层共有8个电子
√
《物质结构与性质》
第一节 原子结构(第2课时)
构造原理与电子排布式
《物质结构与性质》
学习目标:
1.了解原子核外电子排布的构造原理。
2.能根据思维模型熟练书写1~36号元素的电子排布式。
《物质结构与性质》
1.构造原理
(1)含义
以 事实为基础,从氢开始,随核电荷数递增,新增电子填入的 顺序
称为构造原理。
(2)示意图
光谱学
能级
能层
能级
《物质结构与性质》
2.电子排布式
将 上所容纳的电子数标在该能级符号 ,并按照能层从左到右的顺序排列的式子叫电子排布式。
如氮原子的电子排布式为
能级
右上角
能级
电子数
《物质结构与性质》
例题:书写下列元素基态原子的电子排布式
H O Si K Ca Fe
《物质结构与性质》
《物质结构与性质》
8O
1s22s22p63s23p2
1s1
按构造原理填充电子,但要按能层顺序书写。
1H
14Si
基态原子
电子填充顺序
电子排布式
1s1
1s22s22p4
1s22s22p4
1s22s22p63s23p2
《物质结构与性质》
基态原子
电子填充顺序
电子排布式
19K
20Ca
26Fe
1s22s22p63s23p64s1
1s22s22p63s23p64s1
1s22s22p63s23p64s2
1s22s22p63s23p64s2
1s22s22p63s23p64s23d6
1s22s22p63s23p63d64s2
《物质结构与性质》
书写原则
按照构造原理将电子依次填充到能量逐渐升高的能级中
(1)相同能层的不同能级的能量高低顺序 :
(2)英文字母相同的不同能级的能量高低顺序:
(3) 不同层不同能级可由下面的公式得出:
各能级的能量高低顺序
ns<np<nd<nf
1s<2s<3s<4s;2p<3p<4p;3d<4d
ns<(n-2)f<(n-1)d<np (n为能层序数) 称为能级交错现象
《物质结构与性质》
能级交错
从第三能层开始出现能级交错现象,能级交错排列的顺序即电子能量由低到高的顺序,即Ens<E(n-2)f<E(n-1)d<Enp
随着电荷数递增,电子并不总是填满一个能层后再开始填入下一个能层的,电子是按能量由低到高的顺序填充的,这种现象被称为能级交错。
源于光谱学事实
《物质结构与性质》
按照构造原理将电子依次填充到能量逐渐升高的能级中
一般情况下,能层低的能级要写在左边,而不是按照构造原理顺序写
如:26Fe 1s22s22p63s23p63d64s2
基态铬、铜的核外电子排布不符合构造原理
Cr基态原子的电子排布式:
Cu基态原子的电子排布式:
1s22s22p63s23p63d54s1
1s22s22p63s23p63d104s1
半充满
全充满
练习1.根据构造原理,试比较下列能级的能量高低(填“>”或“<”)。
①2p____3p____4p
②4s____4p____4d____4f
③4s____3d
④6s____4f____5d
<
<
<
<
<
<
<
<
《物质结构与性质》
《物质结构与性质》
练习2:按构造原理写出稀有气体氦、氖、氩、氪、氙、氡的基态原子的最外层电子排布; 除氦外它们的通式是什么?
He 1s2
Ne 2s22p6
Ar 3s23p6
Kr 4s 24p6
Xe 5s 25p6
Rn 6s 26p6
通式:ns2np6
3.简化电子排布式
Na的电子排布式为1s22s22p63s1,可简化为[Ne]3s1,Na的内层电子排布与稀有气体元素Ne的核外电子排布相同。
《物质结构与性质》
练习3:根据构造原理,写出下列基态原子的核外电子排布式和简化电子排布式。
(1)8O:____________________;
(2)14Si:_________________________;
(3)18Ar:_________________________;
(4)19K:________________________;
(5)21Sc:______________________________;
(6)26Fe:______________________________。
1s22s22p4 [He]2s22p4
1s22s22p63s23p2 [Ne]3s23p2
1s22s22p63s23p6 [Ne]3s23p6
1s22s22p63s23p64s1 [Ar]4s1
1s22s22p63s23p63d14s2 [Ar]3d14s2
1s22s22p63s23p63d64s2 [Ar]3d64s2
《物质结构与性质》
4.价层电子排布式
为突出化合价与电子排布的关系,将在化学反应中可能发生电子变动的能级称为价电子层(简称价层)。
如:Ni的简化电子排布式为_______,价层电子排布为 _______。
练习4:试写出下列原子的价层电子排布:
①13Al:_______;②32Ge:_______;③34Se:_______。
[Ar]3d84s2
3d84s2
3s23p1
4s24p2
4s24p4
《物质结构与性质》
《物质结构与性质》
先写原子的电子排布式,然后再考虑得失得失电子的情况。
如O2-的电子排布式,先写O原子的电子排布式为1s22s22p4,再得2个电子知O2-的电子排布式为1s22s22p6。
5、简单离子电子排布式:
《物质结构与性质》
课堂小结:原子核外电子排布的表示方法
电子排布式
简化电子排布式
价电子排布式
轨道表示式
课堂巩固:
1.下列各原子或离子的电子排布式错误的是
A.Mg2+ 1s22s22p6
B.Br 1s22s22p63s23p63d104s24p5
C.O2- 1s22s22p6
D.Cr 1s22s22p63s23p63d44s2
√
《物质结构与性质》
2.某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法不正确的是
A.该元素原子中共有25个电子
B.该元素原子核外有4个能层
C.该元素原子最外层共有2个电子
D.该元素原子M能层共有8个电子
√
《物质结构与性质》
