第四单元 课题3 水的组成(含解析)—2022-2023学年九年级化学上册最新命题导向假期培优
文档属性
| 名称 | 第四单元 课题3 水的组成(含解析)—2022-2023学年九年级化学上册最新命题导向假期培优 |
|
|
| 格式 | zip | ||
| 文件大小 | 195.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-25 00:00:00 | ||
图片预览


文档简介
第四单元 自然界的水
课题3 水的组成
一、单选题
1.下列各组物质,按混合物、化合物、单质的顺序排列的是 ( )
A.冰水共存物、干冰、氮气 B.石油、天然气、煤
C.洁净的空气、氯化钠、液态氧 D.石灰水、水银、铜
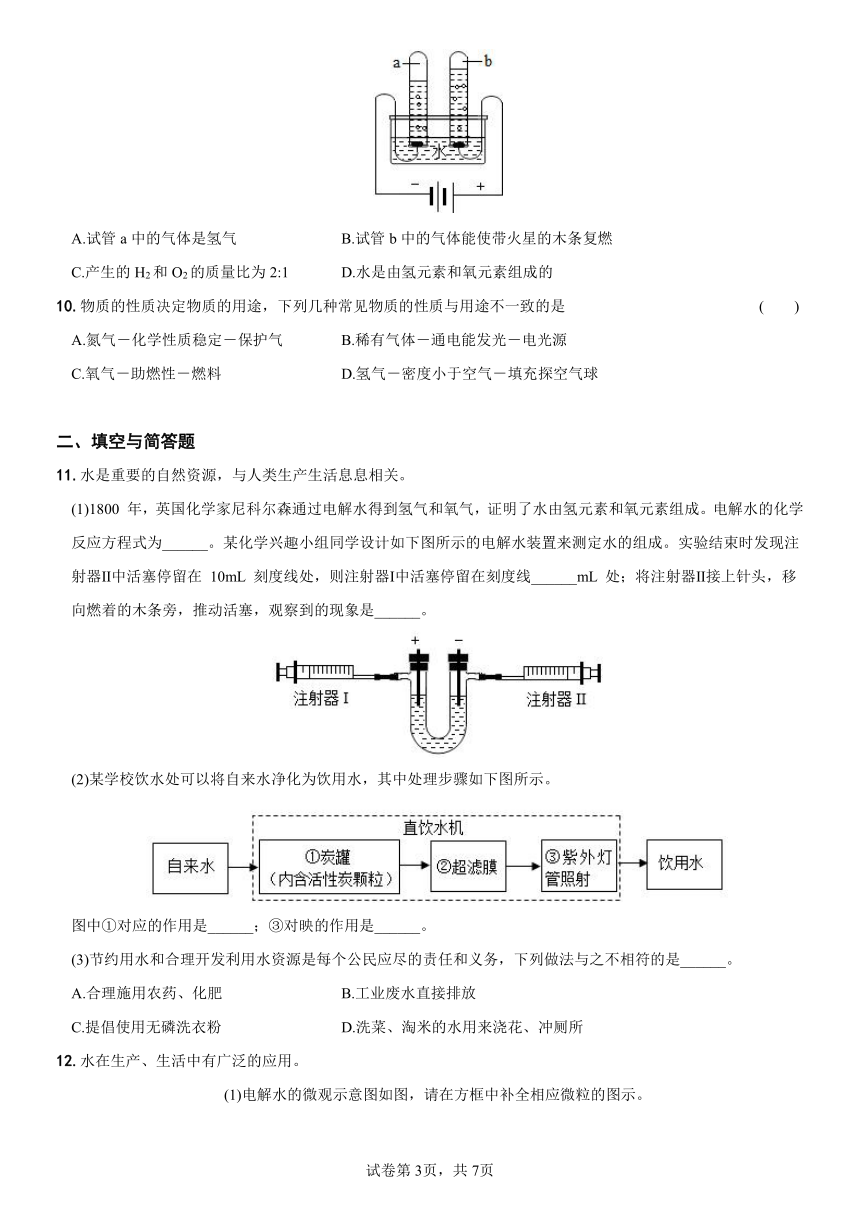
2.电解水实验如图所示。下列说法正确的是 ( )
A.a玻璃管上方产生的气体是氢气
B.产生氢气和氧气的体积比为1:2
C.可用燃着的木条检验产生的气体
D.该实验说明水是由氢气和氧气组成的
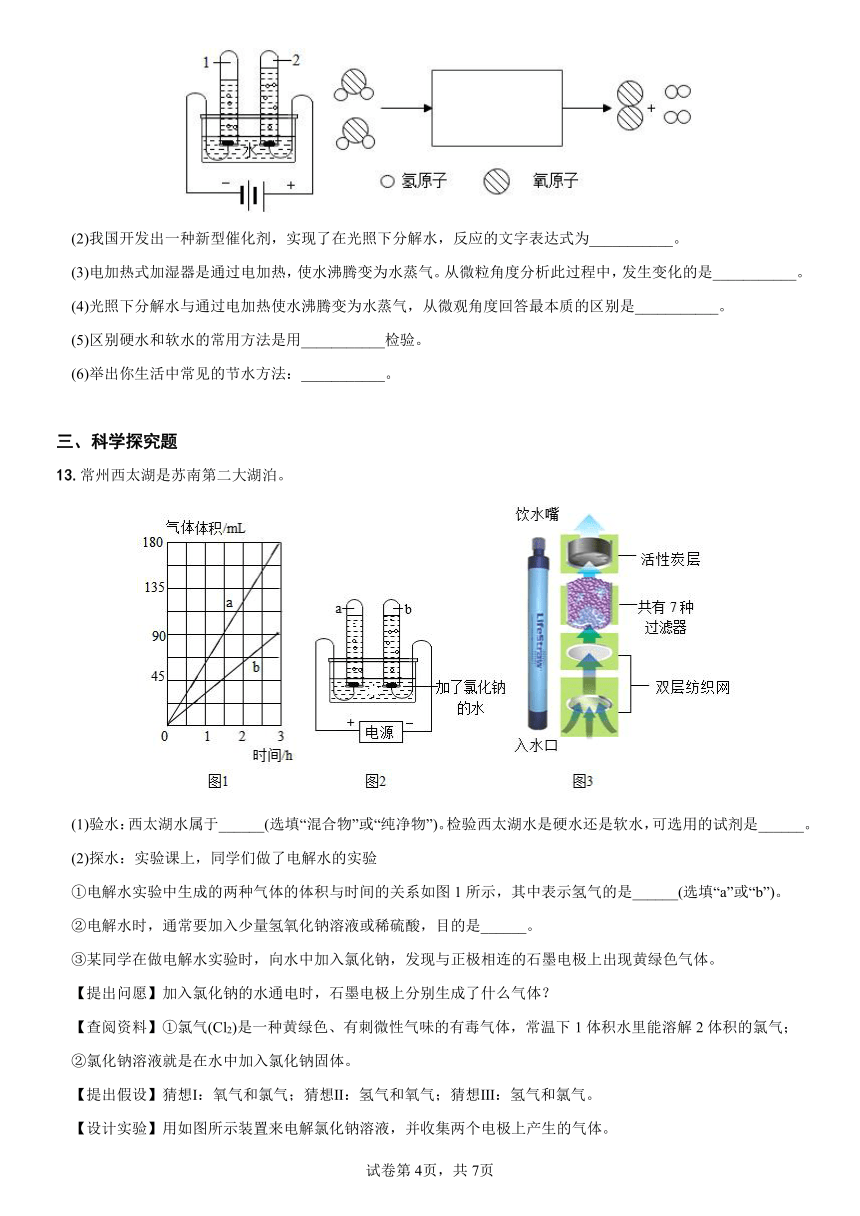
3.某同学用如图所示的装置进行电解水实验,并作了以下描述: ( )
①向水中加入少量硫酸钠,可加快气体产生的速率;
②甲、乙两试管内收集到气体的体积比约为2:1;
③该实验证明水是由氢气和氧气组成的;
④乙试管内产生的气体能使带火星的木条复燃。 以上描述正确的是
A.①②③④ B.①②④ C.①②③ D.①③④
4.下列符号表达式书写和基本反应类型均正确的是 ( )
A.氢气在氧气中燃烧: 氧化反应
B.冬季燃煤中含硫产生有刺激性气味的气体: 化合反应
C.工业制取氧气: 分解反应
D.定量的方法测定空气中氧气的含量: 分解反应
5.如图为氢气还原氧化铜的实验装置,下列有关说法错误的是 ( )
A.药品需平铺在试管底部,使反应更加充分
B.试管口需略向下倾斜,防止冷凝水倒流引起试管破裂
C.试管内药品加热前需先通氢气排尽试管内空气
D.反应结束后,先停止通氢气、再撤去并熄灭酒精灯
6.下列有关氢气性质、用途的描述,错误的是 ( )
A.通常条件下,氢气是无色、无味的气体
B.氢气难溶于水、密度比空气小
C.氢气在空气中燃烧,产生黄色火焰
D.氢气燃烧后的产物是水,不污染空气,是最理想的清洁能源
7.实验室用锌和稀硫酸制取氢气反应的化学方程式是Zn+H2SO4=ZnSO4+H2↑可用排水法收集氢气,也可用向下排空气法收集氢气,这是因为氢气 ( )
A.难溶于水,比空气轻 B.难溶于水,比空气重
C.微溶于水,比空气轻 D.易溶于水,比空气重
8.下列属于氧化物的是 ( )
A.O2 B.H2O C.Cu(OH)2 D.H2CO3
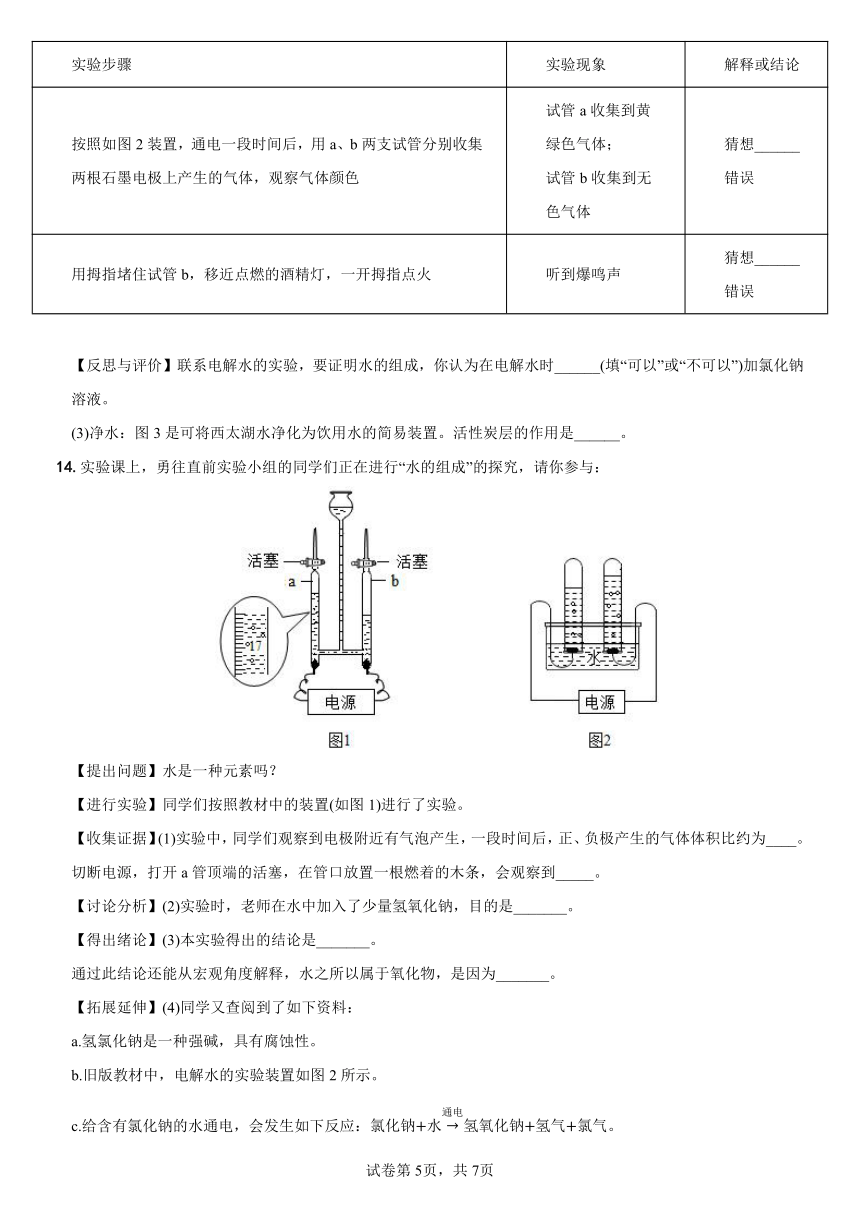
9.如图,关于电解水实验的现象和结论叙述错误的是 ( )
A.试管a中的气体是氢气 B.试管b中的气体能使带火星的木条复燃
C.产生的H2和O2的质量比为2:1 D.水是由氢元素和氧元素组成的
10.物质的性质决定物质的用途,下列几种常见物质的性质与用途不一致的是 ( )
A.氮气-化学性质稳定-保护气 B.稀有气体-通电能发光-电光源
C.氧气-助燃性-燃料 D.氢气-密度小于空气-填充探空气球
二、填空与简答题
11.水是重要的自然资源,与人类生产生活息息相关。
(1)1800 年,英国化学家尼科尔森通过电解水得到氢气和氧气,证明了水由氢元素和氧元素组成。电解水的化学反应方程式为______。某化学兴趣小组同学设计如下图所示的电解水装置来测定水的组成。实验结束时发现注射器Ⅱ中活塞停留在 10mL 刻度线处,则注射器Ⅰ中活塞停留在刻度线______mL 处;将注射器Ⅱ接上针头,移向燃着的木条旁,推动活塞,观察到的现象是______。
(2)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如下图所示。
图中①对应的作用是______;③对映的作用是______。
(3)节约用水和合理开发利用水资源是每个公民应尽的责任和义务,下列做法与之不相符的是______。
A.合理施用农药、化肥 B.工业废水直接排放
C.提倡使用无磷洗衣粉 D.洗菜、淘米的水用来浇花、冲厕所
12.水在生产、生活中有广泛的应用。
(1)电解水的微观示意图如图,请在方框中补全相应微粒的图示。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的文字表达式为___________。
(3)电加热式加湿器是通过电加热,使水沸腾变为水蒸气。从微粒角度分析此过程中,发生变化的是___________。
(4)光照下分解水与通过电加热使水沸腾变为水蒸气,从微观角度回答最本质的区别是___________。
(5)区别硬水和软水的常用方法是用___________检验。
(6)举出你生活中常见的节水方法:___________。
三、科学探究题
13.常州西太湖是苏南第二大湖泊。
(1)验水:西太湖水属于______(选填“混合物”或“纯净物”)。检验西太湖水是硬水还是软水,可选用的试剂是______。
(2)探水:实验课上,同学们做了电解水的实验
①电解水实验中生成的两种气体的体积与时间的关系如图1所示,其中表示氢气的是______(选填“a”或“b”)。
②电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是______。
③某同学在做电解水实验时,向水中加入氯化钠,发现与正极相连的石墨电极上出现黄绿色气体。
【提出问愿】加入氯化钠的水通电时,石墨电极上分别生成了什么气体?
【查阅资料】①氯气(Cl2)是一种黄绿色、有刺微性气味的有毒气体,常温下1体积水里能溶解2体积的氯气;②氯化钠溶液就是在水中加入氯化钠固体。
【提出假设】猜想Ⅰ:氧气和氯气;猜想Ⅱ:氢气和氧气;猜想Ⅲ:氢气和氯气。
【设计实验】用如图所示装置来电解氯化钠溶液,并收集两个电极上产生的气体。
实验步骤 实验现象 解释或结论
按照如图2装置,通电一段时间后,用a、b两支试管分别收集两根石墨电极上产生的气体,观察气体颜色 试管a收集到黄绿色气体; 试管b收集到无色气体 猜想______错误
用拇指堵住试管b,移近点燃的酒精灯,一开拇指点火 听到爆鸣声 猜想______错误
【反思与评价】联系电解水的实验,要证明水的组成,你认为在电解水时______(填“可以”或“不可以”)加氯化钠溶液。
(3)净水:图3是可将西太湖水净化为饮用水的简易装置。活性炭层的作用是______。
14.实验课上,勇往直前实验小组的同学们正在进行“水的组成”的探究,请你参与:
【提出问题】水是一种元素吗?
【进行实验】同学们按照教材中的装置(如图1)进行了实验。
【收集证据】(1)实验中,同学们观察到电极附近有气泡产生,一段时间后,正、负极产生的气体体积比约为____。切断电源,打开a管顶端的活塞,在管口放置一根燃着的木条,会观察到_____。
【讨论分析】(2)实验时,老师在水中加入了少量氢氧化钠,目的是_______。
【得出绪论】(3)本实验得出的结论是_______。
通过此结论还能从宏观角度解释,水之所以属于氧化物,是因为_______。
【拓展延伸】(4)同学又查阅到了如下资料:
a.氢氯化钠是一种强碱,具有腐蚀性。
b.旧版教材中,电解水的实验装置如图2所示。
c.给含有氯化钠的水通电,会发生如下反应:。
请你分析思考,和图2的装置相比,现行教材(图1)装置的优点是_______。(任意写一点)。进行实验时,_______(填“能”或“不能”)将氢氧化钠换为氯化钠。
15.水是生命之源,是“永远值得探究的物质”,人类从未停止过对水的研究。
【提出问题】水是由什么组成的?
【查阅资料】通过点燃氢气和电解水的实验方法均可证明水的组成。
【经典回顾】
(1)1783年,拉瓦锡利用如图1所示装置探究水的组成。
往A杯中滴加少量的水,水通过灼热的铁管时发生汽化,水蒸气与灼热的铁反应,生成一种黑色固体四氧化三铁和“可燃空气”,将气体通过放在冷水中的铜管,在B装置中收集到纯净的“可燃空气”。最终拉瓦锡证明了水的组成。
①将气体通过放在冷水中的铜管,目的是除去__________。
②将B装置收集到的“可燃空气”在氧气中点燃,生成了水。“可燃空气”是一种气体单质,其名称为氢气。写出水蒸气与灼热的铁反应的文字表达式___________。
(2)1800年,英国化学家尼科尔森通过电解水得到氢气和氧气,后人不断研究和改进该实验。现有某兴趣小组的同学设计了如图2所示实验来探究水的组成。
【实验步骤】
①先用大注射器抽取一定量的硫酸钠溶液,从A中的圆孔注入;
②用两个橡胶帽塞住右边两个出气口,用带针头的小注射器分别在出气口1和2处抽气,液面上升,直至水充满正负两极;
③接通电源,待C中气体体积达到最大刻度时,关闭电源,仔细观察实验装置中的现象;
④分别用带针头的注射器抽取气体并检验。
【交流与反思】
Ⅰ步骤①,在水中加入硫酸钠溶液的作用是__________________。
II步骤②的目的是__________________。
III步骤③中的现象:两极上均有气泡出现,B、C两电极上产生的气体体积比约为_________,并且A中液面_________(填“上升”或“下降”)。
IV步骤④中检验C中气体的方法是__________________。
【总结交流】
以上实验都可以得出结论:水是由氢元素和氧元素组成的。
试卷第2页,共7页
试卷第1页,共7页
【参考答案及解析】
1.C
【详解】A、冰水共存物属于化合物,干冰属于化合物,氮气是单质,故选项错误;
B、石油、天然气、煤都属于混合物,故选项错误;
C、洁净的空气属于混合物,氯化钠属于化合物,液态氧属于单质,故选项正确;
D、石灰水属于混合物,水银属于单质,铜属于单质,故选项错误。
故选C。
2.C
【详解】A、根据“正氧负氢,氢二氧一”,可知与正极连接产生的是氧气,所以a玻璃管上方产生的气体是氧气,错误;
B、产生氢气和氧气的体积比应该为2:1,错误;
C、产生的氧气具有助燃性,可以使燃着的木条烧得更旺;氢气具有可燃性,被燃着的木条点燃会发出淡蓝色火焰,可用燃着的木条检验产生的气体,正确;
D、水是由氢、氧两种元素组成的纯净物,错误。
故选C。
3.B
【详解】①向水中加入少量硫酸钠,硫酸钠在水中可以解离出钠离子、硫酸根离子,可增强水的导电性,描述正确;
②甲试管与电源负极相连,收集到的是氢气,乙试管与电源的正极相连,收集到的是氧气,收集到的氢气和氧气的体积比约为2:1,描述正确;
③电解水生成氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,化学反应前后,元素的种类不变,该实验证明水是由氢元素和氧元素组成的,描述错误;
④乙试管产生的气体是氧气,氧气具有助燃性,能使带火星的木条复燃,描述正确。
故选B。
4.B
【详解】A、氢气燃烧生成水,该反应的符号表达式正确,但氧化反应不属于基本反应类型,该选项不正确;
B、硫燃烧生成二氧化硫,该反应的符号表达式正确,且该反应为多种物质生成一种物质的反应,属于化合反应,该选项正确;
C、工业利用分离液态空气的方法制取氧气,该选项不正确;
D、碳燃烧生成二氧化碳气体,则不能用碳燃烧测定空气中氧气的含量,该选项不符合题意。
故选B。
5.D
【详解】A、药品需平铺在试管底部,能增大反应物之间的接触面积,使反应更加充分,此选项正确;
B、试管口需略向下倾斜,可防止冷凝水倒流引起试管破裂,此选项正确;
C、试管内药品加热前需先通氢气排尽试管内空气,以防氢气不纯,加热时发生爆炸,此选项正确;
D、反应结束后,需先撤去酒精灯,停止加热,等装置冷却至室温,再停止通入氢气,以防止生成的铜被氧化为氧化铜,此选项错误。
故选D。
6.C
【详解】A、通常情况下,氢气是无色、无味的气体,不符合题意;
B、氢气难溶于水,密度比空气小,不符合题意;
C、氢气在空气中燃烧,发出淡蓝色火焰,符合题意;
D、氢气燃烧产物只有水,比较环保,且燃烧值大,是比较理想的清洁燃料,不符合题意。
故选C。
7.A
【详解】可用排水法收集氢气,是因为氢气难溶于水;用向下排空气法收集氢气,是因为氢气的密度小于空气,故选A。
8.B
【分析】氧化物是由两种元素组成,其中一种是氧元素的纯净物
【详解】A、O2是由一种元素组成的纯净物,属于单质,故选项错误;
B、H2O是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故选项正确;
C、Cu(OH)2是由铜、氧、氢三种元素组成的化合物,不属于氧化物,故选项错误;
D、H2CO3是由氢、碳、氧三种元素组成的化合物,不属于氧化物,故选项错误。
故选B。
9.C
【分析】电解水时,正极产生的是氧气,氧气能使带火星的木条复燃,负极产生的是氢气,氢气燃烧生成水,氧气和氢气的体积比约为1:2,质量比是8:1。
【详解】A、由实验操作图,a端试管内气体体积大于另一端试管内的气体,说明a端试管内产生的为氢气,故A正确;
B、试管b中的气体产生的体积较少,是氧气,氧气具有助燃性,能使带火星的木条复燃,故B正确;
C、水通电分解时,产生氢气的体积与氧气的体积比为2:1,故C错误;
D、水在电解的条件下生成氢气和氧气,说明水是由氢元素和氧元素组成的,故D正确。
故选C。
10.C
【详解】A、氮气的化学性质稳定,可用作保护气,故A性质与用途一致,不符合题意;
B、稀有气体通电能发出不同颜色的光,可用作电光源,故B性质与用途一致,不符合题意;
C、 氧气具有助燃性,可用作助燃剂,但是氧气不具有可燃性,不可作燃料,故C性质与用途不一致,符合题意;
D、氦气密度小于空气,可用于填充探空气球,故D性质与用途一致,不符合题意;
故选C。
11.(1) 5 气体燃烧,产生淡蓝色火焰
(2) 吸附作用 杀菌消毒
(3)B
【详解】(1)水通电生成氢气和氧气,该反应方程式为;电解水实验中,根据正氧负氢,氧一氢二,注射器Ⅱ与电源的负极相连产生的是氢气,注射器Ⅰ与电源的正极相连,产生的是氧气,产生的氢气与氧气的体积比为2:1,故实验结束时发现注射器Ⅱ中活塞停留在 10mL 刻度线处,则注射器Ⅰ中活塞停留在刻度线5mL 处;由于注射器Ⅱ中的气体是氢气,具有可燃性,将注射器Ⅱ接上针头,移向燃着的木条旁,推动活塞,观察到的现象是气体能燃烧,产生淡蓝色的火焰;
(2)活性炭具有吸附性,能吸附水中色素及有异味的杂质,因此在自来水的净化中活性炭的作用为吸附作用;紫外线有消毒杀菌的作用;
(3)A、合理施用农药、化肥,可以防止水污染,故A选项正确;
B、工业废水直接排放会污染水资源,故B选项错误;
C、提倡使用无磷洗衣粉可以防止水污染,故C选项正确;
D、洗菜、淘米的水用来浇花、冲厕所可以节约用水,故D选项正确;
故选B。
12.(1)
(2)水氢气+氧气
(3)水分子间的间隔变大了
(4)分子种类是否改变
(5)肥皂水
(6)随手关闭水龙头(或用淘米水浇花或用洗衣水拖地等,合理即可)
【详解】(1)电解水过程中,水分子分解为氢原子和氧原子,氢原子和氧原子分别结合为氢分子和氧分子,最小的微粒是氢、氧原子;方框中补全相应微粒的图示为:;
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的文字表达式为:水氢气+氧气;
(3)通过电加热,使水沸腾变为水蒸气,从微粒角度分析此过程中,发生变化的是:水分子间的间隔变大了;
(4)光照下分解水生成氢气和氧气,分子的种类发生改变,通过电加热,使水沸腾变为水蒸气,分子的种类没有改变,水分子间的间隔变大了,最本质的区别是分子种类是否改变;
(5)区分硬水和软水最常用的方法为加肥皂水,泡沫多,浮渣少的为软水,泡沫少,浮渣多的为硬水;
(6)生活中常见的节水方法有随手关闭水龙头、用淘米水浇花、用洗衣水拖地等。
13.(1) 混合物 肥皂水
(2) b 增强水的导电性 Ⅱ Ⅰ 不可以
(3)吸附水中的异味和色素
【详解】(1)湖水中含有水和一些钙镁化合物,属于混合物;将肥皂水加入西太湖水中,若产生较少的泡沫,为硬水;若产生较多的泡沫,为软水;
(2)①电解水实验中,“正氧负氢”,负极产生的是氢气,故b管是氢气;
②纯水不导电,电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是为了增强水的导电性;
③设计实验:观察到试管a收集到黄绿色气体;试管b收集到无色气体,说明产生了氯气,则猜想Ⅱ是错误的;
用拇指堵住试管b,移近点燃的酒精灯,一开拇指点火,听到爆鸣声,说明b管产生的是氢气,故猜想Ⅰ是错误的;
反思与评价:联系电解水的实验,要证明水的组成,在电解水时不可以加氯化钠溶液;
(3)活性炭具有吸附性,能吸附水中的色素和异味。
14. 1:2 木条燃烧更旺 增强导电性 水是由氢、氧两种元素组成的##水由氢元素和氧元素组成 水是由两种元素组成的纯净物,且其中一种是氧元素 管上有刻度更准确##更便于检验生成的气体##防止从水槽中取出试管时碱性液体腐蚀手 不能
【详解】(1)水通电分解生成氢气和氧气,所以观察到电极附近有气泡产生,一段时间后,正、负极产生的气体体积比约为1:2.切断电源,打开a管顶端的活塞,由于a管产生的是氧气,在管口放置一根燃着的木条,会观察到火焰燃烧更旺;
(2)水通电分解加入了少量氢氧化钠,目的是增强导电性;
(3)水通电分解生成氢气和氧气,所以本实验得出的结论是水是由氢、氧元素组成的化合物。通过此结论还能从宏观角度解释,水之所以属于氧化物,是因为水是由两种元素组成的纯净物,且其中一种是氧元素;
(4)和图2的装置相比,现行教材(图1)装置的优点是管上有刻度,更准确;更便于检验生成的气体;防止从水槽中取出试管时碱性液体腐蚀手,电解氯化钠溶液生成氢气和氯气,所以不能用氯化钠代替氢氧化钠;
【点睛】本题主要考查水电解实验,掌握相关物质性质进行解题。
15. 水蒸气 铁+水 四氧化三铁+氢气 增强导电性 排尽空气,以防止检验时发生爆炸 1:2 上升 用燃着的木条放于出气口,若气体被点燃,产生淡蓝色火焰,则该气体是氢气
【详解】经典回顾:
(1)
①水蒸气遇冷凝结成水滴,将气体通过放在冷水中的铜管,目的是除去水蒸气;
②水蒸气与灼热的铁反应,生成一种黑色固体四氧化三铁和“可燃空气”,“可燃空气“是一种气体单质,其名称为氢气,铁与水蒸气在高温下反应生成四氧化三铁和氢气,反应的文字表达式为:铁+水 四氧化三铁+氢气;
交流与反思:
Ⅰ硫酸钠溶于水离解成可自由的钠离子和硫酸根离子。步骤①在水中加入硫酸钠溶液的作用是增强导电性;
II步骤②的目的是排尽空气,以防止检验时发生爆炸;
III电解水时,负极产生氢气,正极产生氧气,体积比约为2:1。步骤③中的现象:两极上均有气泡出现,B与正极相连,C与负极相连,两电极上产生的气体体积比约为1:2 ,两管生成气体,管内压强增大,A中液面上升;
IV C与负极相连,C管中的气体是氢气,氢气具有可燃性,能在空气中燃烧。步骤④中检验C中气体的方法是用燃着的木条放于出气口,若气体被点燃,产生淡蓝色火焰,则该气体是氢气。
课题3 水的组成
一、单选题
1.下列各组物质,按混合物、化合物、单质的顺序排列的是 ( )
A.冰水共存物、干冰、氮气 B.石油、天然气、煤
C.洁净的空气、氯化钠、液态氧 D.石灰水、水银、铜
2.电解水实验如图所示。下列说法正确的是 ( )
A.a玻璃管上方产生的气体是氢气
B.产生氢气和氧气的体积比为1:2
C.可用燃着的木条检验产生的气体
D.该实验说明水是由氢气和氧气组成的
3.某同学用如图所示的装置进行电解水实验,并作了以下描述: ( )
①向水中加入少量硫酸钠,可加快气体产生的速率;
②甲、乙两试管内收集到气体的体积比约为2:1;
③该实验证明水是由氢气和氧气组成的;
④乙试管内产生的气体能使带火星的木条复燃。 以上描述正确的是
A.①②③④ B.①②④ C.①②③ D.①③④
4.下列符号表达式书写和基本反应类型均正确的是 ( )
A.氢气在氧气中燃烧: 氧化反应
B.冬季燃煤中含硫产生有刺激性气味的气体: 化合反应
C.工业制取氧气: 分解反应
D.定量的方法测定空气中氧气的含量: 分解反应
5.如图为氢气还原氧化铜的实验装置,下列有关说法错误的是 ( )
A.药品需平铺在试管底部,使反应更加充分
B.试管口需略向下倾斜,防止冷凝水倒流引起试管破裂
C.试管内药品加热前需先通氢气排尽试管内空气
D.反应结束后,先停止通氢气、再撤去并熄灭酒精灯
6.下列有关氢气性质、用途的描述,错误的是 ( )
A.通常条件下,氢气是无色、无味的气体
B.氢气难溶于水、密度比空气小
C.氢气在空气中燃烧,产生黄色火焰
D.氢气燃烧后的产物是水,不污染空气,是最理想的清洁能源
7.实验室用锌和稀硫酸制取氢气反应的化学方程式是Zn+H2SO4=ZnSO4+H2↑可用排水法收集氢气,也可用向下排空气法收集氢气,这是因为氢气 ( )
A.难溶于水,比空气轻 B.难溶于水,比空气重
C.微溶于水,比空气轻 D.易溶于水,比空气重
8.下列属于氧化物的是 ( )
A.O2 B.H2O C.Cu(OH)2 D.H2CO3
9.如图,关于电解水实验的现象和结论叙述错误的是 ( )
A.试管a中的气体是氢气 B.试管b中的气体能使带火星的木条复燃
C.产生的H2和O2的质量比为2:1 D.水是由氢元素和氧元素组成的
10.物质的性质决定物质的用途,下列几种常见物质的性质与用途不一致的是 ( )
A.氮气-化学性质稳定-保护气 B.稀有气体-通电能发光-电光源
C.氧气-助燃性-燃料 D.氢气-密度小于空气-填充探空气球
二、填空与简答题
11.水是重要的自然资源,与人类生产生活息息相关。
(1)1800 年,英国化学家尼科尔森通过电解水得到氢气和氧气,证明了水由氢元素和氧元素组成。电解水的化学反应方程式为______。某化学兴趣小组同学设计如下图所示的电解水装置来测定水的组成。实验结束时发现注射器Ⅱ中活塞停留在 10mL 刻度线处,则注射器Ⅰ中活塞停留在刻度线______mL 处;将注射器Ⅱ接上针头,移向燃着的木条旁,推动活塞,观察到的现象是______。
(2)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如下图所示。
图中①对应的作用是______;③对映的作用是______。
(3)节约用水和合理开发利用水资源是每个公民应尽的责任和义务,下列做法与之不相符的是______。
A.合理施用农药、化肥 B.工业废水直接排放
C.提倡使用无磷洗衣粉 D.洗菜、淘米的水用来浇花、冲厕所
12.水在生产、生活中有广泛的应用。
(1)电解水的微观示意图如图,请在方框中补全相应微粒的图示。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的文字表达式为___________。
(3)电加热式加湿器是通过电加热,使水沸腾变为水蒸气。从微粒角度分析此过程中,发生变化的是___________。
(4)光照下分解水与通过电加热使水沸腾变为水蒸气,从微观角度回答最本质的区别是___________。
(5)区别硬水和软水的常用方法是用___________检验。
(6)举出你生活中常见的节水方法:___________。
三、科学探究题
13.常州西太湖是苏南第二大湖泊。
(1)验水:西太湖水属于______(选填“混合物”或“纯净物”)。检验西太湖水是硬水还是软水,可选用的试剂是______。
(2)探水:实验课上,同学们做了电解水的实验
①电解水实验中生成的两种气体的体积与时间的关系如图1所示,其中表示氢气的是______(选填“a”或“b”)。
②电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是______。
③某同学在做电解水实验时,向水中加入氯化钠,发现与正极相连的石墨电极上出现黄绿色气体。
【提出问愿】加入氯化钠的水通电时,石墨电极上分别生成了什么气体?
【查阅资料】①氯气(Cl2)是一种黄绿色、有刺微性气味的有毒气体,常温下1体积水里能溶解2体积的氯气;②氯化钠溶液就是在水中加入氯化钠固体。
【提出假设】猜想Ⅰ:氧气和氯气;猜想Ⅱ:氢气和氧气;猜想Ⅲ:氢气和氯气。
【设计实验】用如图所示装置来电解氯化钠溶液,并收集两个电极上产生的气体。
实验步骤 实验现象 解释或结论
按照如图2装置,通电一段时间后,用a、b两支试管分别收集两根石墨电极上产生的气体,观察气体颜色 试管a收集到黄绿色气体; 试管b收集到无色气体 猜想______错误
用拇指堵住试管b,移近点燃的酒精灯,一开拇指点火 听到爆鸣声 猜想______错误
【反思与评价】联系电解水的实验,要证明水的组成,你认为在电解水时______(填“可以”或“不可以”)加氯化钠溶液。
(3)净水:图3是可将西太湖水净化为饮用水的简易装置。活性炭层的作用是______。
14.实验课上,勇往直前实验小组的同学们正在进行“水的组成”的探究,请你参与:
【提出问题】水是一种元素吗?
【进行实验】同学们按照教材中的装置(如图1)进行了实验。
【收集证据】(1)实验中,同学们观察到电极附近有气泡产生,一段时间后,正、负极产生的气体体积比约为____。切断电源,打开a管顶端的活塞,在管口放置一根燃着的木条,会观察到_____。
【讨论分析】(2)实验时,老师在水中加入了少量氢氧化钠,目的是_______。
【得出绪论】(3)本实验得出的结论是_______。
通过此结论还能从宏观角度解释,水之所以属于氧化物,是因为_______。
【拓展延伸】(4)同学又查阅到了如下资料:
a.氢氯化钠是一种强碱,具有腐蚀性。
b.旧版教材中,电解水的实验装置如图2所示。
c.给含有氯化钠的水通电,会发生如下反应:。
请你分析思考,和图2的装置相比,现行教材(图1)装置的优点是_______。(任意写一点)。进行实验时,_______(填“能”或“不能”)将氢氧化钠换为氯化钠。
15.水是生命之源,是“永远值得探究的物质”,人类从未停止过对水的研究。
【提出问题】水是由什么组成的?
【查阅资料】通过点燃氢气和电解水的实验方法均可证明水的组成。
【经典回顾】
(1)1783年,拉瓦锡利用如图1所示装置探究水的组成。
往A杯中滴加少量的水,水通过灼热的铁管时发生汽化,水蒸气与灼热的铁反应,生成一种黑色固体四氧化三铁和“可燃空气”,将气体通过放在冷水中的铜管,在B装置中收集到纯净的“可燃空气”。最终拉瓦锡证明了水的组成。
①将气体通过放在冷水中的铜管,目的是除去__________。
②将B装置收集到的“可燃空气”在氧气中点燃,生成了水。“可燃空气”是一种气体单质,其名称为氢气。写出水蒸气与灼热的铁反应的文字表达式___________。
(2)1800年,英国化学家尼科尔森通过电解水得到氢气和氧气,后人不断研究和改进该实验。现有某兴趣小组的同学设计了如图2所示实验来探究水的组成。
【实验步骤】
①先用大注射器抽取一定量的硫酸钠溶液,从A中的圆孔注入;
②用两个橡胶帽塞住右边两个出气口,用带针头的小注射器分别在出气口1和2处抽气,液面上升,直至水充满正负两极;
③接通电源,待C中气体体积达到最大刻度时,关闭电源,仔细观察实验装置中的现象;
④分别用带针头的注射器抽取气体并检验。
【交流与反思】
Ⅰ步骤①,在水中加入硫酸钠溶液的作用是__________________。
II步骤②的目的是__________________。
III步骤③中的现象:两极上均有气泡出现,B、C两电极上产生的气体体积比约为_________,并且A中液面_________(填“上升”或“下降”)。
IV步骤④中检验C中气体的方法是__________________。
【总结交流】
以上实验都可以得出结论:水是由氢元素和氧元素组成的。
试卷第2页,共7页
试卷第1页,共7页
【参考答案及解析】
1.C
【详解】A、冰水共存物属于化合物,干冰属于化合物,氮气是单质,故选项错误;
B、石油、天然气、煤都属于混合物,故选项错误;
C、洁净的空气属于混合物,氯化钠属于化合物,液态氧属于单质,故选项正确;
D、石灰水属于混合物,水银属于单质,铜属于单质,故选项错误。
故选C。
2.C
【详解】A、根据“正氧负氢,氢二氧一”,可知与正极连接产生的是氧气,所以a玻璃管上方产生的气体是氧气,错误;
B、产生氢气和氧气的体积比应该为2:1,错误;
C、产生的氧气具有助燃性,可以使燃着的木条烧得更旺;氢气具有可燃性,被燃着的木条点燃会发出淡蓝色火焰,可用燃着的木条检验产生的气体,正确;
D、水是由氢、氧两种元素组成的纯净物,错误。
故选C。
3.B
【详解】①向水中加入少量硫酸钠,硫酸钠在水中可以解离出钠离子、硫酸根离子,可增强水的导电性,描述正确;
②甲试管与电源负极相连,收集到的是氢气,乙试管与电源的正极相连,收集到的是氧气,收集到的氢气和氧气的体积比约为2:1,描述正确;
③电解水生成氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,化学反应前后,元素的种类不变,该实验证明水是由氢元素和氧元素组成的,描述错误;
④乙试管产生的气体是氧气,氧气具有助燃性,能使带火星的木条复燃,描述正确。
故选B。
4.B
【详解】A、氢气燃烧生成水,该反应的符号表达式正确,但氧化反应不属于基本反应类型,该选项不正确;
B、硫燃烧生成二氧化硫,该反应的符号表达式正确,且该反应为多种物质生成一种物质的反应,属于化合反应,该选项正确;
C、工业利用分离液态空气的方法制取氧气,该选项不正确;
D、碳燃烧生成二氧化碳气体,则不能用碳燃烧测定空气中氧气的含量,该选项不符合题意。
故选B。
5.D
【详解】A、药品需平铺在试管底部,能增大反应物之间的接触面积,使反应更加充分,此选项正确;
B、试管口需略向下倾斜,可防止冷凝水倒流引起试管破裂,此选项正确;
C、试管内药品加热前需先通氢气排尽试管内空气,以防氢气不纯,加热时发生爆炸,此选项正确;
D、反应结束后,需先撤去酒精灯,停止加热,等装置冷却至室温,再停止通入氢气,以防止生成的铜被氧化为氧化铜,此选项错误。
故选D。
6.C
【详解】A、通常情况下,氢气是无色、无味的气体,不符合题意;
B、氢气难溶于水,密度比空气小,不符合题意;
C、氢气在空气中燃烧,发出淡蓝色火焰,符合题意;
D、氢气燃烧产物只有水,比较环保,且燃烧值大,是比较理想的清洁燃料,不符合题意。
故选C。
7.A
【详解】可用排水法收集氢气,是因为氢气难溶于水;用向下排空气法收集氢气,是因为氢气的密度小于空气,故选A。
8.B
【分析】氧化物是由两种元素组成,其中一种是氧元素的纯净物
【详解】A、O2是由一种元素组成的纯净物,属于单质,故选项错误;
B、H2O是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故选项正确;
C、Cu(OH)2是由铜、氧、氢三种元素组成的化合物,不属于氧化物,故选项错误;
D、H2CO3是由氢、碳、氧三种元素组成的化合物,不属于氧化物,故选项错误。
故选B。
9.C
【分析】电解水时,正极产生的是氧气,氧气能使带火星的木条复燃,负极产生的是氢气,氢气燃烧生成水,氧气和氢气的体积比约为1:2,质量比是8:1。
【详解】A、由实验操作图,a端试管内气体体积大于另一端试管内的气体,说明a端试管内产生的为氢气,故A正确;
B、试管b中的气体产生的体积较少,是氧气,氧气具有助燃性,能使带火星的木条复燃,故B正确;
C、水通电分解时,产生氢气的体积与氧气的体积比为2:1,故C错误;
D、水在电解的条件下生成氢气和氧气,说明水是由氢元素和氧元素组成的,故D正确。
故选C。
10.C
【详解】A、氮气的化学性质稳定,可用作保护气,故A性质与用途一致,不符合题意;
B、稀有气体通电能发出不同颜色的光,可用作电光源,故B性质与用途一致,不符合题意;
C、 氧气具有助燃性,可用作助燃剂,但是氧气不具有可燃性,不可作燃料,故C性质与用途不一致,符合题意;
D、氦气密度小于空气,可用于填充探空气球,故D性质与用途一致,不符合题意;
故选C。
11.(1) 5 气体燃烧,产生淡蓝色火焰
(2) 吸附作用 杀菌消毒
(3)B
【详解】(1)水通电生成氢气和氧气,该反应方程式为;电解水实验中,根据正氧负氢,氧一氢二,注射器Ⅱ与电源的负极相连产生的是氢气,注射器Ⅰ与电源的正极相连,产生的是氧气,产生的氢气与氧气的体积比为2:1,故实验结束时发现注射器Ⅱ中活塞停留在 10mL 刻度线处,则注射器Ⅰ中活塞停留在刻度线5mL 处;由于注射器Ⅱ中的气体是氢气,具有可燃性,将注射器Ⅱ接上针头,移向燃着的木条旁,推动活塞,观察到的现象是气体能燃烧,产生淡蓝色的火焰;
(2)活性炭具有吸附性,能吸附水中色素及有异味的杂质,因此在自来水的净化中活性炭的作用为吸附作用;紫外线有消毒杀菌的作用;
(3)A、合理施用农药、化肥,可以防止水污染,故A选项正确;
B、工业废水直接排放会污染水资源,故B选项错误;
C、提倡使用无磷洗衣粉可以防止水污染,故C选项正确;
D、洗菜、淘米的水用来浇花、冲厕所可以节约用水,故D选项正确;
故选B。
12.(1)
(2)水氢气+氧气
(3)水分子间的间隔变大了
(4)分子种类是否改变
(5)肥皂水
(6)随手关闭水龙头(或用淘米水浇花或用洗衣水拖地等,合理即可)
【详解】(1)电解水过程中,水分子分解为氢原子和氧原子,氢原子和氧原子分别结合为氢分子和氧分子,最小的微粒是氢、氧原子;方框中补全相应微粒的图示为:;
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的文字表达式为:水氢气+氧气;
(3)通过电加热,使水沸腾变为水蒸气,从微粒角度分析此过程中,发生变化的是:水分子间的间隔变大了;
(4)光照下分解水生成氢气和氧气,分子的种类发生改变,通过电加热,使水沸腾变为水蒸气,分子的种类没有改变,水分子间的间隔变大了,最本质的区别是分子种类是否改变;
(5)区分硬水和软水最常用的方法为加肥皂水,泡沫多,浮渣少的为软水,泡沫少,浮渣多的为硬水;
(6)生活中常见的节水方法有随手关闭水龙头、用淘米水浇花、用洗衣水拖地等。
13.(1) 混合物 肥皂水
(2) b 增强水的导电性 Ⅱ Ⅰ 不可以
(3)吸附水中的异味和色素
【详解】(1)湖水中含有水和一些钙镁化合物,属于混合物;将肥皂水加入西太湖水中,若产生较少的泡沫,为硬水;若产生较多的泡沫,为软水;
(2)①电解水实验中,“正氧负氢”,负极产生的是氢气,故b管是氢气;
②纯水不导电,电解水时,通常要加入少量氢氧化钠溶液或稀硫酸,目的是为了增强水的导电性;
③设计实验:观察到试管a收集到黄绿色气体;试管b收集到无色气体,说明产生了氯气,则猜想Ⅱ是错误的;
用拇指堵住试管b,移近点燃的酒精灯,一开拇指点火,听到爆鸣声,说明b管产生的是氢气,故猜想Ⅰ是错误的;
反思与评价:联系电解水的实验,要证明水的组成,在电解水时不可以加氯化钠溶液;
(3)活性炭具有吸附性,能吸附水中的色素和异味。
14. 1:2 木条燃烧更旺 增强导电性 水是由氢、氧两种元素组成的##水由氢元素和氧元素组成 水是由两种元素组成的纯净物,且其中一种是氧元素 管上有刻度更准确##更便于检验生成的气体##防止从水槽中取出试管时碱性液体腐蚀手 不能
【详解】(1)水通电分解生成氢气和氧气,所以观察到电极附近有气泡产生,一段时间后,正、负极产生的气体体积比约为1:2.切断电源,打开a管顶端的活塞,由于a管产生的是氧气,在管口放置一根燃着的木条,会观察到火焰燃烧更旺;
(2)水通电分解加入了少量氢氧化钠,目的是增强导电性;
(3)水通电分解生成氢气和氧气,所以本实验得出的结论是水是由氢、氧元素组成的化合物。通过此结论还能从宏观角度解释,水之所以属于氧化物,是因为水是由两种元素组成的纯净物,且其中一种是氧元素;
(4)和图2的装置相比,现行教材(图1)装置的优点是管上有刻度,更准确;更便于检验生成的气体;防止从水槽中取出试管时碱性液体腐蚀手,电解氯化钠溶液生成氢气和氯气,所以不能用氯化钠代替氢氧化钠;
【点睛】本题主要考查水电解实验,掌握相关物质性质进行解题。
15. 水蒸气 铁+水 四氧化三铁+氢气 增强导电性 排尽空气,以防止检验时发生爆炸 1:2 上升 用燃着的木条放于出气口,若气体被点燃,产生淡蓝色火焰,则该气体是氢气
【详解】经典回顾:
(1)
①水蒸气遇冷凝结成水滴,将气体通过放在冷水中的铜管,目的是除去水蒸气;
②水蒸气与灼热的铁反应,生成一种黑色固体四氧化三铁和“可燃空气”,“可燃空气“是一种气体单质,其名称为氢气,铁与水蒸气在高温下反应生成四氧化三铁和氢气,反应的文字表达式为:铁+水 四氧化三铁+氢气;
交流与反思:
Ⅰ硫酸钠溶于水离解成可自由的钠离子和硫酸根离子。步骤①在水中加入硫酸钠溶液的作用是增强导电性;
II步骤②的目的是排尽空气,以防止检验时发生爆炸;
III电解水时,负极产生氢气,正极产生氧气,体积比约为2:1。步骤③中的现象:两极上均有气泡出现,B与正极相连,C与负极相连,两电极上产生的气体体积比约为1:2 ,两管生成气体,管内压强增大,A中液面上升;
IV C与负极相连,C管中的气体是氢气,氢气具有可燃性,能在空气中燃烧。步骤④中检验C中气体的方法是用燃着的木条放于出气口,若气体被点燃,产生淡蓝色火焰,则该气体是氢气。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
