2023高考化学必考选择题分类突破 微题型12 常见无机物的性质及转化(含答案)
文档属性
| 名称 | 2023高考化学必考选择题分类突破 微题型12 常见无机物的性质及转化(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 497.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-27 00:00:00 | ||
图片预览



文档简介
微题型12 常见无机物的性质及转化
1.(2022·江苏,8)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将N2转化为NH3
B.侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
C.工业上通过NH3催化氧化等反应过程生产HNO3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
2.(2021·福建,4)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是( )
A.FeSO4的分解产物X为FeO
B.本流程涉及复分解反应
C.HNO3的沸点比H2SO4的低
D.制备使用的铁锅易损坏
3.(2021·广东,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
4.(2021·江苏,7)N2是合成氨工业的重要原料,NH3不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。2NO(g)+O2(g)===2NO2(g) ΔH=-116.4 kJ·mol-1。大气中过量的NOx和水体中过量的NH、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO转化为N2。在指定条件下,下列选项所示的物质间转化能实现的是( )
A.NO(g)HNO3(aq)
B.稀HNO3(aq)NO2(g)
C.NO(g)N2(g)
D.NO(aq)N2(g)
熟知典型元素及其化合物的转化关系
1.活泼金属代表——钠及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ 。
2.变价过渡金属代表——铁及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ 。
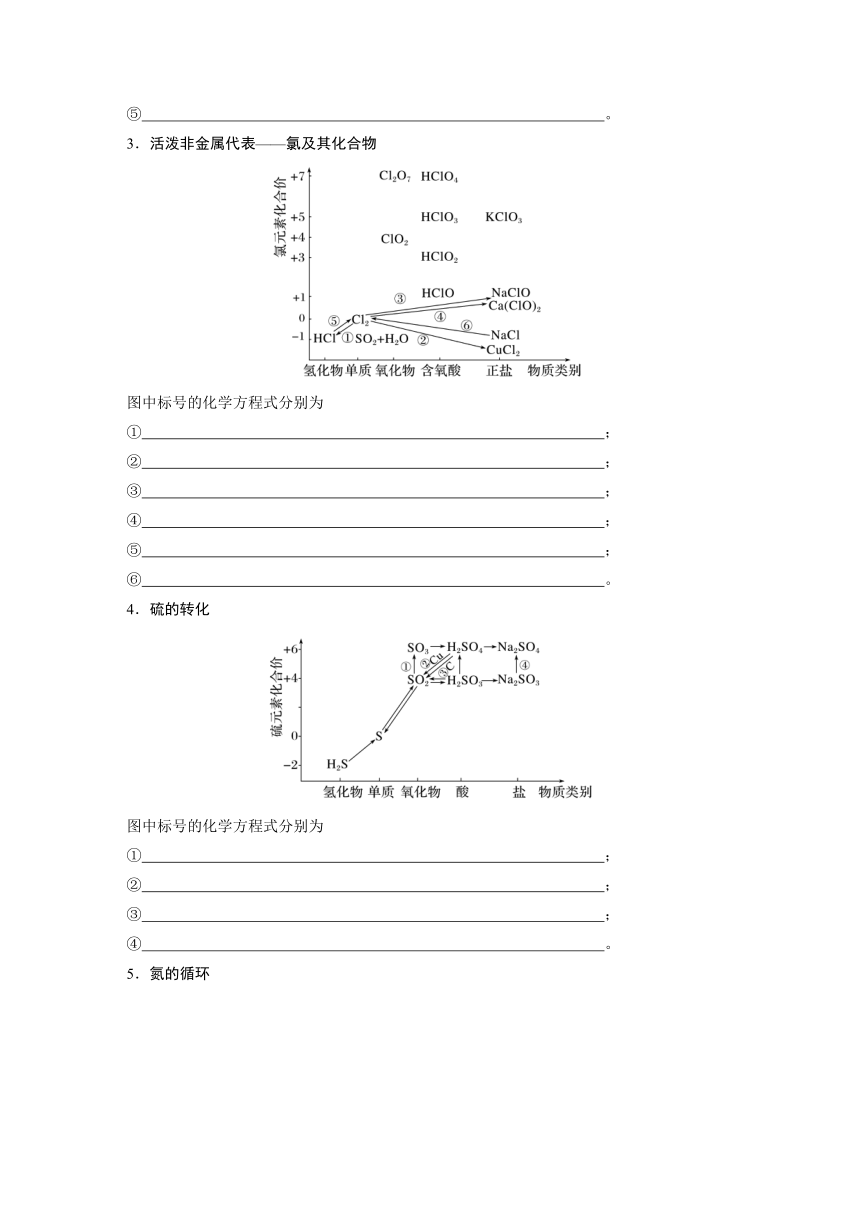
3.活泼非金属代表——氯及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ 。
4.硫的转化
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ 。
5.氮的循环
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ 。
1.化学反应中常伴有颜色变化,下列描述颜色变化的化学方程式不正确的是( )
A.Cl2通入H2O2溶液产生无色气体:Cl2+H2O2===2HCl+O2
B.Mg在CO2中燃烧产生白色和黑色固体:2Mg+CO22MgO+C
C.向FeCl3溶液中加入少量Zn粉,溶液黄色褪去:2FeCl3+3Zn===2Fe+3ZnCl2
D.将表面覆盖黑色Ag2S的银器放入盛装食盐水的铝锅中煮沸后,银器重新变光亮:3Ag2S+2Al+6H2O6Ag+2Al(OH)3+3H2S↑
2.下列关于金属镁、铝及其化合物的说法正确的是( )
A.将MgO与Al粉混合,再加入助燃剂可制成铝热剂
B.等质量的铝分别与足量的HCl、NaOH溶液反应,所得H2物质的量一定相等
C.将AlCl3加入Ca(HCO3)2溶液中,因相互促进水解而生成CO2气体和CaCO3沉淀
D.金属镁性质活泼,制取镁粉时可将镁蒸气在保护气N2中冷却
3.氧气转炉炼钢工艺可以利用废氧化铁经过必要的造球、码垛堆集或烧结工艺处理。将石灰与废氧化铁加工成适当的团状,然后用水雾进行水化,最后在铺满铁皮球的填料床上通入CO2进行硬化。硬化后的铁皮球耐压、耐磨、下落强度都有很大的提高。下列关于上述过程的说法错误的是( )
A.用水雾进行水化发生反应的离子方程式为CaO+H2O===Ca(OH)2
B.通入CO2进行硬化发生反应的化学方程式为Ca(OH)2+CO2===CaCO3↓+H2O
C.硬化后的铁皮球浸入盐酸中发生反应的离子方程式为CaCO3+2H+===Ca2++CO2↑+H2O
D.该方法用废氧化铁代替铁矿石,对金属资源进行了循环利用
4.如图所示,和水相连的物质都能和水发生反应,下列说法正确的是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①④⑧反应中,水都既不作氧化剂也不作还原剂
C.①和⑦中都有氧气生成,且生成1 mol O2转移的电子数相同
D.⑦中水作氧化剂,②中水作还原剂
5.能实现下列物质间直接转化的元素是( )
单质氧化物酸或碱盐
A.Fe B.Si C.Na D.Cu
6.下列物质间转化关系(反应条件已略去)正确的是( )
A.SSO3H2SO4SO2
B.NaNa2O2NaOHNaNO3
C.FeFe2O3Fe3FeCl3
D.N2NO2HNO3NO
7.价—类二维图是学习元素化合物知识的重要方法,某同学绘制某常见元素的价—类二维图如图所示。下列推断合理的是( )
A.f中阴、阳离子个数比一定为1∶2
B.图中按箭头所示的转化均可一步实现
C.标准状况下,1 mol b和c的混合物体积为22.4 L
D.可用盐酸酸化的氯化钡溶液检验e是否变质
8.甲、乙、丙三种不同的物质中均含有同一种元素,反应④为置换反应,往乙溶液中滴加KSCN溶液,乙溶液变为红色。它们之间的转化关系如图所示(部分反应物及生成物已略去)。下列说法错误的是( )
A.反应①、②可能均为化合反应
B.反应④的另一反应物可以为离子化合物的水溶液
C.甲一定为金属单质
D.若甲为金属单质,甲、乙、丙中的相同元素化合价不同
9.已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
A.X使蔗糖变黑的现象主要体现了X的强氧化性
B.若A为铁,则足量的A与X在室温下即可完全反应
C.B是无色、无味、有毒的气体
D.工业上,B转化为D的反应条件为加热、使用催化剂
10.已知在酸性或碱性条件下,单质铝均可与溶液中的NO发生反应,转化关系如图,已知:气体乙能使酚酞溶液变红。下列说法不正确的是( )
A.乙溶液中含有大量AlO
B.气体乙→气体甲反应为4NH3+5O24NO+6H2O
C.甲溶液→乙溶液可以加入过量的氨水
D.碱性条件下,参加反应的n(Al)∶n(NO)=8∶3
微题型12 常见无机物的性质及转化
真题示范
1.A [自然固氮是将N2转化为含氮化合物,不一定是转化为NH3,比如大气固氮是将N2转化为NO,A错误;侯氏制碱法发生反应的化学方程式为H2O+NH3+CO2+NaCl=== NaHCO3↓+NH4Cl,B正确;氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循环”,D正确。]
2.A [据图可知FeSO4分解时生成SO2和SO3,部分S元素被还原,则Fe元素应被氧化,X为Fe2O3,A错误;H2SO4与KNO3在蒸馏条件下生成HNO3和K2SO4,为复分解反应,B正确;H2SO4与KNO3混合后,蒸馏过程中生成HNO3,说明HNO3的沸点比H2SO4的低,C正确;硫酸、硝酸均可以和铁反应,所以制备使用的铁锅易损坏,D正确。]
3.C [Fe与Fe(Ⅲ)的盐类物质可发生反应生成Fe(Ⅱ)的盐类物质,如Fe+2FeCl3===3FeCl2,故不选A;Fe(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既可被氧化,也可被还原,故不选B;Fe(Ⅲ)的盐类物质与浓碱液反应生成Fe(OH)3沉淀,制备Fe(OH)3胶体的操作为向沸水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,故选C;b→c→d→e→b的转化如FeCl2Fe(OH)2Fe(OH)3FeCl3FeCl2,故不选D。]
4.C [NO不溶于水也不与水反应,A错误;稀HNO3与Cu反应得到硝酸铜、水和NO,得不到NO2,B错误;NO有氧化性,CO有还原性,在高温、催化剂条件下二者可发生氧化还原反应转化为无毒的N2和CO2,C正确;O3有强氧化性,不能作还原剂将硝酸根离子还原,D错误。]
疑难精讲
1.①2Na+O2Na2O2
②2Na2O2+2H2O===4NaOH+O2↑
③2Na2O2+2CO2===2Na2CO3+O2
④2NaOH+CO2===Na2CO3+H2O
⑤NaOH+CO2===NaHCO3
⑥Na2CO3+H2O+CO2===2NaHCO3
2.①2Fe+3Cl22FeCl3
②Fe2O3+3CO2Fe+3CO2(或Fe2O3+2Al2Fe+Al2O3)
③2FeCl3+Cu===2FeCl2+CuCl2(或2FeCl3+Fe===3FeCl2)
④2FeCl2+Cl2===2FeCl3
⑤4Fe(OH)2+O2+2H2O===4Fe(OH)3
3.①Cl2+SO2+2H2O===H2SO4+2HCl
②Cu+Cl2CuCl2
③Cl2+2NaOH===NaCl+NaClO+H2O
④2Cl2+2Ca(OH)2===Ca(ClO)2+CaCl2+2H2O
⑤MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
⑥2NaCl+2H2O2NaOH+Cl2↑+H2↑
4.①2SO2+O22SO3
②Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
③C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
④2Na2SO3+O2===2Na2SO4
5.①Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O
②4NH3+5O24NO+6H2O
③3NO2+H2O===2HNO3+NO
④C+4HNO3(浓)CO2↑+4NO2↑+2H2O
⑤Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O或3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
模拟演练
1.C 2.B 3.C 4.B
5.C [Fe与氧气点燃会生成四氧化三铁,四氧化三铁不溶于水,也不与水发生反应,不能实现直接转化,Fe与氧气反应,缓慢氧化生成氧化铁,氧化铁不溶于水,也不与水反应,不能实现直接转化,A不符合题意;Si与氧气在加热条件下可生成二氧化硅,但二氧化硅不溶于水,也不与水发生反应,不能实现直接转化,B不符合题意;Na与氧气常温下可生成氧化钠,氧化钠与水反应可生成氢氧化钠(碱),氢氧化钠再与HCl发生中和反应生成氯化钠(盐)和水,均可实现物质间直接转化,C符合题意;Cu与氧气在加热条件下可生成氧化铜,但氧化铜不溶于水,也不与水发生反应,不能实现直接转化,D不符合题意。]
6.B 7.D 8.C
9.D [X为浓硫酸、B为二氧化硫、D为三氧化硫;浓硫酸使蔗糖变黑的现象主要体现了浓硫酸的脱水性,A错误;若A为铁,常温下,铁与浓硫酸反应生成致密的氧化物保护膜,发生钝化,所以铁不能完全溶解,B错误;B为SO2,SO2是一种无色、有刺激性气味的有毒气体,C错误。]
10.C [酸性条件下,单质铝与溶液中的NO 发生反应的离子方程式为Al+4H++NO===Al3+
+NO↑+2H2O;碱性条件下,单质铝与溶液中的NO发生反应的离子方程式为8Al+5OH-+3NO+2H2O8AlO+3NH3↑。]
1.(2022·江苏,8)氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将N2转化为NH3
B.侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
C.工业上通过NH3催化氧化等反应过程生产HNO3
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
2.(2021·福建,4)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是( )
A.FeSO4的分解产物X为FeO
B.本流程涉及复分解反应
C.HNO3的沸点比H2SO4的低
D.制备使用的铁锅易损坏
3.(2021·广东,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
4.(2021·江苏,7)N2是合成氨工业的重要原料,NH3不仅可制造化肥,还能通过催化氧化生产HNO3;HNO3能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N2与O2反应生成NO,NO进一步氧化生成NO2。2NO(g)+O2(g)===2NO2(g) ΔH=-116.4 kJ·mol-1。大气中过量的NOx和水体中过量的NH、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2,也可将水体中的NO转化为N2。在指定条件下,下列选项所示的物质间转化能实现的是( )
A.NO(g)HNO3(aq)
B.稀HNO3(aq)NO2(g)
C.NO(g)N2(g)
D.NO(aq)N2(g)
熟知典型元素及其化合物的转化关系
1.活泼金属代表——钠及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ 。
2.变价过渡金属代表——铁及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ 。
3.活泼非金属代表——氯及其化合物
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ 。
4.硫的转化
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ 。
5.氮的循环
图中标号的化学方程式分别为
① ;
② ;
③ ;
④ ;
⑤ 。
1.化学反应中常伴有颜色变化,下列描述颜色变化的化学方程式不正确的是( )
A.Cl2通入H2O2溶液产生无色气体:Cl2+H2O2===2HCl+O2
B.Mg在CO2中燃烧产生白色和黑色固体:2Mg+CO22MgO+C
C.向FeCl3溶液中加入少量Zn粉,溶液黄色褪去:2FeCl3+3Zn===2Fe+3ZnCl2
D.将表面覆盖黑色Ag2S的银器放入盛装食盐水的铝锅中煮沸后,银器重新变光亮:3Ag2S+2Al+6H2O6Ag+2Al(OH)3+3H2S↑
2.下列关于金属镁、铝及其化合物的说法正确的是( )
A.将MgO与Al粉混合,再加入助燃剂可制成铝热剂
B.等质量的铝分别与足量的HCl、NaOH溶液反应,所得H2物质的量一定相等
C.将AlCl3加入Ca(HCO3)2溶液中,因相互促进水解而生成CO2气体和CaCO3沉淀
D.金属镁性质活泼,制取镁粉时可将镁蒸气在保护气N2中冷却
3.氧气转炉炼钢工艺可以利用废氧化铁经过必要的造球、码垛堆集或烧结工艺处理。将石灰与废氧化铁加工成适当的团状,然后用水雾进行水化,最后在铺满铁皮球的填料床上通入CO2进行硬化。硬化后的铁皮球耐压、耐磨、下落强度都有很大的提高。下列关于上述过程的说法错误的是( )
A.用水雾进行水化发生反应的离子方程式为CaO+H2O===Ca(OH)2
B.通入CO2进行硬化发生反应的化学方程式为Ca(OH)2+CO2===CaCO3↓+H2O
C.硬化后的铁皮球浸入盐酸中发生反应的离子方程式为CaCO3+2H+===Ca2++CO2↑+H2O
D.该方法用废氧化铁代替铁矿石,对金属资源进行了循环利用
4.如图所示,和水相连的物质都能和水发生反应,下列说法正确的是( )
A.上述反应中属于氧化还原反应的有①②④⑥⑦⑧
B.①④⑧反应中,水都既不作氧化剂也不作还原剂
C.①和⑦中都有氧气生成,且生成1 mol O2转移的电子数相同
D.⑦中水作氧化剂,②中水作还原剂
5.能实现下列物质间直接转化的元素是( )
单质氧化物酸或碱盐
A.Fe B.Si C.Na D.Cu
6.下列物质间转化关系(反应条件已略去)正确的是( )
A.SSO3H2SO4SO2
B.NaNa2O2NaOHNaNO3
C.FeFe2O3Fe3FeCl3
D.N2NO2HNO3NO
7.价—类二维图是学习元素化合物知识的重要方法,某同学绘制某常见元素的价—类二维图如图所示。下列推断合理的是( )
A.f中阴、阳离子个数比一定为1∶2
B.图中按箭头所示的转化均可一步实现
C.标准状况下,1 mol b和c的混合物体积为22.4 L
D.可用盐酸酸化的氯化钡溶液检验e是否变质
8.甲、乙、丙三种不同的物质中均含有同一种元素,反应④为置换反应,往乙溶液中滴加KSCN溶液,乙溶液变为红色。它们之间的转化关系如图所示(部分反应物及生成物已略去)。下列说法错误的是( )
A.反应①、②可能均为化合反应
B.反应④的另一反应物可以为离子化合物的水溶液
C.甲一定为金属单质
D.若甲为金属单质,甲、乙、丙中的相同元素化合价不同
9.已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
A.X使蔗糖变黑的现象主要体现了X的强氧化性
B.若A为铁,则足量的A与X在室温下即可完全反应
C.B是无色、无味、有毒的气体
D.工业上,B转化为D的反应条件为加热、使用催化剂
10.已知在酸性或碱性条件下,单质铝均可与溶液中的NO发生反应,转化关系如图,已知:气体乙能使酚酞溶液变红。下列说法不正确的是( )
A.乙溶液中含有大量AlO
B.气体乙→气体甲反应为4NH3+5O24NO+6H2O
C.甲溶液→乙溶液可以加入过量的氨水
D.碱性条件下,参加反应的n(Al)∶n(NO)=8∶3
微题型12 常见无机物的性质及转化
真题示范
1.A [自然固氮是将N2转化为含氮化合物,不一定是转化为NH3,比如大气固氮是将N2转化为NO,A错误;侯氏制碱法发生反应的化学方程式为H2O+NH3+CO2+NaCl=== NaHCO3↓+NH4Cl,B正确;氮元素在自然界中既有游离态又有化合态,多种形态的氮及其化合物间的转化形成了自然界的“氮循环”,D正确。]
2.A [据图可知FeSO4分解时生成SO2和SO3,部分S元素被还原,则Fe元素应被氧化,X为Fe2O3,A错误;H2SO4与KNO3在蒸馏条件下生成HNO3和K2SO4,为复分解反应,B正确;H2SO4与KNO3混合后,蒸馏过程中生成HNO3,说明HNO3的沸点比H2SO4的低,C正确;硫酸、硝酸均可以和铁反应,所以制备使用的铁锅易损坏,D正确。]
3.C [Fe与Fe(Ⅲ)的盐类物质可发生反应生成Fe(Ⅱ)的盐类物质,如Fe+2FeCl3===3FeCl2,故不选A;Fe(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既可被氧化,也可被还原,故不选B;Fe(Ⅲ)的盐类物质与浓碱液反应生成Fe(OH)3沉淀,制备Fe(OH)3胶体的操作为向沸水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,故选C;b→c→d→e→b的转化如FeCl2Fe(OH)2Fe(OH)3FeCl3FeCl2,故不选D。]
4.C [NO不溶于水也不与水反应,A错误;稀HNO3与Cu反应得到硝酸铜、水和NO,得不到NO2,B错误;NO有氧化性,CO有还原性,在高温、催化剂条件下二者可发生氧化还原反应转化为无毒的N2和CO2,C正确;O3有强氧化性,不能作还原剂将硝酸根离子还原,D错误。]
疑难精讲
1.①2Na+O2Na2O2
②2Na2O2+2H2O===4NaOH+O2↑
③2Na2O2+2CO2===2Na2CO3+O2
④2NaOH+CO2===Na2CO3+H2O
⑤NaOH+CO2===NaHCO3
⑥Na2CO3+H2O+CO2===2NaHCO3
2.①2Fe+3Cl22FeCl3
②Fe2O3+3CO2Fe+3CO2(或Fe2O3+2Al2Fe+Al2O3)
③2FeCl3+Cu===2FeCl2+CuCl2(或2FeCl3+Fe===3FeCl2)
④2FeCl2+Cl2===2FeCl3
⑤4Fe(OH)2+O2+2H2O===4Fe(OH)3
3.①Cl2+SO2+2H2O===H2SO4+2HCl
②Cu+Cl2CuCl2
③Cl2+2NaOH===NaCl+NaClO+H2O
④2Cl2+2Ca(OH)2===Ca(ClO)2+CaCl2+2H2O
⑤MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
⑥2NaCl+2H2O2NaOH+Cl2↑+H2↑
4.①2SO2+O22SO3
②Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
③C+2H2SO4(浓)CO2↑+2SO2↑+2H2O
④2Na2SO3+O2===2Na2SO4
5.①Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O
②4NH3+5O24NO+6H2O
③3NO2+H2O===2HNO3+NO
④C+4HNO3(浓)CO2↑+4NO2↑+2H2O
⑤Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O或3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
模拟演练
1.C 2.B 3.C 4.B
5.C [Fe与氧气点燃会生成四氧化三铁,四氧化三铁不溶于水,也不与水发生反应,不能实现直接转化,Fe与氧气反应,缓慢氧化生成氧化铁,氧化铁不溶于水,也不与水反应,不能实现直接转化,A不符合题意;Si与氧气在加热条件下可生成二氧化硅,但二氧化硅不溶于水,也不与水发生反应,不能实现直接转化,B不符合题意;Na与氧气常温下可生成氧化钠,氧化钠与水反应可生成氢氧化钠(碱),氢氧化钠再与HCl发生中和反应生成氯化钠(盐)和水,均可实现物质间直接转化,C符合题意;Cu与氧气在加热条件下可生成氧化铜,但氧化铜不溶于水,也不与水发生反应,不能实现直接转化,D不符合题意。]
6.B 7.D 8.C
9.D [X为浓硫酸、B为二氧化硫、D为三氧化硫;浓硫酸使蔗糖变黑的现象主要体现了浓硫酸的脱水性,A错误;若A为铁,常温下,铁与浓硫酸反应生成致密的氧化物保护膜,发生钝化,所以铁不能完全溶解,B错误;B为SO2,SO2是一种无色、有刺激性气味的有毒气体,C错误。]
10.C [酸性条件下,单质铝与溶液中的NO 发生反应的离子方程式为Al+4H++NO===Al3+
+NO↑+2H2O;碱性条件下,单质铝与溶液中的NO发生反应的离子方程式为8Al+5OH-+3NO+2H2O8AlO+3NH3↑。]
同课章节目录
