专题3 第一单元 脂肪烃的性质及应用 第1课时 脂肪烃的类别 烷烃的性质 对点训练(含答案)
文档属性
| 名称 | 专题3 第一单元 脂肪烃的性质及应用 第1课时 脂肪烃的类别 烷烃的性质 对点训练(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 389.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-27 21:08:56 | ||
图片预览


文档简介
第一单元 脂肪烃的性质及应用
第1课时 脂肪烃的类别 烷烃的性质
题组一 烃的分类
1.如图所示的有机物因为酷似奥运五元环而被称为奥运分子,则该有机物属于( )
A.苯的同系物 B.烃的衍生物
C.高分子化合物 D.芳香烃
2.(2022·青岛高二期中)下列对烃的分类错误的是( )
A.乙烯、甲苯、环己烷都属于脂肪烃
B.、和同属于环烷烃,也属于饱和烃
C.乙烯、乙炔、1,3-丁二烯同属于不饱和烃
D.、和都属于芳香烃,但不都互为同系物
题组二 烷烃的物理性质及变化规律
3.根据以下数据推断丙烷的沸点可能是( )
物质 甲烷 乙烷 正丁烷 正戊烷
沸点 -164 ℃ -89 ℃ -0.5 ℃ 36 ℃
A.约-40 ℃ B.低于-164 ℃
C.低于-89 ℃ D.高于36 ℃
4.城市居民所用液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等,在使用过程中,常有一些液态杂质沉积于钢瓶底部,这些杂质可能是( )
A.甲烷和乙烷 B.乙烷和乙醇
C.乙烷和丁烷 D.戊烷和己烷
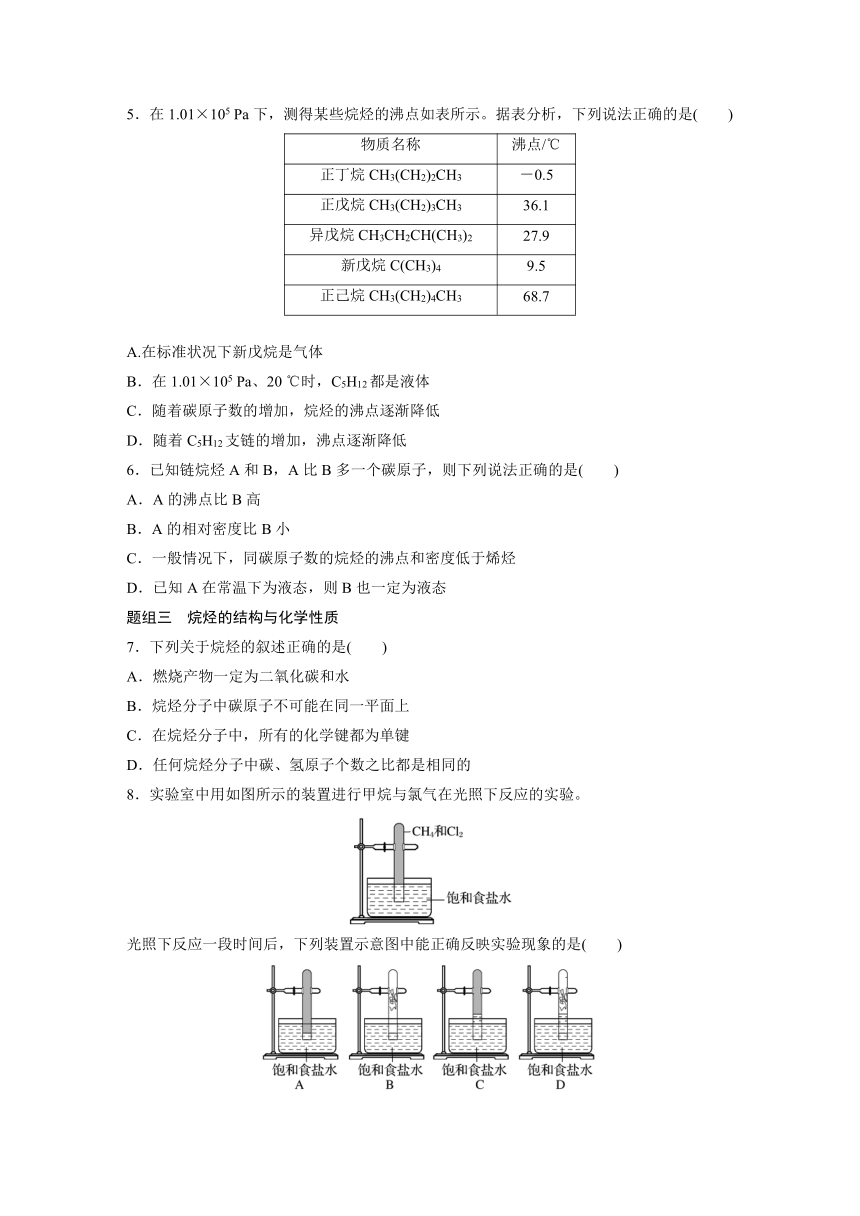
5.在1.01×105 Pa下,测得某些烷烃的沸点如表所示。据表分析,下列说法正确的是( )
物质名称 沸点/℃
正丁烷CH3(CH2)2CH3 -0.5
正戊烷CH3(CH2)3CH3 36.1
异戊烷CH3CH2CH(CH3)2 27.9
新戊烷C(CH3)4 9.5
正己烷CH3(CH2)4CH3 68.7
A.在标准状况下新戊烷是气体
B.在1.01×105 Pa、20 ℃时,C5H12都是液体
C.随着碳原子数的增加,烷烃的沸点逐渐降低
D.随着C5H12支链的增加,沸点逐渐降低
6.已知链烷烃A和B,A比B多一个碳原子,则下列说法正确的是( )
A.A的沸点比B高
B.A的相对密度比B小
C.一般情况下,同碳原子数的烷烃的沸点和密度低于烯烃
D.已知A在常温下为液态,则B也一定为液态
题组三 烷烃的结构与化学性质
7.下列关于烷烃的叙述正确的是( )
A.燃烧产物一定为二氧化碳和水
B.烷烃分子中碳原子不可能在同一平面上
C.在烷烃分子中,所有的化学键都为单键
D.任何烷烃分子中碳、氢原子个数之比都是相同的
8.实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
9.在120 ℃、1.01×105 Pa时,将两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是( )
A.CH4、C2H4 B.CH4、C2H6
C.C2H2、C2H4 D.C6H6、C2H6
10.在光照条件下,CH4与Cl2能发生取代反应。使1 mol CH4与Cl2反应,待反应完全后测得四种有机取代产物的物质的量之比n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=3∶2∶1∶4,则消耗的Cl2的物质的量为( )
A.1.0 mol B.1.8 mol
C.2.2 mol D.2.6 mol
11.分子中含有2~5个碳原子的直链烷烃沸点和标准燃烧热的数据见下表:
烷烃名称 乙烷 丙烷 丁烷 戊烷
沸点/℃ -89 -42 -0.5 36.0
标准燃烧热/ (kJ·mol-1) -1 559.8 -2 217.8 -2 653 -3 245
根据表中数据,下列判断错误的是( )
A.正庚烷在常温、常压下肯定不是气体
B.随分子中碳原子数增加,烷烃的标准燃烧热数值逐渐增大
C.随分子中碳原子数增加,烷烃沸点逐渐升高
D.随分子中碳原子数增加,烷烃沸点和标准燃烧热数值都成比例增加
12.燃烧0.1 mol两种气态烃的混合物,生成3.58 L CO2(标准状况)和3.60 g H2O,则混合气体中( )
A.一定有甲烷 B.一定有乙烷
C.一定无甲烷 D.一定有丙烷
13.(2021·天津耀华中学高二下期中)某烷是优良的有机溶剂,其球棍模型为,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )
A.X分子中可能含有三个甲基
B.X的一氯代物可能有三种
C.将标准状况下2.24 L的X完全燃烧,使所生成的气体通过装有足量无水CaCl2的干燥管,干燥管会增重12.6 g
D.X能使溴的四氯化碳溶液褪色
14.烃A分子的空间结构为(其中碳、氢原子已略去),因其分子中碳原子排列类似金刚石故名“金刚烷”,下列说法错误的是( )
A.金刚烷分子式是C10H16
B.金刚烷分子的二氯代物有4种
C.金刚烷分子由4个六元环组成
D.金刚烷分子的一氯代物有2种
15.(1)写出下列各链烷烃的分子式。
①烷烃B的分子中含有200个氢原子:_________________________________________。
②1 L烷烃D的蒸气完全燃烧时,生成同温同压下15 L水蒸气:________。
③0.01 mol烷烃E完全燃烧时,消耗标准状况下的氧气2.464 L:________。
(2)有两种气态烷烃的混合物,在标准状况下密度为1.16 g·L-1,则此混合物组成中一定含有的烃的化学式是________。该烃和氯气在光照下反应生成的有机物共有________种,其中________(填写化学式)在常温下呈气态。
(3)燃烧法是测定有机化合物分子式的一种重要方法。完全燃烧0.1 mol某烃后,将生成的气体先通过足量的浓硫酸,浓硫酸增重9.0 g,再将剩余气体通过澄清石灰水,生成沉淀40 g。写出该烃可能的结构简式:_____________________________________________________。
16.利用甲烷与氯气发生卤代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:
(1)B装置有三种功能:
①____________;②____________;③__________。
(2)设=x,若理论上欲获得最多的氯化氢,则x值的取值范围为________。
(3)D装置的石棉中均匀混有KI粉末,其作用是
________________________________________________________________________。
(4)E装置的作用是____________(填字母)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,置换出黑色小颗粒的化学方程式为______________________________________________,可见有机反应有很多副反应。
(6)E装置除生成盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
A.萃取法 B.蒸馏法
C.过滤法 D.分液法
该装置还有缺陷,原因是没有进行尾气处理,其尾气的主要成分是__________和__________。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
第1课时 脂肪烃的类别 烷烃的性质
1.D 2.A 3.A 4.D
5.D [由表中数据可知,新戊烷的沸点为9.5 ℃,所以在标准状况下其为液体,在1.01×105 Pa、20 ℃时新戊烷为气体,A、B项错误;随着碳原子数的增加,烷烃的沸点逐渐升高,C项错误;由C5H12同分异构体的沸点可知,随着烷烃支链的增加,沸点逐渐降低,D项正确。]
6.A [烷烃分子中碳原子数越多,则分子间作用力越大,沸点越高,密度越大。]
7.C [烷烃中含有碳、氢元素,完全燃烧的产物为二氧化碳和水,但如果氧气不足,烷烃不完全燃烧,产物有可能为一氧化碳和水;烷烃中乙烷的2个碳原子可以在同一直线上,除此之外,多碳烷烃主链是锯齿形,碳原子可能在同一平面上;烷烃属于饱和烃,不存在不饱和键,分子中所有的化学键都为单键;链烷烃的通式为CnH2n+2,碳、氢原子个数之比为n∶(2n+2),碳原子数不同时碳、氢原子个数之比不同。]
8.D 9.A
10.D [在光照条件下,1 mol CH4与Cl2能发生取代反应,测得四种有机取代产物的物质的量之比n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=3∶2∶1∶4,由碳原子守恒可知:n(CH3Cl)+n(CH2Cl2)+n(CHCl3)+n(CCl4)=1 mol,所以n(CH3Cl)=0.3 mol,n(CH2Cl2)=0.2 mol,n(CHCl3)=0.1 mol,n(CCl4)=0.4 mol,该四种取代产物中取代的n(H)=n(Cl)=0.3 mol×1+0.2 mol×2+0.1 mol×3+0.4 mol×4=2.6 mol,根据取代反应的特点可知,取代1 mol H,消耗1 mol Cl2,则消耗的n(Cl2)=n(H)=2.6 mol,D正确。]
11.D [由于正庚烷的相对分子质量大于戊烷,所以正庚烷在常温、常压下不是气体;随分子中碳原子数增加,烷烃沸点和标准燃烧热数值都增加,但是并不是成比例增加。]
12.A [ 生成n(CO2)=≈0.16 mol,生成n(H2O)==0.2 mol,因此两种气态烃的平均组成为C1.6H4,根据混合物的平均组成可知,碳原子数小于1.6的烃只有甲烷,而另一种烃中氢原子数必为4,且碳原子数大于或等于2。]
13.B [X的结构简式可能为(CH3)2CHCH(CH3)2或(CH3)3CCH2CH3,分子中都含有4个甲基,A项错误;(CH3)2CHCH(CH3)2中有2种氢原子,一氯代物只有2种,(CH3)3CCH2CH3中有3种氢原子,一氯代物有3种,B项正确;标准状况下X为液态,无法用气体摩尔体积进行计算,C项错误;(CH3)2CHCH(CH3)2或(CH3)3CCH2CH3都属于烷烃,与溴的四氯化碳溶液互溶,不能使溴的四氯化碳溶液褪色,D项错误。]
14.B [A项,由结构可知,含4个,6个—CH2—,则分子式为C10H16,正确;B项,金刚烷中氢有两种:、—CH2—,故二氯取代时可以固定一个氯原子,移动另一个氯原子,①固定,故另一个氯原子可位于六元环的邻、间、对三种,②固定—CH2—,另一个氯原子可位于同环的1号、3号碳原子和异环的—CH2—位,有三种,所以二氯代物共6种,错误;C项,由金刚烷的键线式可知,分子内由碳原子构成的最小的环上有6个碳原子,这种环有4个,正确;D项,含4个,6个—CH2—,含2种位置的氢原子,则一氯代物有2种,正确。]
15.(1)①C99H200 ②C14H30 ③C7H16 (2)CH4 4 CH3Cl
(3)CH3CH2CH2CH3、CH3CH(CH3)2
解析 (1)①链烷烃的通式为CnH2n+2,烷烃B的分子中含有200个氢原子,则2n+2=200,解得n=99,故B的分子式为C99H200。②1 L烷烃D的蒸气完全燃烧时,生成同温同压下15 L水蒸气,根据氢原子守恒,分子中氢原子数目为=30,链烷烃的通式为CnH2n+2,则2n+2=30,解得n=14,故D的分子式为C14H30。③链烷烃燃烧的通式为CnH2n+2+O2nCO2+(n+1)H2O,0.01 mol烷烃E完全燃烧时,消耗标准状况下的氧气2.464 L,则0.01 mol××22.4 L·mol-1=2.464 L,解得n=7,故E的分子式为C7H16。(2)有两种气态烷烃的混合物,在标准状况下密度为1.16 g·L-1,该混合烃的平均摩尔质量为1.16 g·L-1 ×22.4 L·mol-1≈26 g·mol-1,即平均相对分子质量为26,相对分子质量小于26的烷烃是甲烷,其相对分子质量为16,其他烷烃相对分子质量都大于26,所以此混合物中一定有甲烷,化学式为CH4;该烃和氯气在光照下反应生成的有机物有一氯甲烷、二氯甲烷、三氯甲烷以及四氯化碳共4种,其中CH3Cl为气体。(3)将生成的气体先通过足量的浓硫酸,浓硫酸增重9.0 g,9.0 g为水的质量,则n(H2O)==0.5 mol,n(H)=1 mol,再将剩余气体通过澄清石灰水,生成沉淀40 g,生成的沉淀为碳酸钙,可知n(CO2)=n(CaCO3)==
0.4 mol,可知1 mol烃含有4 mol C、10 mol H,则该烃分子式为C4H10,为丁烷,可能的结构简式为CH3CH2CH2CH3、CH3CH(CH3)2。
16.(1)①控制气流速度 ②均匀混合气体 ③干燥混合气体
(2)x≥4 (3)吸收过量的氯气 (4)CD (5)CH4+2Cl2C+4HCl (6)D A B
第1课时 脂肪烃的类别 烷烃的性质
题组一 烃的分类
1.如图所示的有机物因为酷似奥运五元环而被称为奥运分子,则该有机物属于( )
A.苯的同系物 B.烃的衍生物
C.高分子化合物 D.芳香烃
2.(2022·青岛高二期中)下列对烃的分类错误的是( )
A.乙烯、甲苯、环己烷都属于脂肪烃
B.、和同属于环烷烃,也属于饱和烃
C.乙烯、乙炔、1,3-丁二烯同属于不饱和烃
D.、和都属于芳香烃,但不都互为同系物
题组二 烷烃的物理性质及变化规律
3.根据以下数据推断丙烷的沸点可能是( )
物质 甲烷 乙烷 正丁烷 正戊烷
沸点 -164 ℃ -89 ℃ -0.5 ℃ 36 ℃
A.约-40 ℃ B.低于-164 ℃
C.低于-89 ℃ D.高于36 ℃
4.城市居民所用液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等,在使用过程中,常有一些液态杂质沉积于钢瓶底部,这些杂质可能是( )
A.甲烷和乙烷 B.乙烷和乙醇
C.乙烷和丁烷 D.戊烷和己烷
5.在1.01×105 Pa下,测得某些烷烃的沸点如表所示。据表分析,下列说法正确的是( )
物质名称 沸点/℃
正丁烷CH3(CH2)2CH3 -0.5
正戊烷CH3(CH2)3CH3 36.1
异戊烷CH3CH2CH(CH3)2 27.9
新戊烷C(CH3)4 9.5
正己烷CH3(CH2)4CH3 68.7
A.在标准状况下新戊烷是气体
B.在1.01×105 Pa、20 ℃时,C5H12都是液体
C.随着碳原子数的增加,烷烃的沸点逐渐降低
D.随着C5H12支链的增加,沸点逐渐降低
6.已知链烷烃A和B,A比B多一个碳原子,则下列说法正确的是( )
A.A的沸点比B高
B.A的相对密度比B小
C.一般情况下,同碳原子数的烷烃的沸点和密度低于烯烃
D.已知A在常温下为液态,则B也一定为液态
题组三 烷烃的结构与化学性质
7.下列关于烷烃的叙述正确的是( )
A.燃烧产物一定为二氧化碳和水
B.烷烃分子中碳原子不可能在同一平面上
C.在烷烃分子中,所有的化学键都为单键
D.任何烷烃分子中碳、氢原子个数之比都是相同的
8.实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
9.在120 ℃、1.01×105 Pa时,将两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是( )
A.CH4、C2H4 B.CH4、C2H6
C.C2H2、C2H4 D.C6H6、C2H6
10.在光照条件下,CH4与Cl2能发生取代反应。使1 mol CH4与Cl2反应,待反应完全后测得四种有机取代产物的物质的量之比n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=3∶2∶1∶4,则消耗的Cl2的物质的量为( )
A.1.0 mol B.1.8 mol
C.2.2 mol D.2.6 mol
11.分子中含有2~5个碳原子的直链烷烃沸点和标准燃烧热的数据见下表:
烷烃名称 乙烷 丙烷 丁烷 戊烷
沸点/℃ -89 -42 -0.5 36.0
标准燃烧热/ (kJ·mol-1) -1 559.8 -2 217.8 -2 653 -3 245
根据表中数据,下列判断错误的是( )
A.正庚烷在常温、常压下肯定不是气体
B.随分子中碳原子数增加,烷烃的标准燃烧热数值逐渐增大
C.随分子中碳原子数增加,烷烃沸点逐渐升高
D.随分子中碳原子数增加,烷烃沸点和标准燃烧热数值都成比例增加
12.燃烧0.1 mol两种气态烃的混合物,生成3.58 L CO2(标准状况)和3.60 g H2O,则混合气体中( )
A.一定有甲烷 B.一定有乙烷
C.一定无甲烷 D.一定有丙烷
13.(2021·天津耀华中学高二下期中)某烷是优良的有机溶剂,其球棍模型为,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )
A.X分子中可能含有三个甲基
B.X的一氯代物可能有三种
C.将标准状况下2.24 L的X完全燃烧,使所生成的气体通过装有足量无水CaCl2的干燥管,干燥管会增重12.6 g
D.X能使溴的四氯化碳溶液褪色
14.烃A分子的空间结构为(其中碳、氢原子已略去),因其分子中碳原子排列类似金刚石故名“金刚烷”,下列说法错误的是( )
A.金刚烷分子式是C10H16
B.金刚烷分子的二氯代物有4种
C.金刚烷分子由4个六元环组成
D.金刚烷分子的一氯代物有2种
15.(1)写出下列各链烷烃的分子式。
①烷烃B的分子中含有200个氢原子:_________________________________________。
②1 L烷烃D的蒸气完全燃烧时,生成同温同压下15 L水蒸气:________。
③0.01 mol烷烃E完全燃烧时,消耗标准状况下的氧气2.464 L:________。
(2)有两种气态烷烃的混合物,在标准状况下密度为1.16 g·L-1,则此混合物组成中一定含有的烃的化学式是________。该烃和氯气在光照下反应生成的有机物共有________种,其中________(填写化学式)在常温下呈气态。
(3)燃烧法是测定有机化合物分子式的一种重要方法。完全燃烧0.1 mol某烃后,将生成的气体先通过足量的浓硫酸,浓硫酸增重9.0 g,再将剩余气体通过澄清石灰水,生成沉淀40 g。写出该烃可能的结构简式:_____________________________________________________。
16.利用甲烷与氯气发生卤代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,其设计的模拟装置如下:
(1)B装置有三种功能:
①____________;②____________;③__________。
(2)设=x,若理论上欲获得最多的氯化氢,则x值的取值范围为________。
(3)D装置的石棉中均匀混有KI粉末,其作用是
________________________________________________________________________。
(4)E装置的作用是____________(填字母)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,置换出黑色小颗粒的化学方程式为______________________________________________,可见有机反应有很多副反应。
(6)E装置除生成盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
A.萃取法 B.蒸馏法
C.过滤法 D.分液法
该装置还有缺陷,原因是没有进行尾气处理,其尾气的主要成分是__________和__________。
A.CH4 B.CH3Cl C.CH2Cl2 D.CHCl3 E.CCl4
第1课时 脂肪烃的类别 烷烃的性质
1.D 2.A 3.A 4.D
5.D [由表中数据可知,新戊烷的沸点为9.5 ℃,所以在标准状况下其为液体,在1.01×105 Pa、20 ℃时新戊烷为气体,A、B项错误;随着碳原子数的增加,烷烃的沸点逐渐升高,C项错误;由C5H12同分异构体的沸点可知,随着烷烃支链的增加,沸点逐渐降低,D项正确。]
6.A [烷烃分子中碳原子数越多,则分子间作用力越大,沸点越高,密度越大。]
7.C [烷烃中含有碳、氢元素,完全燃烧的产物为二氧化碳和水,但如果氧气不足,烷烃不完全燃烧,产物有可能为一氧化碳和水;烷烃中乙烷的2个碳原子可以在同一直线上,除此之外,多碳烷烃主链是锯齿形,碳原子可能在同一平面上;烷烃属于饱和烃,不存在不饱和键,分子中所有的化学键都为单键;链烷烃的通式为CnH2n+2,碳、氢原子个数之比为n∶(2n+2),碳原子数不同时碳、氢原子个数之比不同。]
8.D 9.A
10.D [在光照条件下,1 mol CH4与Cl2能发生取代反应,测得四种有机取代产物的物质的量之比n(CH3Cl)∶n(CH2Cl2)∶n(CHCl3)∶n(CCl4)=3∶2∶1∶4,由碳原子守恒可知:n(CH3Cl)+n(CH2Cl2)+n(CHCl3)+n(CCl4)=1 mol,所以n(CH3Cl)=0.3 mol,n(CH2Cl2)=0.2 mol,n(CHCl3)=0.1 mol,n(CCl4)=0.4 mol,该四种取代产物中取代的n(H)=n(Cl)=0.3 mol×1+0.2 mol×2+0.1 mol×3+0.4 mol×4=2.6 mol,根据取代反应的特点可知,取代1 mol H,消耗1 mol Cl2,则消耗的n(Cl2)=n(H)=2.6 mol,D正确。]
11.D [由于正庚烷的相对分子质量大于戊烷,所以正庚烷在常温、常压下不是气体;随分子中碳原子数增加,烷烃沸点和标准燃烧热数值都增加,但是并不是成比例增加。]
12.A [ 生成n(CO2)=≈0.16 mol,生成n(H2O)==0.2 mol,因此两种气态烃的平均组成为C1.6H4,根据混合物的平均组成可知,碳原子数小于1.6的烃只有甲烷,而另一种烃中氢原子数必为4,且碳原子数大于或等于2。]
13.B [X的结构简式可能为(CH3)2CHCH(CH3)2或(CH3)3CCH2CH3,分子中都含有4个甲基,A项错误;(CH3)2CHCH(CH3)2中有2种氢原子,一氯代物只有2种,(CH3)3CCH2CH3中有3种氢原子,一氯代物有3种,B项正确;标准状况下X为液态,无法用气体摩尔体积进行计算,C项错误;(CH3)2CHCH(CH3)2或(CH3)3CCH2CH3都属于烷烃,与溴的四氯化碳溶液互溶,不能使溴的四氯化碳溶液褪色,D项错误。]
14.B [A项,由结构可知,含4个,6个—CH2—,则分子式为C10H16,正确;B项,金刚烷中氢有两种:、—CH2—,故二氯取代时可以固定一个氯原子,移动另一个氯原子,①固定,故另一个氯原子可位于六元环的邻、间、对三种,②固定—CH2—,另一个氯原子可位于同环的1号、3号碳原子和异环的—CH2—位,有三种,所以二氯代物共6种,错误;C项,由金刚烷的键线式可知,分子内由碳原子构成的最小的环上有6个碳原子,这种环有4个,正确;D项,含4个,6个—CH2—,含2种位置的氢原子,则一氯代物有2种,正确。]
15.(1)①C99H200 ②C14H30 ③C7H16 (2)CH4 4 CH3Cl
(3)CH3CH2CH2CH3、CH3CH(CH3)2
解析 (1)①链烷烃的通式为CnH2n+2,烷烃B的分子中含有200个氢原子,则2n+2=200,解得n=99,故B的分子式为C99H200。②1 L烷烃D的蒸气完全燃烧时,生成同温同压下15 L水蒸气,根据氢原子守恒,分子中氢原子数目为=30,链烷烃的通式为CnH2n+2,则2n+2=30,解得n=14,故D的分子式为C14H30。③链烷烃燃烧的通式为CnH2n+2+O2nCO2+(n+1)H2O,0.01 mol烷烃E完全燃烧时,消耗标准状况下的氧气2.464 L,则0.01 mol××22.4 L·mol-1=2.464 L,解得n=7,故E的分子式为C7H16。(2)有两种气态烷烃的混合物,在标准状况下密度为1.16 g·L-1,该混合烃的平均摩尔质量为1.16 g·L-1 ×22.4 L·mol-1≈26 g·mol-1,即平均相对分子质量为26,相对分子质量小于26的烷烃是甲烷,其相对分子质量为16,其他烷烃相对分子质量都大于26,所以此混合物中一定有甲烷,化学式为CH4;该烃和氯气在光照下反应生成的有机物有一氯甲烷、二氯甲烷、三氯甲烷以及四氯化碳共4种,其中CH3Cl为气体。(3)将生成的气体先通过足量的浓硫酸,浓硫酸增重9.0 g,9.0 g为水的质量,则n(H2O)==0.5 mol,n(H)=1 mol,再将剩余气体通过澄清石灰水,生成沉淀40 g,生成的沉淀为碳酸钙,可知n(CO2)=n(CaCO3)==
0.4 mol,可知1 mol烃含有4 mol C、10 mol H,则该烃分子式为C4H10,为丁烷,可能的结构简式为CH3CH2CH2CH3、CH3CH(CH3)2。
16.(1)①控制气流速度 ②均匀混合气体 ③干燥混合气体
(2)x≥4 (3)吸收过量的氯气 (4)CD (5)CH4+2Cl2C+4HCl (6)D A B
