第八单元 课题3 金属资源的利用和保护-【课件19页】2022-2023学年九年级化学下册同步精品课件(人教版)
文档属性
| 名称 | 第八单元 课题3 金属资源的利用和保护-【课件19页】2022-2023学年九年级化学下册同步精品课件(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-29 00:00:00 | ||
图片预览



文档简介
(共19张PPT)
第八单元 金属和金属材料
课题3 金属资源的利用和保护
金属活动性顺序表:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
导入新课(第1课时)
单质
多数金属都以化合物形式存在
少数很不活泼的金属如Au、Ag等有单质形式存在
知识点 1 常见的金属矿物
赤铁矿(主要成分是Fe2O3 )
磁铁矿(主要成分是Fe3O4)
铝土矿(主要成分Al2O3)
硫铁矿(主要成分是FeS2 )
都是混合物
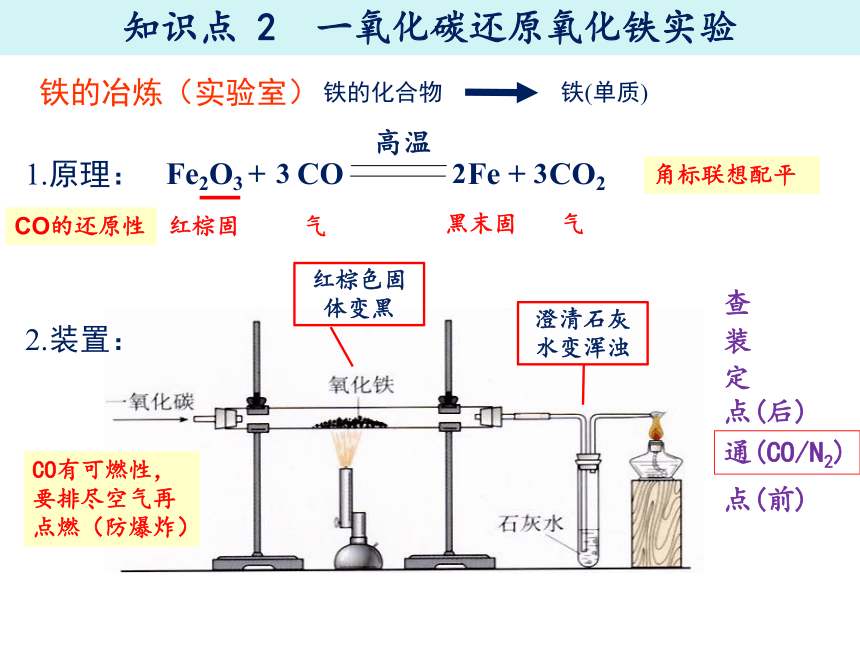
知识点 2 一氧化碳还原氧化铁实验
铁的化合物
铁(单质)
1.原理:
Fe2O3 + CO Fe + CO2
高温
铁的冶炼(实验室)
CO的还原性
3
3
2
角标联想配平
红棕固
气
黑末固
气
2.装置:
查
装
定
通(CO/N2)
点(后)
点(前)
CO有可燃性,要排尽空气再点燃(防爆炸)
红棕色固体变黑
澄清石灰水变浑浊
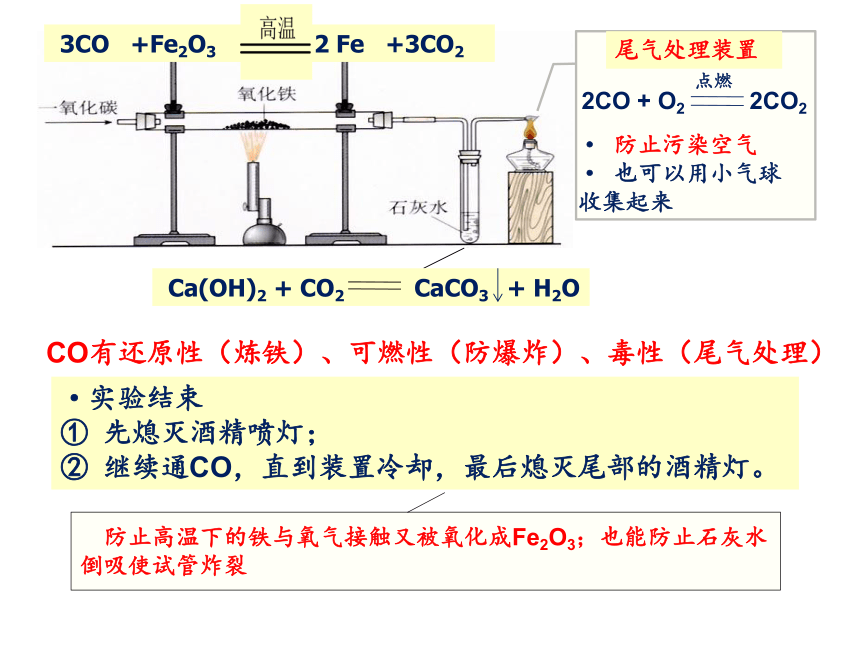
3CO +Fe2O3 2 Fe +3CO2
Ca(OH)2 + CO2 CaCO3 + H2O
尾气处理装置
2CO + O2 2CO2
点燃
· 防止污染空气
· 也可以用小气球收集起来
CO有还原性(炼铁)、可燃性(防爆炸)、毒性(尾气处理)
·实验结束
先熄灭酒精喷灯;
继续通CO,直到装置冷却,最后熄灭尾部的酒精灯。
防止高温下的铁与氧气接触又被氧化成Fe2O3;也能防止石灰水倒吸使试管炸裂
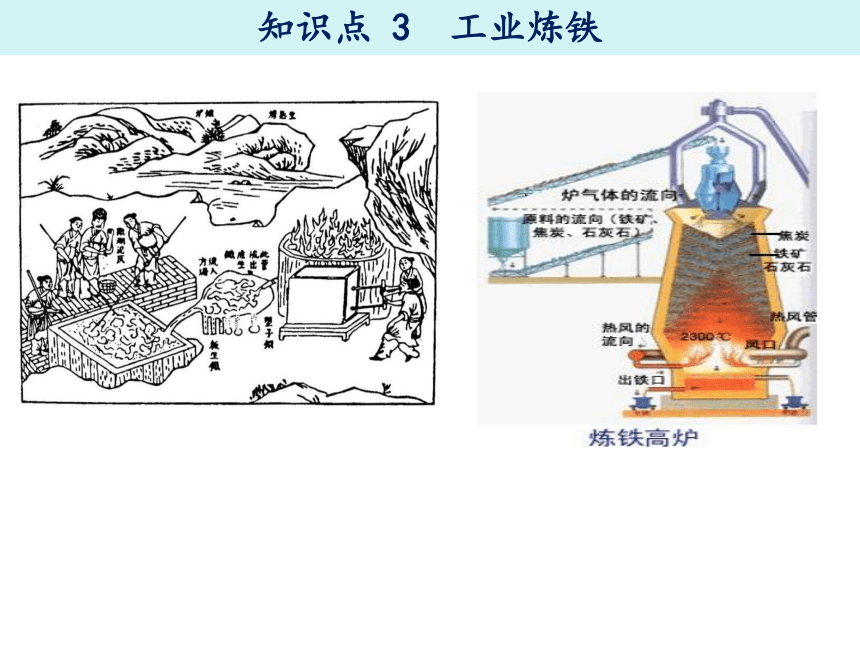
知识点 3 工业炼铁
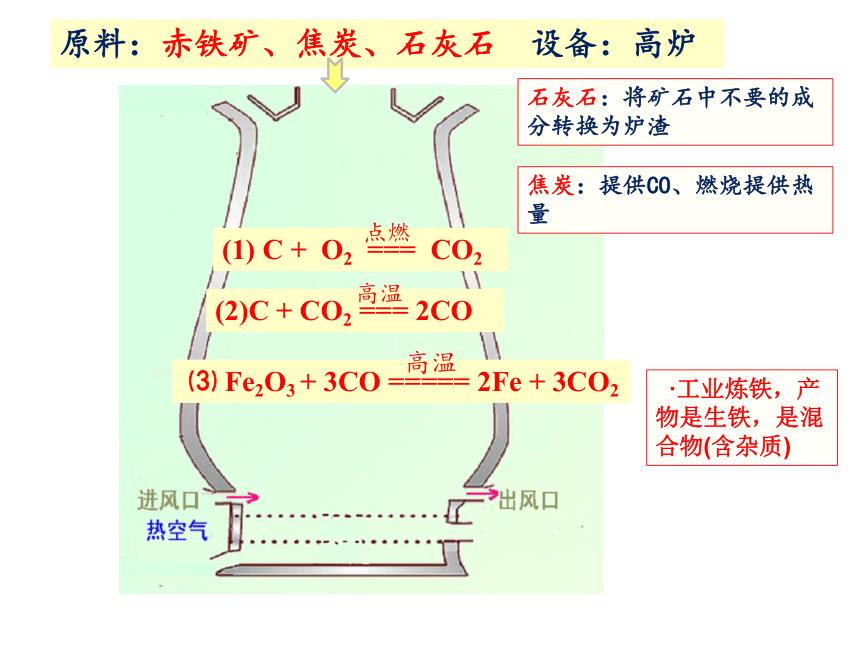
原料:赤铁矿、焦炭、石灰石 设备:高炉
石灰石:将矿石中不要的成分转换为炉渣
焦炭:提供CO、燃烧提供热量
(1) C + O2 === CO2
点燃
(2)C + CO2 === 2CO
高温
⑶ Fe2O3 + 3CO ===== 2Fe + 3CO2
高温
·工业炼铁,产物是生铁,是混合物(含杂质)
知识点 4 含杂质物质的计算
混合物(含杂质)和纯净物的转换关系:
纯净物质量 = 混合物质量 x 物质质量分数%
【例】用1000 t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁多少 t
纯净物
混合物
纯净物
混合物
Fe2O3 + 3CO ===== 2Fe + 3CO2
高温
解:设炼出生铁的质量是x。
Fe(纯)=生铁(混)x 80%
= x·96%
氧化铁 Fe2O3(纯)
= 赤铁矿(混)x 80%
= 1000 t x 80%
160 112
1000t×80% x·96%
160 112
800t 0.96x
x = 583 t
答:炼出生铁的质量是583 t。
【学以致用】
要炼出含杂质3%的生铁2000吨,需要含四氧化三铁质量分数为90%的磁铁矿石多少?
Fe3O4 + 4CO ===== 3Fe + 4CO2
高温
解:需要磁铁矿石的质量为x。
232 168
x ·90% 2000t×(1-3%)
232 168
0.9x 1940 t
x = 2977 t
答:需要磁铁矿石的质量为2977 t。
Fe(纯)=生铁(混)x (1-3%)
= 2000t×(1-3%)
Fe3O4(纯)= 磁铁矿(混)x 90%
= x ·90%
◆ 铁的冶炼
1.原料:焦炭、石灰石、铁矿石
2.原理:
在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来
◆ 涉及杂质问题的计算
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应注意杂质问题。
Fe2O3+3CO 2Fe+3CO2
高温
课堂小结
导入新课(第2课时)
金属锈蚀到底与哪些因素有关呢?
知识点 1 金属锈蚀的条件和防护
【探究】金属锈蚀的条件
一半蒸馏水
一半空气
纯蒸馏水
无空气
纯空气
无水分
干燥剂:生石灰或无水氯化钙
现象 结论
1
2
3
生锈
铁钉接触空气和水会生锈
不生锈
铁钉只接触水不生锈
不生锈
铁钉只接触空气不生锈
植物油:隔绝空气
用煮沸过的蒸馏水可防止水中溶有氧气
铁与氧气反应生成的铁锈成分复杂,并且疏松多孔、易吸水,不能形成致密的保护膜。
结论:在水、氧气同时存在的环境中铁能生锈。(缓慢氧化,放热)
铁锈 (Fe2O3) 氧化铝 (Al2O3)
结构特点
若不除去结果
疏松多孔
完全锈蚀
致密结实
使铝“自我保护”
①为了使月饼保鲜,月饼包装盒中常常放入一小袋黑色铁粉,其主要作用是什么?
吸收氧气和水分,延长月饼的保质期。
②根据铜绿的化学式Cu2(OH)2CO3分析铜生锈的条件又是什么?
与氧气O2、水H2O和二氧化碳CO2接触。
迁移应用
元素守恒
涂油
喷漆
制成合金
镀铬
防止生锈的方法
自行车的构件如支架、链条、钢圈等,分别采取了什么防锈措施?
刷油漆
制成合金
涂油
①物理除锈:用砂纸打磨
②化学除锈:用酸
Fe2O3 + HCl =
如何除锈呢?
铁锈主要成分:Fe2O3 红棕色固体
盐酸:HCl 硫酸:H2SO4
Fe2O3 + H2SO4 =
FeCl3 + H2O
6 2 3
交换,价不变
Fe2(SO4)3 + H2O
3 3
现象:
铁锈逐渐溶解,溶液由无色变为黄色。
FeCl3 、 Fe(SO4)3
+3 +3
黄色
对于金属资源除了采取防止金属腐蚀的措施外,还可以通过什么途径来使金属资源得到保护呢?
废品收购站为什么要收购废铁、废铜、和易拉罐等金属?
知识点 2 金属资源的保护
怎样保护金属资源?
1.防止金属的腐蚀;
2.回收利用废旧金属;
3.合理有效地开采矿物;
4.寻找金属的代用品。
讲授新课
◆ 铁生锈的主要条件是与空气和水(或水蒸气)直接接触,如果隔绝了空气和水,就能在一定程度上防止钢铁生锈。在钢铁表面涂油、刷漆、镀耐磨和耐腐蚀的合金如不锈钢等,都能防止钢铁生锈。
◆ 保护金属资源的有效途径是防止金属的腐蚀,回收利用废旧金属,合理有效地开采矿物,寻找金属的代用品。
课堂小结
第八单元 金属和金属材料
课题3 金属资源的利用和保护
金属活动性顺序表:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
导入新课(第1课时)
单质
多数金属都以化合物形式存在
少数很不活泼的金属如Au、Ag等有单质形式存在
知识点 1 常见的金属矿物
赤铁矿(主要成分是Fe2O3 )
磁铁矿(主要成分是Fe3O4)
铝土矿(主要成分Al2O3)
硫铁矿(主要成分是FeS2 )
都是混合物
知识点 2 一氧化碳还原氧化铁实验
铁的化合物
铁(单质)
1.原理:
Fe2O3 + CO Fe + CO2
高温
铁的冶炼(实验室)
CO的还原性
3
3
2
角标联想配平
红棕固
气
黑末固
气
2.装置:
查
装
定
通(CO/N2)
点(后)
点(前)
CO有可燃性,要排尽空气再点燃(防爆炸)
红棕色固体变黑
澄清石灰水变浑浊
3CO +Fe2O3 2 Fe +3CO2
Ca(OH)2 + CO2 CaCO3 + H2O
尾气处理装置
2CO + O2 2CO2
点燃
· 防止污染空气
· 也可以用小气球收集起来
CO有还原性(炼铁)、可燃性(防爆炸)、毒性(尾气处理)
·实验结束
先熄灭酒精喷灯;
继续通CO,直到装置冷却,最后熄灭尾部的酒精灯。
防止高温下的铁与氧气接触又被氧化成Fe2O3;也能防止石灰水倒吸使试管炸裂
知识点 3 工业炼铁
原料:赤铁矿、焦炭、石灰石 设备:高炉
石灰石:将矿石中不要的成分转换为炉渣
焦炭:提供CO、燃烧提供热量
(1) C + O2 === CO2
点燃
(2)C + CO2 === 2CO
高温
⑶ Fe2O3 + 3CO ===== 2Fe + 3CO2
高温
·工业炼铁,产物是生铁,是混合物(含杂质)
知识点 4 含杂质物质的计算
混合物(含杂质)和纯净物的转换关系:
纯净物质量 = 混合物质量 x 物质质量分数%
【例】用1000 t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁多少 t
纯净物
混合物
纯净物
混合物
Fe2O3 + 3CO ===== 2Fe + 3CO2
高温
解:设炼出生铁的质量是x。
Fe(纯)=生铁(混)x 80%
= x·96%
氧化铁 Fe2O3(纯)
= 赤铁矿(混)x 80%
= 1000 t x 80%
160 112
1000t×80% x·96%
160 112
800t 0.96x
x = 583 t
答:炼出生铁的质量是583 t。
【学以致用】
要炼出含杂质3%的生铁2000吨,需要含四氧化三铁质量分数为90%的磁铁矿石多少?
Fe3O4 + 4CO ===== 3Fe + 4CO2
高温
解:需要磁铁矿石的质量为x。
232 168
x ·90% 2000t×(1-3%)
232 168
0.9x 1940 t
x = 2977 t
答:需要磁铁矿石的质量为2977 t。
Fe(纯)=生铁(混)x (1-3%)
= 2000t×(1-3%)
Fe3O4(纯)= 磁铁矿(混)x 90%
= x ·90%
◆ 铁的冶炼
1.原料:焦炭、石灰石、铁矿石
2.原理:
在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石中还原出来
◆ 涉及杂质问题的计算
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应注意杂质问题。
Fe2O3+3CO 2Fe+3CO2
高温
课堂小结
导入新课(第2课时)
金属锈蚀到底与哪些因素有关呢?
知识点 1 金属锈蚀的条件和防护
【探究】金属锈蚀的条件
一半蒸馏水
一半空气
纯蒸馏水
无空气
纯空气
无水分
干燥剂:生石灰或无水氯化钙
现象 结论
1
2
3
生锈
铁钉接触空气和水会生锈
不生锈
铁钉只接触水不生锈
不生锈
铁钉只接触空气不生锈
植物油:隔绝空气
用煮沸过的蒸馏水可防止水中溶有氧气
铁与氧气反应生成的铁锈成分复杂,并且疏松多孔、易吸水,不能形成致密的保护膜。
结论:在水、氧气同时存在的环境中铁能生锈。(缓慢氧化,放热)
铁锈 (Fe2O3) 氧化铝 (Al2O3)
结构特点
若不除去结果
疏松多孔
完全锈蚀
致密结实
使铝“自我保护”
①为了使月饼保鲜,月饼包装盒中常常放入一小袋黑色铁粉,其主要作用是什么?
吸收氧气和水分,延长月饼的保质期。
②根据铜绿的化学式Cu2(OH)2CO3分析铜生锈的条件又是什么?
与氧气O2、水H2O和二氧化碳CO2接触。
迁移应用
元素守恒
涂油
喷漆
制成合金
镀铬
防止生锈的方法
自行车的构件如支架、链条、钢圈等,分别采取了什么防锈措施?
刷油漆
制成合金
涂油
①物理除锈:用砂纸打磨
②化学除锈:用酸
Fe2O3 + HCl =
如何除锈呢?
铁锈主要成分:Fe2O3 红棕色固体
盐酸:HCl 硫酸:H2SO4
Fe2O3 + H2SO4 =
FeCl3 + H2O
6 2 3
交换,价不变
Fe2(SO4)3 + H2O
3 3
现象:
铁锈逐渐溶解,溶液由无色变为黄色。
FeCl3 、 Fe(SO4)3
+3 +3
黄色
对于金属资源除了采取防止金属腐蚀的措施外,还可以通过什么途径来使金属资源得到保护呢?
废品收购站为什么要收购废铁、废铜、和易拉罐等金属?
知识点 2 金属资源的保护
怎样保护金属资源?
1.防止金属的腐蚀;
2.回收利用废旧金属;
3.合理有效地开采矿物;
4.寻找金属的代用品。
讲授新课
◆ 铁生锈的主要条件是与空气和水(或水蒸气)直接接触,如果隔绝了空气和水,就能在一定程度上防止钢铁生锈。在钢铁表面涂油、刷漆、镀耐磨和耐腐蚀的合金如不锈钢等,都能防止钢铁生锈。
◆ 保护金属资源的有效途径是防止金属的腐蚀,回收利用废旧金属,合理有效地开采矿物,寻找金属的代用品。
课堂小结
同课章节目录
