第六单元碳和碳的氧化物单元测试卷(含答案)-2022-2023学年九年级化学人教版上册
文档属性
| 名称 | 第六单元碳和碳的氧化物单元测试卷(含答案)-2022-2023学年九年级化学人教版上册 |

|
|
| 格式 | zip | ||
| 文件大小 | 239.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-28 00:00:00 | ||
图片预览




文档简介
第六单元碳和碳的氧化物单元测试卷
姓名:___________班级:___________考号:___________
一、单选题
1.中国政府向世界宣布2030年前实现碳达峰,2060年前实现碳中和。下列做法不利于实现“碳达峰、碳中和”的是
A.绿色出行 B.火力发电 C.植树造林 D.节约用电
2.物质的性质决定物质的用途,下列物质的用途与其化学性质有关的是
A.铜丝用作导线 B.活性炭用作除味剂
C.干冰用作人工降雨 D.氧气用于潜水和医疗急救
3.完成下列实验所用方案错误的是
选项 实验目的 方 案
A 附水中的色素和异味 用活性炭
B H2O2 溶液制取 O2,需控制反应的速率 用长颈漏斗替代分液漏斗
C 实验室检验二氧化碳 用澄清石灰水
D 蒸馏时防止水暴沸 烧瓶里放少量碎石
A.A B.B C.C D.D
4.同学们将燃着的蜡烛粘在盘子底部,向盘中加入适量澄清石灰水,再将干而冷的玻璃杯罩在蜡烛上方并倒扣在盘子中(如图)。有关实验现象与分析的描述,正确的是
A.实验初,玻璃杯内壁出现水雾 B.实验中,澄清石灰水无明显变化
C.实验结束后,玻璃杯内的水面下降 D.蜡烛熄灭后,玻璃杯内气体只有水蒸气
5.推理是学习化学的一种重要方法,下列推理中,正确的是
A.稀有气体原子的结构是相对稳定结构,所以具有相对稳定结构的粒子一定是稀有气体原子
B.阳离子一定带正电荷,所以带有正电荷的粒子一定是阳离子
C.催化剂在反应前后质量不变,则反应前后质量不变的物质一定是催化剂
D.碳、氢气和一氧化碳都具有可燃性,所以都可以用作燃料
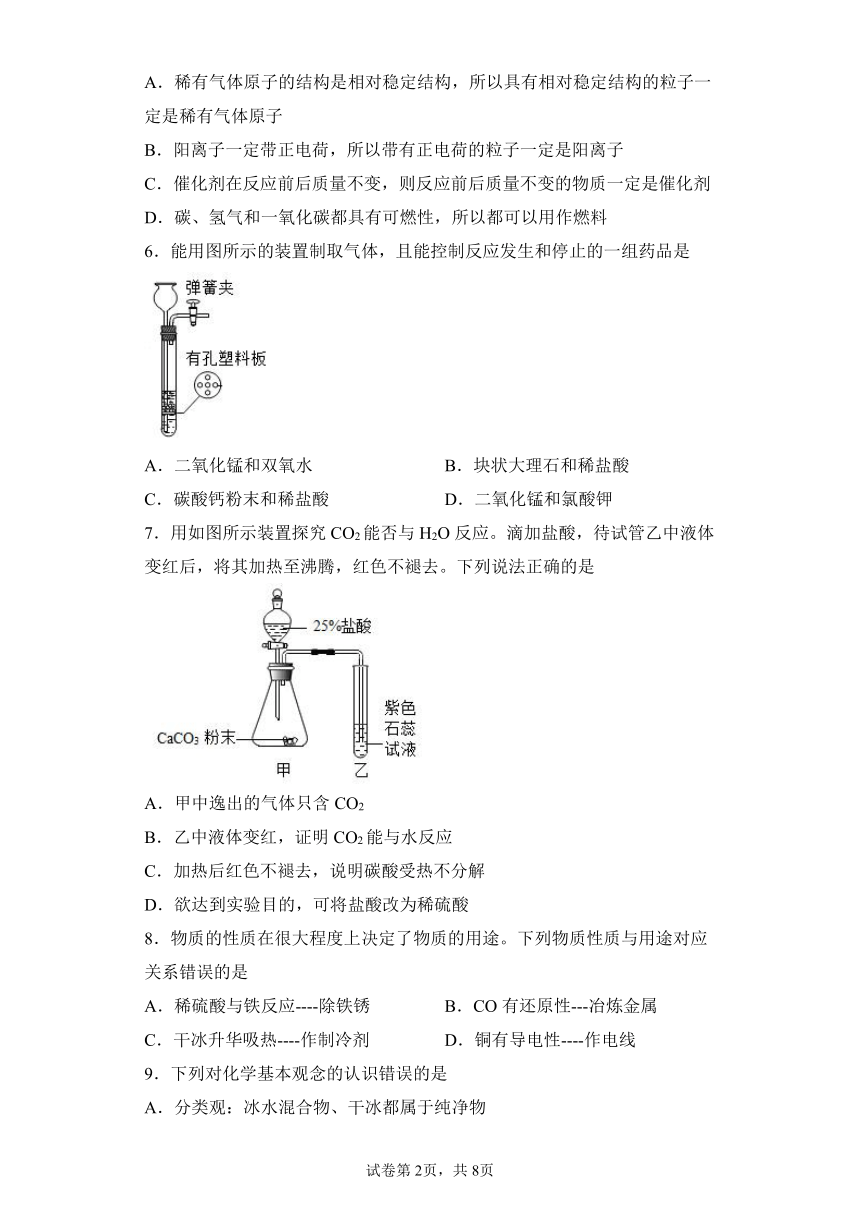
6.能用图所示的装置制取气体,且能控制反应发生和停止的一组药品是
A.二氧化锰和双氧水 B.块状大理石和稀盐酸
C.碳酸钙粉末和稀盐酸 D.二氧化锰和氯酸钾
7.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
8.物质的性质在很大程度上决定了物质的用途。下列物质性质与用途对应关系错误的是
A.稀硫酸与铁反应----除铁锈 B.CO有还原性---冶炼金属
C.干冰升华吸热----作制冷剂 D.铜有导电性----作电线
9.下列对化学基本观念的认识错误的是
A.分类观:冰水混合物、干冰都属于纯净物
B.守恒观:10g氢气与10g氧气充分反应后,一定生成20g水
C.转化观:CO和CO2在一定条件下,可以相互转化
D.结构观:金刚石、石墨、C60物理性质差异大,是因为碳原子的排列方式不同
10.化学学习要建构若干基本观念,以下四类化学基本观念中认识正确的是
A.元素观:水和过氧化氢组成元素不同
B.守恒观:碳和氧气反应,一定生成二氧化碳
C.变化观:同种元素的原子和离子在一定条件下是可以相互转化的
D.微粒观:一个二氧化硫分子由一个硫原子和一个氧分子构成
11.下列对一些事实的解释正确的是
事实 解释
A 金刚石、石墨和碳纳米管物理性质差异很大 构成它们的原子不同
B O2和O3组成元素相同但化学性质不同 构成它们的分子不同
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色以制白糖 活性炭化学性质很活泼
A.A B.B C.C D.D
12.除去下列各物质中少量杂质,所选用的试剂及操作方法均正确的是
选项 物质 所含杂质 试剂及操作方法
A 氯化钾 氯酸钾 加入二氧化锰充分加热
B 氧化钙 碳酸钙 加足量水搅拌过滤
C CO O2 点燃
D 水 有异味物质 加入活性炭吸附后过滤
A.A B.B C.C D.D
13.下列有关二氧化碳的说法正确的是
A.二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳能使石蕊变红
B.二氧化碳的过度排放会加剧温室效应,因此应禁止使用化石燃料
C.二氧化碳和一氧化碳的组成元素相同,在一定条件下可以相互转化
D.进入久未开启的菜窖之前,必须做灯火实验,是因为二氧化碳有毒
14.山西低碳转型迎来新“风口”。云冈热电厂排出的烟气补集加工成为高纯度液态二氧化碳,最终转化为碳纳米管,它是汽车锂电池的电极材料。关于碳纳米管说法正确的是
A.提炼过程发生物理变化 B.是一种新型化合物
C.完全燃烧生成二氧化碳和水 D.由碳原子构成
15.干冰的用途是利用其化学性质的是( )
A.人工降雨 B.无水灭火 C.保存食物 D.舞台“雾气缭绕”
二、填空题
16.二氧化碳的循环:_____;_____;_____。
17.现有下列物质:①干冰②稀有气体③液体氮气④肥皂水。选择合适物质,用序号填写。
(1)可以区别硬水和软水的是___________;
(2)制造多种用途电光源的是___________;
(3)制造舞台烟雾效果的是___________;
(4)用于冷冻血液的是___________。
18.陶瓷是火与土的结晶,是中华民族文化的象征之一
(1)下列中学实验室常见用品中,材质为陶瓷的是 (填标号)。
A.烧杯 B.集气瓶 C.蒸发皿 D.坩埚钳
(2)烧制陶瓷的原料为黏土,某黏土的成分如下表,所列出的四种氧化物中属于非金属氧化物的是_______。(写化学式)
成分 二氧化硅 氧化铝 氧化铁 氧化镁 其它
质量分数/% 69.51 14.15 2.55 1.31 12.48
(3)“九秋风露越窑开,夺得千峰翠色来”描述的是著名的青瓷。
①手工制作陶瓷的过程如下图,陶瓷丰富的色彩与烧制过程中的还原反应有关。燃料(以木炭为例)在窑体内燃烧,通过两步反应生成CO,化学方程式为_______、_______。
②青瓷的“翠色”来源十分复杂。涉及窑体内的CO和瓷器表面粙料中的氧化铁在高温下反应生成氧化亚铁,化学方程式为_______。
(4)古代窑炉(如下图)构造不断变迁。为了提高窑体内CO的体积分数,下列措施中可行的有哪些? 。(填标号)
A.相对增加燃料用量 B.相对增加空气鼓入
C.增加排气口数量 D.减少排气口数量
19.如图装置可用来收集气体,试回答下列问题:
(1)若收集氢气(氢气的密度比空气小),则氢气应从___________导管口通入,空气从___________导管口排出。
(2)若用排水法收集氧气,瓶内装满水,气体从___________端通入。
20.下表表示汽车的行驶速度与所产生的大气污染物的质量之间的关系。
污染物 速率(km/h)
50 80 120
一氧化碳/g 8.7 5.4 9.6
氮的氧化物/g 1.0 1.2 3.8
碳氢化合物/g 0.7 0.6 0.8
问:
(1)从上表中你认为,要使污染程度最小,汽车的速度应保持在____。
(2)汽车尾气产生的CO气体,能与血液中的______结合会导致人体中毒;CO燃烧时产生的______气体,大量排放到空气中会加剧温室效应。
(3)随着工业的发展,排放到空气中的有害气体和____对空气造成了污染;请你写出两条减少大气污染的措施:____、______(其他合理答案均可)。
三、实验题
21.下面所示为常见气体制备、干燥和性质实验的部分仪器。试根据题目要求,回答下列问题:
(1)以石灰石和稀盐酸(有挥发性)为原料,在实验室中制备并收集一瓶干燥纯净的二氧化碳气体。
①所选仪器的连接顺序为____________(填写仪器序号字母)
②仪器A中,发生反应的化学方程式为_____________。
③仪器E的作用是______________。
(2)欲用一氧化碳气体测定某不纯黑色氧化铜样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:CO→C→F→B。
①仪器C中看到的现象是____________。
②通过测量反应前、后仪器C处大玻璃管的质量变化,来计算氧化铜样品的纯度。若实验结束后大玻璃管中的物质里还有少许黑色氧化铜,则计算出样品纯度的结果将________(填“偏大”、“偏小”、“不受影响”其中之一)。
22.结合下列实验装置,回答问题。
(1)写出一个实验室用 A 装置制取氧气的化学方程式:______。
(2)实验室制取 O2和 CO2可用的同一个发生装置为______。图中 M 的仪器名称是:______。
(3)一种洗气装置如图 C 所示,为了除去一氧化碳中混入的少量二氧化碳,气体应从______(选填“a”或“b”)端导管口通入。
(4)若用 D 图装置采用排空气法收集氢气,应做的一点改动是:______。
四、计算题
23.化学与农业生产密切相关。某温室蔬菜大棚需用到440L CO2(按该条件下计算,CO2密度为2.0g/L),用足量盐酸与含CaCO3 80%的石灰石反应制取,需要这种石灰石的质量是多少?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.B
4.A
5.D
6.B
7.D
8.A
9.B
10.C
11.B
12.D
13.C
14.D
15.B
16. 光合作用 燃烧 呼吸
17.(1)④
(2)②
(3)①
(4)③
18.(1)C
(2)SiO2
(3)
(4)AD
19. a b a
20. 80km/h 血红蛋白 二氧化碳 烟尘 减少化石燃料的使用 开发利用新能源
21.(1) AEDG CaCO3+2HCl=CaCl2+H2O+CO2↑ 除去混合气体中的氯化氢气体
(2) 黑色固体变为红色 偏小
22.(1)
(2) B 长颈漏斗
(3)b
(4)把导管 b 伸入到集气瓶底部
23.解:CO2的质量为:440L × 2.0 g/L=880 g;
设需要CaCO3的质量为x
x=2000 g
所以,需要这种石灰石的质量为:2000g÷80%=2500g
答:需要这种石灰石的质量是2500g。
答案第1页,共2页
答案第1页,共2页
姓名:___________班级:___________考号:___________
一、单选题
1.中国政府向世界宣布2030年前实现碳达峰,2060年前实现碳中和。下列做法不利于实现“碳达峰、碳中和”的是
A.绿色出行 B.火力发电 C.植树造林 D.节约用电
2.物质的性质决定物质的用途,下列物质的用途与其化学性质有关的是
A.铜丝用作导线 B.活性炭用作除味剂
C.干冰用作人工降雨 D.氧气用于潜水和医疗急救
3.完成下列实验所用方案错误的是
选项 实验目的 方 案
A 附水中的色素和异味 用活性炭
B H2O2 溶液制取 O2,需控制反应的速率 用长颈漏斗替代分液漏斗
C 实验室检验二氧化碳 用澄清石灰水
D 蒸馏时防止水暴沸 烧瓶里放少量碎石
A.A B.B C.C D.D
4.同学们将燃着的蜡烛粘在盘子底部,向盘中加入适量澄清石灰水,再将干而冷的玻璃杯罩在蜡烛上方并倒扣在盘子中(如图)。有关实验现象与分析的描述,正确的是
A.实验初,玻璃杯内壁出现水雾 B.实验中,澄清石灰水无明显变化
C.实验结束后,玻璃杯内的水面下降 D.蜡烛熄灭后,玻璃杯内气体只有水蒸气
5.推理是学习化学的一种重要方法,下列推理中,正确的是
A.稀有气体原子的结构是相对稳定结构,所以具有相对稳定结构的粒子一定是稀有气体原子
B.阳离子一定带正电荷,所以带有正电荷的粒子一定是阳离子
C.催化剂在反应前后质量不变,则反应前后质量不变的物质一定是催化剂
D.碳、氢气和一氧化碳都具有可燃性,所以都可以用作燃料
6.能用图所示的装置制取气体,且能控制反应发生和停止的一组药品是
A.二氧化锰和双氧水 B.块状大理石和稀盐酸
C.碳酸钙粉末和稀盐酸 D.二氧化锰和氯酸钾
7.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
8.物质的性质在很大程度上决定了物质的用途。下列物质性质与用途对应关系错误的是
A.稀硫酸与铁反应----除铁锈 B.CO有还原性---冶炼金属
C.干冰升华吸热----作制冷剂 D.铜有导电性----作电线
9.下列对化学基本观念的认识错误的是
A.分类观:冰水混合物、干冰都属于纯净物
B.守恒观:10g氢气与10g氧气充分反应后,一定生成20g水
C.转化观:CO和CO2在一定条件下,可以相互转化
D.结构观:金刚石、石墨、C60物理性质差异大,是因为碳原子的排列方式不同
10.化学学习要建构若干基本观念,以下四类化学基本观念中认识正确的是
A.元素观:水和过氧化氢组成元素不同
B.守恒观:碳和氧气反应,一定生成二氧化碳
C.变化观:同种元素的原子和离子在一定条件下是可以相互转化的
D.微粒观:一个二氧化硫分子由一个硫原子和一个氧分子构成
11.下列对一些事实的解释正确的是
事实 解释
A 金刚石、石墨和碳纳米管物理性质差异很大 构成它们的原子不同
B O2和O3组成元素相同但化学性质不同 构成它们的分子不同
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色以制白糖 活性炭化学性质很活泼
A.A B.B C.C D.D
12.除去下列各物质中少量杂质,所选用的试剂及操作方法均正确的是
选项 物质 所含杂质 试剂及操作方法
A 氯化钾 氯酸钾 加入二氧化锰充分加热
B 氧化钙 碳酸钙 加足量水搅拌过滤
C CO O2 点燃
D 水 有异味物质 加入活性炭吸附后过滤
A.A B.B C.C D.D
13.下列有关二氧化碳的说法正确的是
A.二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳能使石蕊变红
B.二氧化碳的过度排放会加剧温室效应,因此应禁止使用化石燃料
C.二氧化碳和一氧化碳的组成元素相同,在一定条件下可以相互转化
D.进入久未开启的菜窖之前,必须做灯火实验,是因为二氧化碳有毒
14.山西低碳转型迎来新“风口”。云冈热电厂排出的烟气补集加工成为高纯度液态二氧化碳,最终转化为碳纳米管,它是汽车锂电池的电极材料。关于碳纳米管说法正确的是
A.提炼过程发生物理变化 B.是一种新型化合物
C.完全燃烧生成二氧化碳和水 D.由碳原子构成
15.干冰的用途是利用其化学性质的是( )
A.人工降雨 B.无水灭火 C.保存食物 D.舞台“雾气缭绕”
二、填空题
16.二氧化碳的循环:_____;_____;_____。
17.现有下列物质:①干冰②稀有气体③液体氮气④肥皂水。选择合适物质,用序号填写。
(1)可以区别硬水和软水的是___________;
(2)制造多种用途电光源的是___________;
(3)制造舞台烟雾效果的是___________;
(4)用于冷冻血液的是___________。
18.陶瓷是火与土的结晶,是中华民族文化的象征之一
(1)下列中学实验室常见用品中,材质为陶瓷的是 (填标号)。
A.烧杯 B.集气瓶 C.蒸发皿 D.坩埚钳
(2)烧制陶瓷的原料为黏土,某黏土的成分如下表,所列出的四种氧化物中属于非金属氧化物的是_______。(写化学式)
成分 二氧化硅 氧化铝 氧化铁 氧化镁 其它
质量分数/% 69.51 14.15 2.55 1.31 12.48
(3)“九秋风露越窑开,夺得千峰翠色来”描述的是著名的青瓷。
①手工制作陶瓷的过程如下图,陶瓷丰富的色彩与烧制过程中的还原反应有关。燃料(以木炭为例)在窑体内燃烧,通过两步反应生成CO,化学方程式为_______、_______。
②青瓷的“翠色”来源十分复杂。涉及窑体内的CO和瓷器表面粙料中的氧化铁在高温下反应生成氧化亚铁,化学方程式为_______。
(4)古代窑炉(如下图)构造不断变迁。为了提高窑体内CO的体积分数,下列措施中可行的有哪些? 。(填标号)
A.相对增加燃料用量 B.相对增加空气鼓入
C.增加排气口数量 D.减少排气口数量
19.如图装置可用来收集气体,试回答下列问题:
(1)若收集氢气(氢气的密度比空气小),则氢气应从___________导管口通入,空气从___________导管口排出。
(2)若用排水法收集氧气,瓶内装满水,气体从___________端通入。
20.下表表示汽车的行驶速度与所产生的大气污染物的质量之间的关系。
污染物 速率(km/h)
50 80 120
一氧化碳/g 8.7 5.4 9.6
氮的氧化物/g 1.0 1.2 3.8
碳氢化合物/g 0.7 0.6 0.8
问:
(1)从上表中你认为,要使污染程度最小,汽车的速度应保持在____。
(2)汽车尾气产生的CO气体,能与血液中的______结合会导致人体中毒;CO燃烧时产生的______气体,大量排放到空气中会加剧温室效应。
(3)随着工业的发展,排放到空气中的有害气体和____对空气造成了污染;请你写出两条减少大气污染的措施:____、______(其他合理答案均可)。
三、实验题
21.下面所示为常见气体制备、干燥和性质实验的部分仪器。试根据题目要求,回答下列问题:
(1)以石灰石和稀盐酸(有挥发性)为原料,在实验室中制备并收集一瓶干燥纯净的二氧化碳气体。
①所选仪器的连接顺序为____________(填写仪器序号字母)
②仪器A中,发生反应的化学方程式为_____________。
③仪器E的作用是______________。
(2)欲用一氧化碳气体测定某不纯黑色氧化铜样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:CO→C→F→B。
①仪器C中看到的现象是____________。
②通过测量反应前、后仪器C处大玻璃管的质量变化,来计算氧化铜样品的纯度。若实验结束后大玻璃管中的物质里还有少许黑色氧化铜,则计算出样品纯度的结果将________(填“偏大”、“偏小”、“不受影响”其中之一)。
22.结合下列实验装置,回答问题。
(1)写出一个实验室用 A 装置制取氧气的化学方程式:______。
(2)实验室制取 O2和 CO2可用的同一个发生装置为______。图中 M 的仪器名称是:______。
(3)一种洗气装置如图 C 所示,为了除去一氧化碳中混入的少量二氧化碳,气体应从______(选填“a”或“b”)端导管口通入。
(4)若用 D 图装置采用排空气法收集氢气,应做的一点改动是:______。
四、计算题
23.化学与农业生产密切相关。某温室蔬菜大棚需用到440L CO2(按该条件下计算,CO2密度为2.0g/L),用足量盐酸与含CaCO3 80%的石灰石反应制取,需要这种石灰石的质量是多少?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.B
4.A
5.D
6.B
7.D
8.A
9.B
10.C
11.B
12.D
13.C
14.D
15.B
16. 光合作用 燃烧 呼吸
17.(1)④
(2)②
(3)①
(4)③
18.(1)C
(2)SiO2
(3)
(4)AD
19. a b a
20. 80km/h 血红蛋白 二氧化碳 烟尘 减少化石燃料的使用 开发利用新能源
21.(1) AEDG CaCO3+2HCl=CaCl2+H2O+CO2↑ 除去混合气体中的氯化氢气体
(2) 黑色固体变为红色 偏小
22.(1)
(2) B 长颈漏斗
(3)b
(4)把导管 b 伸入到集气瓶底部
23.解:CO2的质量为:440L × 2.0 g/L=880 g;
设需要CaCO3的质量为x
x=2000 g
所以,需要这种石灰石的质量为:2000g÷80%=2500g
答:需要这种石灰石的质量是2500g。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
