化学人教版九下:10.1常见的酸和碱(第一课时)课件(共21张PPT)
文档属性
| 名称 | 化学人教版九下:10.1常见的酸和碱(第一课时)课件(共21张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-29 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
第十单元 课题1
常见的酸和碱(第一课时)
初
学
化
中
素养目标
会用酸碱指示剂检验溶液的酸碱性,了解酸的通性及其原理,能写出有关的化学方程式。
通过对酸性物质的梳理和归纳,感悟对比、推理及理论联系实际的方法。
体会化学与人类的密切关系,培养学生学习化学的兴趣。
素养
目标
1
2
3
新课导入
生活中的酸有哪些?
“酸”一词从有酸味的酒而来。最早,在制酒的时候,有时把比较珍贵的酒放在窖中保存,在微生物作用下,产生了酸。
知识点1 酸碱指示剂
4
酸碱指示剂
1.酸碱指示剂:——定性角度
能跟酸或碱的溶液反应而显示不同的颜色的物质。
常见的有:紫色石蕊溶液、无色酚酞溶液。
知识点1 酸碱指示剂
5
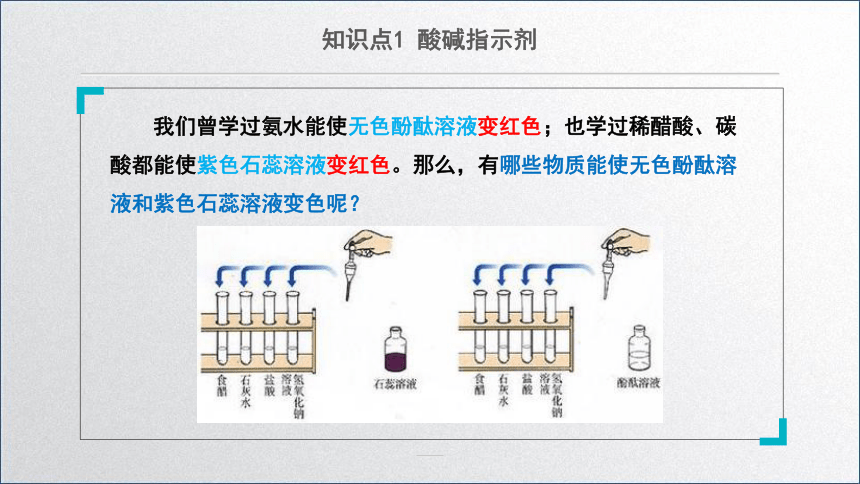
我们曾学过氨水能使无色酚酞溶液变红色;也学过稀醋酸、碳酸都能使紫色石蕊溶液变红色。那么,有哪些物质能使无色酚酞溶液和紫色石蕊溶液变色呢?
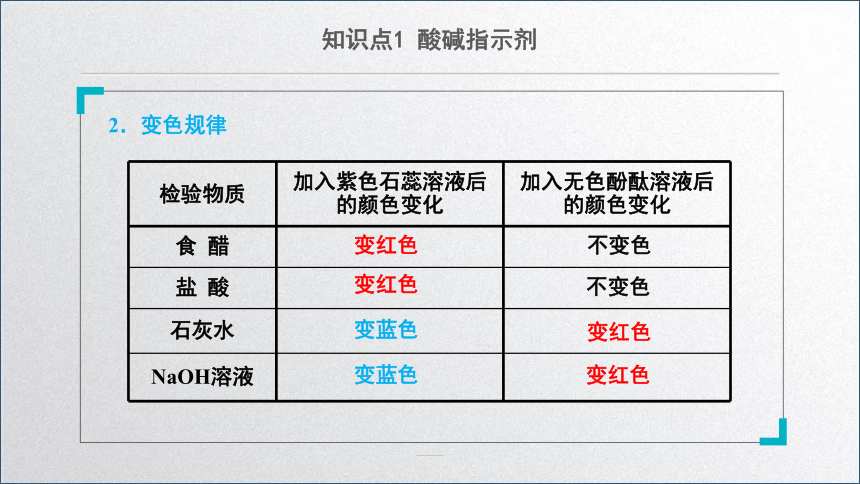
检验物质 加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
食 醋
盐 酸
石灰水
NaOH溶液
知识点1 酸碱指示剂
不变色
不变色
6
变红色
变红色
变蓝色
变蓝色
变红色
变红色
2.变色规律
知识点1 酸碱指示剂
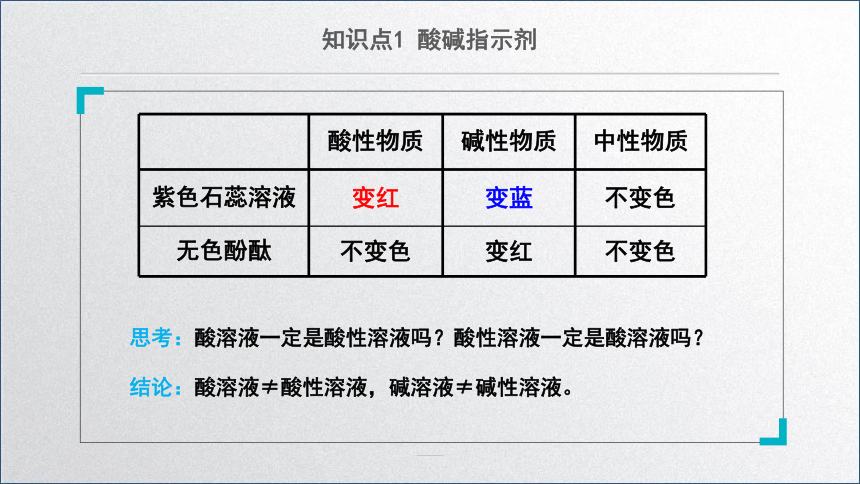
酸性物质 碱性物质 中性物质
紫色石蕊溶液 变红 变蓝 不变色
无色酚酞 不变色 变红 不变色
思考:酸溶液一定是酸性溶液吗?酸性溶液一定是酸溶液吗?
结论:酸溶液≠酸性溶液,碱溶液≠碱性溶液。
知识点2 常见的酸
浓盐酸和浓硫酸的物理性质
观察浓硫酸和浓盐酸的状态、颜色;打开瓶塞,观察发生的现象;闻一闻是否有气味?
盐酸 硫酸
颜色、状态 无色液体 无色粘稠液体
打开瓶盖后的现象 白雾(挥发性) 无现象
气味 有刺激性气味 无气味
白雾是浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气结合形成盐酸小液滴。
知识点2 常见的酸
浓硫酸的性质
1.我们可以用浓硫酸来干燥某些气体,它体现了浓硫酸的什么性质?
浓硫酸具有吸收水分的性质,即吸水性。
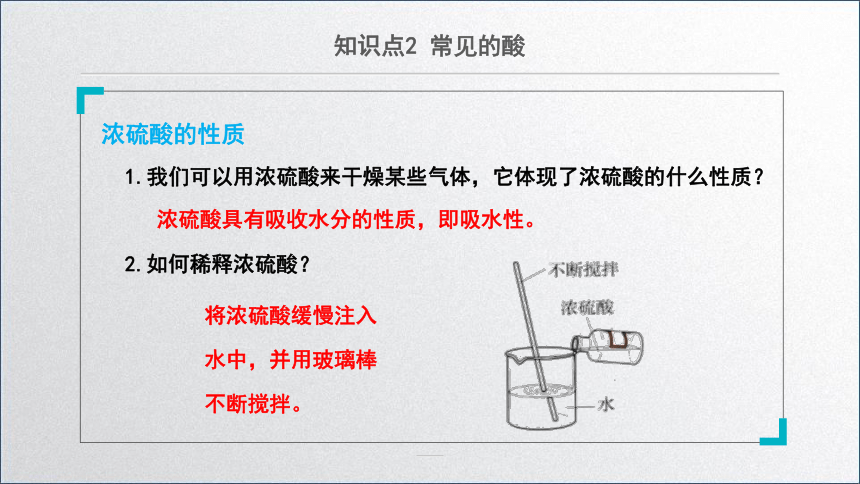
2.如何稀释浓硫酸?
将浓硫酸缓慢注入水中,并用玻璃棒不断搅拌。
知识点2 常见的酸
浓硫酸和浓盐酸敞口放置溶液变化
浓硫酸具有吸收性、浓盐酸中氯化氢气体易挥发
浓盐酸 浓硫酸
溶质质量 减小 不变
溶剂质量 不变(不考虑水分蒸发) 增大
溶液质量 减小 增大
溶质质量分数 降低 降低
实验 放置一会儿后的现象 原理
用玻璃棒蘸浓硫酸在纸上写字
用小木棍蘸少量浓硫酸
将浓硫酸滴到一小块布上
知识点2 常见的酸
蘸有浓硫酸的一端变黑了
写过字的地方变黑了
滴有浓硫酸的布烂了
脱水性原理:浓硫酸能夺取含碳、氢、氧等元素组成的化合物里的水分(氢、氧元素),生成黑色的炭和水
知识点2 常见的酸
酸的化学性质
1.酸和酸碱指示剂的反应:
紫色石蕊溶液 无色酚酞溶液
稀盐酸 变红 不变色
稀硫酸 变红 不变色
点滴板
结论:酸能使紫色石蕊溶液变红;无色酚酞溶液遇酸不变色(仍为无色)
使用点滴板进行实验的优点:①只需要2-3滴液体试剂,可以节约药品;
②反应现象更明显
知识点2 常见的酸
2.酸与金属的反应
金属活动性排在H前面的金属可以和酸反应,但是也有例外:如铁、铝不能和浓硫酸反应,因此可以用铁或铝的容器来盛装浓硫酸;碳酸是一种比较弱的酸,所以它和金属反应的速度非常慢,即使是像镁这样活泼的金属。
与稀盐酸的反应 与稀硫酸的反应
镁
锌
铁
铝
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl= FeCl2+H2↑
2Al+6HCl= 2AlCl3+3H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4= ZnSO4+H2↑
Fe +H2SO4= FeSO4+H2↑
2Al+3H2SO4= Al2(SO4)3+3H2↑
知识点2 常见的酸
3.酸与金属氧化物的反应
现象 化学方程式
铁锈+盐酸
铁锈+硫酸
氧化铜+硫酸
铁钉表面的铁锈被除去,溶液变为黄色
铁钉表面的铁锈被除去,溶液变为黄色
黑色的氧化铜慢慢消失,溶液变成蓝色
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+H2SO4=CuSO4+H2O
知识点2 常见的酸
盐酸、硫酸的用途
用途
盐酸 HCl 重要化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃酸中有盐酸,可帮助消化。
硫酸 H2SO4 重要化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
课堂练习
1.用酒精和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显红色,遇碱溶液显黄色。下列说法不正确的是( )
A.蝴蝶兰花的溶液与酸作用显红色是物理变化
B.能使蝴蝶兰花的溶液显黄色的可能是碱
C.将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D.蝴蝶兰花的溶液可用作酸碱指示剂
A
课堂练习
2.下列物质敞口放置于空气中,质量会增加的是( )
A.食盐水 B.石灰水 C.浓盐酸 D.浓硫酸
D
课堂练习
3.下列关于浓硫酸的描述错误的是( )
A.溶于水时放出大量的热
B.有强烈的腐蚀性
C.稀释浓硫酸时,切不可将水倒进浓硫酸
D.可在量筒中用浓硫酸配制稀硫酸
D
课堂小结
作业布置
请同学们回家后,在家里收集果汁、肥皂水、洗洁剂的水溶液、洗发水的水溶液等,用自制的指示剂检验它们的酸碱性。
本课结束 谢谢观看
第十单元 课题1
常见的酸和碱(第一课时)
初
学
化
中
素养目标
会用酸碱指示剂检验溶液的酸碱性,了解酸的通性及其原理,能写出有关的化学方程式。
通过对酸性物质的梳理和归纳,感悟对比、推理及理论联系实际的方法。
体会化学与人类的密切关系,培养学生学习化学的兴趣。
素养
目标
1
2
3
新课导入
生活中的酸有哪些?
“酸”一词从有酸味的酒而来。最早,在制酒的时候,有时把比较珍贵的酒放在窖中保存,在微生物作用下,产生了酸。
知识点1 酸碱指示剂
4
酸碱指示剂
1.酸碱指示剂:——定性角度
能跟酸或碱的溶液反应而显示不同的颜色的物质。
常见的有:紫色石蕊溶液、无色酚酞溶液。
知识点1 酸碱指示剂
5
我们曾学过氨水能使无色酚酞溶液变红色;也学过稀醋酸、碳酸都能使紫色石蕊溶液变红色。那么,有哪些物质能使无色酚酞溶液和紫色石蕊溶液变色呢?
检验物质 加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
食 醋
盐 酸
石灰水
NaOH溶液
知识点1 酸碱指示剂
不变色
不变色
6
变红色
变红色
变蓝色
变蓝色
变红色
变红色
2.变色规律
知识点1 酸碱指示剂
酸性物质 碱性物质 中性物质
紫色石蕊溶液 变红 变蓝 不变色
无色酚酞 不变色 变红 不变色
思考:酸溶液一定是酸性溶液吗?酸性溶液一定是酸溶液吗?
结论:酸溶液≠酸性溶液,碱溶液≠碱性溶液。
知识点2 常见的酸
浓盐酸和浓硫酸的物理性质
观察浓硫酸和浓盐酸的状态、颜色;打开瓶塞,观察发生的现象;闻一闻是否有气味?
盐酸 硫酸
颜色、状态 无色液体 无色粘稠液体
打开瓶盖后的现象 白雾(挥发性) 无现象
气味 有刺激性气味 无气味
白雾是浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气结合形成盐酸小液滴。
知识点2 常见的酸
浓硫酸的性质
1.我们可以用浓硫酸来干燥某些气体,它体现了浓硫酸的什么性质?
浓硫酸具有吸收水分的性质,即吸水性。
2.如何稀释浓硫酸?
将浓硫酸缓慢注入水中,并用玻璃棒不断搅拌。
知识点2 常见的酸
浓硫酸和浓盐酸敞口放置溶液变化
浓硫酸具有吸收性、浓盐酸中氯化氢气体易挥发
浓盐酸 浓硫酸
溶质质量 减小 不变
溶剂质量 不变(不考虑水分蒸发) 增大
溶液质量 减小 增大
溶质质量分数 降低 降低
实验 放置一会儿后的现象 原理
用玻璃棒蘸浓硫酸在纸上写字
用小木棍蘸少量浓硫酸
将浓硫酸滴到一小块布上
知识点2 常见的酸
蘸有浓硫酸的一端变黑了
写过字的地方变黑了
滴有浓硫酸的布烂了
脱水性原理:浓硫酸能夺取含碳、氢、氧等元素组成的化合物里的水分(氢、氧元素),生成黑色的炭和水
知识点2 常见的酸
酸的化学性质
1.酸和酸碱指示剂的反应:
紫色石蕊溶液 无色酚酞溶液
稀盐酸 变红 不变色
稀硫酸 变红 不变色
点滴板
结论:酸能使紫色石蕊溶液变红;无色酚酞溶液遇酸不变色(仍为无色)
使用点滴板进行实验的优点:①只需要2-3滴液体试剂,可以节约药品;
②反应现象更明显
知识点2 常见的酸
2.酸与金属的反应
金属活动性排在H前面的金属可以和酸反应,但是也有例外:如铁、铝不能和浓硫酸反应,因此可以用铁或铝的容器来盛装浓硫酸;碳酸是一种比较弱的酸,所以它和金属反应的速度非常慢,即使是像镁这样活泼的金属。
与稀盐酸的反应 与稀硫酸的反应
镁
锌
铁
铝
Mg+2HCl=MgCl2+H2↑
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl= FeCl2+H2↑
2Al+6HCl= 2AlCl3+3H2↑
Mg+H2SO4=MgSO4+H2↑
Zn +H2SO4= ZnSO4+H2↑
Fe +H2SO4= FeSO4+H2↑
2Al+3H2SO4= Al2(SO4)3+3H2↑
知识点2 常见的酸
3.酸与金属氧化物的反应
现象 化学方程式
铁锈+盐酸
铁锈+硫酸
氧化铜+硫酸
铁钉表面的铁锈被除去,溶液变为黄色
铁钉表面的铁锈被除去,溶液变为黄色
黑色的氧化铜慢慢消失,溶液变成蓝色
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
CuO+H2SO4=CuSO4+H2O
知识点2 常见的酸
盐酸、硫酸的用途
用途
盐酸 HCl 重要化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃酸中有盐酸,可帮助消化。
硫酸 H2SO4 重要化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。
浓硫酸有吸水性,在实验室中常用它做干燥剂。
课堂练习
1.用酒精和水浸泡蝴蝶兰花可得到紫色溶液,该溶液遇酸溶液显红色,遇碱溶液显黄色。下列说法不正确的是( )
A.蝴蝶兰花的溶液与酸作用显红色是物理变化
B.能使蝴蝶兰花的溶液显黄色的可能是碱
C.将氯化钠溶液滴入蝴蝶兰花的溶液后,溶液仍为紫色
D.蝴蝶兰花的溶液可用作酸碱指示剂
A
课堂练习
2.下列物质敞口放置于空气中,质量会增加的是( )
A.食盐水 B.石灰水 C.浓盐酸 D.浓硫酸
D
课堂练习
3.下列关于浓硫酸的描述错误的是( )
A.溶于水时放出大量的热
B.有强烈的腐蚀性
C.稀释浓硫酸时,切不可将水倒进浓硫酸
D.可在量筒中用浓硫酸配制稀硫酸
D
课堂小结
作业布置
请同学们回家后,在家里收集果汁、肥皂水、洗洁剂的水溶液、洗发水的水溶液等,用自制的指示剂检验它们的酸碱性。
本课结束 谢谢观看
同课章节目录
