浙江省衢州五校联盟2022-2023学年高二上学期1月期末联考试题 化学 pdf版含答案
文档属性
| 名称 | 浙江省衢州五校联盟2022-2023学年高二上学期1月期末联考试题 化学 pdf版含答案 |
|
|
| 格式 | |||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-29 00:00:00 | ||
图片预览


文档简介
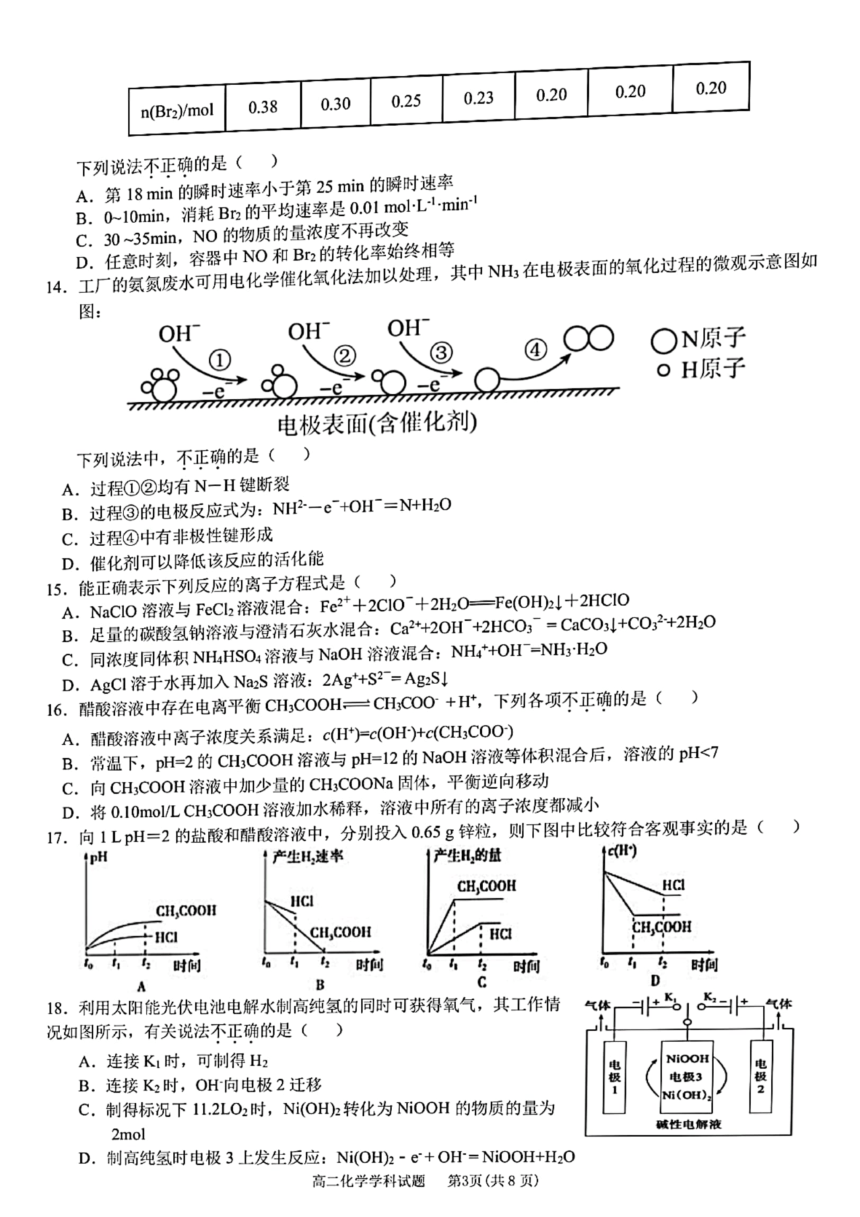
绝密★考试结束前
2022学年第一学期衢温“5+1”联盟期末联考
高二年级化学学科试题
考生须知:
1.本卷共8页满分100分,考试时间90分钟。
2.答题前,在指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
5.可能用到的相对原子质量:H-1C-12N-140-16Na-23S-32Cl-35.5K-39Fe-56Cu-64
Ag-108Ba-137Sn-119P-31
选择题部分
一、选择题(本大题共22小题,1-16每小题2分,17-22每小题3分,共50分。每小题列出的四个备选
项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1,在水溶液中呈酸性且促进水电离的是()
D.KNO3
A.NaHSO4
B.BeCl2
C.NaHCO3
2.下列物质属于弱电解质的是()
A.BaSO4
B.CH3CH2OH
C.HF
D.S02
3.酸碱中和滴定实验中不需要的仪器是()
B.
4.下列化学用语表示正确的是(
A.Ca+的结构示意图:
1s 2s 2p
3s
B.基态镁原子核外电子的轨道表示式为回西四四
C.甲烷的球棍模型:
D.基态铜原子的价层电子排布式:3d14s1
5.下列说法不正确的是()
A.电解精栋铜的阴极反应:Cu2+2e=Cu
B.纯银器表面在空气中因电化学腐蚀渐渐变暗
C.稀土元素可以用来制造合金
D.储氢材料一镧镍合金(LaNis)贮存氢气时发生了化学变化
6.关于反应3FeS04+203+3NO一Fe2z(S04)3+FeN03)3,下列说法正确的是()
A.Fe2(SO4)3既是氧化产物又是还原产物
B.氧化剂与还原剂的物质的量之比为2:3
C.该反应中被NO氧化的O3占消耗掉O3的1/4
高二化学学科试题第1页(共8页)
D.3 mol FeSO4反应时转移电子数为12Na
7.下列说法不正确的是(
)
A,pH计、酚酞和甲基橙均能用于NaOH溶液滴定盐酸终点的判断
B.受溴腐蚀致伤时,先用甘油清洗伤口,再用大量的水洗
C.萃取前,向分液漏斗中加少量水,检查旋塞芯处不漏水,即可使用
D.不可用溴水溶液检验丙烯醛中的碳碳双键
8.常温下,下列各组离子在相应条件下可能大量共存的是()
A.水电离的c(H)=10-1 mol-L的溶液中:A13+、C、K+、SO4
B.遇甲基橙变红色的溶液中:Fe2+、Na、NO3、SO42-
C.t史=1×10的溶液中:K*、Na、C、HC0
c(OH-)
D.pH=1溶液中:Na、Mg2+、NO3、SO32
9.某反应A+B=C+D在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确
的是()
A.△H<0,△S>0
B.△H>0,△S>0
C.△H<0,△$<0
D.△H>0,△S<0
10.设Na为阿伏加德罗常数的值,下列说法正确的是(
)
A.0,1 mol-L-!Ba(OH)2溶液中含有OH的数目为0.2Wa
B.49.5gCOC2中的碳氯键数目为NA
C.31gP4中的共价键数目为NA
D.120 g NaHSO4和KHSO3的水溶液中含有的阳离子数为Na
11.X、Y、Z、W为短周期元素,X2和Y+核外电子排布相同,X、Z位于同一主族,Y、Z、W位于同一
周期,W的最外层电子数是X、Y最外层电子数之和。下列说法不正确的是()
A.离子半径:Z>X>Y
B.第一电离能:YC.Y、W均属于元素周期表中的p区元素
D.X、Y、Z、W核电荷数逐渐增大
12.已知儿种化学键的键能和热化学方程式如下:
化学键
H-N
NN
CICI
NEN
H-CI
键能/kJ'mol厂)
391
193
243
946
432
NH4(g)+2C2(g)=N2(g)+4HC1(g)△H,下列推断正确的是()
A.H(g)+Cl(g)=HCI(g)=+432 kJ-mol
B.断裂1 molHCI键吸收能量比断裂1molN三N键多514kJ
C.上述反应中,△H=-431kJmo1
D.上述反应中,断裂极性键和非极性键,只形成极性键
13.某温度下,向2L密闭容器中通入1 mol NO和0.5molB2,发生如下反应:
2NO(g+Br2(g)=2NOBr(g),B2的物质的量随时间变化的实验数据如下表:
时间min
5
10
15
20
25
30
35
高二化学学科试题
第2页(共8页)
2022学年第一学期衢温“5+1”联盟期末联考
高二年级化学学科试题
考生须知:
1.本卷共8页满分100分,考试时间90分钟。
2.答题前,在指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
5.可能用到的相对原子质量:H-1C-12N-140-16Na-23S-32Cl-35.5K-39Fe-56Cu-64
Ag-108Ba-137Sn-119P-31
选择题部分
一、选择题(本大题共22小题,1-16每小题2分,17-22每小题3分,共50分。每小题列出的四个备选
项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1,在水溶液中呈酸性且促进水电离的是()
D.KNO3
A.NaHSO4
B.BeCl2
C.NaHCO3
2.下列物质属于弱电解质的是()
A.BaSO4
B.CH3CH2OH
C.HF
D.S02
3.酸碱中和滴定实验中不需要的仪器是()
B.
4.下列化学用语表示正确的是(
A.Ca+的结构示意图:
1s 2s 2p
3s
B.基态镁原子核外电子的轨道表示式为回西四四
C.甲烷的球棍模型:
D.基态铜原子的价层电子排布式:3d14s1
5.下列说法不正确的是()
A.电解精栋铜的阴极反应:Cu2+2e=Cu
B.纯银器表面在空气中因电化学腐蚀渐渐变暗
C.稀土元素可以用来制造合金
D.储氢材料一镧镍合金(LaNis)贮存氢气时发生了化学变化
6.关于反应3FeS04+203+3NO一Fe2z(S04)3+FeN03)3,下列说法正确的是()
A.Fe2(SO4)3既是氧化产物又是还原产物
B.氧化剂与还原剂的物质的量之比为2:3
C.该反应中被NO氧化的O3占消耗掉O3的1/4
高二化学学科试题第1页(共8页)
D.3 mol FeSO4反应时转移电子数为12Na
7.下列说法不正确的是(
)
A,pH计、酚酞和甲基橙均能用于NaOH溶液滴定盐酸终点的判断
B.受溴腐蚀致伤时,先用甘油清洗伤口,再用大量的水洗
C.萃取前,向分液漏斗中加少量水,检查旋塞芯处不漏水,即可使用
D.不可用溴水溶液检验丙烯醛中的碳碳双键
8.常温下,下列各组离子在相应条件下可能大量共存的是()
A.水电离的c(H)=10-1 mol-L的溶液中:A13+、C、K+、SO4
B.遇甲基橙变红色的溶液中:Fe2+、Na、NO3、SO42-
C.t史=1×10的溶液中:K*、Na、C、HC0
c(OH-)
D.pH=1溶液中:Na、Mg2+、NO3、SO32
9.某反应A+B=C+D在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确
的是()
A.△H<0,△S>0
B.△H>0,△S>0
C.△H<0,△$<0
D.△H>0,△S<0
10.设Na为阿伏加德罗常数的值,下列说法正确的是(
)
A.0,1 mol-L-!Ba(OH)2溶液中含有OH的数目为0.2Wa
B.49.5gCOC2中的碳氯键数目为NA
C.31gP4中的共价键数目为NA
D.120 g NaHSO4和KHSO3的水溶液中含有的阳离子数为Na
11.X、Y、Z、W为短周期元素,X2和Y+核外电子排布相同,X、Z位于同一主族,Y、Z、W位于同一
周期,W的最外层电子数是X、Y最外层电子数之和。下列说法不正确的是()
A.离子半径:Z>X>Y
B.第一电离能:Y
D.X、Y、Z、W核电荷数逐渐增大
12.已知儿种化学键的键能和热化学方程式如下:
化学键
H-N
NN
CICI
NEN
H-CI
键能/kJ'mol厂)
391
193
243
946
432
NH4(g)+2C2(g)=N2(g)+4HC1(g)△H,下列推断正确的是()
A.H(g)+Cl(g)=HCI(g)=+432 kJ-mol
B.断裂1 molHCI键吸收能量比断裂1molN三N键多514kJ
C.上述反应中,△H=-431kJmo1
D.上述反应中,断裂极性键和非极性键,只形成极性键
13.某温度下,向2L密闭容器中通入1 mol NO和0.5molB2,发生如下反应:
2NO(g+Br2(g)=2NOBr(g),B2的物质的量随时间变化的实验数据如下表:
时间min
5
10
15
20
25
30
35
高二化学学科试题
第2页(共8页)
同课章节目录
