9.3溶液的浓度(第一课时)课件(共18张PPT)—2022-2023学年九年级化学人教版下册
文档属性
| 名称 | 9.3溶液的浓度(第一课时)课件(共18张PPT)—2022-2023学年九年级化学人教版下册 |
|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-29 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
素养目标
认识溶质的质量分数的含义。
能进行有关溶质的质量分数的简单计算。
通过质量分数的计算,引导学生查看商标的标签,认识化学在生活中的意义。
素养
目标
1
2
3
新课导入
比较三种CuSO4溶液的颜色。
在这三支试管中溶液的组成是否相同
判断溶液浓稀的根据是什么
新课导入
飞机喷洒农药
喷洒药水
药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木。
知识点1 溶质的质量分数及综合计算
溶质的质量分数表达式
溶质的质量
溶液的质量
×
100%
溶质的质量
溶质的质量+溶剂的质量
×
100%
千万别丢下我啊! 谢谢噢!
定义:溶质质量与溶液质量之比
溶质的质量分数:表示溶液组成的一种方法
知识点1 溶质的质量分数及综合计算
溶质的质量分数36% 是指:
请问溶质的质量分数与溶解度有什么区别?
100克溶液中含有36克溶质。
溶质T ℃时溶解度36克是指:
在T℃ 时,100克水最多溶解该溶质36克。溶液质量应该为136克。
溶质质量分数 溶解度
意义
温度
溶剂量
是否饱和
单位
关系式
知识点1 溶质的质量分数及综合计算
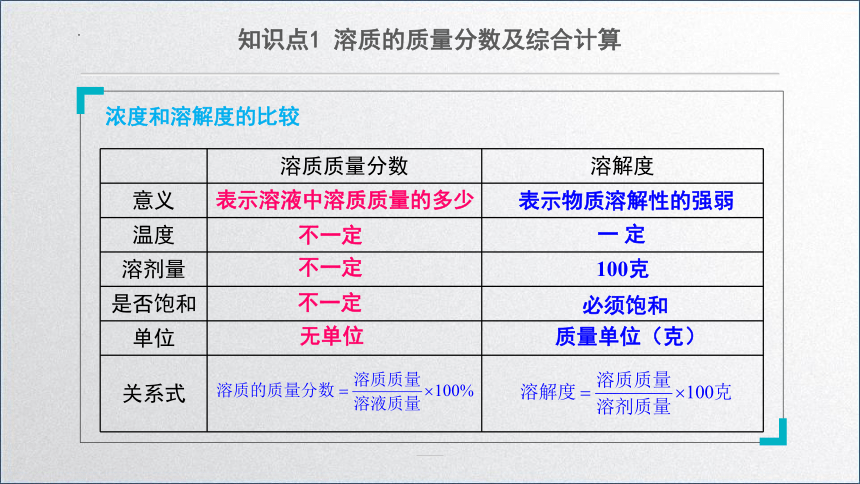
表示溶液中溶质质量的多少
表示物质溶解性的强弱
不一定
一 定
不一定
不一定
100克
无单位
必须饱和
质量单位(克)
浓度和溶解度的比较
知识点1 溶质的质量分数及综合计算
×100%
溶质质量分数 =
溶质质量分数和溶解度(S)的转化
知识点1 溶质的质量分数及综合计算
算一算:
溶质质量/g 溶剂质量/g 溶液质量/g 溶质的质量分数
10 200
96 100
150 10%
50 100
190
5%
4%
15
135
150
33.3%
4
m液 = m质 + m剂
m质 = m液 × 溶质的质量分数
知识点1 溶质的质量分数及综合计算
【思考题】
实验1:称取10 g白糖倒入一烧杯中,加入40 g水,搅拌使白糖全部溶解。
实验2:称取12 g白糖于另一烧杯中,加入48 g水,搅拌使白糖全部溶解。
问题:实验1、2所得两份糖水,谁更甜?你的依据是什么?
实验1:白糖浓度 = 100% = 20%
实验2:白糖浓度 = 100% = 20%
实验1、2两份糖水浓度相同,故一样甜。
知识点1 溶质的质量分数及综合计算
【例题】
在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg这种溶液,需要氯化钠和水的质量各是多少?
溶质质量分数=×100%
溶质质量=溶液质量×溶质质量分数
溶剂质量=溶液质量-溶质质量
=150 kg×16%=24 kg
=150 kg-24 kg=126 kg
【解】
答:配制150 kg这种溶液,需要氯化钠24 kg和水126 kg。
知识点1 溶质的质量分数及综合计算
有关溶液稀释或浓缩的计算
计算的依据:溶质不变
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
公式:m浓×c浓%=m稀×c稀%
知识点1 溶质的质量分数及综合计算
【例题】
将100 g溶质质量分数为20%的蔗糖溶液稀释到10%,需要加入水的质量是多少?
m浓×c浓%=m稀×c稀%
100 g×20%
=(100+x)g ×10%
【解】设加入水的质量为x g。
答:需要加入水的质量是100 g。
x = 100 g
课堂练习
1.将50 g98%的浓硫酸溶于450 g水中,所得溶液中溶质质量分数为( )
A.9.8% B.10.2% C.10.8% D.19.6%
A
课堂练习
2.现有一杯20℃的硝酸钾饱和溶液,欲改变其溶质质量分数,下列方法可行的是( )
A.加入一定量的硝酸钾
B.恒温蒸发部分水
C.升温到60℃
D.加入一定量的水
D
课堂练习
3.在100 g稀硫酸中加入适量的锌粒后二者恰好完全反应,溶液的质量减少0.4 g。最后反应所得溶液的溶质质量分数是多少?(保留到小数点后一位)
解:溶液的质量减少0.4 g,所以氢气的质量就为0.4 g。
设参加反应的锌质量为x,生成ZnSO4的质量为y。
Zn + H2SO4 ==== ZnSO4 + H2↑
65 161 2
x y 0.4 g
解得:x=13.0 g,y=32.2 g。
所以溶质的质量分数为:32.2 g÷(100 g+13 g-0.4 g)×100%≈28.6%
答:最后反应所得溶液的溶质质量分数是28.6%。
课堂小结
作业布置
生活中你们都见过哪些溶液,请你们找到溶液标签、记录的内容并计算其中各种溶质的含量。
本课结束 谢谢观看
素养目标
认识溶质的质量分数的含义。
能进行有关溶质的质量分数的简单计算。
通过质量分数的计算,引导学生查看商标的标签,认识化学在生活中的意义。
素养
目标
1
2
3
新课导入
比较三种CuSO4溶液的颜色。
在这三支试管中溶液的组成是否相同
判断溶液浓稀的根据是什么
新课导入
飞机喷洒农药
喷洒药水
药液太稀不能杀死害虫和病菌,但药液太浓又会毒害农作物或树木。
知识点1 溶质的质量分数及综合计算
溶质的质量分数表达式
溶质的质量
溶液的质量
×
100%
溶质的质量
溶质的质量+溶剂的质量
×
100%
千万别丢下我啊! 谢谢噢!
定义:溶质质量与溶液质量之比
溶质的质量分数:表示溶液组成的一种方法
知识点1 溶质的质量分数及综合计算
溶质的质量分数36% 是指:
请问溶质的质量分数与溶解度有什么区别?
100克溶液中含有36克溶质。
溶质T ℃时溶解度36克是指:
在T℃ 时,100克水最多溶解该溶质36克。溶液质量应该为136克。
溶质质量分数 溶解度
意义
温度
溶剂量
是否饱和
单位
关系式
知识点1 溶质的质量分数及综合计算
表示溶液中溶质质量的多少
表示物质溶解性的强弱
不一定
一 定
不一定
不一定
100克
无单位
必须饱和
质量单位(克)
浓度和溶解度的比较
知识点1 溶质的质量分数及综合计算
×100%
溶质质量分数 =
溶质质量分数和溶解度(S)的转化
知识点1 溶质的质量分数及综合计算
算一算:
溶质质量/g 溶剂质量/g 溶液质量/g 溶质的质量分数
10 200
96 100
150 10%
50 100
190
5%
4%
15
135
150
33.3%
4
m液 = m质 + m剂
m质 = m液 × 溶质的质量分数
知识点1 溶质的质量分数及综合计算
【思考题】
实验1:称取10 g白糖倒入一烧杯中,加入40 g水,搅拌使白糖全部溶解。
实验2:称取12 g白糖于另一烧杯中,加入48 g水,搅拌使白糖全部溶解。
问题:实验1、2所得两份糖水,谁更甜?你的依据是什么?
实验1:白糖浓度 = 100% = 20%
实验2:白糖浓度 = 100% = 20%
实验1、2两份糖水浓度相同,故一样甜。
知识点1 溶质的质量分数及综合计算
【例题】
在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg这种溶液,需要氯化钠和水的质量各是多少?
溶质质量分数=×100%
溶质质量=溶液质量×溶质质量分数
溶剂质量=溶液质量-溶质质量
=150 kg×16%=24 kg
=150 kg-24 kg=126 kg
【解】
答:配制150 kg这种溶液,需要氯化钠24 kg和水126 kg。
知识点1 溶质的质量分数及综合计算
有关溶液稀释或浓缩的计算
计算的依据:溶质不变
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
公式:m浓×c浓%=m稀×c稀%
知识点1 溶质的质量分数及综合计算
【例题】
将100 g溶质质量分数为20%的蔗糖溶液稀释到10%,需要加入水的质量是多少?
m浓×c浓%=m稀×c稀%
100 g×20%
=(100+x)g ×10%
【解】设加入水的质量为x g。
答:需要加入水的质量是100 g。
x = 100 g
课堂练习
1.将50 g98%的浓硫酸溶于450 g水中,所得溶液中溶质质量分数为( )
A.9.8% B.10.2% C.10.8% D.19.6%
A
课堂练习
2.现有一杯20℃的硝酸钾饱和溶液,欲改变其溶质质量分数,下列方法可行的是( )
A.加入一定量的硝酸钾
B.恒温蒸发部分水
C.升温到60℃
D.加入一定量的水
D
课堂练习
3.在100 g稀硫酸中加入适量的锌粒后二者恰好完全反应,溶液的质量减少0.4 g。最后反应所得溶液的溶质质量分数是多少?(保留到小数点后一位)
解:溶液的质量减少0.4 g,所以氢气的质量就为0.4 g。
设参加反应的锌质量为x,生成ZnSO4的质量为y。
Zn + H2SO4 ==== ZnSO4 + H2↑
65 161 2
x y 0.4 g
解得:x=13.0 g,y=32.2 g。
所以溶质的质量分数为:32.2 g÷(100 g+13 g-0.4 g)×100%≈28.6%
答:最后反应所得溶液的溶质质量分数是28.6%。
课堂小结
作业布置
生活中你们都见过哪些溶液,请你们找到溶液标签、记录的内容并计算其中各种溶质的含量。
本课结束 谢谢观看
同课章节目录
