化学人教版九下:9.3溶液的浓度(第二课时)作业(含解析)
文档属性
| 名称 | 化学人教版九下:9.3溶液的浓度(第二课时)作业(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 329.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 00:00:00 | ||
图片预览

文档简介
9.3 溶液的浓度(第二课时)
一、选择题
1.用密度为1.03 g·cm-3,质量分数为5%的食盐溶液配制成50 g质量分数为1%的食盐溶液,其操作顺序为( )
A.量取→溶解→计算 B.称量→溶解→计算
C.计算→称量→溶解 D.计算→量取→溶解
2.配制质量分数为20%的某盐溶液,需向100 g水中所加盐的质量是( )
A.20克 B.25克 C.10克 D.40克
3.实验室有下列仪器: ①烧杯 ②量筒 ③药匙 ④托盘天平 ⑤玻璃棒 ⑥漏斗 ⑦蒸发皿。配制一定溶质质量分数的氯化钠溶液必须用到的仪器是( )
A.①②③④⑤ B.①③④⑤ C.⑤⑥⑦ D.全部
4.为了救治病人,需要配制生理盐水(质量分数为0.9%)1000 g,下列配制过程正确的是( )
A.只需要托盘天平和量筒两种仪器 B.用托盘天平称取9 g氯化钠
C.配制生理盐水可以用粗盐 D.用量筒量取1000 mL水
5.为防止灾区疾病传染,需对灾区喷洒消毒剂,进行医疗卫生防疫。质量分数为0.2%~1%的过氧乙酸就是用于环境喷洒和用具浸泡的一种消毒剂。现有市售质量分数为20%的过氧乙酸,要配制1%的过氧乙酸10 kg,需要市售过氧乙酸的质量为( )
A.1 000 g B.500 g C.100 g D.50 g
6.现配制溶质质量分数为5%的NaCl溶液100 g,下列操作错误的图示是( )
A.取用氯化钠固体 B.量取蒸馏水 C.氯化钠溶解 D.溶液装瓶贴签
7.在化学实验操作考查中,小阳同学抽到的考题是“配制50 g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是 ( )
选项 实验操作 目的分析
A 称取氯化钠时,指针向右偏,调节游码至天平平衡 准确称量氯化钠质量
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
8.误差分析是定量实验的一个重要内容。下列有关配制溶液的误差分析,正确的是( )
A.用量筒量取10 mL水,仰视读数,会导致水的实际体积偏小
B.用托盘天平称取10.5 g氯化钠,药品和砝码放反,会导致最终的质量分数偏小
C.按要求配制好的溶液装瓶时洒出一部分会影响溶液的质量分数
D.量筒中的水倒入烧杯中时,有部分残留,导致最终的质量分数偏小
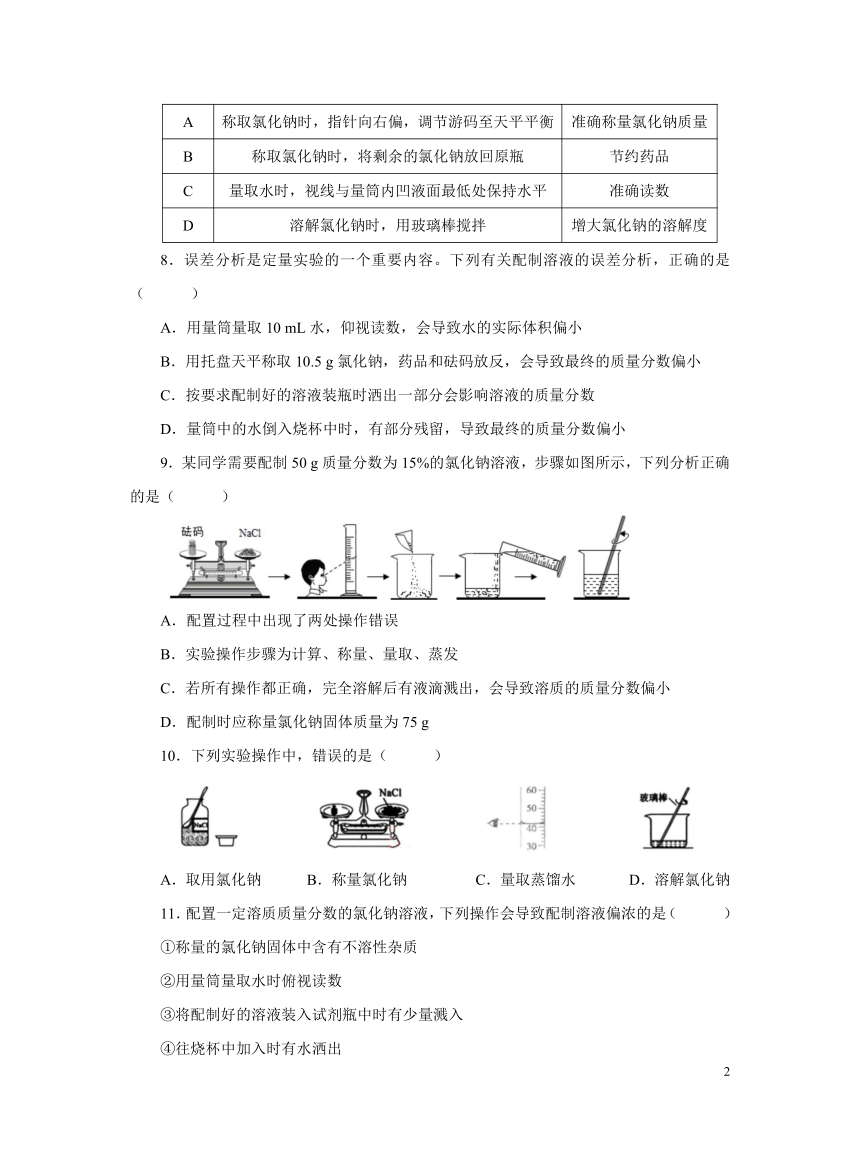
9.某同学需要配制50 g质量分数为15%的氯化钠溶液,步骤如图所示,下列分析正确的是( )
A.配置过程中出现了两处操作错误
B.实验操作步骤为计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为75 g
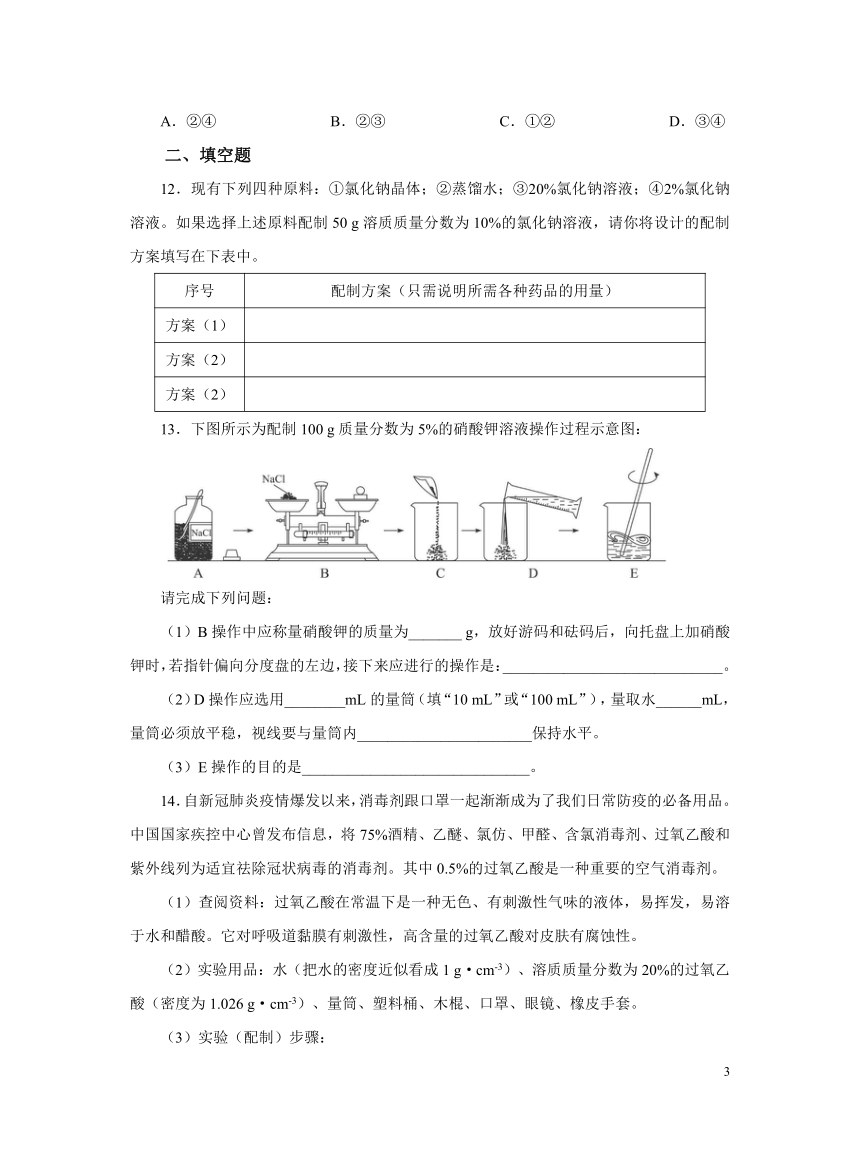
10.下列实验操作中,错误的是( )
A.取用氯化钠 B.称量氯化钠 C.量取蒸馏水 D.溶解氯化钠
11.配置一定溶质质量分数的氯化钠溶液,下列操作会导致配制溶液偏浓的是( )
①称量的氯化钠固体中含有不溶性杂质
②用量筒量取水时俯视读数
③将配制好的溶液装入试剂瓶中时有少量溅入
④往烧杯中加入时有水洒出
A.②④ B.②③ C.①② D.③④
二、填空题
12.现有下列四种原料:①氯化钠晶体;②蒸馏水;③20%氯化钠溶液;④2%氯化钠溶液。如果选择上述原料配制50 g溶质质量分数为10%的氯化钠溶液,请你将设计的配制方案填写在下表中。
序号 配制方案(只需说明所需各种药品的用量)
方案(1)
方案(2)
方案(2)
13.下图所示为配制100 g质量分数为5%的硝酸钾溶液操作过程示意图:
请完成下列问题:
(1)B操作中应称量硝酸钾的质量为_______ g,放好游码和砝码后,向托盘上加硝酸钾时,若指针偏向分度盘的左边,接下来应进行的操作是:_____________________________。
(2)D操作应选用________mL的量筒(填“10 mL”或“100 mL”),量取水______mL,量筒必须放平稳,视线要与量筒内_______________________保持水平。
(3)E操作的目的是______________________________。
14.自新冠肺炎疫情爆发以来,消毒剂跟口罩一起渐渐成为了我们日常防疫的必备用品。中国国家疾控中心曾发布信息,将75%酒精、乙醚、氯仿、甲醛、含氯消毒剂、过氧乙酸和紫外线列为适宜祛除冠状病毒的消毒剂。其中0.5%的过氧乙酸是一种重要的空气消毒剂。
(1)查阅资料:过氧乙酸在常温下是一种无色、有刺激性气味的液体,易挥发,易溶于水和醋酸。它对呼吸道黏膜有刺激性,高含量的过氧乙酸对皮肤有腐蚀性。
(2)实验用品:水(把水的密度近似看成1 g·cm-3)、溶质质量分数为20%的过氧乙酸(密度为1.026 g·cm-3)、量筒、塑料桶、木棍、口罩、眼镜、橡皮手套。
(3)实验(配制)步骤:
①计算配制比例:将200 mL 20%的过氧乙酸稀释为0.5%的过氧乙酸,需要加水的体积为_______ mL,过氧乙酸与水的配制比例为__________;
②配制时要戴好防护用品,因为过氧乙酸有__________性;
③应用规格为_________mL的量筒量取20%的过氧乙酸,并倒入塑料桶里,按比例加水,用_________搅拌后,盖好桶盖待用。
(4)反思应用:
①过氧乙酸(填“能”或“不能”)_______用铁制容器盛装,原因是____________________;
②不慎让高含量的过氧乙酸沾到皮肤上,应该如何处理?_________________________。
参考答案与解析
一、选择题
1.D
【解析】首先进行计算,看需要密度为1.03 g·cm-3,质量分数为5%的食盐溶液的体积多少毫升,需要蒸馏水多少毫升(蒸馏水的密度为1 g·mol-1)。然后根据计算结果进行溶液的量取,最后把量取的两液体混合。即得到50 g质量分数为1%的食盐溶液。故选D。
2.B
【解析】设加入盐的质量为x,则x/(100 g+x)=20%,x=25 g。故选B。
3.A
【解析】根据配制一定溶质质量分数溶液的实验步骤是①计算;②称量:用到托盘天平、量筒;③溶解:用到烧杯、玻璃棒、药匙。故选A。
4.B
【解析】利用固体溶质配制溶液,步骤为:计算所需固体的质量和水的质量,称量固体溶质的质量并量取蒸馏水的体积、溶解。应该使用托盘天平、烧杯、量筒、玻璃棒。水的体积应该为991毫升。配制时只能使用精盐。故选B。
5.B
【解析】本题是一道稀释问题的计算型选择题,根据稀释前后溶质的质量不变,设需要市售过氧乙酸的质量为x,则x×20%=10 kg×1%,x=0.5 kg=500 g。故选B。
6.A
【解析】实验室的药品有毒或腐蚀性,不可以用手直接取用,图中操作错误。故选A。
7.C
【解析】量取水时,事先与量筒内凹液面的最低处保持水平,是为了准确读数。故选C。
8.B
【解析】用托盘天平称取10.5 g氯化钠,药品和砝码放反,会造成实际所取得溶质的质量偏小,会导致最终的质量分数偏小。故选B。
9.A
【解析】托盘天平的使用遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度;配制过程中出现了两处操作错误。故选A。
10.A
【解析】试剂瓶塞应倒放在桌面上,故A错误;使用托盘天平称量药瓶应左物右码,故B正确;量筒量取液体与凹液面最低处保持水平,故C正确;用玻璃棒搅拌溶解,故D正确。故选D。
11.A
【解析】配置一定溶质质量分数的氯化钠溶液,下列操作会导致配制溶液偏浓的是:用量筒量取水时俯视读数;往烧杯中加入时有水洒出。故选A。
二、填空题
12.方案(1):NaCl晶体5 g,蒸馏水45 g;
方案(2):25 g20%的NaCl溶液,25 g蒸馏水;
方案(3):22.2 g20%的NaCl溶液,27.8 g 2%的NaCl溶液。
【解析】可以利用溶液的配制方法,再进行计算。
13.(1)5;减少一些硝酸钾固体,直至天平平衡;(2)100;95;凹液面的最低处;(3)加快硝酸钾固体的溶解。
【解析】依据溶质质量分数的溶液配制方法解答。
14.(3)①7800;1∶39;②挥发性和腐蚀性;③200;木棍;(4)①不能;过氧乙酸会与铁发生反应;②可立即用大量的水冲洗。
【解析】根据溶质质量分数计算公式、过氧乙酸的物理性质以及化学性质即可解答此题。
1
一、选择题
1.用密度为1.03 g·cm-3,质量分数为5%的食盐溶液配制成50 g质量分数为1%的食盐溶液,其操作顺序为( )
A.量取→溶解→计算 B.称量→溶解→计算
C.计算→称量→溶解 D.计算→量取→溶解
2.配制质量分数为20%的某盐溶液,需向100 g水中所加盐的质量是( )
A.20克 B.25克 C.10克 D.40克
3.实验室有下列仪器: ①烧杯 ②量筒 ③药匙 ④托盘天平 ⑤玻璃棒 ⑥漏斗 ⑦蒸发皿。配制一定溶质质量分数的氯化钠溶液必须用到的仪器是( )
A.①②③④⑤ B.①③④⑤ C.⑤⑥⑦ D.全部
4.为了救治病人,需要配制生理盐水(质量分数为0.9%)1000 g,下列配制过程正确的是( )
A.只需要托盘天平和量筒两种仪器 B.用托盘天平称取9 g氯化钠
C.配制生理盐水可以用粗盐 D.用量筒量取1000 mL水
5.为防止灾区疾病传染,需对灾区喷洒消毒剂,进行医疗卫生防疫。质量分数为0.2%~1%的过氧乙酸就是用于环境喷洒和用具浸泡的一种消毒剂。现有市售质量分数为20%的过氧乙酸,要配制1%的过氧乙酸10 kg,需要市售过氧乙酸的质量为( )
A.1 000 g B.500 g C.100 g D.50 g
6.现配制溶质质量分数为5%的NaCl溶液100 g,下列操作错误的图示是( )
A.取用氯化钠固体 B.量取蒸馏水 C.氯化钠溶解 D.溶液装瓶贴签
7.在化学实验操作考查中,小阳同学抽到的考题是“配制50 g质量分数为6%的氯化钠溶液”,小阳的实验操作与目的分析均正确的一组是 ( )
选项 实验操作 目的分析
A 称取氯化钠时,指针向右偏,调节游码至天平平衡 准确称量氯化钠质量
B 称取氯化钠时,将剩余的氯化钠放回原瓶 节约药品
C 量取水时,视线与量筒内凹液面最低处保持水平 准确读数
D 溶解氯化钠时,用玻璃棒搅拌 增大氯化钠的溶解度
8.误差分析是定量实验的一个重要内容。下列有关配制溶液的误差分析,正确的是( )
A.用量筒量取10 mL水,仰视读数,会导致水的实际体积偏小
B.用托盘天平称取10.5 g氯化钠,药品和砝码放反,会导致最终的质量分数偏小
C.按要求配制好的溶液装瓶时洒出一部分会影响溶液的质量分数
D.量筒中的水倒入烧杯中时,有部分残留,导致最终的质量分数偏小
9.某同学需要配制50 g质量分数为15%的氯化钠溶液,步骤如图所示,下列分析正确的是( )
A.配置过程中出现了两处操作错误
B.实验操作步骤为计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为75 g
10.下列实验操作中,错误的是( )
A.取用氯化钠 B.称量氯化钠 C.量取蒸馏水 D.溶解氯化钠
11.配置一定溶质质量分数的氯化钠溶液,下列操作会导致配制溶液偏浓的是( )
①称量的氯化钠固体中含有不溶性杂质
②用量筒量取水时俯视读数
③将配制好的溶液装入试剂瓶中时有少量溅入
④往烧杯中加入时有水洒出
A.②④ B.②③ C.①② D.③④
二、填空题
12.现有下列四种原料:①氯化钠晶体;②蒸馏水;③20%氯化钠溶液;④2%氯化钠溶液。如果选择上述原料配制50 g溶质质量分数为10%的氯化钠溶液,请你将设计的配制方案填写在下表中。
序号 配制方案(只需说明所需各种药品的用量)
方案(1)
方案(2)
方案(2)
13.下图所示为配制100 g质量分数为5%的硝酸钾溶液操作过程示意图:
请完成下列问题:
(1)B操作中应称量硝酸钾的质量为_______ g,放好游码和砝码后,向托盘上加硝酸钾时,若指针偏向分度盘的左边,接下来应进行的操作是:_____________________________。
(2)D操作应选用________mL的量筒(填“10 mL”或“100 mL”),量取水______mL,量筒必须放平稳,视线要与量筒内_______________________保持水平。
(3)E操作的目的是______________________________。
14.自新冠肺炎疫情爆发以来,消毒剂跟口罩一起渐渐成为了我们日常防疫的必备用品。中国国家疾控中心曾发布信息,将75%酒精、乙醚、氯仿、甲醛、含氯消毒剂、过氧乙酸和紫外线列为适宜祛除冠状病毒的消毒剂。其中0.5%的过氧乙酸是一种重要的空气消毒剂。
(1)查阅资料:过氧乙酸在常温下是一种无色、有刺激性气味的液体,易挥发,易溶于水和醋酸。它对呼吸道黏膜有刺激性,高含量的过氧乙酸对皮肤有腐蚀性。
(2)实验用品:水(把水的密度近似看成1 g·cm-3)、溶质质量分数为20%的过氧乙酸(密度为1.026 g·cm-3)、量筒、塑料桶、木棍、口罩、眼镜、橡皮手套。
(3)实验(配制)步骤:
①计算配制比例:将200 mL 20%的过氧乙酸稀释为0.5%的过氧乙酸,需要加水的体积为_______ mL,过氧乙酸与水的配制比例为__________;
②配制时要戴好防护用品,因为过氧乙酸有__________性;
③应用规格为_________mL的量筒量取20%的过氧乙酸,并倒入塑料桶里,按比例加水,用_________搅拌后,盖好桶盖待用。
(4)反思应用:
①过氧乙酸(填“能”或“不能”)_______用铁制容器盛装,原因是____________________;
②不慎让高含量的过氧乙酸沾到皮肤上,应该如何处理?_________________________。
参考答案与解析
一、选择题
1.D
【解析】首先进行计算,看需要密度为1.03 g·cm-3,质量分数为5%的食盐溶液的体积多少毫升,需要蒸馏水多少毫升(蒸馏水的密度为1 g·mol-1)。然后根据计算结果进行溶液的量取,最后把量取的两液体混合。即得到50 g质量分数为1%的食盐溶液。故选D。
2.B
【解析】设加入盐的质量为x,则x/(100 g+x)=20%,x=25 g。故选B。
3.A
【解析】根据配制一定溶质质量分数溶液的实验步骤是①计算;②称量:用到托盘天平、量筒;③溶解:用到烧杯、玻璃棒、药匙。故选A。
4.B
【解析】利用固体溶质配制溶液,步骤为:计算所需固体的质量和水的质量,称量固体溶质的质量并量取蒸馏水的体积、溶解。应该使用托盘天平、烧杯、量筒、玻璃棒。水的体积应该为991毫升。配制时只能使用精盐。故选B。
5.B
【解析】本题是一道稀释问题的计算型选择题,根据稀释前后溶质的质量不变,设需要市售过氧乙酸的质量为x,则x×20%=10 kg×1%,x=0.5 kg=500 g。故选B。
6.A
【解析】实验室的药品有毒或腐蚀性,不可以用手直接取用,图中操作错误。故选A。
7.C
【解析】量取水时,事先与量筒内凹液面的最低处保持水平,是为了准确读数。故选C。
8.B
【解析】用托盘天平称取10.5 g氯化钠,药品和砝码放反,会造成实际所取得溶质的质量偏小,会导致最终的质量分数偏小。故选B。
9.A
【解析】托盘天平的使用遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了;量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度;配制过程中出现了两处操作错误。故选A。
10.A
【解析】试剂瓶塞应倒放在桌面上,故A错误;使用托盘天平称量药瓶应左物右码,故B正确;量筒量取液体与凹液面最低处保持水平,故C正确;用玻璃棒搅拌溶解,故D正确。故选D。
11.A
【解析】配置一定溶质质量分数的氯化钠溶液,下列操作会导致配制溶液偏浓的是:用量筒量取水时俯视读数;往烧杯中加入时有水洒出。故选A。
二、填空题
12.方案(1):NaCl晶体5 g,蒸馏水45 g;
方案(2):25 g20%的NaCl溶液,25 g蒸馏水;
方案(3):22.2 g20%的NaCl溶液,27.8 g 2%的NaCl溶液。
【解析】可以利用溶液的配制方法,再进行计算。
13.(1)5;减少一些硝酸钾固体,直至天平平衡;(2)100;95;凹液面的最低处;(3)加快硝酸钾固体的溶解。
【解析】依据溶质质量分数的溶液配制方法解答。
14.(3)①7800;1∶39;②挥发性和腐蚀性;③200;木棍;(4)①不能;过氧乙酸会与铁发生反应;②可立即用大量的水冲洗。
【解析】根据溶质质量分数计算公式、过氧乙酸的物理性质以及化学性质即可解答此题。
1
同课章节目录
