人教版化学九下:9.2 溶解度(第1课时)课件(共28张PPT)
文档属性
| 名称 | 人教版化学九下:9.2 溶解度(第1课时)课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第九单 溶液
课题2 溶解度
第1课时
饱和溶液与不饱和溶液的转化方法
2
结晶
3
饱和溶液与不饱和溶液
1
本节重点
本节难点
还能再坐人吗?
等等我
不能,火车已超载
将溶质溶解到一定量溶剂里面也会出现“超载”的现象吗?
在室温下,向盛有20 mL水的烧杯中加入5 g氯化钠,搅拌;等溶解后,再加5 g氯化钠,搅拌,观察现象。然后再加入15 mL水,搅拌,观察现象。
实验探究一
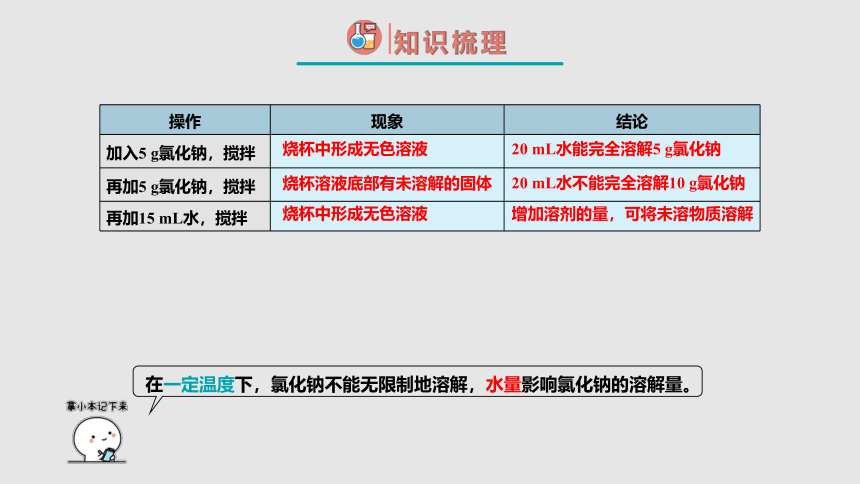
操作 现象 结论
加入5 g氯化钠,搅拌
再加5 g氯化钠,搅拌
再加15 mL水,搅拌
烧杯中形成无色溶液
20 mL水能完全溶解5 g氯化钠
烧杯溶液底部有未溶解的固体
20 mL水不能完全溶解10 g氯化钠
烧杯中形成无色溶液
增加溶剂的量,可将未溶物质溶解
在一定温度下,氯化钠不能无限制地溶解,水量影响氯化钠的溶解量。
在室温下,向盛有20 mL水的烧杯中加入5 g硝酸钾,搅拌;等溶解后,再加5 g硝酸钾,搅拌,观察现象。当烧杯中硝酸钾固体有剩余而不再继续溶解时,加热烧杯一段时间,观察剩余固体有什么变化。然后再加入5 g硝酸钾,搅拌,观察现象。待溶液冷却后,又有什么现象发生?
实验探究二
操作 现象 结论
加入5 g硝酸钾,搅拌
再加5 g硝酸钾,搅拌
加热
再加5 g硝酸钾,搅拌
冷却
烧杯中形成无色溶液
烧杯溶液底部有未溶解的固体
20 mL水能完全溶解5 g硝酸钾
20 mL水不能完全溶解10 g硝酸钾
未溶解的固体溶解了,烧杯中形成无色溶液
温度升高,硝酸钾溶解能力增强
溶液为不饱和溶液
烧杯中形成无色溶液
温度降低,硝酸钾溶解能力减小
有固体从溶液中析出来
在一定量的水中,硝酸钾也不能无限制地溶解在水中,温度影响硝酸钾的溶解量。
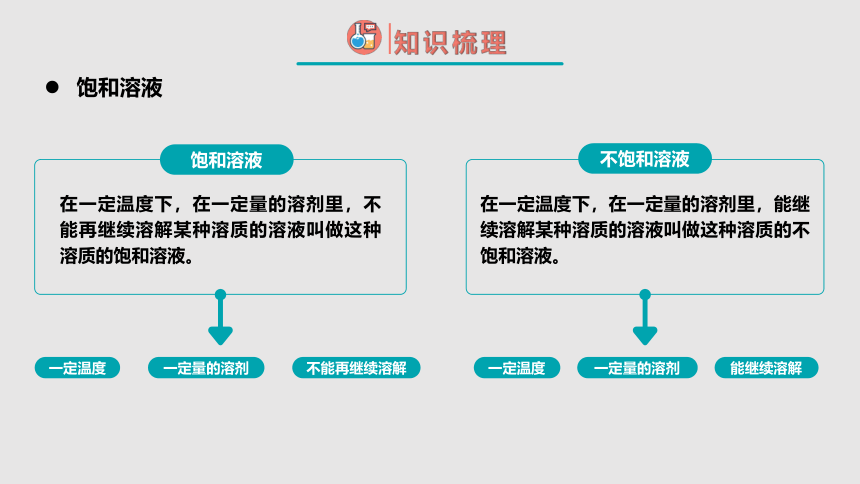
饱和溶液
在一定温度下,在一定量的溶剂里,能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液。
不饱和溶液
饱和溶液
在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液叫做这种溶质的饱和溶液。
一定温度
一定量的溶剂
不能再继续溶解
一定温度
一定量的溶剂
能继续溶解
能,饱和溶液是相对于一定温度、一定溶剂和某种溶质,再加入其他溶质仍能继续溶解。
向一定温度下的氯化钠饱和溶液中再加入少量硝酸钾,能溶解吗?
判断溶液是否饱和的方法
概念上:
外观上:
判断溶质是否还能继续溶解。
如果溶液底部存在未溶完的物质,说明溶液在此温度下,不能再溶解该物质,肯定是饱和溶液;
如果溶液中不存在未溶完的固体,那么所得的溶液可能是饱和溶液。
硝酸钾不能继续溶解后我们怎样使加入的硝酸钾固体又溶解了?
如何使接近饱和的硝酸钾溶液变成饱和溶液?有没有办法使溶剂减少一些?具体可以怎样操作?
加热
加水
加入硝酸钾固体
蒸发溶剂
请同学们回顾实验,思考并回答下列问题:
问题1
问题2
饱和溶液和不饱和溶液的相互转化
不饱和溶液
饱和溶液
降温
蒸发溶剂
增加溶质
升温
增加溶剂
最简单且适用于任何溶液的方法
饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
饱和溶液与不饱和溶液 浓溶液与稀溶液
区别 含义不同
温度影响
关系 在相同温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液的浓度大。
溶液是否饱和取决于溶质在一定温度下、一定量溶剂里的含量是否达到最大限度
溶液的浓与稀取决于溶质在一定量的溶液里含量的相对多少
受温度影响,必须指明温度
与温度无关
溶液的饱和和不饱和与溶液的浓和稀没有必然的关系。
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定不饱和溶液。
浓溶液
稀溶液
饱和溶液
不饱和溶液
【例1】室温下,向一定质量的氯化钠溶液中加入10 g氯化钠固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解。下列判断正确的是( )
A.加水前一定是饱和溶液
B.加氯化钠前可能是饱和溶液
C.加水后一定是饱和溶液
D.加水后一定是不饱和溶液
A
【例2】室温下,将盛有接近饱和的硝酸钾溶液的小烧杯放在盛水的大烧杯中,如图所示,欲使硝酸钾溶液变为饱和溶液,可向大烧杯中加入的固体物质是( )
A.生石灰 B.氯化钠 C.硝酸铵 D.氢氧化钠
C
烧杯底部出现固体
冷却热的饱和溶液时,硝酸钾晶体从溶液中析出
热的硝酸钾溶液
硝酸钾溶液为饱和溶液
结晶
硝酸钾晶体
冷却
继
续
降
低
硝酸钾溶液为不饱和溶液
这种获得结晶的方法称之为:冷却热的饱和溶液(降温结晶)
你知道海水晒盐吗?
海水晒盐的过程
氯化钠
海水
贮水池
蒸发池
结晶池
粗盐
母液
(苦卤)
多种化工产品
蒸发溶剂(蒸发结晶)
这种获得结晶的方法称之为:
(沉降泥沙)
(蒸发水分)
(蒸发水分)
(氯化钠的饱和溶液)
海水晒盐过程中,有哪些环节得到的溶液一定是饱和溶液?
结晶池
母液
【例1】下列有关结晶的说法正确的是( )
A.饱和溶液降低温度一定会析出晶体
B.只有蒸发溶剂才会出现结晶现象
C.腌菜晾晒时表面出现很多小晶体,是因为发生化学变化
D.析出晶体后的溶液一定是饱和溶液
D
【例2】海水晒盐是海水在常温下蒸发得到氯化钠的过程。小露用氯化钠溶液模拟该过程,如图所示:
(1)乙烧杯中的溶液________(填“是”“不是”或“可能是”)氯化钠饱和溶液。
(2)要使氯化钠晶体从溶液中析出,常采用的方法是____________。
可能是
蒸发结晶
雪花结晶的过程
1.下列说法正确的是( )
A.饱和溶液一定是浓溶液
B.不饱和溶液转化为饱和溶液,溶质的质量可能不变
C.向某种溶质的饱和溶液中再加入这种溶质,溶液质量会增加
D.对同一种溶质来讲,饱和溶液一定比不饱和溶液浓
B
2.要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法,其中可行的是( )
①加入CaO ②加入Ca(OH)2 ③升高温度 ④降低温度
A.②③ B.②④ C.①②③ D.①②④
C
3.下图是利用海水提取粗盐的过程:
(1) 上页图中①是______池(填“蒸发”或“冷却”)。
(2) 根据海水晒盐的原理,下列说法中正确的是( )
A. 海水进入贮水池,海水的成分基本不变
B. 在①中,海水中氯化钠的质量逐渐增加
C. 在①中,海水中水的质量逐渐减少
D. 析出晶体后的母液是氯化纳的不饱和溶液
海水
贮水池
①
结晶池
粗盐
母液
氯化钠
多种化工产品
蒸发
A、C
5. 为什么汗水带有咸味?被汗水浸湿的衣服晾干后,常出现白色的斑迹。这是为什么?
汗水中含有一些盐,如氯化钠,因此有咸味;被汗水浸湿的衣服晾干后水分蒸发了,但盐分仍留在衣服上,就形成了白色斑迹。
课题2 溶解度
第1课时
饱和溶液
定义
判断方法
饱和溶液与不饱和溶液之间的转化
结晶及结晶的方法
第九单 溶液
课题2 溶解度
第1课时
饱和溶液与不饱和溶液的转化方法
2
结晶
3
饱和溶液与不饱和溶液
1
本节重点
本节难点
还能再坐人吗?
等等我
不能,火车已超载
将溶质溶解到一定量溶剂里面也会出现“超载”的现象吗?
在室温下,向盛有20 mL水的烧杯中加入5 g氯化钠,搅拌;等溶解后,再加5 g氯化钠,搅拌,观察现象。然后再加入15 mL水,搅拌,观察现象。
实验探究一
操作 现象 结论
加入5 g氯化钠,搅拌
再加5 g氯化钠,搅拌
再加15 mL水,搅拌
烧杯中形成无色溶液
20 mL水能完全溶解5 g氯化钠
烧杯溶液底部有未溶解的固体
20 mL水不能完全溶解10 g氯化钠
烧杯中形成无色溶液
增加溶剂的量,可将未溶物质溶解
在一定温度下,氯化钠不能无限制地溶解,水量影响氯化钠的溶解量。
在室温下,向盛有20 mL水的烧杯中加入5 g硝酸钾,搅拌;等溶解后,再加5 g硝酸钾,搅拌,观察现象。当烧杯中硝酸钾固体有剩余而不再继续溶解时,加热烧杯一段时间,观察剩余固体有什么变化。然后再加入5 g硝酸钾,搅拌,观察现象。待溶液冷却后,又有什么现象发生?
实验探究二
操作 现象 结论
加入5 g硝酸钾,搅拌
再加5 g硝酸钾,搅拌
加热
再加5 g硝酸钾,搅拌
冷却
烧杯中形成无色溶液
烧杯溶液底部有未溶解的固体
20 mL水能完全溶解5 g硝酸钾
20 mL水不能完全溶解10 g硝酸钾
未溶解的固体溶解了,烧杯中形成无色溶液
温度升高,硝酸钾溶解能力增强
溶液为不饱和溶液
烧杯中形成无色溶液
温度降低,硝酸钾溶解能力减小
有固体从溶液中析出来
在一定量的水中,硝酸钾也不能无限制地溶解在水中,温度影响硝酸钾的溶解量。
饱和溶液
在一定温度下,在一定量的溶剂里,能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液。
不饱和溶液
饱和溶液
在一定温度下,在一定量的溶剂里,不能再继续溶解某种溶质的溶液叫做这种溶质的饱和溶液。
一定温度
一定量的溶剂
不能再继续溶解
一定温度
一定量的溶剂
能继续溶解
能,饱和溶液是相对于一定温度、一定溶剂和某种溶质,再加入其他溶质仍能继续溶解。
向一定温度下的氯化钠饱和溶液中再加入少量硝酸钾,能溶解吗?
判断溶液是否饱和的方法
概念上:
外观上:
判断溶质是否还能继续溶解。
如果溶液底部存在未溶完的物质,说明溶液在此温度下,不能再溶解该物质,肯定是饱和溶液;
如果溶液中不存在未溶完的固体,那么所得的溶液可能是饱和溶液。
硝酸钾不能继续溶解后我们怎样使加入的硝酸钾固体又溶解了?
如何使接近饱和的硝酸钾溶液变成饱和溶液?有没有办法使溶剂减少一些?具体可以怎样操作?
加热
加水
加入硝酸钾固体
蒸发溶剂
请同学们回顾实验,思考并回答下列问题:
问题1
问题2
饱和溶液和不饱和溶液的相互转化
不饱和溶液
饱和溶液
降温
蒸发溶剂
增加溶质
升温
增加溶剂
最简单且适用于任何溶液的方法
饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
饱和溶液与不饱和溶液 浓溶液与稀溶液
区别 含义不同
温度影响
关系 在相同温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液的浓度大。
溶液是否饱和取决于溶质在一定温度下、一定量溶剂里的含量是否达到最大限度
溶液的浓与稀取决于溶质在一定量的溶液里含量的相对多少
受温度影响,必须指明温度
与温度无关
溶液的饱和和不饱和与溶液的浓和稀没有必然的关系。
饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定不饱和溶液。
浓溶液
稀溶液
饱和溶液
不饱和溶液
【例1】室温下,向一定质量的氯化钠溶液中加入10 g氯化钠固体,充分搅拌后,尚有部分固体未溶解,加入10 g水后,固体全部溶解。下列判断正确的是( )
A.加水前一定是饱和溶液
B.加氯化钠前可能是饱和溶液
C.加水后一定是饱和溶液
D.加水后一定是不饱和溶液
A
【例2】室温下,将盛有接近饱和的硝酸钾溶液的小烧杯放在盛水的大烧杯中,如图所示,欲使硝酸钾溶液变为饱和溶液,可向大烧杯中加入的固体物质是( )
A.生石灰 B.氯化钠 C.硝酸铵 D.氢氧化钠
C
烧杯底部出现固体
冷却热的饱和溶液时,硝酸钾晶体从溶液中析出
热的硝酸钾溶液
硝酸钾溶液为饱和溶液
结晶
硝酸钾晶体
冷却
继
续
降
低
硝酸钾溶液为不饱和溶液
这种获得结晶的方法称之为:冷却热的饱和溶液(降温结晶)
你知道海水晒盐吗?
海水晒盐的过程
氯化钠
海水
贮水池
蒸发池
结晶池
粗盐
母液
(苦卤)
多种化工产品
蒸发溶剂(蒸发结晶)
这种获得结晶的方法称之为:
(沉降泥沙)
(蒸发水分)
(蒸发水分)
(氯化钠的饱和溶液)
海水晒盐过程中,有哪些环节得到的溶液一定是饱和溶液?
结晶池
母液
【例1】下列有关结晶的说法正确的是( )
A.饱和溶液降低温度一定会析出晶体
B.只有蒸发溶剂才会出现结晶现象
C.腌菜晾晒时表面出现很多小晶体,是因为发生化学变化
D.析出晶体后的溶液一定是饱和溶液
D
【例2】海水晒盐是海水在常温下蒸发得到氯化钠的过程。小露用氯化钠溶液模拟该过程,如图所示:
(1)乙烧杯中的溶液________(填“是”“不是”或“可能是”)氯化钠饱和溶液。
(2)要使氯化钠晶体从溶液中析出,常采用的方法是____________。
可能是
蒸发结晶
雪花结晶的过程
1.下列说法正确的是( )
A.饱和溶液一定是浓溶液
B.不饱和溶液转化为饱和溶液,溶质的质量可能不变
C.向某种溶质的饱和溶液中再加入这种溶质,溶液质量会增加
D.对同一种溶质来讲,饱和溶液一定比不饱和溶液浓
B
2.要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法,其中可行的是( )
①加入CaO ②加入Ca(OH)2 ③升高温度 ④降低温度
A.②③ B.②④ C.①②③ D.①②④
C
3.下图是利用海水提取粗盐的过程:
(1) 上页图中①是______池(填“蒸发”或“冷却”)。
(2) 根据海水晒盐的原理,下列说法中正确的是( )
A. 海水进入贮水池,海水的成分基本不变
B. 在①中,海水中氯化钠的质量逐渐增加
C. 在①中,海水中水的质量逐渐减少
D. 析出晶体后的母液是氯化纳的不饱和溶液
海水
贮水池
①
结晶池
粗盐
母液
氯化钠
多种化工产品
蒸发
A、C
5. 为什么汗水带有咸味?被汗水浸湿的衣服晾干后,常出现白色的斑迹。这是为什么?
汗水中含有一些盐,如氯化钠,因此有咸味;被汗水浸湿的衣服晾干后水分蒸发了,但盐分仍留在衣服上,就形成了白色斑迹。
课题2 溶解度
第1课时
饱和溶液
定义
判断方法
饱和溶液与不饱和溶液之间的转化
结晶及结晶的方法
同课章节目录
