人教版化学九下:10.2 酸和碱的中和反应(第1课时)课件(共22张PPT)
文档属性
| 名称 | 人教版化学九下:10.2 酸和碱的中和反应(第1课时)课件(共22张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第十单元 酸和碱
课题2 酸和碱的中和反应
第1课时
中和反应的概念及其应用
1
本节重点
中和反应的理解和应用
2
本节难点
同学们,夏天被蚊虫叮咬后是什么感觉?你们是采用什么方法消痛止痒的呢?
那么,酸与碱能否发生反应呢?
HCl=H++Cl-
H2SO4=2H+ + SO42-
NaOH=Na++OH-
Ca(OH)2=Ca2+ + 2OH-
酸具有相似化学性质的原因是在酸溶液中都含有相同的H+;
碱具有相似化学性质的原因是在碱溶液中都含有相同的OH-。
用两支试管分别取少量的稀盐酸和氢氧化钠溶液,一起倒入小烧杯中,搅拌,并观察现象。
实验探究一
据此现象能否判断盐酸和氢氧化钠溶液发生了化学反应?为什么?
观察到什么现象?
(没有明显现象)
(不能,没有明显现象能证明有新物质生成或原有的物质减少消失)
如何能证明盐酸和氢氧化钠这两种物质确实发生了反应?
证明:无现象反应的发生实验设计思路
(HCl或NaOH被消耗)
01
证明反应物被消耗
02
证明有新物质生成
酸、碱与指示剂的作用
反应现象明显
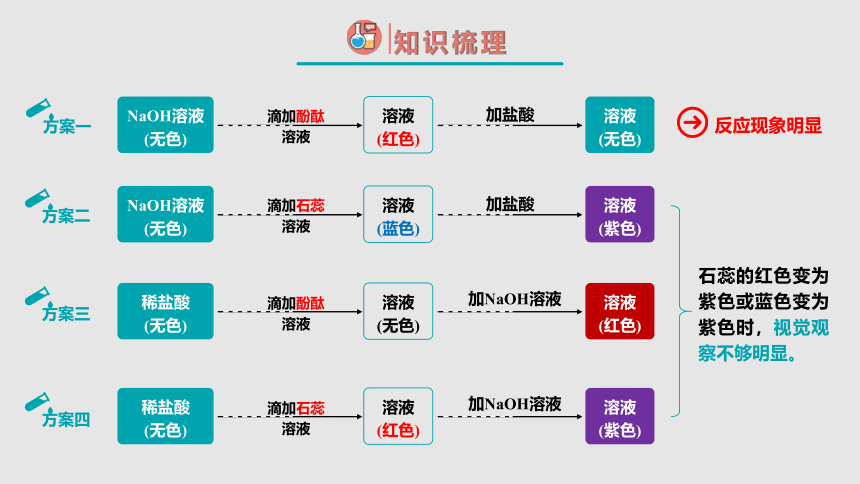
NaOH溶液
(无色)
滴加酚酞溶液
溶液 (红色)
加盐酸
溶液 (无色)
NaOH溶液
(无色)
滴加石蕊溶液
溶液 (蓝色)
加盐酸
溶液 (紫色)
溶液 (红色)
稀盐酸
(无色)
滴加酚酞溶液
溶液 (无色)
加NaOH溶液
溶液 (紫色)
稀盐酸
(无色)
滴加石蕊溶液
溶液 (红色)
加NaOH溶液
石蕊的红色变为紫色或蓝色变为紫色时,视觉观察不够明显。
方案一
方案二
方案三
方案四
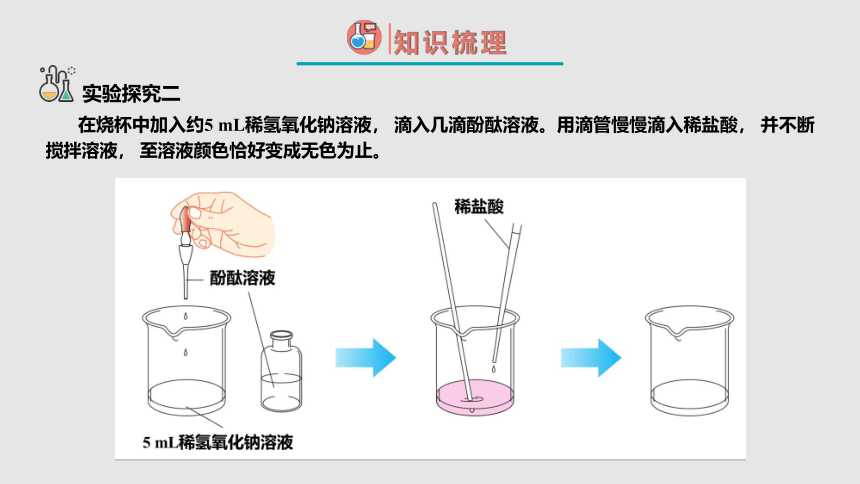
实验探究二
在烧杯中加入约5 mL稀氢氧化钠溶液, 滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸, 并不断搅拌溶液, 至溶液颜色恰好变成无色为止。
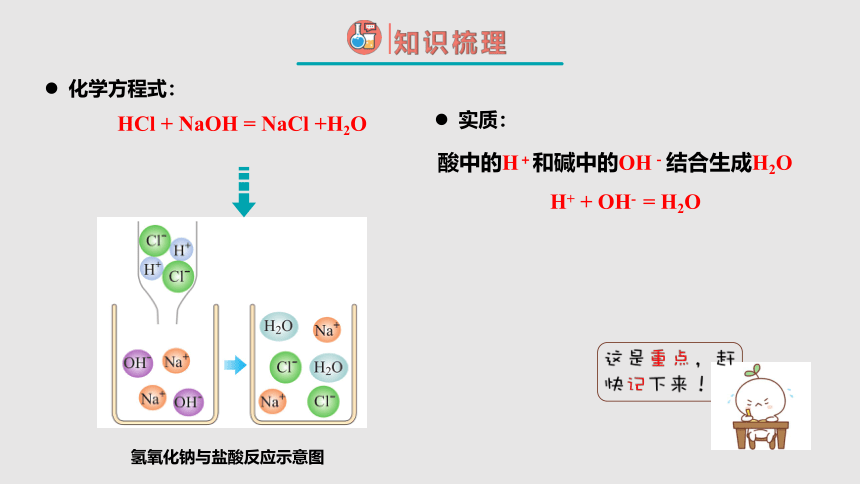
HCl + NaOH = NaCl +H2O
化学方程式:
实质:
氢氧化钠与盐酸反应示意图
酸中的H+和碱中的OH-结合生成H2O
H+ + OH- = H2O
稀盐酸
Ca(OH)2+2HCl= CaCl2+H2O
2NaOH+H2SO4=Na2SO4+2H2O
氢氧化钙溶液
氢氧化钠溶液
稀硫酸
HCl + NaOH NaCl + H2O
2HCl + Ca(OH)2 CaCl2 + 2H2O
H2SO4 + 2NaOH Na2SO4 + 2H2O
酸
碱
盐
水
金属离子和酸根离子构成的化合物
酸和碱作用生成盐和水的反应
中和反应
注意
中和反应不是基本反应类型;
中和反应是放热反应。
Fe2O3+ 6HCl = 2FeCl3 + 3H2O ( )
2NaOH + CO2 = Na2CO3 + H2O ( )Al(OH)3 + 3HCl = AlCl3 + 3H2O ( )
判断下列反应是否是中和反应。
×
中和反应生成盐和水,故生成盐和水的反应一定是中和反应?
×
√
不是,金属氧化物与酸、非金属氧化物与碱反应不是中和反应
下列物质能跟盐酸发生中和反应的是( )
A. 锌粒 B. 氢氧化钠 C. 氧化铜 D. 铜
B
练习1
练习2
练习3
改良土壤酸碱性
农业生产中可以利用中和反应来调节土壤的酸碱性,以利于农作物的生长。例如人们常在酸性土壤中加入熟石灰来改良。
中和反应在实际中的应用
处理工业污水
硫酸厂的污水中常含有硫酸等物质,可以用熟石灰进行中和处理。
中和反应在实际中的应用
H2SO4 + Ca(OH )2 ==CaSO4 +2H2O
用于医药卫生
人的胃液里含有适量的盐酸用来帮助消化。当人饮食过量时,胃会分泌大量的胃酸,造成胃酸过多胃部不适,此时医生常给患者服用含氢氧化铝的药物来中和过多的胃酸。
3HCl +Al(OH)3 ==AlCl3 +3H2O
中和反应在实际中的应用
当人被蚊虫叮咬后,蚊虫会在人的皮肤内分泌出蚁酸,使叮咬处很快肿大而疼痒。如果涂一些稀的含碱性物质的溶液,就可以减少痛痒。如肥皂水、稀氨水等。
同学们,夏天被蚊虫叮咬后是什么感觉?你们是采用什么方法消痛止痒的呢?
洗发水和护发素要搭配使用
洗发水是碱性的,能够洗去油污,但是对头发有一定的伤害;
护发素是酸性的,和洗发水发生中和反应,减少对头发的伤害,起到护发的作用。
1.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。下列说法不正确的是( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.反应后溶液呈中性
D.反应前后元素种类不变
A
2.下列有关中和反应的用途中不正确的是( )
A.服用含氢氧化铝的药物治疗胃酸过多症
B.用熟石灰处理硫酸厂排放的废水
C.酸溅到皮肤上时,立即涂上氢氧化钠溶液
D.吃松花皮蛋时,常加入醋以中和制作过程中产生的碱
C
3.某工厂化学验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40 g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?
解:设这一定量石油产品中含H2SO4的质量为x。
H2SO4+2NaOH=Na2SO4+2H2O
98 80
x 40 g×15%
解得:x=7.35 g。
答:这一定量石油产品中含H2SO4的质量为7.35 g。
课题2
酸和碱的中和反应
第1课时
概念
酸和碱作用生成盐和水的反应
氢离子和氢氧根离子结合生成水
实质
应用
工业废水的处理
改良酸性或碱性土壤
医药或生活中的应用
第十单元 酸和碱
课题2 酸和碱的中和反应
第1课时
中和反应的概念及其应用
1
本节重点
中和反应的理解和应用
2
本节难点
同学们,夏天被蚊虫叮咬后是什么感觉?你们是采用什么方法消痛止痒的呢?
那么,酸与碱能否发生反应呢?
HCl=H++Cl-
H2SO4=2H+ + SO42-
NaOH=Na++OH-
Ca(OH)2=Ca2+ + 2OH-
酸具有相似化学性质的原因是在酸溶液中都含有相同的H+;
碱具有相似化学性质的原因是在碱溶液中都含有相同的OH-。
用两支试管分别取少量的稀盐酸和氢氧化钠溶液,一起倒入小烧杯中,搅拌,并观察现象。
实验探究一
据此现象能否判断盐酸和氢氧化钠溶液发生了化学反应?为什么?
观察到什么现象?
(没有明显现象)
(不能,没有明显现象能证明有新物质生成或原有的物质减少消失)
如何能证明盐酸和氢氧化钠这两种物质确实发生了反应?
证明:无现象反应的发生实验设计思路
(HCl或NaOH被消耗)
01
证明反应物被消耗
02
证明有新物质生成
酸、碱与指示剂的作用
反应现象明显
NaOH溶液
(无色)
滴加酚酞溶液
溶液 (红色)
加盐酸
溶液 (无色)
NaOH溶液
(无色)
滴加石蕊溶液
溶液 (蓝色)
加盐酸
溶液 (紫色)
溶液 (红色)
稀盐酸
(无色)
滴加酚酞溶液
溶液 (无色)
加NaOH溶液
溶液 (紫色)
稀盐酸
(无色)
滴加石蕊溶液
溶液 (红色)
加NaOH溶液
石蕊的红色变为紫色或蓝色变为紫色时,视觉观察不够明显。
方案一
方案二
方案三
方案四
实验探究二
在烧杯中加入约5 mL稀氢氧化钠溶液, 滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸, 并不断搅拌溶液, 至溶液颜色恰好变成无色为止。
HCl + NaOH = NaCl +H2O
化学方程式:
实质:
氢氧化钠与盐酸反应示意图
酸中的H+和碱中的OH-结合生成H2O
H+ + OH- = H2O
稀盐酸
Ca(OH)2+2HCl= CaCl2+H2O
2NaOH+H2SO4=Na2SO4+2H2O
氢氧化钙溶液
氢氧化钠溶液
稀硫酸
HCl + NaOH NaCl + H2O
2HCl + Ca(OH)2 CaCl2 + 2H2O
H2SO4 + 2NaOH Na2SO4 + 2H2O
酸
碱
盐
水
金属离子和酸根离子构成的化合物
酸和碱作用生成盐和水的反应
中和反应
注意
中和反应不是基本反应类型;
中和反应是放热反应。
Fe2O3+ 6HCl = 2FeCl3 + 3H2O ( )
2NaOH + CO2 = Na2CO3 + H2O ( )Al(OH)3 + 3HCl = AlCl3 + 3H2O ( )
判断下列反应是否是中和反应。
×
中和反应生成盐和水,故生成盐和水的反应一定是中和反应?
×
√
不是,金属氧化物与酸、非金属氧化物与碱反应不是中和反应
下列物质能跟盐酸发生中和反应的是( )
A. 锌粒 B. 氢氧化钠 C. 氧化铜 D. 铜
B
练习1
练习2
练习3
改良土壤酸碱性
农业生产中可以利用中和反应来调节土壤的酸碱性,以利于农作物的生长。例如人们常在酸性土壤中加入熟石灰来改良。
中和反应在实际中的应用
处理工业污水
硫酸厂的污水中常含有硫酸等物质,可以用熟石灰进行中和处理。
中和反应在实际中的应用
H2SO4 + Ca(OH )2 ==CaSO4 +2H2O
用于医药卫生
人的胃液里含有适量的盐酸用来帮助消化。当人饮食过量时,胃会分泌大量的胃酸,造成胃酸过多胃部不适,此时医生常给患者服用含氢氧化铝的药物来中和过多的胃酸。
3HCl +Al(OH)3 ==AlCl3 +3H2O
中和反应在实际中的应用
当人被蚊虫叮咬后,蚊虫会在人的皮肤内分泌出蚁酸,使叮咬处很快肿大而疼痒。如果涂一些稀的含碱性物质的溶液,就可以减少痛痒。如肥皂水、稀氨水等。
同学们,夏天被蚊虫叮咬后是什么感觉?你们是采用什么方法消痛止痒的呢?
洗发水和护发素要搭配使用
洗发水是碱性的,能够洗去油污,但是对头发有一定的伤害;
护发素是酸性的,和洗发水发生中和反应,减少对头发的伤害,起到护发的作用。
1.将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意图如图。下列说法不正确的是( )
A.反应前后阴、阳离子的总数目不变
B.反应前后溶液的总质量不变
C.反应后溶液呈中性
D.反应前后元素种类不变
A
2.下列有关中和反应的用途中不正确的是( )
A.服用含氢氧化铝的药物治疗胃酸过多症
B.用熟石灰处理硫酸厂排放的废水
C.酸溅到皮肤上时,立即涂上氢氧化钠溶液
D.吃松花皮蛋时,常加入醋以中和制作过程中产生的碱
C
3.某工厂化学验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40 g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?
解:设这一定量石油产品中含H2SO4的质量为x。
H2SO4+2NaOH=Na2SO4+2H2O
98 80
x 40 g×15%
解得:x=7.35 g。
答:这一定量石油产品中含H2SO4的质量为7.35 g。
课题2
酸和碱的中和反应
第1课时
概念
酸和碱作用生成盐和水的反应
氢离子和氢氧根离子结合生成水
实质
应用
工业废水的处理
改良酸性或碱性土壤
医药或生活中的应用
同课章节目录
