第七章 第二节 第1课时 乙烯 课件(共68张PPT)
文档属性
| 名称 | 第七章 第二节 第1课时 乙烯 课件(共68张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 20:22:44 | ||
图片预览










文档简介
(共68张PPT)
第1课时
DIYIKESHI
乙烯的组成、结构与物理性质 / 乙烯的化学性质及用途 / 随堂演练 知识落实 / 课时对点练
乙烯
第七章
核心素养
发展目标
1.掌握乙烯的组成及结构特点,体会“结构决定性质”的观念,增强“宏观辨识与微观探析”能力。
2.掌握乙烯的化学性质,知道氧化、加成、聚合反应等有机反应类型,培养“证据推理与模型认知”能力。
3.了解乙烯在生产及生活中的应用,培养“科学态度与社会责任”。
内容索引
随堂演练 知识落实
课时对点练
一、乙烯的组成、结构与物理性质
二、乙烯的化学性质及用途
乙烯的组成、结构与物理性质
一
1.乙烯的物理性质
颜色 状态 气味 密度 水溶性
_____ _____ 稍有气味 比空气的略___ ___溶于水
无色
气体
小
难
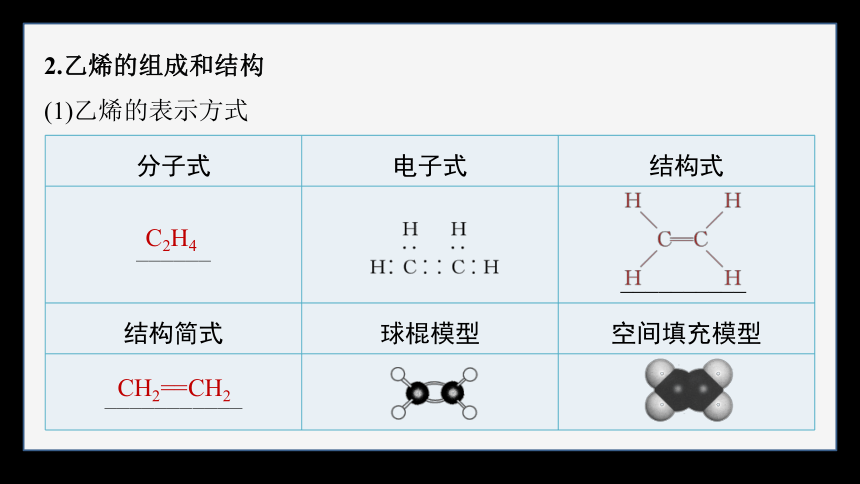
2.乙烯的组成和结构
(1)乙烯的表示方式
分子式 电子式 结构式
______
__________
结构简式 球棍模型 空间填充模型
___________
C2H4
CH2==CH2
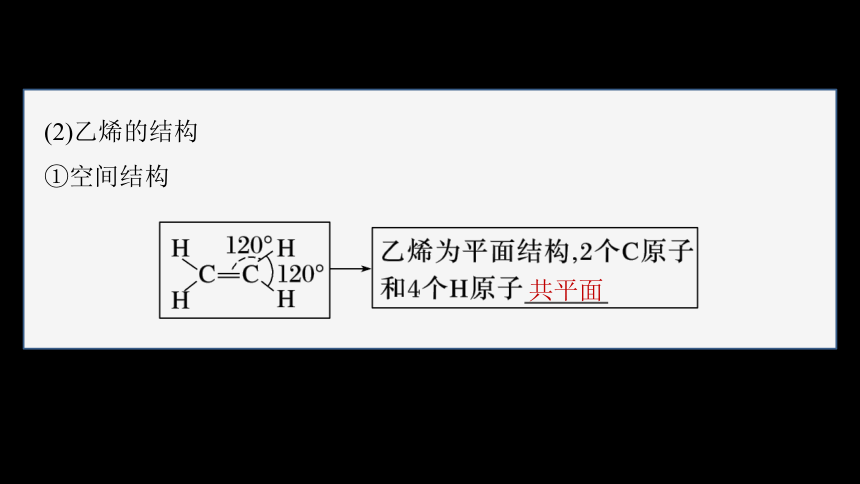
(2)乙烯的结构
①空间结构
共平面
②结构特点
乙烯分子中氢原子数_____乙烷分子中的氢原子数。碳原子的价键没有全部被氢原子“_____”。乙烯分子中的碳碳双键使乙烯表现出较活泼的化学性质。
少于
饱和
特别提醒 碳碳双键决定着乙烯的重要化学性质,所以乙烯的结构简式不能写成CH2CH2(双键不能省略)。
(1)乙烯分子中碳碳双键中的两个键强度相同( )
(2)乙烯的空间填充模型为 ( )
(3)乙烯分子中所有原子共平面,可推断丙烯(CH2==CH—CH3)分子中所
有原子也共平面( )
(4)乙烯分子中碳原子的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃( )
×
正误判断
√
×
×
返回
乙烯的化学性质及用途
二
1.乙烯的化学性质
(1)氧化反应
实验 现象及反应
点燃乙烯 火焰_____且伴有_____,同时放出大量的热,化学方程式为___________________________
通入酸性高锰酸钾溶液中 酸性高锰酸钾溶液_____,CH2==CH2 CO2
明亮
黑烟
褪色
(2)加成反应
①实验探究
实验装置
现象 溴的四氯化碳溶液_____
微观探析
乙烯双键中的_______断裂,两个溴原子分别加在两个价键_______的碳原子上
褪色
一个键
不饱和
化学方程式
+Br—Br―→ _ _____________________
1,2-二溴乙烷
也可以写成:CH2==CH2+Br2―→ ________________
②概念:有机物分子中的_______碳原子与其他原子或原子团直接结合生成新的化合物的反应。
③乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
不饱和
反应 化学方程式
与Cl2加成 _______________________________
与H2加成 _____________________________
与HCl加成 ______________________________
与H2O加成 _____________________________________
(工业制乙醇)
CH2==CH2+Cl2―→ CH2ClCH2Cl
(3)聚合反应
①乙烯的聚合反应
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的_______断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物——聚乙烯,反应的化学方程式:____________
____________________。
一个键
nCH2==CH2
②聚合反应的概念
由_______________的化合物分子互相结合成_______________的聚合物的反应叫做聚合反应。乙烯的聚合反应同时也是加成反应,这样的反应又被称为_____________,简称_________。
相对分子质量小
相对分子质量大
加成聚合反应
加聚反应
③聚合反应的相关概念
概念 含义 示例
链节 高分子中重复的结构单元
聚合度 高分子中链节的数目n 单体 能合成高分子的小分子物质 聚合物 由单体聚合形成的相对分子质量很大的物质
2.乙烯的用途
(1)乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。__________可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中乙烯可以_____________,可用于催熟果实。
乙烯的产量
调节植物生长
(1)乙烯的化学性质比乙烷活泼( )
(2)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( )
(3)酸性KMnO4既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯( )
(4)乙烷中混有乙烯,可通过与H2在一定条件下反应,使乙烯转化为乙烷( )
(5)聚乙烯也可以使酸性KMnO4溶液和溴水褪色( )
×
正误判断
√
×
×
×
深度思考
1.下列物质中,可以通过乙烯的加成反应得到的是_____(填字母)。
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
A项,乙烯和氢气发生加成反应生成CH3CH3,正确;
B项,CH3CHCl2不能通过乙烯的加成反应制得,错误;
C项,CH2==CH2和H2O发生加成反应可生成CH3CH2OH,正确;
D项,CH2==CH2可以和HBr发生加成反应生成CH3CH2Br,正确。
ACD
深度思考
2.体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl
b.CH2==CH2+HCl CH3CH2Cl
深度思考
你认为制备氯乙烷的最好方案为___(填“a”或“b”),并说出选择该方案及不选择另一方案的理由:____________________________________
______________________________________________________________________________________________________________________________________________________________。
b
a方案中CH3CH3和Cl2在光照条件下发生取代反应,产物除CH3CH2Cl和HCl外,还有很多副产物,产物不纯,产率低;b方案中CH2==CH2和HCl在一定条件下发生加成反应,产物只有CH3CH2Cl,产品纯度高,产率高
归纳总结
加成反应与取代反应的比较
类型 取代反应 加成反应
反应物的 结构特征 含有易被取代的原子或原子团 含有不饱和键(如碳碳双键等)
生成物 两种(一般是一种有机物和一种无机物) 一种(有机物)
碳碳键变 化情况 无变化 不饱和键断裂
归纳总结
结构变化 形式举例 等量替换式,如CH3CH3+ Cl2 CH3CH2Cl+HCl 开键加合式,如CH2==CH2
+HCl CH3CH2Cl
返回
随堂演练 知识落实
1.(2022·珠海高一检测)关于乙烯的结构,下列说法正确的是
A.乙烯的电子式为
B.乙烯的球棍模型为
C.乙烯分子在空间上呈平面结构
D.乙烯的结构简式为CH2CH2
1
2
3
4
√
乙烯分子中碳原子间形成的是双键,有两对共用电子对,A项错误;
碳原子的半径应比氢原子的半径大,B项错误;
乙烯的结构简式为CH2==CH2,D项错误。
1
2
3
4
2.下列有关乙烯和乙烷的说法中错误的是
A.乙烯分子中所有原子一定共平面,而乙烷分子中所有原子不可能在同
一平面内
B.乙烯的化学性质比乙烷的化学性质活泼,乙烯中组成碳碳双键的两个
键活性完全相同
C.乙烷中混有乙烯,不能用酸性KMnO4溶液除杂
D.酸性KMnO4溶液可以鉴别乙烯和乙烷
1
2
3
4
√
乙烯分子为平面结构,所有原子一定共平面,乙烷分子中含有甲基,所有原子不可能在同一平面内,A项正确;
乙烯分子中组成双键的两个键有一个易断裂,两个键的活性不同,B项错误;
乙烯可与酸性KMnO4溶液反应生成CO2,会引入新的杂质CO2,C项正确;
乙烯可与酸性KMnO4溶液反应而使其褪色,乙烷不与酸性KMnO4溶液反应,故酸性KMnO4溶液可以鉴别乙烯和乙烷,D项正确。
1
2
3
4
3.(2022·杭州高一检测)下列各反应不属于加成反应的是
A.CH2==CH2+H—OH CH3—CH2—OH
B.CH3CH==CH2+Br2―→ CH3CHBrCH2Br
C. +H2 CH3—CH2—OH
D.CH3—CH3+2Cl2 CH2Cl—CH2Cl+2HCl
1
2
3
4
√
D项中反应为取代反应。
4.根据乙烯的转化图,完成下列问题:
(1)①③的反应类型为_________。
(2)丙的结构简式为____________。
(3)反应②的化学方程式为________________________________。
(4)反应④为工业上乙烯制乙醇的反应,其化学方程式为______________
______________________。
1
2
3
4
加成反应
BrCH2CH2Br
CH2==CH2+3O2 2CO2+2H2O
CH3CH2OH
CH2==CH2+H2O
返回
课时对点练
题组一 乙烯的组成及结构
1.(2022·济南高一月考)现有a、b、c三种碳氢化合物,其球棍模型如下图:
下列有关说法错误的是
A.分子中所有原子共平面的只有b
B.a和c分子结构相似,互为同系物
C.b分子的结构简式为
D.b分子中含有 ,c分子中所有的共价键都为单键
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
因为a、b、c三种分子都为碳氢化合物,
由三种物质的球棍模型可知,a为甲烷、
b为乙烯、c为乙烷,据碳原子成键特点,CH4和CH3CH3分子应为以碳原子为中心的四面体结构,乙烯分子中六个原子共平面,其结构简式为CH2==CH2,故C错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
2.下列有关乙烯的说法正确的是
A.乙烯分子中的碳碳双键中有一个键较易断裂
B.乙烯分子中所有原子都在同一平面上,且有4个原子在同一条直线上
C.乙烯与氢气发生加成反应所得的生成物分子中,所有原子在同一平面上
D.乙烯和环丙烷( )的分子组成都符合通式CnH2n,因此它们互为同
系物
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
乙烯分子中碳原子间共用的两对电子性质不同,其中的一对强度相对较弱,形成的化学键易断裂发生化学反应,A项正确;
乙烯分子中最多只有2个原子在同一条直线上,B项错误;
乙烯与氢气发生加成反应后的产物是乙烷,乙烷分子中的所有原子不可能在同一平面上,C项错误;
乙烯分子中含有碳碳双键,环丙烷分子中含有碳碳单键,二者虽然满足同一通式,但结构不同,不互为同系物,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组二 乙烯的性质与用途
3.下列关于乙烯的用途叙述不正确的是
A.以乙烯为原料不能直接合成聚氯乙烯( )
B.乙烯可以用来制备1,2-二溴乙烷(BrCH2CH2Br)
C.乙烯可以与水发生加成反应制备乙醇(CH3CH2OH)
D.乙烯可以与Br2发生加成反应制备1,1-二溴乙烷( )
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
4.下列关于乙烯的说法不正确的是
A.乙烯可以调节植物生长,可用于催熟果实
B.乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,且原理相同
C.乙烯可发生加聚反应生成聚乙烯,是聚乙烯的单体
D.乙烯分子中6个原子一定在同一平面上
乙烯中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,与溴单质发生加成反应,使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的原理不同。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
5.利用图中所示装置及试剂,能达到相应实验目的的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
选项 甲中试剂 实验目的
A 溴水 除去C2H4中的CH4
B 溴水 除去C2H4中的SO2
C 饱和NaHCO3溶液 除去CO2中的HCl
D 酸性高锰酸钾溶液 除去乙烷中的乙烯,得到纯净的乙烷
√
溴水中的Br2能与C2H4发生加成反应,但与CH4不
反应,所以溴水不能除去C2H4中的CH4,A项不
正确;
C2H4能与Br2发生加成反应,SO2能被溴水氧化为硫酸,二者都能被溴水吸收,B项不正确;
饱和NaHCO3溶液能与CO2中的HCl反应,生成CO2气体等,C项正确;
酸性高锰酸钾溶液能将乙烯氧化为二氧化碳,混在乙烷气体中,使乙烷气体中混入新的杂质,所以不能得到纯净的乙烷,D项不正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组三 加成反应概念的理解及判断
6.下列各组中两个反应所属反应类型相同的是
A.光照甲烷和氯气的混合气体,混合气体颜色变浅;乙烯能使溴的四氯
化碳溶液褪色
B.乙烷在氧气中燃烧;乙烯在空气中燃烧
C.乙烯能使溴的四氯化碳溶液褪色;乙烯能使酸性KMnO4溶液褪色
D.用乙烯与氯化氢反应制取氯乙烷;用乙烷与氯气反应制取氯乙烷
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
7.下列反应属于加成反应的是
A.CH4+2O2 CO2+2H2O
B.CH3CH==CH2+Br2―→ CH3CHBr—CH2Br
C.CH3CH2CH3+Cl2 CH3CH2CH2Cl+HCl
D.CH3CH2CH2CH3―→ CH2==CH2+CH3CH3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
A项,CH4在O2中燃烧属于氧化反应;
B项,CH3CH==CH2与Br2发生加成反应;
C项,CH3CH2CH3与Cl2在光照条件下发生取代反应;
D项,CH3CH2CH2CH3发生分解反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.1体积某气态烃只能与1体积氯气发生加成反应,生成氯代烷。此氯代烷0.5 mol可与3 mol氯气发生完全取代反应,则该烃的结构简式为
A.CH3CH3
B.CH2==CH2
C.CH3CH==CH2
D.CH2==CHCH==CH2
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
1体积某气态烃只能与1体积Cl2发生加成反应,说明1个该烃分子中含有一个 ,加成后的氯代烷0.5 mol可与3 mol Cl2发生取代反应,说明1个该氯代烷分子中含6个氢原子,CH3CH==CH2符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2022·银川高一检测)如图表示结构模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都达到稳定结构。下列有关说法正确的是
A.M分子中的所有原子共面
B.实验室中,N溶液贮存在玻璃试剂瓶中
C.L存在同分异构体
D.L能使酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
小球表示原子序数小于10的原子,短
线表示化学键,每个原子都达到稳定
结构,由图可知,发生的反应为CH2==CH2+HF―→ CH3CH2F。M为乙烯,含碳碳双键,为平面结构,M分子中的所有原子共面,故A正确;
N为HF,可腐蚀玻璃,故B错误;
由乙烷中6个H相同可知,L(CH3CH2F)只有一种结构,不存在同分异构体,故C错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
10.由乙烯推测丙烯(CH2==CHCH3)的结构或性质,下列关于丙烯的说法不正确的是
A.分子中3个碳原子不在同一直线上
B.与HCl在一定条件下加成只得到一种产物
C.最多有7个原子在同一平面上
D.在空气中燃烧时火焰明亮且伴有黑烟
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CHCH3与HCl在一定条件下加成可以得到 、
两种产物。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.(2022·石家庄高一月考)某单烯烃与H2加成后的产物如图,则该单烯烃可能的结构有
A.4种
B.5种
C.6种
D.7种
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
根据烯烃加成反应的特点可知,存在碳碳双键的位置应该是相邻的2
个C原子都有H原子,其可能的位置编号为 ,
因此共有6种不同的结构。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
12.降冰片二烯在紫外线照射下可以发生下列转化:
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
降冰片二烯与四环烷分子式相同、结构不
同,二者互为同分异构体,A正确;
降冰片二烯分子中含有碳碳双键,能使酸
性高锰酸钾溶液褪色,B正确;
四环烷含有三种类型的H原子,其一氯代物有三种,C错误;
根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上可知,降冰片二烯分子中位于同一平面的碳原子最多为4个,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还可以调节植物生长,A
可发生如图所示的一系列化学反应,其中①②③
属于同种反应类型。根据下图回答下列问题:
(1)写出A、B、C、D的结构简式:
A__________,B________,C__________,D___________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CH2 CH3CH3 CH3CH2Cl CH3CH2OH
由已知信息及图可知,A是乙烯;
A与H2在Ni作催化剂和加热的条件下发生加成反应
得到的B为乙烷;
A与H2O在一定条件下发生加成反应得到的D为乙醇;
A与HCl在催化剂和加热的条件下发生加成反应得到
的C为氯乙烷;
乙烷与Cl2在光照条件下发生取代反应得到氯乙烷;
A在催化剂条件下反应得到的高分子E为聚乙烯。
物质A、B、C、D的结构简式分别是CH2==CH2、CH3CH3、CH3CH2Cl、CH3CH2OH。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)写出反应①②的化学方程式,并注明反应类型:
①__________________________(反应类型:__________)。
②________________________________(反应类型:_________)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
加成反应
加成反应
14.乙烯是一种重要的化工原料,某同学设计
实验探究工业制备乙烯的原理和乙烯的主要
化学性质,实验装置如图所示(已知A装置可
产生乙烯气体)。
(1)用化学方程式解释B装置中的实验现象:
________________________________。
乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应的化学方程式为CH2==CH2+Br2―→ CH2Br—CH2Br。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CH2+Br2―→ CH2Br—CH2Br
(2)C装置中的现象是___________________,
其发生反应的反应类型是_________。
乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化反应而使酸性高锰酸钾溶液褪色。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
氧化反应
酸性高锰酸钾溶液褪色
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置____(填字母,下同)中的实验现象可判断该资料是否真实。
乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,澄清石灰水变浑浊。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
(4)通过上述实验探究可知,检验甲烷和乙烯
的方法是___;除去甲烷中乙烯的方法是__。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
BC
B
A项,甲烷、乙烯均难溶于水,且常温下
与水都不反应,不能用于鉴别和除杂;
B项,乙烯中含有 ,能与溴水发生
加成反应生成1,2-二溴乙烷液体,甲烷不与
溴水反应,所以可用溴水除去甲烷中混有的乙烯,也可以鉴别甲烷与乙烯;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
C项,甲烷与酸性高锰酸钾溶液不反应,
乙烯能够与酸性高锰酸钾溶液反应而使
其褪色,可以鉴别甲烷与乙烯,但是乙
烯被氧化生成二氧化碳气体,故不能用
于除去甲烷中混有的乙烯;
D项,甲烷、乙烯都不溶于氢氧化钠溶液,不能用来鉴别和除杂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.CH3CH==CHCH3存在以下转化关系:
(1)正丁烷的同分异构体的结构简式为___________。
反应①②均是加成反应。正丁烷的同分异构体是异丁烷。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH(CH3)3
(2)写出框图中反应①在催化剂和加热条件下的化学方程式:
__________________________________________。
(3)CH3CH==CHCH3能使溴水和酸性KMnO4溶液褪色,二者褪色的原理相同吗?_____。说明原因:_____________________________________
_______________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH3CH==CHCH3+H2 CH3CH2CH2CH3
不同
使溴水褪色是发生了加成反应,使酸性KMnO4溶液褪色是发生了氧化反应
(4)烯烃A是CH3CH==CHCH3的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁烷,则A的结构简式为_______________;A分子中共平面的碳原子个数为___。
CH3CH==CHCH3的同分异构体有CH2==CHCH2CH3、CH2==C(CH3)2,前者与氢气加成的产物是正丁烷,因此,A为后者。A分子中含有碳碳双键,与碳碳双键直接相连的原子及碳碳双键中的两个碳原子肯定共平面,故A分子中共平面的碳原子个数为4。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==C(CH3)2
4
(5)反应②的产物的同分异构体有___种。
反应②的产物的同分异构体有CH3CH2CH2CH2Br、(CH3)2CHCH2Br、(CH3)3CBr,共3种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3
返回
本课结束
第七章
第1课时
DIYIKESHI
乙烯的组成、结构与物理性质 / 乙烯的化学性质及用途 / 随堂演练 知识落实 / 课时对点练
乙烯
第七章
核心素养
发展目标
1.掌握乙烯的组成及结构特点,体会“结构决定性质”的观念,增强“宏观辨识与微观探析”能力。
2.掌握乙烯的化学性质,知道氧化、加成、聚合反应等有机反应类型,培养“证据推理与模型认知”能力。
3.了解乙烯在生产及生活中的应用,培养“科学态度与社会责任”。
内容索引
随堂演练 知识落实
课时对点练
一、乙烯的组成、结构与物理性质
二、乙烯的化学性质及用途
乙烯的组成、结构与物理性质
一
1.乙烯的物理性质
颜色 状态 气味 密度 水溶性
_____ _____ 稍有气味 比空气的略___ ___溶于水
无色
气体
小
难
2.乙烯的组成和结构
(1)乙烯的表示方式
分子式 电子式 结构式
______
__________
结构简式 球棍模型 空间填充模型
___________
C2H4
CH2==CH2
(2)乙烯的结构
①空间结构
共平面
②结构特点
乙烯分子中氢原子数_____乙烷分子中的氢原子数。碳原子的价键没有全部被氢原子“_____”。乙烯分子中的碳碳双键使乙烯表现出较活泼的化学性质。
少于
饱和
特别提醒 碳碳双键决定着乙烯的重要化学性质,所以乙烯的结构简式不能写成CH2CH2(双键不能省略)。
(1)乙烯分子中碳碳双键中的两个键强度相同( )
(2)乙烯的空间填充模型为 ( )
(3)乙烯分子中所有原子共平面,可推断丙烯(CH2==CH—CH3)分子中所
有原子也共平面( )
(4)乙烯分子中碳原子的价键没有全部被氢原子“饱和”,因此乙烯属于不饱和烃( )
×
正误判断
√
×
×
返回
乙烯的化学性质及用途
二
1.乙烯的化学性质
(1)氧化反应
实验 现象及反应
点燃乙烯 火焰_____且伴有_____,同时放出大量的热,化学方程式为___________________________
通入酸性高锰酸钾溶液中 酸性高锰酸钾溶液_____,CH2==CH2 CO2
明亮
黑烟
褪色
(2)加成反应
①实验探究
实验装置
现象 溴的四氯化碳溶液_____
微观探析
乙烯双键中的_______断裂,两个溴原子分别加在两个价键_______的碳原子上
褪色
一个键
不饱和
化学方程式
+Br—Br―→ _ _____________________
1,2-二溴乙烷
也可以写成:CH2==CH2+Br2―→ ________________
②概念:有机物分子中的_______碳原子与其他原子或原子团直接结合生成新的化合物的反应。
③乙烯不仅可以与溴发生加成反应,在一定条件下,还可以与氯气、氢气、氯化氢和水等物质发生加成反应。
不饱和
反应 化学方程式
与Cl2加成 _______________________________
与H2加成 _____________________________
与HCl加成 ______________________________
与H2O加成 _____________________________________
(工业制乙醇)
CH2==CH2+Cl2―→ CH2ClCH2Cl
(3)聚合反应
①乙烯的聚合反应
在适当的温度、压强和催化剂存在的条件下,乙烯分子中碳碳双键中的_______断裂,分子间通过碳原子相互结合形成很长的碳链,生成相对分子质量很大的聚合物——聚乙烯,反应的化学方程式:____________
____________________。
一个键
nCH2==CH2
②聚合反应的概念
由_______________的化合物分子互相结合成_______________的聚合物的反应叫做聚合反应。乙烯的聚合反应同时也是加成反应,这样的反应又被称为_____________,简称_________。
相对分子质量小
相对分子质量大
加成聚合反应
加聚反应
③聚合反应的相关概念
概念 含义 示例
链节 高分子中重复的结构单元
聚合度 高分子中链节的数目n 单体 能合成高分子的小分子物质 聚合物 由单体聚合形成的相对分子质量很大的物质
2.乙烯的用途
(1)乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。__________可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中乙烯可以_____________,可用于催熟果实。
乙烯的产量
调节植物生长
(1)乙烯的化学性质比乙烷活泼( )
(2)乙烯能使酸性KMnO4溶液和溴水褪色,反应原理相同( )
(3)酸性KMnO4既可以验证乙烷和乙烯,还可以除去乙烷中混有的乙烯( )
(4)乙烷中混有乙烯,可通过与H2在一定条件下反应,使乙烯转化为乙烷( )
(5)聚乙烯也可以使酸性KMnO4溶液和溴水褪色( )
×
正误判断
√
×
×
×
深度思考
1.下列物质中,可以通过乙烯的加成反应得到的是_____(填字母)。
A.CH3CH3 B.CH3CHCl2
C.CH3CH2OH D.CH3CH2Br
A项,乙烯和氢气发生加成反应生成CH3CH3,正确;
B项,CH3CHCl2不能通过乙烯的加成反应制得,错误;
C项,CH2==CH2和H2O发生加成反应可生成CH3CH2OH,正确;
D项,CH2==CH2可以和HBr发生加成反应生成CH3CH2Br,正确。
ACD
深度思考
2.体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl
b.CH2==CH2+HCl CH3CH2Cl
深度思考
你认为制备氯乙烷的最好方案为___(填“a”或“b”),并说出选择该方案及不选择另一方案的理由:____________________________________
______________________________________________________________________________________________________________________________________________________________。
b
a方案中CH3CH3和Cl2在光照条件下发生取代反应,产物除CH3CH2Cl和HCl外,还有很多副产物,产物不纯,产率低;b方案中CH2==CH2和HCl在一定条件下发生加成反应,产物只有CH3CH2Cl,产品纯度高,产率高
归纳总结
加成反应与取代反应的比较
类型 取代反应 加成反应
反应物的 结构特征 含有易被取代的原子或原子团 含有不饱和键(如碳碳双键等)
生成物 两种(一般是一种有机物和一种无机物) 一种(有机物)
碳碳键变 化情况 无变化 不饱和键断裂
归纳总结
结构变化 形式举例 等量替换式,如CH3CH3+ Cl2 CH3CH2Cl+HCl 开键加合式,如CH2==CH2
+HCl CH3CH2Cl
返回
随堂演练 知识落实
1.(2022·珠海高一检测)关于乙烯的结构,下列说法正确的是
A.乙烯的电子式为
B.乙烯的球棍模型为
C.乙烯分子在空间上呈平面结构
D.乙烯的结构简式为CH2CH2
1
2
3
4
√
乙烯分子中碳原子间形成的是双键,有两对共用电子对,A项错误;
碳原子的半径应比氢原子的半径大,B项错误;
乙烯的结构简式为CH2==CH2,D项错误。
1
2
3
4
2.下列有关乙烯和乙烷的说法中错误的是
A.乙烯分子中所有原子一定共平面,而乙烷分子中所有原子不可能在同
一平面内
B.乙烯的化学性质比乙烷的化学性质活泼,乙烯中组成碳碳双键的两个
键活性完全相同
C.乙烷中混有乙烯,不能用酸性KMnO4溶液除杂
D.酸性KMnO4溶液可以鉴别乙烯和乙烷
1
2
3
4
√
乙烯分子为平面结构,所有原子一定共平面,乙烷分子中含有甲基,所有原子不可能在同一平面内,A项正确;
乙烯分子中组成双键的两个键有一个易断裂,两个键的活性不同,B项错误;
乙烯可与酸性KMnO4溶液反应生成CO2,会引入新的杂质CO2,C项正确;
乙烯可与酸性KMnO4溶液反应而使其褪色,乙烷不与酸性KMnO4溶液反应,故酸性KMnO4溶液可以鉴别乙烯和乙烷,D项正确。
1
2
3
4
3.(2022·杭州高一检测)下列各反应不属于加成反应的是
A.CH2==CH2+H—OH CH3—CH2—OH
B.CH3CH==CH2+Br2―→ CH3CHBrCH2Br
C. +H2 CH3—CH2—OH
D.CH3—CH3+2Cl2 CH2Cl—CH2Cl+2HCl
1
2
3
4
√
D项中反应为取代反应。
4.根据乙烯的转化图,完成下列问题:
(1)①③的反应类型为_________。
(2)丙的结构简式为____________。
(3)反应②的化学方程式为________________________________。
(4)反应④为工业上乙烯制乙醇的反应,其化学方程式为______________
______________________。
1
2
3
4
加成反应
BrCH2CH2Br
CH2==CH2+3O2 2CO2+2H2O
CH3CH2OH
CH2==CH2+H2O
返回
课时对点练
题组一 乙烯的组成及结构
1.(2022·济南高一月考)现有a、b、c三种碳氢化合物,其球棍模型如下图:
下列有关说法错误的是
A.分子中所有原子共平面的只有b
B.a和c分子结构相似,互为同系物
C.b分子的结构简式为
D.b分子中含有 ,c分子中所有的共价键都为单键
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
因为a、b、c三种分子都为碳氢化合物,
由三种物质的球棍模型可知,a为甲烷、
b为乙烯、c为乙烷,据碳原子成键特点,CH4和CH3CH3分子应为以碳原子为中心的四面体结构,乙烯分子中六个原子共平面,其结构简式为CH2==CH2,故C错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
2.下列有关乙烯的说法正确的是
A.乙烯分子中的碳碳双键中有一个键较易断裂
B.乙烯分子中所有原子都在同一平面上,且有4个原子在同一条直线上
C.乙烯与氢气发生加成反应所得的生成物分子中,所有原子在同一平面上
D.乙烯和环丙烷( )的分子组成都符合通式CnH2n,因此它们互为同
系物
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
乙烯分子中碳原子间共用的两对电子性质不同,其中的一对强度相对较弱,形成的化学键易断裂发生化学反应,A项正确;
乙烯分子中最多只有2个原子在同一条直线上,B项错误;
乙烯与氢气发生加成反应后的产物是乙烷,乙烷分子中的所有原子不可能在同一平面上,C项错误;
乙烯分子中含有碳碳双键,环丙烷分子中含有碳碳单键,二者虽然满足同一通式,但结构不同,不互为同系物,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组二 乙烯的性质与用途
3.下列关于乙烯的用途叙述不正确的是
A.以乙烯为原料不能直接合成聚氯乙烯( )
B.乙烯可以用来制备1,2-二溴乙烷(BrCH2CH2Br)
C.乙烯可以与水发生加成反应制备乙醇(CH3CH2OH)
D.乙烯可以与Br2发生加成反应制备1,1-二溴乙烷( )
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
4.下列关于乙烯的说法不正确的是
A.乙烯可以调节植物生长,可用于催熟果实
B.乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,且原理相同
C.乙烯可发生加聚反应生成聚乙烯,是聚乙烯的单体
D.乙烯分子中6个原子一定在同一平面上
乙烯中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,与溴单质发生加成反应,使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的原理不同。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
5.利用图中所示装置及试剂,能达到相应实验目的的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
选项 甲中试剂 实验目的
A 溴水 除去C2H4中的CH4
B 溴水 除去C2H4中的SO2
C 饱和NaHCO3溶液 除去CO2中的HCl
D 酸性高锰酸钾溶液 除去乙烷中的乙烯,得到纯净的乙烷
√
溴水中的Br2能与C2H4发生加成反应,但与CH4不
反应,所以溴水不能除去C2H4中的CH4,A项不
正确;
C2H4能与Br2发生加成反应,SO2能被溴水氧化为硫酸,二者都能被溴水吸收,B项不正确;
饱和NaHCO3溶液能与CO2中的HCl反应,生成CO2气体等,C项正确;
酸性高锰酸钾溶液能将乙烯氧化为二氧化碳,混在乙烷气体中,使乙烷气体中混入新的杂质,所以不能得到纯净的乙烷,D项不正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组三 加成反应概念的理解及判断
6.下列各组中两个反应所属反应类型相同的是
A.光照甲烷和氯气的混合气体,混合气体颜色变浅;乙烯能使溴的四氯
化碳溶液褪色
B.乙烷在氧气中燃烧;乙烯在空气中燃烧
C.乙烯能使溴的四氯化碳溶液褪色;乙烯能使酸性KMnO4溶液褪色
D.用乙烯与氯化氢反应制取氯乙烷;用乙烷与氯气反应制取氯乙烷
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
7.下列反应属于加成反应的是
A.CH4+2O2 CO2+2H2O
B.CH3CH==CH2+Br2―→ CH3CHBr—CH2Br
C.CH3CH2CH3+Cl2 CH3CH2CH2Cl+HCl
D.CH3CH2CH2CH3―→ CH2==CH2+CH3CH3
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
A项,CH4在O2中燃烧属于氧化反应;
B项,CH3CH==CH2与Br2发生加成反应;
C项,CH3CH2CH3与Cl2在光照条件下发生取代反应;
D项,CH3CH2CH2CH3发生分解反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.1体积某气态烃只能与1体积氯气发生加成反应,生成氯代烷。此氯代烷0.5 mol可与3 mol氯气发生完全取代反应,则该烃的结构简式为
A.CH3CH3
B.CH2==CH2
C.CH3CH==CH2
D.CH2==CHCH==CH2
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
1体积某气态烃只能与1体积Cl2发生加成反应,说明1个该烃分子中含有一个 ,加成后的氯代烷0.5 mol可与3 mol Cl2发生取代反应,说明1个该氯代烷分子中含6个氢原子,CH3CH==CH2符合题意。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2022·银川高一检测)如图表示结构模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都达到稳定结构。下列有关说法正确的是
A.M分子中的所有原子共面
B.实验室中,N溶液贮存在玻璃试剂瓶中
C.L存在同分异构体
D.L能使酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
小球表示原子序数小于10的原子,短
线表示化学键,每个原子都达到稳定
结构,由图可知,发生的反应为CH2==CH2+HF―→ CH3CH2F。M为乙烯,含碳碳双键,为平面结构,M分子中的所有原子共面,故A正确;
N为HF,可腐蚀玻璃,故B错误;
由乙烷中6个H相同可知,L(CH3CH2F)只有一种结构,不存在同分异构体,故C错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
10.由乙烯推测丙烯(CH2==CHCH3)的结构或性质,下列关于丙烯的说法不正确的是
A.分子中3个碳原子不在同一直线上
B.与HCl在一定条件下加成只得到一种产物
C.最多有7个原子在同一平面上
D.在空气中燃烧时火焰明亮且伴有黑烟
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CHCH3与HCl在一定条件下加成可以得到 、
两种产物。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.(2022·石家庄高一月考)某单烯烃与H2加成后的产物如图,则该单烯烃可能的结构有
A.4种
B.5种
C.6种
D.7种
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
根据烯烃加成反应的特点可知,存在碳碳双键的位置应该是相邻的2
个C原子都有H原子,其可能的位置编号为 ,
因此共有6种不同的结构。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
12.降冰片二烯在紫外线照射下可以发生下列转化:
下列说法错误的是
A.降冰片二烯与四环烷互为同分异构体
B.降冰片二烯能使酸性高锰酸钾溶液褪色
C.四环烷的一氯代物超过三种(不考虑立体异构)
D.降冰片二烯分子中位于同一平面的碳原子不超过4个
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
降冰片二烯与四环烷分子式相同、结构不
同,二者互为同分异构体,A正确;
降冰片二烯分子中含有碳碳双键,能使酸
性高锰酸钾溶液褪色,B正确;
四环烷含有三种类型的H原子,其一氯代物有三种,C错误;
根据乙烯分子是平面分子,与碳碳双键连接的C原子在碳碳双键所在的平面上可知,降冰片二烯分子中位于同一平面的碳原子最多为4个,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还可以调节植物生长,A
可发生如图所示的一系列化学反应,其中①②③
属于同种反应类型。根据下图回答下列问题:
(1)写出A、B、C、D的结构简式:
A__________,B________,C__________,D___________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CH2 CH3CH3 CH3CH2Cl CH3CH2OH
由已知信息及图可知,A是乙烯;
A与H2在Ni作催化剂和加热的条件下发生加成反应
得到的B为乙烷;
A与H2O在一定条件下发生加成反应得到的D为乙醇;
A与HCl在催化剂和加热的条件下发生加成反应得到
的C为氯乙烷;
乙烷与Cl2在光照条件下发生取代反应得到氯乙烷;
A在催化剂条件下反应得到的高分子E为聚乙烯。
物质A、B、C、D的结构简式分别是CH2==CH2、CH3CH3、CH3CH2Cl、CH3CH2OH。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)写出反应①②的化学方程式,并注明反应类型:
①__________________________(反应类型:__________)。
②________________________________(反应类型:_________)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
加成反应
加成反应
14.乙烯是一种重要的化工原料,某同学设计
实验探究工业制备乙烯的原理和乙烯的主要
化学性质,实验装置如图所示(已知A装置可
产生乙烯气体)。
(1)用化学方程式解释B装置中的实验现象:
________________________________。
乙烯含有碳碳双键,能够与溴发生加成反应而使溴水褪色,反应的化学方程式为CH2==CH2+Br2―→ CH2Br—CH2Br。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==CH2+Br2―→ CH2Br—CH2Br
(2)C装置中的现象是___________________,
其发生反应的反应类型是_________。
乙烯具有还原性,能够与酸性高锰酸钾溶液发生氧化反应而使酸性高锰酸钾溶液褪色。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
氧化反应
酸性高锰酸钾溶液褪色
(3)查阅资料可知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置____(填字母,下同)中的实验现象可判断该资料是否真实。
乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙溶液反应生成碳酸钙沉淀,澄清石灰水变浑浊。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
(4)通过上述实验探究可知,检验甲烷和乙烯
的方法是___;除去甲烷中乙烯的方法是__。
A.将气体通入水中
B.将气体通过装溴水的洗气瓶
C.将气体通过装酸性高锰酸钾溶液的洗气瓶
D.将气体通入氢氧化钠溶液中
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
BC
B
A项,甲烷、乙烯均难溶于水,且常温下
与水都不反应,不能用于鉴别和除杂;
B项,乙烯中含有 ,能与溴水发生
加成反应生成1,2-二溴乙烷液体,甲烷不与
溴水反应,所以可用溴水除去甲烷中混有的乙烯,也可以鉴别甲烷与乙烯;
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
C项,甲烷与酸性高锰酸钾溶液不反应,
乙烯能够与酸性高锰酸钾溶液反应而使
其褪色,可以鉴别甲烷与乙烯,但是乙
烯被氧化生成二氧化碳气体,故不能用
于除去甲烷中混有的乙烯;
D项,甲烷、乙烯都不溶于氢氧化钠溶液,不能用来鉴别和除杂。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.CH3CH==CHCH3存在以下转化关系:
(1)正丁烷的同分异构体的结构简式为___________。
反应①②均是加成反应。正丁烷的同分异构体是异丁烷。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH(CH3)3
(2)写出框图中反应①在催化剂和加热条件下的化学方程式:
__________________________________________。
(3)CH3CH==CHCH3能使溴水和酸性KMnO4溶液褪色,二者褪色的原理相同吗?_____。说明原因:_____________________________________
_______________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH3CH==CHCH3+H2 CH3CH2CH2CH3
不同
使溴水褪色是发生了加成反应,使酸性KMnO4溶液褪色是发生了氧化反应
(4)烯烃A是CH3CH==CHCH3的一种同分异构体,它在催化剂作用下与氢气反应的产物不是正丁烷,则A的结构简式为_______________;A分子中共平面的碳原子个数为___。
CH3CH==CHCH3的同分异构体有CH2==CHCH2CH3、CH2==C(CH3)2,前者与氢气加成的产物是正丁烷,因此,A为后者。A分子中含有碳碳双键,与碳碳双键直接相连的原子及碳碳双键中的两个碳原子肯定共平面,故A分子中共平面的碳原子个数为4。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CH2==C(CH3)2
4
(5)反应②的产物的同分异构体有___种。
反应②的产物的同分异构体有CH3CH2CH2CH2Br、(CH3)2CHCH2Br、(CH3)3CBr,共3种。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3
返回
本课结束
第七章
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
