第七章 第三节 第1课时 乙醇 课件(共81张PPT)
文档属性
| 名称 | 第七章 第三节 第1课时 乙醇 课件(共81张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-30 00:00:00 | ||
图片预览











文档简介
(共81张PPT)
第1课时
DIYIKESHI
乙醇的物理性质及分子结构 / 乙醇的化学性质及用途 / 随堂演练 知识落实 / 课时对点练
乙醇
第七章
核心素养
发展目标
1.认识乙醇的结构及其主要性质与应用,培养宏观辨识与微观探析的能力。
2.理解烃的衍生物、官能团的概念,结合实例认识官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。
内容索引
随堂演练 知识落实
课时对点练
一、乙醇的物理性质及分子结构
二、乙醇的化学性质及用途
乙醇的物理性质及分子结构
一
1.乙醇的物理性质
乙醇俗称_____,是无色、有特殊香味的液体,密度比水的___,易_____,能溶解多种有机物和无机物,并能与水以_________互溶。
酒精
小
挥发
任意比例
特别提醒 通过蒸馏法分离乙醇和水时,当乙醇的体积分数达到95%左右时,乙醇和水会形成共沸物。应在体积分数为95%的乙醇中先加生石灰,再蒸馏。
2.乙醇的组成与结构
分子式 结构式 结构简式 球棍模型
C2H6O ___________或________
CH3CH2OH
C2H5OH
3.烃的衍生物和官能团
(1)烃的衍生物
乙醇可以看成是乙烷分子中的一个_______被_____(—OH)取代后的产物。烃分子中的氢原子被________或_______所取代而生成的一系列化合物称为烃的衍生物。烃分子失去1个氢原子后所剩余的部分叫做烃基,乙醇可看作是由乙基和羟基组成的: 。
(2)官能团
烃的衍生物与其母体化合物相比,其性质因分子中________的存在而不同。决定有机化合物特性的_____或______叫做官能团,_____就是醇类物质的官能团。
氢原子
羟基
其他原子
原子团
取代基团
原子
原子团
羟基
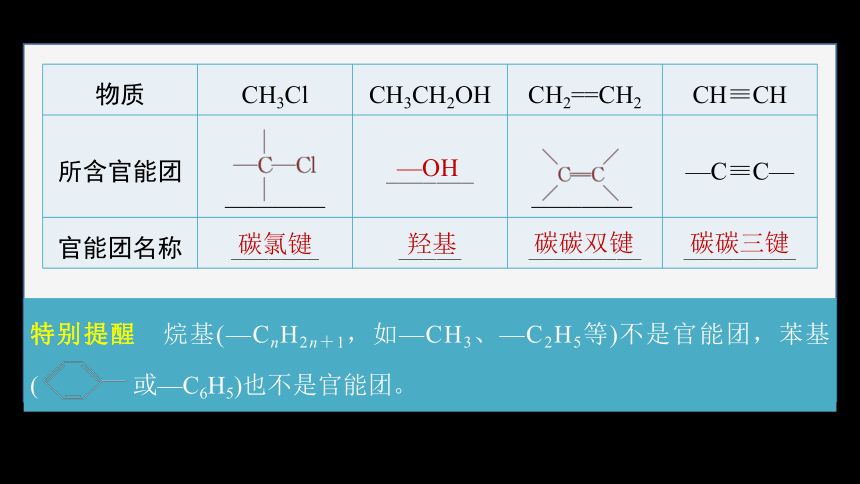
物质 CH3Cl CH3CH2OH CH2==CH2 CH≡CH
所含官能团 ________ _______ ________ —C≡C—
官能团名称 _______ _____ _________ _________
—OH
碳氯键
羟基
碳碳双键
碳碳三键
特别提醒 烷基(—CnH2n+1,如—CH3、—C2H5等)不是官能团,苯基( 或—C6H5)也不是官能团。
(1)常用无水CuSO4检验乙醇中是否有水( )
(2)乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物( )
(3)乙醇可以看作乙烷分子中氢原子被氢氧根离子(OH-)取代后的产物,故乙醇水溶液应呈碱性( )
(4)“酒香不怕巷子深”体现了乙醇易挥发的性质( )
×
正误判断
√
×
√
深度思考
乙醇的官能团为羟基(—OH),认真分析—OH与OH-的区别和联系并填写下表。
羟基 氢氧根离子
不同点 电子式 _______
_________
电子数 ___ ____
电性 __________________ _________
稳定程度 ________ _______
9
10
不显电性或电中性
显负电性
不稳定
较稳定
深度思考
不同点 存在 _____独立存在,必须与其他基团结合在一起 ___独立存在
书写方法 _______ _____
相同点 组成元素相同;质子数相同,均为__ 不能
能
—OH
OH-
9
应用体验
1.比较乙烷和乙醇的结构,下列说法错误的是
A.分子中的化学键都包括极性键和非极性键
B.分子中都含6个氢原子且6个氢原子的化学环境完全相同
C.乙基与1个氢原子相连就是乙烷分子
D.乙基与1个羟基相连就是乙醇分子
√
乙烷和乙醇的结构简式分别是CH3CH3、CH3CH2OH,故A、C、D项均正确;
CH3CH3分子中的6个氢原子完全等效,而CH3CH2OH分子中有3种不同化学环境的氢原子(分别为—CH3、—CH2—、—OH上的氢原子),故B项错误。
2.下列物质中含有两种官能团的是
A.氯乙烯(CH2==CHCl)
B.苯乙烯( )
C.丙三醇( )
D.甲苯( )
√
决定有机化合物特性的原子或原子团叫做官能团。氯乙烯中含有
和碳氯键两种官能团;苯乙烯中含有 一种官能团;丙三醇中含有—OH一种官能团;甲苯中没有官能团。
返回
乙醇的化学性质及用途
二
1.乙醇的化学性质
(1)乙醇与钠反应
实验操作
实验现象 a.钠开始沉于试管底部,有_________气泡产生,钠被气体带着上浮,慢慢变小直至消失;b.点燃,火焰呈________;c.试管内壁有______产生;d.向试管中加入澄清石灰水,澄清石灰水__________
无色无味
淡蓝色
液滴
不变浑浊
实验 结论 乙醇与钠反应生成_____,化学方程式为_________________
______________________
反应 实质 钠置换了羟基中的氢,生成氢气和乙醇钠
与钠和H2O反 应比较 现象:剧烈程度比水___,钠沉在乙醇底部,且没有熔化成金属小球。
物理性质:ρ(H2O)>ρ(Na)>ρ(C2H5OH)
化学性质:乙醇羟基中的氢原子不如水分子中的氢原子活泼
氢气
―→ 2CH3CH2ONa+H2↑
2CH3CH2OH+2Na
弱
(2)氧化反应
①燃烧
化学方程式:_________________________________。现象:乙醇在空气中燃烧,产生_______火焰,放出_________。
CH3CH2OH+3O2 2CO2+3H2O
淡蓝色
大量的热
②催化氧化
实验操作
实验现象 红色的铜丝 变为_____ 变为_____,反复
几次,闻到_______气味
实验结论 乙醇在加热和有催化剂(如铜或银)存在的条件下被空气中的
氧气氧化为乙醛,化学方程式为_______________________
_________________
黑色
红色
刺激性
2CH3CHO+2H2O
2CH3CH2OH+O2
知识拓展 乙醛的官能团为醛基( ,或写作—CHO),乙醛在适
当条件下可被进一步氧化,生成乙酸(CH3COOH)
③与强氧化剂反应
反应原理:CH3CH2OH __________ 。
2.乙醇的用途
CH3COOH
75%
(1)乙醇分子式为C2H6O,故1 mol乙醇和足量的钠反应,可生成3 mol氢气
( )
(2)乙醇和金属钠反应时,是乙醇分子中的O—H断裂( )
(3)乙醇分子中羟基上的氢原子不如水中的氢原子活泼( )
(4)乙醇催化氧化生成乙醛,乙醇能使酸性KMnO4溶液褪色,上述乙醇都表现还原性( )
×
正误判断
√
√
√
深度思考
提示 在实验中铜丝参与了化学反应,后来又生成了铜,铜丝在反应中起到催化作用。反应的化学方程式为2Cu+O2 2CuO,CuO+
CH3CH2OH Cu+CH3CHO+H2O,总反应的化学方程式为
2CH3CH2OH+O2 2CH3CHO+2H2O。
1.结合实验现象,在乙醇和氧气催化氧化反应实验中铜丝是否参与反应?铜丝的作用是什么?写出相关的化学方程式。
深度思考
2.已知乙醇在催化氧化反应中断裂的为如图所示的化学键:
试完成下列问题:
(1)如将乙醇改为 ,试写出在该条件下反应的化学方程式:
__________________________________________。
+O2 +2H2O
深度思考
(2)如醇为 ,在该条件下,醇还能被催化氧化吗?为什么?
___________________________________________________________________。
不能。因为该分子中和羟基相连的碳原子上没有氢原子,不能被催化氧化
在乙醇和O2的催化氧化反应中,实质是CH3CH2OH分子中的O—H及和—OH相连的碳原子上的C—H断裂,最终生成CH3CHO,若和
—OH相连的碳原子上只有一个H原子,则被氧化为 ,若和
—OH相连的碳原子上没有H原子,则不能被催化氧化。
应用体验
1.(2022·河北邯郸市高一检测)乙醇分子结构中各种化学键如图所示,下列对乙醇的有关说法不正确的是
A.与金属钠反应时断裂①
B.乙醇燃烧时所有键都断裂
C.乙醇在铜催化下和氧气反应键①和③断裂
D.向乙醇的水溶液中滴入几滴酚酞,溶液变红色
√
根据乙醇与钠反应的实质,应该是羟基上氧氢键断
裂,即断裂①键,A项错误;
燃烧是有机物最剧烈的反应,生成二氧化碳和水,所有的化学键都要断裂,B项正确;
乙醇在铜催化下与O2反应生成乙醛和水:2CH3CH2OH+O2
2CH3CHO+2H2O,故乙醇断键的位置为①和③,C项正确;
乙醇溶液呈中性,D错误。
2.(2022·西安高一检测)根据乙醇的性质可以推测异丙醇( )的性质,下列说法不正确的是
A.异丙醇能在空气中燃烧
B.异丙醇能使酸性高锰酸钾溶液褪色
C.异丙醇可与金属钠发生反应生成异丙醇钠和氢气
D.异丙醇在加热和有催化剂(Cu或Ag)存在的条件下,被氧气氧化为丙醛
√
乙醇可以燃烧,所以根据乙醇的性质可以推测异丙醇能在空气中燃烧,故A项正确;
乙醇具有还原性,能使酸性高锰酸钾溶液褪色,根据乙醇的性质推测异丙醇也能使酸性高锰酸钾溶液褪色,故B项正确;
乙醇可以和钠反应生成乙醇钠和氢气,异丙醇含有羟基,可以和钠反应生成异丙醇钠和氢气,故C项正确;
在乙醇中与羟基相连的碳原子上有两个氢原子,异丙醇中与羟基相连的碳原子上只有一个氢原子,在加热和有催化剂(Cu或Ag)存在的条件下,能被氧气氧化为丙酮,故D项错误。
归纳总结
(1)醇与金属钠反应的数量关系
1 mol —OH~1 mol Na~0.5 mol H2。
(2)醇的催化氧化反应规律
①凡为R—CH2OH(R代表烃基)结构的醇,在一定条件下都能被氧化成醛(R—CHO)。
归纳总结
②凡为R—CH(OH)—R′结构的醇,在一定条件下也能被氧化,
但生成物不是醛,而是酮( )。
③凡为 结构的醇,通常情况下不能被氧化。
返回
随堂演练 知识落实
1.下列有关乙醇的表述正确的是
A.乙醇分子中含有甲基,甲基的电子式为
B.乙醇的结构简式为C2H6O
C.乙醇分子中羟基的电子式为
D.乙醇分子的空间填充模型为
√
1
2
3
4
5
甲基的电子式为 ,A项错误;
乙醇的结构简式为CH3CH2OH或C2H5OH,B项错误;
羟基的电子式为 ,为中性基团,C项错误。
1
2
3
4
5
2.(2022·山东泰安一中高一月考)下列关于乙醇结构与性质的说法正确的是
A.乙醇分子中含有—OH,所以乙醇可溶于水,也可电离出OH-
B.乙醇能电离出H+,所以是电解质
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇分子中羟基上的氢原子不如水中的
氢原子活泼
1
2
3
4
5
√
乙醇的结构简式为CH3CH2OH,分子中含有—OH,不能电离出OH-,A项错误;
乙醇的水溶液不能导电,不是电解质,B项错误;
乙醇显中性,C项错误;
乙醇与钠反应比水与钠反应平缓得多,则表明乙醇分子中羟基上的氢原子不如水中的氢原子活泼,D项正确。
1
2
3
4
5
3.交警检查司机是否饮酒的原理:橙色的酸性K2Cr2O7溶液遇到呼出的乙醇蒸气时迅速变绿(Cr3+)。下列对乙醇的描述与此原理有关的是
①乙醇易挥发 ②乙醇的密度比水的小 ③乙醇具有还原性 ④乙醇是烃的含氧衍生物
A.②④ B.②③
C.①③ D.①④
√
乙醇具有还原性,可被酸性K2Cr2O7溶液氧化,溶液由橙色变为绿色;检查时,需要呼出乙醇蒸气,说明乙醇易挥发。
1
2
3
4
5
4.某醇在铜作催化剂的条件下和氧气反应生成的产物为 ,
则该醇为
A. B.
C. D.
1
2
3
4
5
√
能被催化氧化生成相同碳原子数醛的醇,在分子中应含有—CH2OH结构,则该醇的结构为 ,故选A;
B、D项中的醇不能被催化氧化生成醛,C项中的醇其催化氧化生成
的醛为 。
1
2
3
4
5
5.已知分子结构中含有—OH的有机物可以和钠反应放出氢气,某实验小
组为了测定乙醇的结构式是 还是 ,利用乙醇
和钠的反应,设计如图装置进行实验探究:
(1)实验前检验该装置的气密性的实验操作是______
_____________________________________________
_____________________________________________
_______________________________________________________。
1
2
3
4
5
连接
好装置,关闭分液漏斗的活塞,将右侧导管插入水
槽,微热烧瓶,右侧导管若有气泡冒出,冷却后形
成一段水柱,且一段时间内水柱不变化,证明装置气密性良好
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为_______(填“正确”或“不正确”)。
该实验的关键是准确测量反应产生气体的体积,根据产生气体的体积可以确定被置换的氢原子的个数。虽然装置中存在空气,但只有生成氢气时,才会改变装置内气体的压强,从而使水进入c的量筒中,排出水的体积等于氢气的体积,与装置内空气的体积无关,故该说法不正确。
1
2
3
4
5
不正确
(3)如果实验开始前b导管内未充满水,实验结束后b导管内充满水,则实验结果将______(填“偏大”或“偏小”)。
如果实验开始前b导管内未充满水,则会使排出水的体积减小,故实验结果偏小。
1
2
3
4
5
偏小
(4)若测得有1.15 g C2H6O参加反应,把量筒c中水的体积换算成标准状况下H2的体积为280 mL,试结合计算和讨论,判断下面Ⅰ和Ⅱ中,哪个正确?___(填“Ⅰ”或“Ⅱ”)。
1
2
3
4
5
Ⅰ Ⅱ
Ⅱ
参加反应的乙醇的物质的量是0.025 mol,生成氢气的物质的量是0.012 5 mol,即乙醇分子中的6个氢原子的类型并不完全相同,有1个应不同于其他的氢原子,从而确定乙醇的结构式为Ⅱ。
返回
1
2
3
4
5
Ⅰ Ⅱ
课时对点练
题组一 乙醇的结构、物理性质及用途
1.酒精是常用的医疗物资。下列有关酒精的说法不正确的是
A.乙醇的结构式为C2H6O
B.酒精可以溶解碘制备碘酒
C.75%的酒精溶液用于医疗消毒
D.工业酒精可由乙烯为原料制备
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
乙醇的分子式为C2H6O,结构式为 ,A项错误;
酒精可以溶解碘制备碘酒,即为碘的酒精溶液,B项正确;
75%的酒精溶液可用于医疗消毒,C项正确;
工业酒精可由乙烯与水在一定条件下发生加成反应来制备,D项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
2.下列有关酒和酒精的说法正确的是
A.检验乙醇中是否含水,可加入少量的金属钠,若生成气体则含水
B.酒精结构中含有—OH,可推测乙醇溶液呈碱性
C.获取无水乙醇的方法是先加入熟石灰,然后再蒸馏
D.酒精是一种很好的溶剂,能溶解许多无机物和有机化合物,人们用白
酒浸泡中药制成药酒就是利用了这一性质
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
金属钠和水及乙醇都可以反应生成H2,A错误;
酒精的结构简式为C2H5OH,分子在溶液中不能发生电离,溶液呈中性,B错误;
熟石灰[Ca(OH)2]不能吸水,故无法彻底去除乙醇中的水,C错误;
酒精能溶解许多无机物和有机物,故白酒可以浸泡中药制药酒,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇与足量的Na作用得0.5 mol H2
D.乙醇能和水以任意比例互溶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O,无法证明乙醇分子中有一个氢原子与其他氢原子不同,错误;
B项,无法证明,错误;
C项,乙醇与足量钠反应,参与反应的氢原子占乙醇分子中氢原子总
数的 ,说明其中一个氢原子与另外五个不同,正确;
D项,为乙醇的物理性质,无法证明。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组二 烃的衍生物与官能团
4.下列有机物不属于烃的衍生物的是
A.CH2==CHCl B.C8H10
C.CH3OCH3 D.CH3NO2
√
根据烃和烃的衍生物的定义进行分析判断,烃中只含有碳、氢元素,而烃的衍生物中还含有其他元素。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
5.(2022·石家庄高一月考)下列有机物和乙醇具有相同官能团的是
A.苯乙烯( )
B.丙三醇( )
C.丙酮( )
D.乙醚(CH3CH2—O—CH2CH3)
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
苯乙烯含有 ,官能团和乙醇不同;
丙三醇含有—OH,官能团和乙醇相同;
丙酮含有 ,官能团和乙醇不同;
乙醚含有 ,官能团和乙醇不同。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组三 乙醇的化学性质
6.下列说法正确的是
A.羟基与氢氧根有相同的化学式和电子式
B.乙醇是含—OH的化合物
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L H2
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
羟基的化学式是—OH,电子式是 ,氢氧根
的化学式是OH-,电子式是 ,A项错误;
1 mol乙醇与足量的Na反应可以生成0.5 mol H2,在标准状况下是11.2 L,C项错误;
乙醇发生催化氧化时断裂的化学键应为①③,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
7.C2H5OH的官能团是—OH,含有—OH的物质具有与乙醇相似的化学性质,在Cu或Ag的催化下,下列物质不能与O2发生催化氧化反应的是
A.CH3CH2CH2OH
B.CH3OH
C.
D.
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A、B、C项分子中与羟基相连的碳原子上均有氢原子,均能发生催化氧化反应;
D项, 分子中与羟基相连的碳原子上没有氢原子,不能发
生催化氧化反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.已知分子中含有羟基的物质都能与钠反应生成氢气。乙醇、乙二醇
( )、丙三醇( )分别与足量钠反应,产生等量的氢气。则
三种醇的物质的量之比为
A.6∶3∶2 B.1∶2∶3
C.3∶2∶1 D.4∶3∶2
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
羟基个数与被置换的氢原子个数之比为1∶1,三种醇与钠反应放出等量的氢气,则三种醇提供的羟基数目相同,因此三种醇的物质的
量之比为 =6∶3∶2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2022·洛阳高一期末)已知乙醛的沸点为20.8 ℃。实验室可用如图所示装置完成乙醇到乙醛的转化,下列叙述正确的是
A.集气瓶中收集到气体的主要成分是O2
B.甲烧杯中盛装热水,乙烧杯中盛装冷水
C.试管a中收集到的液体仅为乙醛
D.反应结束后铜网变黑
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
集气瓶中收集到的主要是不参加反应
的N2,A项错误;
甲烧杯中应盛装热水,其作用是使无
水乙醇变成乙醇蒸气,乙烧杯中应盛装冷水,起到冷却作用,使乙醛蒸气冷凝为液体,B项正确;
试管a中收集到的液体还有乙醇等,C项错误;
在加热条件下,铜和氧气反应生成黑色的氧化铜,氧化铜和乙醇反应生成红色的铜单质,则反应结束后,铜网仍为红色,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
10.某有机物的结构简式为 ,下列关于该有机物的叙述错误的是
A.能与金属钠反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.不能发生取代反应
D.能被催化氧化生成含有—CHO的有机物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
该有机物分子中含有羟基,所以能与Na反应并放出H2,A项正确;
该有机物分子中含有碳碳双键,所以能在催化剂作用下与H2发生加成反应,B项正确;
该有机物分子中含有氢原子,在一定条件下可以发生取代反应,C项错误;
该有机物分子中含有—CH2OH结构,所以可被催化氧化生成含有
—CHO的有机物,D项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.下列探究乙醇的有关实验,得出的结论正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
选项 实验步骤及现象 实验结论
A 在酒精试样中加入少量CuSO4·5H2O,搅拌,试管底部有蓝色晶体 酒精试样中一定含有水
B 在乙醇燃烧火焰上方罩一冷的干燥烧杯,内壁有水珠出现,另罩一内壁涂有澄清石灰水的烧杯,内壁出现白色沉淀 乙醇由C、H、O三种元素组成
C 将灼烧后表面变黑的螺旋状铜丝伸入约50 ℃的乙醇中,铜丝能保持红热一段时间 乙醇催化氧化反应是放热反应
D 在0.01 mol金属钠中加入过量的乙醇充分反应,收集到标准状况下气体112 mL 乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连
√
CuSO4·5H2O不能再结合水,加入后无现象,故无法证明酒精中是否含水,A错误;
由现象知,乙醇燃烧生成CO2和H2O,可以说明乙醇中含有C、H元素,但不能确定是否含有氧元素,B错误;
由现象“铜丝能保持红热一段时间”,可以说明反应为放热反应,C正确;
0.01 mol Na和过量乙醇生成标准状况下112 mL氢气,但因为乙醇过量,无法确定就是一个H与O相连,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
12.关于有机化合物HO-CH2-CH==CH-CH2OH,下列说法不正确的是
A.分子式为C4H8O2,1 mol该物质充分燃烧需消耗氧气为5 mol
B.能发生取代反应、加成反应、氧化反应、加聚反应
C.1 mol该物质和足量的金属钠反应,产生22.4 L的氢气
D.该物质能使溴水及酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
根据结构简式知,分子式为C4H8O2,可写成C4H4(H2O)2,只有C4H4消耗氧气,故1 mol物质充分燃烧消耗O2为5 mol,故A正确;
分子含有羟基和碳碳双键,因此可以发生取代反应、加成反应、氧化反应和加聚反应,故B正确;
1 mol该物质和足量钠反应会生成1 mol H2,在标准状况下为22.4 L,但没有说明条件,故C错误;
分子中含有羟基和碳碳双键,能和Br2发生加成反应,也能被酸性KMnO4氧化,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.“对酒当歌,人生几何”“劝君更进一杯酒,西出阳关无故人”“何以解忧,唯有杜康”等有关于酒的中国古诗词比比皆是。在历史长河中,酒不仅是一种具体的物质,而且成了一种文化的象征。酒的主要成分是一种常见的有机物乙醇。
(1)乙醇是无色有特殊香味的液体,密度比水的___。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为
______________________________(不写反应条件)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
小
CH2==CH2+H2O―→ CH3CH2OH
(3)属于乙醇的同分异构体的是___(填字母)。
A. B.
C.甲醇 D.CH3-O-CH3
E.HO-CH2CH2-OH
和乙醇互为同分异构体的物质应和乙醇有相同的分子式和不同的结构,符合条件的是D项。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
(4)乙醇能够发生氧化反应,46 g乙醇完全燃烧消耗___mol氧气。
(5)乙醇与钠缓慢的反应,放出无色无味的气体,反应的化学方程式为_______________________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3
2CH3CH2OH+2Na―→ 2CH3CH2ONa+H2↑
14.某教师设计了如图所示的实验装置(夹持装
置等已省略)进行乙醇催化氧化实验,其实验
操作步骤为:先连接好实验装置,关闭活塞a、
止水夹b、c,加热铜丝至红热,然后打开活塞a、止水夹b、c,通过控制活塞a和止水夹b,而间歇性地通入气体,在E处观察到明显的实验现象。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
试回答下列问题:
(1)A装置中发生反应的化学方程式为______________________,B装置中浓硫酸的作用是_______;C装置中热水的作用是__________________
_____________________。
干燥O2
使D中的乙醇变为蒸
气进入E管中参加反应
(2)E管中观察到的现象为____________________
_________。
(3)E管中发生反应的化学方程式为____________
_________________________。
(4)实验进行一段时间后,如果撤掉酒精灯,反应___(填“能”或“不能”)继续进行,其原因是_______________________________________
___________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
铜丝交替出现变黑、变
红的现象
2CH3CH2OH
能
乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续进行
A为氧气的简易制备装置;B中浓硫酸的作
用是干燥A中产生的氧气;C装置是利用水
浴加热使D中的乙醇变为蒸气进入E管参加
反应;在E管中Cu的催化作用下,乙醇被O2
氧化成乙醛,进入F试管中。该反应为放热反应,所以撤掉酒精灯后利用放出的热量可维持反应继续进行。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.(2022·广州高一检测)(1)各种酒类的主要成分为乙醇,下列说法正确的是____(填字母)。
A.查酒驾是利用 可被乙醇氧化为Cr3+而使溶液颜色发生变化
B.乙醇分子中的官能团为OH-
C.当138 g乙醇完全转化为CH3CHO时,乙醇分子中有6 mol共价键断裂
D.乙醇能与水以任意比例互溶
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CD
查酒驾是利用 可被乙醇还原为Cr3+而使溶液颜色发生变化,A项错误;
乙醇的官能团为—OH,而不是OH-,B项错误;
1 mol CH3CH2OH催化氧化生成CH3CHO时,断裂1 mol O—H、1 mol C—H,所以当138 g(3 mol)CH3CH2OH完全反应时,乙醇分子中有6 mol共价键断裂,C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)酒中除了含有乙醇外,还含有一些其他
醇类及酯类等物质。下列是一些醇类香料
的结构简式:
①下列说法正确的是___(填字母)。
A.可用酸性KMnO4溶液检验有机物a的分
子中是否含有碳碳双键
B.将有机物a加入溴的四氯化碳溶液中发生的是取代反应
C.0.5 mol有机物e完全燃烧需标准状况下O2的体积为145.6 L
D.等物质的量的上述5种有机物与足量钠反应时消耗钠的量相等
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
②有机物b的同分异构体有很多,其中含有
—CH2OH,且苯环上只有一个取代基的同分
异构体有___种,写出其中一种被催化氧化
的化学方程式:_______________________
_____________________________________
________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
5
2
+
+O2
2
2H2O(合理即可)
返回
本课结束
第七章
第1课时
DIYIKESHI
乙醇的物理性质及分子结构 / 乙醇的化学性质及用途 / 随堂演练 知识落实 / 课时对点练
乙醇
第七章
核心素养
发展目标
1.认识乙醇的结构及其主要性质与应用,培养宏观辨识与微观探析的能力。
2.理解烃的衍生物、官能团的概念,结合实例认识官能团与性质的关系,知道有机物之间在一定条件下是可以转化的,培养变化观念与平衡思想。
内容索引
随堂演练 知识落实
课时对点练
一、乙醇的物理性质及分子结构
二、乙醇的化学性质及用途
乙醇的物理性质及分子结构
一
1.乙醇的物理性质
乙醇俗称_____,是无色、有特殊香味的液体,密度比水的___,易_____,能溶解多种有机物和无机物,并能与水以_________互溶。
酒精
小
挥发
任意比例
特别提醒 通过蒸馏法分离乙醇和水时,当乙醇的体积分数达到95%左右时,乙醇和水会形成共沸物。应在体积分数为95%的乙醇中先加生石灰,再蒸馏。
2.乙醇的组成与结构
分子式 结构式 结构简式 球棍模型
C2H6O ___________或________
CH3CH2OH
C2H5OH
3.烃的衍生物和官能团
(1)烃的衍生物
乙醇可以看成是乙烷分子中的一个_______被_____(—OH)取代后的产物。烃分子中的氢原子被________或_______所取代而生成的一系列化合物称为烃的衍生物。烃分子失去1个氢原子后所剩余的部分叫做烃基,乙醇可看作是由乙基和羟基组成的: 。
(2)官能团
烃的衍生物与其母体化合物相比,其性质因分子中________的存在而不同。决定有机化合物特性的_____或______叫做官能团,_____就是醇类物质的官能团。
氢原子
羟基
其他原子
原子团
取代基团
原子
原子团
羟基
物质 CH3Cl CH3CH2OH CH2==CH2 CH≡CH
所含官能团 ________ _______ ________ —C≡C—
官能团名称 _______ _____ _________ _________
—OH
碳氯键
羟基
碳碳双键
碳碳三键
特别提醒 烷基(—CnH2n+1,如—CH3、—C2H5等)不是官能团,苯基( 或—C6H5)也不是官能团。
(1)常用无水CuSO4检验乙醇中是否有水( )
(2)乙烷(CH3CH3)可以看成CH4分子中的一个H原子被甲基(—CH3)所取代而生成的产物,故乙烷为烃的衍生物( )
(3)乙醇可以看作乙烷分子中氢原子被氢氧根离子(OH-)取代后的产物,故乙醇水溶液应呈碱性( )
(4)“酒香不怕巷子深”体现了乙醇易挥发的性质( )
×
正误判断
√
×
√
深度思考
乙醇的官能团为羟基(—OH),认真分析—OH与OH-的区别和联系并填写下表。
羟基 氢氧根离子
不同点 电子式 _______
_________
电子数 ___ ____
电性 __________________ _________
稳定程度 ________ _______
9
10
不显电性或电中性
显负电性
不稳定
较稳定
深度思考
不同点 存在 _____独立存在,必须与其他基团结合在一起 ___独立存在
书写方法 _______ _____
相同点 组成元素相同;质子数相同,均为__ 不能
能
—OH
OH-
9
应用体验
1.比较乙烷和乙醇的结构,下列说法错误的是
A.分子中的化学键都包括极性键和非极性键
B.分子中都含6个氢原子且6个氢原子的化学环境完全相同
C.乙基与1个氢原子相连就是乙烷分子
D.乙基与1个羟基相连就是乙醇分子
√
乙烷和乙醇的结构简式分别是CH3CH3、CH3CH2OH,故A、C、D项均正确;
CH3CH3分子中的6个氢原子完全等效,而CH3CH2OH分子中有3种不同化学环境的氢原子(分别为—CH3、—CH2—、—OH上的氢原子),故B项错误。
2.下列物质中含有两种官能团的是
A.氯乙烯(CH2==CHCl)
B.苯乙烯( )
C.丙三醇( )
D.甲苯( )
√
决定有机化合物特性的原子或原子团叫做官能团。氯乙烯中含有
和碳氯键两种官能团;苯乙烯中含有 一种官能团;丙三醇中含有—OH一种官能团;甲苯中没有官能团。
返回
乙醇的化学性质及用途
二
1.乙醇的化学性质
(1)乙醇与钠反应
实验操作
实验现象 a.钠开始沉于试管底部,有_________气泡产生,钠被气体带着上浮,慢慢变小直至消失;b.点燃,火焰呈________;c.试管内壁有______产生;d.向试管中加入澄清石灰水,澄清石灰水__________
无色无味
淡蓝色
液滴
不变浑浊
实验 结论 乙醇与钠反应生成_____,化学方程式为_________________
______________________
反应 实质 钠置换了羟基中的氢,生成氢气和乙醇钠
与钠和H2O反 应比较 现象:剧烈程度比水___,钠沉在乙醇底部,且没有熔化成金属小球。
物理性质:ρ(H2O)>ρ(Na)>ρ(C2H5OH)
化学性质:乙醇羟基中的氢原子不如水分子中的氢原子活泼
氢气
―→ 2CH3CH2ONa+H2↑
2CH3CH2OH+2Na
弱
(2)氧化反应
①燃烧
化学方程式:_________________________________。现象:乙醇在空气中燃烧,产生_______火焰,放出_________。
CH3CH2OH+3O2 2CO2+3H2O
淡蓝色
大量的热
②催化氧化
实验操作
实验现象 红色的铜丝 变为_____ 变为_____,反复
几次,闻到_______气味
实验结论 乙醇在加热和有催化剂(如铜或银)存在的条件下被空气中的
氧气氧化为乙醛,化学方程式为_______________________
_________________
黑色
红色
刺激性
2CH3CHO+2H2O
2CH3CH2OH+O2
知识拓展 乙醛的官能团为醛基( ,或写作—CHO),乙醛在适
当条件下可被进一步氧化,生成乙酸(CH3COOH)
③与强氧化剂反应
反应原理:CH3CH2OH __________ 。
2.乙醇的用途
CH3COOH
75%
(1)乙醇分子式为C2H6O,故1 mol乙醇和足量的钠反应,可生成3 mol氢气
( )
(2)乙醇和金属钠反应时,是乙醇分子中的O—H断裂( )
(3)乙醇分子中羟基上的氢原子不如水中的氢原子活泼( )
(4)乙醇催化氧化生成乙醛,乙醇能使酸性KMnO4溶液褪色,上述乙醇都表现还原性( )
×
正误判断
√
√
√
深度思考
提示 在实验中铜丝参与了化学反应,后来又生成了铜,铜丝在反应中起到催化作用。反应的化学方程式为2Cu+O2 2CuO,CuO+
CH3CH2OH Cu+CH3CHO+H2O,总反应的化学方程式为
2CH3CH2OH+O2 2CH3CHO+2H2O。
1.结合实验现象,在乙醇和氧气催化氧化反应实验中铜丝是否参与反应?铜丝的作用是什么?写出相关的化学方程式。
深度思考
2.已知乙醇在催化氧化反应中断裂的为如图所示的化学键:
试完成下列问题:
(1)如将乙醇改为 ,试写出在该条件下反应的化学方程式:
__________________________________________。
+O2 +2H2O
深度思考
(2)如醇为 ,在该条件下,醇还能被催化氧化吗?为什么?
___________________________________________________________________。
不能。因为该分子中和羟基相连的碳原子上没有氢原子,不能被催化氧化
在乙醇和O2的催化氧化反应中,实质是CH3CH2OH分子中的O—H及和—OH相连的碳原子上的C—H断裂,最终生成CH3CHO,若和
—OH相连的碳原子上只有一个H原子,则被氧化为 ,若和
—OH相连的碳原子上没有H原子,则不能被催化氧化。
应用体验
1.(2022·河北邯郸市高一检测)乙醇分子结构中各种化学键如图所示,下列对乙醇的有关说法不正确的是
A.与金属钠反应时断裂①
B.乙醇燃烧时所有键都断裂
C.乙醇在铜催化下和氧气反应键①和③断裂
D.向乙醇的水溶液中滴入几滴酚酞,溶液变红色
√
根据乙醇与钠反应的实质,应该是羟基上氧氢键断
裂,即断裂①键,A项错误;
燃烧是有机物最剧烈的反应,生成二氧化碳和水,所有的化学键都要断裂,B项正确;
乙醇在铜催化下与O2反应生成乙醛和水:2CH3CH2OH+O2
2CH3CHO+2H2O,故乙醇断键的位置为①和③,C项正确;
乙醇溶液呈中性,D错误。
2.(2022·西安高一检测)根据乙醇的性质可以推测异丙醇( )的性质,下列说法不正确的是
A.异丙醇能在空气中燃烧
B.异丙醇能使酸性高锰酸钾溶液褪色
C.异丙醇可与金属钠发生反应生成异丙醇钠和氢气
D.异丙醇在加热和有催化剂(Cu或Ag)存在的条件下,被氧气氧化为丙醛
√
乙醇可以燃烧,所以根据乙醇的性质可以推测异丙醇能在空气中燃烧,故A项正确;
乙醇具有还原性,能使酸性高锰酸钾溶液褪色,根据乙醇的性质推测异丙醇也能使酸性高锰酸钾溶液褪色,故B项正确;
乙醇可以和钠反应生成乙醇钠和氢气,异丙醇含有羟基,可以和钠反应生成异丙醇钠和氢气,故C项正确;
在乙醇中与羟基相连的碳原子上有两个氢原子,异丙醇中与羟基相连的碳原子上只有一个氢原子,在加热和有催化剂(Cu或Ag)存在的条件下,能被氧气氧化为丙酮,故D项错误。
归纳总结
(1)醇与金属钠反应的数量关系
1 mol —OH~1 mol Na~0.5 mol H2。
(2)醇的催化氧化反应规律
①凡为R—CH2OH(R代表烃基)结构的醇,在一定条件下都能被氧化成醛(R—CHO)。
归纳总结
②凡为R—CH(OH)—R′结构的醇,在一定条件下也能被氧化,
但生成物不是醛,而是酮( )。
③凡为 结构的醇,通常情况下不能被氧化。
返回
随堂演练 知识落实
1.下列有关乙醇的表述正确的是
A.乙醇分子中含有甲基,甲基的电子式为
B.乙醇的结构简式为C2H6O
C.乙醇分子中羟基的电子式为
D.乙醇分子的空间填充模型为
√
1
2
3
4
5
甲基的电子式为 ,A项错误;
乙醇的结构简式为CH3CH2OH或C2H5OH,B项错误;
羟基的电子式为 ,为中性基团,C项错误。
1
2
3
4
5
2.(2022·山东泰安一中高一月考)下列关于乙醇结构与性质的说法正确的是
A.乙醇分子中含有—OH,所以乙醇可溶于水,也可电离出OH-
B.乙醇能电离出H+,所以是电解质
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇分子中羟基上的氢原子不如水中的
氢原子活泼
1
2
3
4
5
√
乙醇的结构简式为CH3CH2OH,分子中含有—OH,不能电离出OH-,A项错误;
乙醇的水溶液不能导电,不是电解质,B项错误;
乙醇显中性,C项错误;
乙醇与钠反应比水与钠反应平缓得多,则表明乙醇分子中羟基上的氢原子不如水中的氢原子活泼,D项正确。
1
2
3
4
5
3.交警检查司机是否饮酒的原理:橙色的酸性K2Cr2O7溶液遇到呼出的乙醇蒸气时迅速变绿(Cr3+)。下列对乙醇的描述与此原理有关的是
①乙醇易挥发 ②乙醇的密度比水的小 ③乙醇具有还原性 ④乙醇是烃的含氧衍生物
A.②④ B.②③
C.①③ D.①④
√
乙醇具有还原性,可被酸性K2Cr2O7溶液氧化,溶液由橙色变为绿色;检查时,需要呼出乙醇蒸气,说明乙醇易挥发。
1
2
3
4
5
4.某醇在铜作催化剂的条件下和氧气反应生成的产物为 ,
则该醇为
A. B.
C. D.
1
2
3
4
5
√
能被催化氧化生成相同碳原子数醛的醇,在分子中应含有—CH2OH结构,则该醇的结构为 ,故选A;
B、D项中的醇不能被催化氧化生成醛,C项中的醇其催化氧化生成
的醛为 。
1
2
3
4
5
5.已知分子结构中含有—OH的有机物可以和钠反应放出氢气,某实验小
组为了测定乙醇的结构式是 还是 ,利用乙醇
和钠的反应,设计如图装置进行实验探究:
(1)实验前检验该装置的气密性的实验操作是______
_____________________________________________
_____________________________________________
_______________________________________________________。
1
2
3
4
5
连接
好装置,关闭分液漏斗的活塞,将右侧导管插入水
槽,微热烧瓶,右侧导管若有气泡冒出,冷却后形
成一段水柱,且一段时间内水柱不变化,证明装置气密性良好
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为_______(填“正确”或“不正确”)。
该实验的关键是准确测量反应产生气体的体积,根据产生气体的体积可以确定被置换的氢原子的个数。虽然装置中存在空气,但只有生成氢气时,才会改变装置内气体的压强,从而使水进入c的量筒中,排出水的体积等于氢气的体积,与装置内空气的体积无关,故该说法不正确。
1
2
3
4
5
不正确
(3)如果实验开始前b导管内未充满水,实验结束后b导管内充满水,则实验结果将______(填“偏大”或“偏小”)。
如果实验开始前b导管内未充满水,则会使排出水的体积减小,故实验结果偏小。
1
2
3
4
5
偏小
(4)若测得有1.15 g C2H6O参加反应,把量筒c中水的体积换算成标准状况下H2的体积为280 mL,试结合计算和讨论,判断下面Ⅰ和Ⅱ中,哪个正确?___(填“Ⅰ”或“Ⅱ”)。
1
2
3
4
5
Ⅰ Ⅱ
Ⅱ
参加反应的乙醇的物质的量是0.025 mol,生成氢气的物质的量是0.012 5 mol,即乙醇分子中的6个氢原子的类型并不完全相同,有1个应不同于其他的氢原子,从而确定乙醇的结构式为Ⅱ。
返回
1
2
3
4
5
Ⅰ Ⅱ
课时对点练
题组一 乙醇的结构、物理性质及用途
1.酒精是常用的医疗物资。下列有关酒精的说法不正确的是
A.乙醇的结构式为C2H6O
B.酒精可以溶解碘制备碘酒
C.75%的酒精溶液用于医疗消毒
D.工业酒精可由乙烯为原料制备
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
乙醇的分子式为C2H6O,结构式为 ,A项错误;
酒精可以溶解碘制备碘酒,即为碘的酒精溶液,B项正确;
75%的酒精溶液可用于医疗消毒,C项正确;
工业酒精可由乙烯与水在一定条件下发生加成反应来制备,D项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
2.下列有关酒和酒精的说法正确的是
A.检验乙醇中是否含水,可加入少量的金属钠,若生成气体则含水
B.酒精结构中含有—OH,可推测乙醇溶液呈碱性
C.获取无水乙醇的方法是先加入熟石灰,然后再蒸馏
D.酒精是一种很好的溶剂,能溶解许多无机物和有机化合物,人们用白
酒浸泡中药制成药酒就是利用了这一性质
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
金属钠和水及乙醇都可以反应生成H2,A错误;
酒精的结构简式为C2H5OH,分子在溶液中不能发生电离,溶液呈中性,B错误;
熟石灰[Ca(OH)2]不能吸水,故无法彻底去除乙醇中的水,C错误;
酒精能溶解许多无机物和有机物,故白酒可以浸泡中药制药酒,D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制饮料
C.1 mol乙醇与足量的Na作用得0.5 mol H2
D.乙醇能和水以任意比例互溶
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A项,乙醇燃烧时,所有的氢原子均参与反应生成H2O,无法证明乙醇分子中有一个氢原子与其他氢原子不同,错误;
B项,无法证明,错误;
C项,乙醇与足量钠反应,参与反应的氢原子占乙醇分子中氢原子总
数的 ,说明其中一个氢原子与另外五个不同,正确;
D项,为乙醇的物理性质,无法证明。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组二 烃的衍生物与官能团
4.下列有机物不属于烃的衍生物的是
A.CH2==CHCl B.C8H10
C.CH3OCH3 D.CH3NO2
√
根据烃和烃的衍生物的定义进行分析判断,烃中只含有碳、氢元素,而烃的衍生物中还含有其他元素。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
5.(2022·石家庄高一月考)下列有机物和乙醇具有相同官能团的是
A.苯乙烯( )
B.丙三醇( )
C.丙酮( )
D.乙醚(CH3CH2—O—CH2CH3)
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
苯乙烯含有 ,官能团和乙醇不同;
丙三醇含有—OH,官能团和乙醇相同;
丙酮含有 ,官能团和乙醇不同;
乙醚含有 ,官能团和乙醇不同。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
题组三 乙醇的化学性质
6.下列说法正确的是
A.羟基与氢氧根有相同的化学式和电子式
B.乙醇是含—OH的化合物
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L H2
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
羟基的化学式是—OH,电子式是 ,氢氧根
的化学式是OH-,电子式是 ,A项错误;
1 mol乙醇与足量的Na反应可以生成0.5 mol H2,在标准状况下是11.2 L,C项错误;
乙醇发生催化氧化时断裂的化学键应为①③,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
7.C2H5OH的官能团是—OH,含有—OH的物质具有与乙醇相似的化学性质,在Cu或Ag的催化下,下列物质不能与O2发生催化氧化反应的是
A.CH3CH2CH2OH
B.CH3OH
C.
D.
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
A、B、C项分子中与羟基相连的碳原子上均有氢原子,均能发生催化氧化反应;
D项, 分子中与羟基相连的碳原子上没有氢原子,不能发
生催化氧化反应。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
8.已知分子中含有羟基的物质都能与钠反应生成氢气。乙醇、乙二醇
( )、丙三醇( )分别与足量钠反应,产生等量的氢气。则
三种醇的物质的量之比为
A.6∶3∶2 B.1∶2∶3
C.3∶2∶1 D.4∶3∶2
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
羟基个数与被置换的氢原子个数之比为1∶1,三种醇与钠反应放出等量的氢气,则三种醇提供的羟基数目相同,因此三种醇的物质的
量之比为 =6∶3∶2。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
9.(2022·洛阳高一期末)已知乙醛的沸点为20.8 ℃。实验室可用如图所示装置完成乙醇到乙醛的转化,下列叙述正确的是
A.集气瓶中收集到气体的主要成分是O2
B.甲烧杯中盛装热水,乙烧杯中盛装冷水
C.试管a中收集到的液体仅为乙醛
D.反应结束后铜网变黑
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
集气瓶中收集到的主要是不参加反应
的N2,A项错误;
甲烧杯中应盛装热水,其作用是使无
水乙醇变成乙醇蒸气,乙烧杯中应盛装冷水,起到冷却作用,使乙醛蒸气冷凝为液体,B项正确;
试管a中收集到的液体还有乙醇等,C项错误;
在加热条件下,铜和氧气反应生成黑色的氧化铜,氧化铜和乙醇反应生成红色的铜单质,则反应结束后,铜网仍为红色,D项错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
10.某有机物的结构简式为 ,下列关于该有机物的叙述错误的是
A.能与金属钠反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.不能发生取代反应
D.能被催化氧化生成含有—CHO的有机物
√
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
该有机物分子中含有羟基,所以能与Na反应并放出H2,A项正确;
该有机物分子中含有碳碳双键,所以能在催化剂作用下与H2发生加成反应,B项正确;
该有机物分子中含有氢原子,在一定条件下可以发生取代反应,C项错误;
该有机物分子中含有—CH2OH结构,所以可被催化氧化生成含有
—CHO的有机物,D项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
11.下列探究乙醇的有关实验,得出的结论正确的是
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
选项 实验步骤及现象 实验结论
A 在酒精试样中加入少量CuSO4·5H2O,搅拌,试管底部有蓝色晶体 酒精试样中一定含有水
B 在乙醇燃烧火焰上方罩一冷的干燥烧杯,内壁有水珠出现,另罩一内壁涂有澄清石灰水的烧杯,内壁出现白色沉淀 乙醇由C、H、O三种元素组成
C 将灼烧后表面变黑的螺旋状铜丝伸入约50 ℃的乙醇中,铜丝能保持红热一段时间 乙醇催化氧化反应是放热反应
D 在0.01 mol金属钠中加入过量的乙醇充分反应,收集到标准状况下气体112 mL 乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连
√
CuSO4·5H2O不能再结合水,加入后无现象,故无法证明酒精中是否含水,A错误;
由现象知,乙醇燃烧生成CO2和H2O,可以说明乙醇中含有C、H元素,但不能确定是否含有氧元素,B错误;
由现象“铜丝能保持红热一段时间”,可以说明反应为放热反应,C正确;
0.01 mol Na和过量乙醇生成标准状况下112 mL氢气,但因为乙醇过量,无法确定就是一个H与O相连,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
12.关于有机化合物HO-CH2-CH==CH-CH2OH,下列说法不正确的是
A.分子式为C4H8O2,1 mol该物质充分燃烧需消耗氧气为5 mol
B.能发生取代反应、加成反应、氧化反应、加聚反应
C.1 mol该物质和足量的金属钠反应,产生22.4 L的氢气
D.该物质能使溴水及酸性KMnO4溶液褪色
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
√
根据结构简式知,分子式为C4H8O2,可写成C4H4(H2O)2,只有C4H4消耗氧气,故1 mol物质充分燃烧消耗O2为5 mol,故A正确;
分子含有羟基和碳碳双键,因此可以发生取代反应、加成反应、氧化反应和加聚反应,故B正确;
1 mol该物质和足量钠反应会生成1 mol H2,在标准状况下为22.4 L,但没有说明条件,故C错误;
分子中含有羟基和碳碳双键,能和Br2发生加成反应,也能被酸性KMnO4氧化,故D正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
13.“对酒当歌,人生几何”“劝君更进一杯酒,西出阳关无故人”“何以解忧,唯有杜康”等有关于酒的中国古诗词比比皆是。在历史长河中,酒不仅是一种具体的物质,而且成了一种文化的象征。酒的主要成分是一种常见的有机物乙醇。
(1)乙醇是无色有特殊香味的液体,密度比水的___。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为
______________________________(不写反应条件)。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
小
CH2==CH2+H2O―→ CH3CH2OH
(3)属于乙醇的同分异构体的是___(填字母)。
A. B.
C.甲醇 D.CH3-O-CH3
E.HO-CH2CH2-OH
和乙醇互为同分异构体的物质应和乙醇有相同的分子式和不同的结构,符合条件的是D项。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
(4)乙醇能够发生氧化反应,46 g乙醇完全燃烧消耗___mol氧气。
(5)乙醇与钠缓慢的反应,放出无色无味的气体,反应的化学方程式为_______________________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
3
2CH3CH2OH+2Na―→ 2CH3CH2ONa+H2↑
14.某教师设计了如图所示的实验装置(夹持装
置等已省略)进行乙醇催化氧化实验,其实验
操作步骤为:先连接好实验装置,关闭活塞a、
止水夹b、c,加热铜丝至红热,然后打开活塞a、止水夹b、c,通过控制活塞a和止水夹b,而间歇性地通入气体,在E处观察到明显的实验现象。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
试回答下列问题:
(1)A装置中发生反应的化学方程式为______________________,B装置中浓硫酸的作用是_______;C装置中热水的作用是__________________
_____________________。
干燥O2
使D中的乙醇变为蒸
气进入E管中参加反应
(2)E管中观察到的现象为____________________
_________。
(3)E管中发生反应的化学方程式为____________
_________________________。
(4)实验进行一段时间后,如果撤掉酒精灯,反应___(填“能”或“不能”)继续进行,其原因是_______________________________________
___________________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
铜丝交替出现变黑、变
红的现象
2CH3CH2OH
能
乙醇的催化氧化反应是放热反应,反应放出的热量能维持反应继续进行
A为氧气的简易制备装置;B中浓硫酸的作
用是干燥A中产生的氧气;C装置是利用水
浴加热使D中的乙醇变为蒸气进入E管参加
反应;在E管中Cu的催化作用下,乙醇被O2
氧化成乙醛,进入F试管中。该反应为放热反应,所以撤掉酒精灯后利用放出的热量可维持反应继续进行。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
15.(2022·广州高一检测)(1)各种酒类的主要成分为乙醇,下列说法正确的是____(填字母)。
A.查酒驾是利用 可被乙醇氧化为Cr3+而使溶液颜色发生变化
B.乙醇分子中的官能团为OH-
C.当138 g乙醇完全转化为CH3CHO时,乙醇分子中有6 mol共价键断裂
D.乙醇能与水以任意比例互溶
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
CD
查酒驾是利用 可被乙醇还原为Cr3+而使溶液颜色发生变化,A项错误;
乙醇的官能团为—OH,而不是OH-,B项错误;
1 mol CH3CH2OH催化氧化生成CH3CHO时,断裂1 mol O—H、1 mol C—H,所以当138 g(3 mol)CH3CH2OH完全反应时,乙醇分子中有6 mol共价键断裂,C项正确。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
(2)酒中除了含有乙醇外,还含有一些其他
醇类及酯类等物质。下列是一些醇类香料
的结构简式:
①下列说法正确的是___(填字母)。
A.可用酸性KMnO4溶液检验有机物a的分
子中是否含有碳碳双键
B.将有机物a加入溴的四氯化碳溶液中发生的是取代反应
C.0.5 mol有机物e完全燃烧需标准状况下O2的体积为145.6 L
D.等物质的量的上述5种有机物与足量钠反应时消耗钠的量相等
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
D
②有机物b的同分异构体有很多,其中含有
—CH2OH,且苯环上只有一个取代基的同分
异构体有___种,写出其中一种被催化氧化
的化学方程式:_______________________
_____________________________________
________________。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
5
2
+
+O2
2
2H2O(合理即可)
返回
本课结束
第七章
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
