1.1.1能层与能级课件(19张ppt)2022-2023学年下学期高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 1.1.1能层与能级课件(19张ppt)2022-2023学年下学期高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-31 00:00:00 | ||
图片预览



文档简介
(共19张PPT)
第一章原子结构与性质
1.1.1能层与能级
第一节原子结构
教学目标
1.理解能层能级的概念,以及它们之间的关系。
2.知道原子核外电子的能层和能级分布及其能量关系。
3.知道基态与激发态,知道原子核外电子在一定条件下会发生跃迁产生原子光谱。
问题反馈
1、能层离核远近与能量高低有何关系?
2、第n能层中的不同能级的能量有何关系?
3、多电子原子中,电子的运动区域与其能量的高低之间有何关系?
4、能层与能级(原子轨道的类型)及原子轨道数目有何关系?
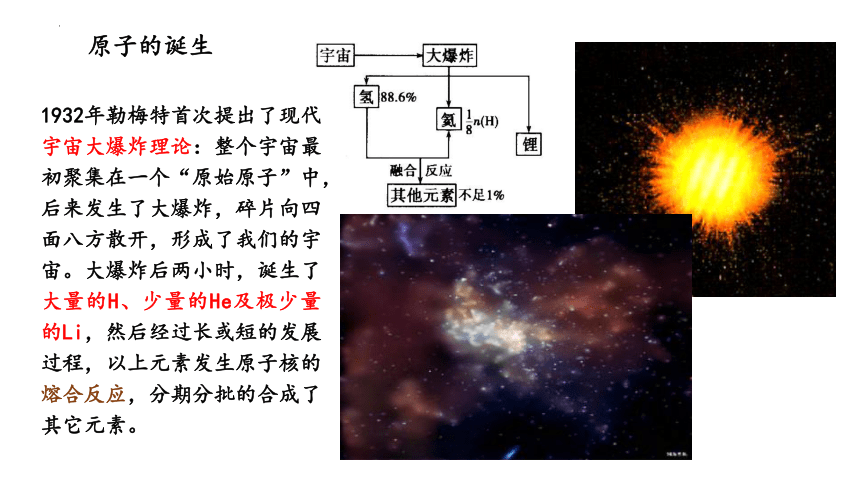
原子的诞生
1932年勒梅特首次提出了现代宇宙大爆炸理论:整个宇宙最初聚集在一个“原始原子”中,后来发生了大爆炸,碎片向四面八方散开,形成了我们的宇宙。大爆炸后两小时,诞生了大量的H、少量的He及极少量的Li,然后经过长或短的发展过程,以上元素发生原子核的熔合反应,分期分批的合成了其它元素。
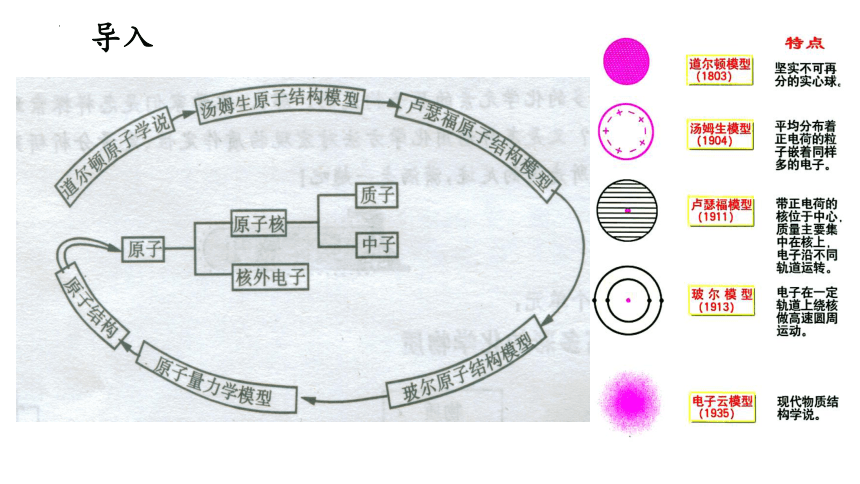
导入
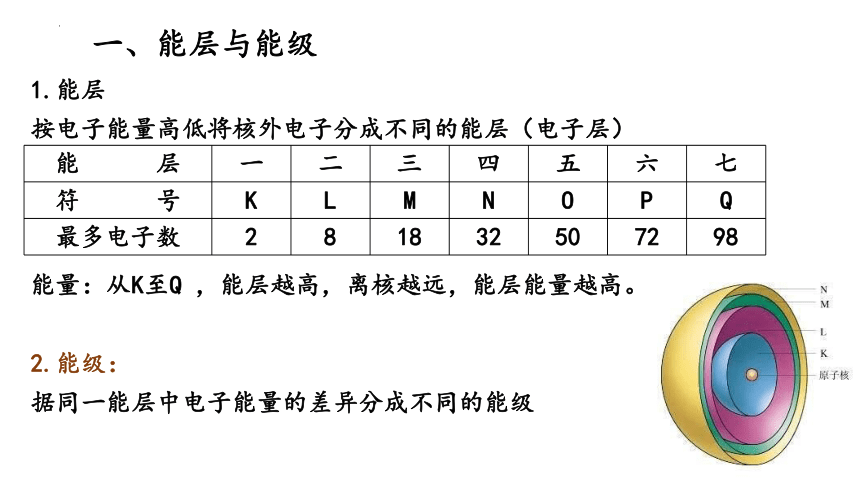
一、能层与能级
1.能层
按电子能量高低将核外电子分成不同的能层(电子层)
能量:从K至Q ,能层越高,离核越远,能层能量越高。
2.能级:
据同一能层中电子能量的差异分成不同的能级
能 层 一 二 三 四 五 六 七
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
1
K
2
L
M
N
O
P
Q
3
4
5
6
7
1s
2s
2p
3s
3p
3d
4s
4p
4d
4f
5s
5p
5d
5f
5g
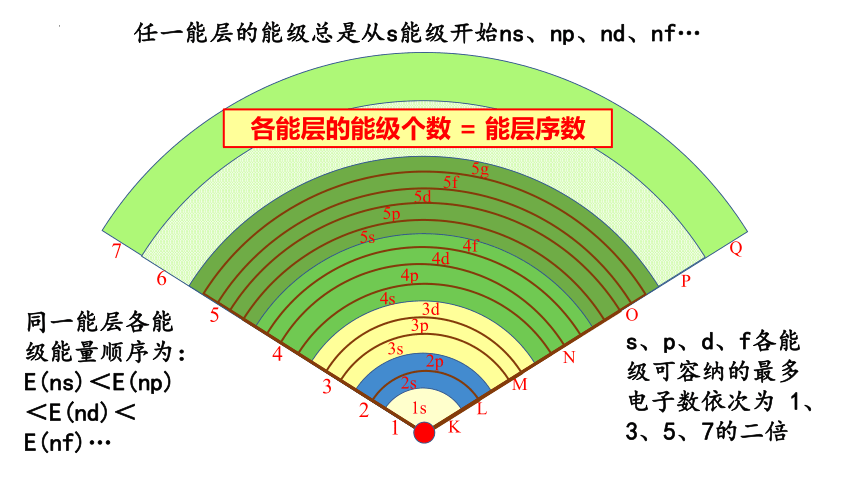
各能层的能级个数 = 能层序数
任一能层的能级总是从s能级开始ns、np、nd、nf…
同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
s、p、d、f各能级可容纳的最多电子数依次为 1、3、5、7的二倍
课本P7:
①能层的能级数等于该能层序数。
②任一能层的能级总是从s能级开始ns、np、nd、nf…
③s、p、d、f各能级可容纳的最多电子数依次为 1、3、5、7的二倍
④同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
能层(n) 能级 最多容纳电子数 序数 符号 各能级 各能层
1 K
2 L
3 M
4 N
… … … … …
n … … …
能层、能级与最多容纳的电子数
思考:1.能层的能级数与能层序数(n)间存在什么关系?一个能层最多可容纳电子数与能层序数(n)存在什么关系?
能层的能级数等于该能层序数。
一个能层最多可容纳的电子数为2n2个。
2.各个能级分别最多可容纳多少个电子?3d、4d、5d能级容纳电子数相同吗?
以s、p、d、f为符号的各能级可容纳的最多电子数依次为1、3、5、7的二倍。
3d、4d、5d能级所能容纳的最多电子数相同。
3.第五能层最多可容纳多少个电子?它们分别容纳在几个能级中?各能级最多容纳多少个电子?
第五能层最多可容纳50个电子;5个能级;
各能级最多容纳电子数分别为2,6,10,14,18个。
原子核外电子分层排布规律:
①各能层最多能容纳2n2个电子。
即: 能 层 序 号 1 2 3 4 5 6 7
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
②最外层电子数目不超过8个(K层为最外层时不超过2个);次外层电子数最多不超过18个;倒数第三层不超过32个。
③核外电子总是尽可能先排满能量最低、离核最近的能层,然后才由里往外,依次排在能量较高能层。而失电子总是先失最外层电子。能量最低原理
1. 下列能层中,不包含p能级的是( )
A.N B.M C.L D.K
2. 以下能级符号正确的是( )
A.6s B.2d C.3f D.1p
3. 判断正误(正确的打“√”,错误的打“×”)
(1)能层就是电子层,包含不同的能级( )
(2)能层越高,离原子核越远( )
(3)ns、np、nd最多容纳的电子数均为2( )
(4)每一能层均包含s、p、d、f能级( )
D
A
√
√
×
×
4. (1)已知短周期元素A、B,A元素原子的最外层电子数为m,次外层电子数为n;B元素原子的M层(有电子)电子数为m-n-1,L层电子数为m+n+2,则A为____(填元素符号,下同),B为_____。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子的多5,则X、Y分别为____、____。
C
Na
N
Mg
5.下列说法中有错误的是
A.某原子K层上只有一个电子
B.某离子M层和L层上的电子数均为K层的4倍
C.某原子M层上的电子数为L层电子数的4倍
D.存在核电荷数与最外层电子数相等的离子
6.下列有关能层和能级的叙述中正确的是
A.M能层有s、p共2个能级,最多能容纳8个电子
B.3d能级最多容纳5个电子,3f能级最多容纳7个电子
C.无论哪一能层的s能级最多容纳的电子数均为2
D.任一能层都有s、p能级,但不一定有d能级
C
C
二、基态与激发态 原子光谱
1.基态与激发态:
处于最低能量的原子叫做基态原子,当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。
H 1s1(最稳定) H 3s1
在日常生活中,我们看到的许多可见光,如灯光、霓虹灯光、激光、焰火等都与原子核外电子发生跃迁释放能量有关。
光(辐射)是电子跃迁释放能量的重要形式。
基态原子 激发态原子
吸收能量
释放能量
2.光谱:不同元素的原子发生跃迁时会吸收或放出不同的光,可以用光谱仪摄取各种元素的电子吸收光谱或发射光谱,总称原子光谱。
锂、氦、汞的吸收光谱
锂、氦、汞的发射光谱
基态原子 激发态原子
吸收光谱
发射光谱
氢原子的光谱
光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
小结
一、能级与能层
1、能层的能级数等于该能层序数
2、任一能层的能级总是从s能级开始ns、np、nd、nf…
3、s、p、d、f…各能级可容纳的最多电子数
4、同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
二、基态与激发态 原子光谱
第一章原子结构与性质
1.1.1能层与能级
第一节原子结构
教学目标
1.理解能层能级的概念,以及它们之间的关系。
2.知道原子核外电子的能层和能级分布及其能量关系。
3.知道基态与激发态,知道原子核外电子在一定条件下会发生跃迁产生原子光谱。
问题反馈
1、能层离核远近与能量高低有何关系?
2、第n能层中的不同能级的能量有何关系?
3、多电子原子中,电子的运动区域与其能量的高低之间有何关系?
4、能层与能级(原子轨道的类型)及原子轨道数目有何关系?
原子的诞生
1932年勒梅特首次提出了现代宇宙大爆炸理论:整个宇宙最初聚集在一个“原始原子”中,后来发生了大爆炸,碎片向四面八方散开,形成了我们的宇宙。大爆炸后两小时,诞生了大量的H、少量的He及极少量的Li,然后经过长或短的发展过程,以上元素发生原子核的熔合反应,分期分批的合成了其它元素。
导入
一、能层与能级
1.能层
按电子能量高低将核外电子分成不同的能层(电子层)
能量:从K至Q ,能层越高,离核越远,能层能量越高。
2.能级:
据同一能层中电子能量的差异分成不同的能级
能 层 一 二 三 四 五 六 七
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
1
K
2
L
M
N
O
P
Q
3
4
5
6
7
1s
2s
2p
3s
3p
3d
4s
4p
4d
4f
5s
5p
5d
5f
5g
各能层的能级个数 = 能层序数
任一能层的能级总是从s能级开始ns、np、nd、nf…
同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
s、p、d、f各能级可容纳的最多电子数依次为 1、3、5、7的二倍
课本P7:
①能层的能级数等于该能层序数。
②任一能层的能级总是从s能级开始ns、np、nd、nf…
③s、p、d、f各能级可容纳的最多电子数依次为 1、3、5、7的二倍
④同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
能层(n) 能级 最多容纳电子数 序数 符号 各能级 各能层
1 K
2 L
3 M
4 N
… … … … …
n … … …
能层、能级与最多容纳的电子数
思考:1.能层的能级数与能层序数(n)间存在什么关系?一个能层最多可容纳电子数与能层序数(n)存在什么关系?
能层的能级数等于该能层序数。
一个能层最多可容纳的电子数为2n2个。
2.各个能级分别最多可容纳多少个电子?3d、4d、5d能级容纳电子数相同吗?
以s、p、d、f为符号的各能级可容纳的最多电子数依次为1、3、5、7的二倍。
3d、4d、5d能级所能容纳的最多电子数相同。
3.第五能层最多可容纳多少个电子?它们分别容纳在几个能级中?各能级最多容纳多少个电子?
第五能层最多可容纳50个电子;5个能级;
各能级最多容纳电子数分别为2,6,10,14,18个。
原子核外电子分层排布规律:
①各能层最多能容纳2n2个电子。
即: 能 层 序 号 1 2 3 4 5 6 7
符 号 K L M N O P Q
最多电子数 2 8 18 32 50 72 98
②最外层电子数目不超过8个(K层为最外层时不超过2个);次外层电子数最多不超过18个;倒数第三层不超过32个。
③核外电子总是尽可能先排满能量最低、离核最近的能层,然后才由里往外,依次排在能量较高能层。而失电子总是先失最外层电子。能量最低原理
1. 下列能层中,不包含p能级的是( )
A.N B.M C.L D.K
2. 以下能级符号正确的是( )
A.6s B.2d C.3f D.1p
3. 判断正误(正确的打“√”,错误的打“×”)
(1)能层就是电子层,包含不同的能级( )
(2)能层越高,离原子核越远( )
(3)ns、np、nd最多容纳的电子数均为2( )
(4)每一能层均包含s、p、d、f能级( )
D
A
√
√
×
×
4. (1)已知短周期元素A、B,A元素原子的最外层电子数为m,次外层电子数为n;B元素原子的M层(有电子)电子数为m-n-1,L层电子数为m+n+2,则A为____(填元素符号,下同),B为_____。
(2)已知X元素原子的L层比Y元素原子的L层少3个电子,Y元素原子的核外电子总数比X元素原子的多5,则X、Y分别为____、____。
C
Na
N
Mg
5.下列说法中有错误的是
A.某原子K层上只有一个电子
B.某离子M层和L层上的电子数均为K层的4倍
C.某原子M层上的电子数为L层电子数的4倍
D.存在核电荷数与最外层电子数相等的离子
6.下列有关能层和能级的叙述中正确的是
A.M能层有s、p共2个能级,最多能容纳8个电子
B.3d能级最多容纳5个电子,3f能级最多容纳7个电子
C.无论哪一能层的s能级最多容纳的电子数均为2
D.任一能层都有s、p能级,但不一定有d能级
C
C
二、基态与激发态 原子光谱
1.基态与激发态:
处于最低能量的原子叫做基态原子,当基态原子的电子吸收能量后,电子会跃迁到较高能级,变成激发态原子。
H 1s1(最稳定) H 3s1
在日常生活中,我们看到的许多可见光,如灯光、霓虹灯光、激光、焰火等都与原子核外电子发生跃迁释放能量有关。
光(辐射)是电子跃迁释放能量的重要形式。
基态原子 激发态原子
吸收能量
释放能量
2.光谱:不同元素的原子发生跃迁时会吸收或放出不同的光,可以用光谱仪摄取各种元素的电子吸收光谱或发射光谱,总称原子光谱。
锂、氦、汞的吸收光谱
锂、氦、汞的发射光谱
基态原子 激发态原子
吸收光谱
发射光谱
氢原子的光谱
光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析。
小结
一、能级与能层
1、能层的能级数等于该能层序数
2、任一能层的能级总是从s能级开始ns、np、nd、nf…
3、s、p、d、f…各能级可容纳的最多电子数
4、同一能层各能级能量顺序为: E(ns)<E(np)<E(nd)<E(nf)…
二、基态与激发态 原子光谱
