第三章第3节 金属晶体与离子晶体(氯化钠晶体) 课件 (27张ppt) 2022-2023学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 第三章第3节 金属晶体与离子晶体(氯化钠晶体) 课件 (27张ppt) 2022-2023学年高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-31 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
NaCl
氯化钠晶体
人教版2019《选修2》第三章 第3节
咸阳市实验中学
赵迪
食用盐
氯碱工业
生理盐水
2NaCl + 2H2O 2NaOH + Cl2 ↑+H2 ↑
通电
制漂白液
制盐酸
制烧碱
NaCl
氯化钠晶体的物理性质
1
NaCl
氯化钠晶体
组成粒子:
粒子间相互作用:
Cl—
Na+
离子键
物理性质:
氯化钠晶体的物理性质
熔点 801 ℃
沸点 1413 ℃
无色立方晶体
氯化钠晶体
氯化钠晶体的物理性质
晶体不导电
水溶液可导电
熔融状态可导电
组成粒子:
粒子间相互作用:
Cl—
Na+
离子键
物理性质:
无色立方晶体
氯化钠晶体的结构特征
2
NaCl
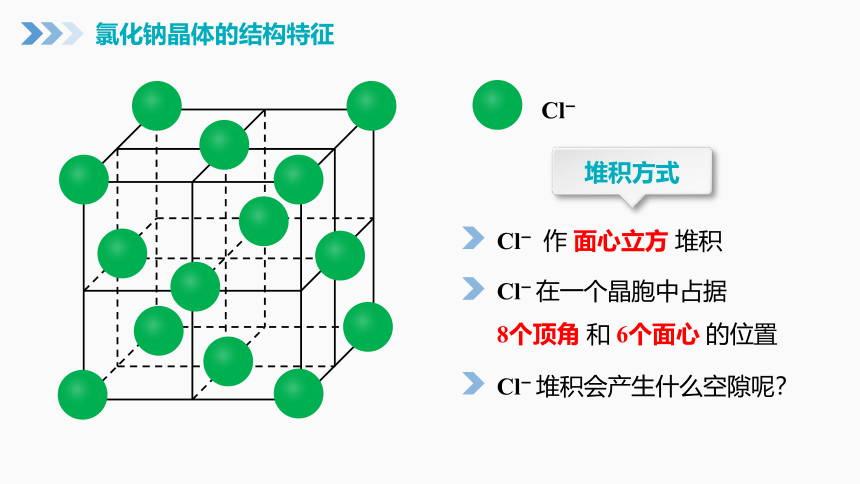
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
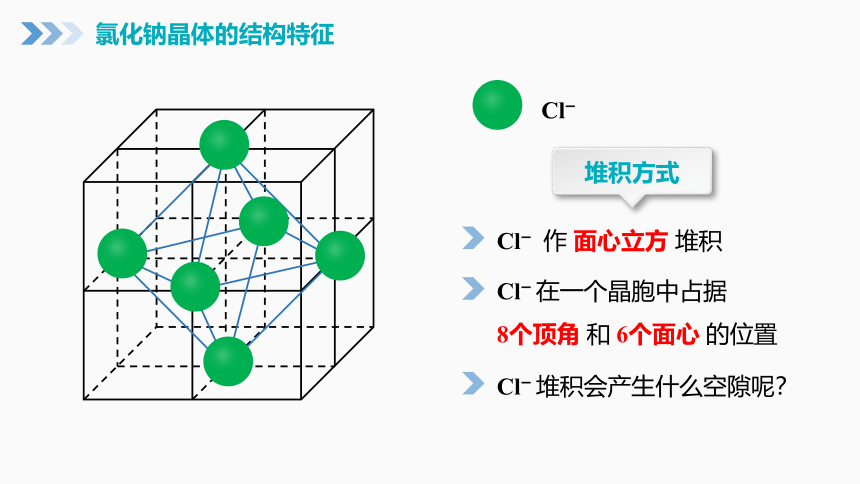
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
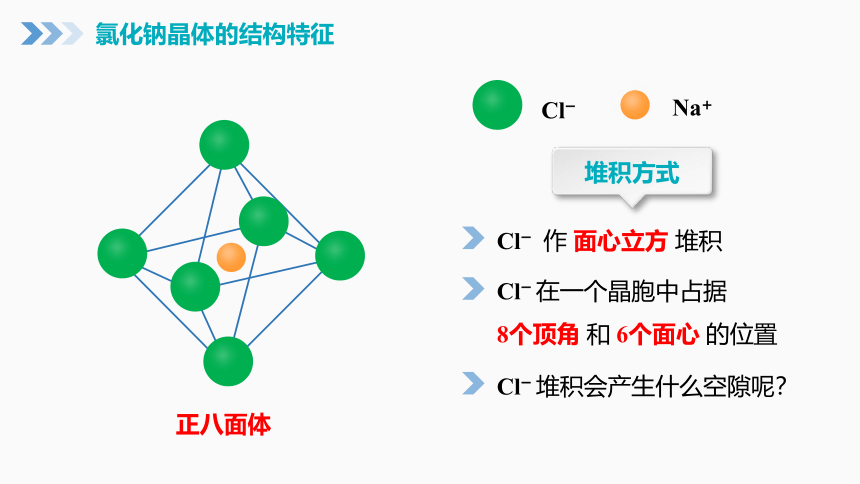
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
正八面体
Na+
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Na+ 填充在 正八面体 空隙中
正八面体
Na+
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Na+ 填充在 正八面体 空隙中
Na+ 在一个晶胞中占据
12个棱心 和 体心 的位置
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 ?
Na+ 的配位数是 ?
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 6
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 6
Na+ 的配位数是 6
Na+
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有几个 Cl— ?
Na+
8× = 1
顶角:
面心:
6× = 3
共:
1+3 = 4
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有几个 Na+ ?
Na+
12× = 3
棱心:
体心:
1×1 = 1
共:
3+1 = 4
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有 4 个 Cl—
Na+
1个晶胞中含有 4 个 Na+
1个晶胞中含有 4 个 结构基元
氯化钠晶体的结构特征
晶胞离子的分数坐标
Cl—
Cl— 的分数坐标
Na+
顶角:
面心:
(0,0,0)
( , ,0 )
( , 0, )
( 0, , )
氯化钠晶体的结构特征
晶胞离子的分数坐标
Cl—
Na+ 的分数坐标
Na+
棱心:
体心:
( , , )
( , 0, 0)
(0, , 0)
(0 , 0, )
氯化钠晶体的结构特征
NaCl 型离子晶体
Cl—
Na+
LiCl 晶体
KCl 晶体
NaBr 晶体
MgO 晶体
氯化钠晶体的密度计算
3
NaCl
氯化钠晶体的密度计算
ρ =
假设 r(Cl—) = q nm,r(Na+) = p nm,NaCl 的摩尔质量为 M g·mol-1 ,阿伏伽德罗常数为NA ,求氯化钠晶体的密度 的表达式。
1个NaCl 晶胞中含有4个结构基元,N = 4
NaCl 晶胞体积 V 如何计算?
思考
氯化钠晶体的密度计算
Cl—
Na+
a
a
氯化钠晶体的密度计算
Cl—
Na+
a
a =
2r(Cl—) + 2r(Na+)
r(Cl—) = q nm,r(Na+) = p nm
a = 2q+2p
V = a3 = (2q+2p) 3
氯化钠晶体的密度计算
ρ =
假设 r(Cl—) = q nm,r(Na+) = p nm,NaCl 的摩尔质量为 M g·mol-1 ,阿伏伽德罗常数为NA ,求氯化钠晶体的密度 的表达式。
带入相关数据可得
ρ =
NaCl 晶体的生长过程
认真细致,徐徐而行,最美结晶,不负未来
NaCl
谢谢您的观看
氯化钠晶体
咸阳市实验中学
赵迪
NaCl
氯化钠晶体
人教版2019《选修2》第三章 第3节
咸阳市实验中学
赵迪
食用盐
氯碱工业
生理盐水
2NaCl + 2H2O 2NaOH + Cl2 ↑+H2 ↑
通电
制漂白液
制盐酸
制烧碱
NaCl
氯化钠晶体的物理性质
1
NaCl
氯化钠晶体
组成粒子:
粒子间相互作用:
Cl—
Na+
离子键
物理性质:
氯化钠晶体的物理性质
熔点 801 ℃
沸点 1413 ℃
无色立方晶体
氯化钠晶体
氯化钠晶体的物理性质
晶体不导电
水溶液可导电
熔融状态可导电
组成粒子:
粒子间相互作用:
Cl—
Na+
离子键
物理性质:
无色立方晶体
氯化钠晶体的结构特征
2
NaCl
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Cl— 在一个晶胞中占据
8个顶角 和 6个面心 的位置
Cl— 堆积会产生什么空隙呢?
正八面体
Na+
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Na+ 填充在 正八面体 空隙中
正八面体
Na+
氯化钠晶体的结构特征
堆积方式
Cl—
Cl— 作 面心立方 堆积
Na+ 填充在 正八面体 空隙中
Na+ 在一个晶胞中占据
12个棱心 和 体心 的位置
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 ?
Na+ 的配位数是 ?
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 6
Na+
氯化钠晶体的结构特征
配位数
Cl—
Cl— 的配位数是 6
Na+ 的配位数是 6
Na+
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有几个 Cl— ?
Na+
8× = 1
顶角:
面心:
6× = 3
共:
1+3 = 4
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有几个 Na+ ?
Na+
12× = 3
棱心:
体心:
1×1 = 1
共:
3+1 = 4
氯化钠晶体的结构特征
晶胞所含结构基元
Cl—
1个晶胞中含有 4 个 Cl—
Na+
1个晶胞中含有 4 个 Na+
1个晶胞中含有 4 个 结构基元
氯化钠晶体的结构特征
晶胞离子的分数坐标
Cl—
Cl— 的分数坐标
Na+
顶角:
面心:
(0,0,0)
( , ,0 )
( , 0, )
( 0, , )
氯化钠晶体的结构特征
晶胞离子的分数坐标
Cl—
Na+ 的分数坐标
Na+
棱心:
体心:
( , , )
( , 0, 0)
(0, , 0)
(0 , 0, )
氯化钠晶体的结构特征
NaCl 型离子晶体
Cl—
Na+
LiCl 晶体
KCl 晶体
NaBr 晶体
MgO 晶体
氯化钠晶体的密度计算
3
NaCl
氯化钠晶体的密度计算
ρ =
假设 r(Cl—) = q nm,r(Na+) = p nm,NaCl 的摩尔质量为 M g·mol-1 ,阿伏伽德罗常数为NA ,求氯化钠晶体的密度 的表达式。
1个NaCl 晶胞中含有4个结构基元,N = 4
NaCl 晶胞体积 V 如何计算?
思考
氯化钠晶体的密度计算
Cl—
Na+
a
a
氯化钠晶体的密度计算
Cl—
Na+
a
a =
2r(Cl—) + 2r(Na+)
r(Cl—) = q nm,r(Na+) = p nm
a = 2q+2p
V = a3 = (2q+2p) 3
氯化钠晶体的密度计算
ρ =
假设 r(Cl—) = q nm,r(Na+) = p nm,NaCl 的摩尔质量为 M g·mol-1 ,阿伏伽德罗常数为NA ,求氯化钠晶体的密度 的表达式。
带入相关数据可得
ρ =
NaCl 晶体的生长过程
认真细致,徐徐而行,最美结晶,不负未来
NaCl
谢谢您的观看
氯化钠晶体
咸阳市实验中学
赵迪
