5.1降低化学反应活化能的酶(共44张PPT)
文档属性
| 名称 | 5.1降低化学反应活化能的酶(共44张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2025-09-18 00:00:00 | ||
图片预览











文档简介
(共44张PPT)
第1节 降低化学反应活化能的酶
第五章 细胞的能量供应和利用
1773年,意大利科学家斯帕兰扎尼做了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鹰把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内的肉块消失了。
讨论
1、为什么要将肉块放在金属笼内?
便于取出实验材料,排除物理性消化对肉块的影响,确定其是否发生了化学性消化
2、是什么物质使肉块消失了?
胃内的化学物质
3、怎样才能证明你的推测?
(收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解)
一、细胞代谢
从斯帕兰扎尼的实验中可知:胃液具有化学性消化的作用。然而体内不仅仅消化是化学反应,各种生命活动的进行都离不开化学反应。细胞中每时每刻都进行着许多化学反应,这统称为细胞代谢。细胞代谢离不开酶。
思考:细胞代谢的意义是什么?
细胞代谢是细胞生命活动的基础
二、酶在细胞代谢中的作用
细胞代谢是细胞生命活动的基础,但细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢。幸而细胞中含有另一种物质,能降过氧化氢及时分解为氧气和水,这种物质就是过氧化氢酶。除了过氧化氢酶,加热、FeCl3溶液也能使过氧化氢分解,但他们之间的效率一样吗?
探究1
比较过氧化氢在不同条件下的分解
实验原理
实验目的
通过比较H2O2过氧化氢在不同条件下分解的快慢,了解酶的作用和意义。
2 H2O2 2 H2O + O2
加热或Fe3+或过氧化氢酶
实验材料
新配制的体积分数为3%的H2O2溶液
新鲜的质量分数为20%的肝脏研磨液
质量分数为3.5%的FeCl3溶液
卫生香等
【经计算,质量分数为3.5%的FeCl3溶液和质量分数为20%的肝脏研磨液相比,每滴FeCl3溶液中的Fe3+数,大约是每滴肝脏研磨液中过氧化氢酶分子数的25万倍】
注意:
(1)要用新鲜肝脏研磨液,过氧化氢酶是一种蛋白质,不新鲜的肝脏研磨液中过氧化氢酶的活性较低或失活
(2)肝脏要磨碎,使肝脏细胞中的过氧化氢酶释放出来,可充分与过氧化氢接触,发挥作用
(3)过氧化氢溶液也要现用现配,因为过氧化氢不稳定
实验步骤
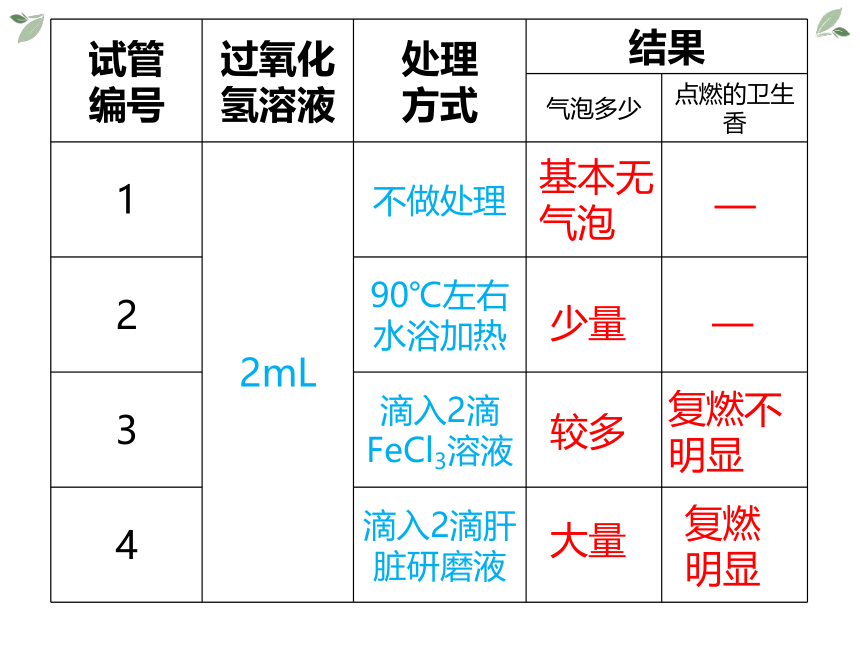
试管 编号 过氧化 氢溶液 处理 方式 结果 气泡多少 点燃的卫生香
1 2mL 不做处理
2 90℃左右水浴加热
3 滴入2滴FeCl3溶液
4 滴入2滴肝脏研磨液
基本无气泡
少量
较多
大量
—
—
复燃不明显
复燃明显
讨论
(1)2号管现象与1号管不同,说明了什么?
2号试管放出的气泡多。这一现象说明加热能促进过氧化氢的分解,提高反应速率
(2)3号和4号管并未加热,也有大量气泡产生,说明什么?
说明FeCl3中的Fe3+和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率。
(3)4号比3号相比,哪支试管的反应速率快说明什么?体现了酶的什么特点?为什么说酶对于细胞内化学反应的顺利进行至关重要?
3号。说明过氧化氢酶比Fe3+的催化效率高得多。体现了酶的高效性。细胞内每时每刻都在进行着成千上万种化学反应,这些化学反应需要在常温、常压下高效率地进行,只有酶能够满足这样的要求,所以说酶对于细胞内化学反应的顺利进行至关重要。
实验结论
(1)加热、FeCl3、过氧化氢酶都能加快过氧化氢分解的速率
(2)与无机催化剂FeCl3相比,过氧化氢酶的催化效率要高得多
实验过程中的注意事项
(1)滴加肝脏研磨液和FeCl3溶液时不能共用一支滴管,原因是少量酶混入FeCl3溶液中也会影响实验的准确性。
(2)气泡产生量越多,说明氧气产生量越多,卫生香燃烧越猛烈。
(3)加入催化剂后要振荡混匀,使催化剂和反应物(底物)充分接触。
(4)H2O2有轻度腐蚀性,使用时要小心,不要接触皮肤,实验后要及时洗手。
自变量 在实验中人为改变的量 试管2 90℃水浴
试管3 FeCl3溶液
试管4 肝脏研磨液
因变量 随自变量变化而变化的量 过氧化氢分解的速率 无关变量 除自变量外,实验中可能对实验结果造成影响的量 过氧化氢溶液的浓度、反应时间、肝脏的新鲜程度 通过以上实验,请思考产生这种结果的原因是什么?
Fe3+和过氧化氢酶降低了过氧化氢分解反应的活化能
分子从常态转变为容易发生化学反应的活跃状态所需要的能量成为活化能
与无机催化剂相比,酶降低活化能的作用更显著,催化效率更高
正是由于酶的催化作用,细胞代谢才能在温和条件(常温、常压、生理pH)下快速有序的进行
那么酶到底是什么物质?
三、酶的本质
发酵是纯化学反应,与生命活动无关
发酵与整个细
胞的活动有关
发酵与细胞中
某些物质有关
酵母细胞中的某物质能在细胞外起作用
酶是蛋白质
巴斯德之前
巴斯德
李比希
毕希纳
萨姆纳
切赫、奥尔特曼
少数RNA也具有生物催化功能
酶是活细胞产生的具有催化作用的有机物。
绝大多数是蛋白质,少数是RNA
来源
功能
化学本质
活细胞产生的
催化剂
酶
四、酶的特性
酶的化学本质不同于无机催化剂。一般来说,酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
酶的催化作用与无机催化剂有什么不同呢?酶有哪些特性?
1、酶具有高效性
大量实验数据表明,酶的催化效率一般是无机催化剂的107~1013倍。
酶高效性的曲线:
无机催化剂催化的化学反应范围比较广。例如,酸既能催化蛋白质水解,也能催化脂肪水解,还能催化淀粉水解。
酶能像无机催化剂一样,催化多种化学反应吗?
探究2
淀粉酶对淀粉和蔗糖的水解作用
实验原理
(1)淀粉和蔗糖都是非还原糖,它们在酶的催化作用下都能水解成还原糖
(2)还原糖与斐林试剂在水浴加热条件下反应生成砖红色沉淀
实验目的
探究淀粉酶是否只能催化特定的化学反应(探究酶的专一性)
实验材料
质量分数为2%的新配制的淀粉酶溶液
质量分数为3%的可溶性淀粉溶液
质量分数为3%的蔗糖溶液
斐林试剂
热水
新配制:
保证淀粉酶有较高的活性
实验步骤
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL —
2 注入蔗糖溶液 — 2mL
3 注入新鲜的淀粉酶溶液 2mL 2mL
4 轻轻震荡,保温5min 60℃ 左右 60℃
左右
5 加入斐林试剂,轻轻震荡 2mL 2mL
6 水浴加热 煮沸并保持1min 7 记录实验结果
砖红色
浅蓝色
注意:
震荡试管的目的:使试管内的液体混合均匀
淀粉酶的最适温度为60℃左右,此温度下酶的活性最高,催化效率最高
思考:
在已知淀粉酶能够催化淀粉水解的情况下,本实验设置1号管还有没有必要?为什么?
有必要。排除无关变量对实验的影响
实验结论
淀粉酶只能催化淀粉水解,即每一种酶只能催化一种或一类化学反应
2、酶具有专一性
每一种酶只能催化一种或一类化学反应。
许多无机催化剂能在高温、高压、强酸或强碱条件下催化化学反应。那么酶起催化作用需要怎样的条件呢?
探究3 影响酶活性的条件
酶催化特定化学反应的能力称为酶活性
酶活性可用在一定条件下酶催化某一化学反应的速率表示
酶活性含义:
单位时间内生物的生成量
单位时间内反应物的减少量
到平衡点所用时间的长短
实验原理
(1)探究温度对酶活性的影响
温度影响酶的活性,从而影响淀粉的水解,滴加碘液后,根据是否出现蓝色及蓝色深浅来判断酶的活性。
(2)探究pH对酶活性的影响
pH影响酶的活性,从而影响O2的生成量,可用带火星的卫生香来检测O2的产生量
2 H2O2 2 H2O + O2
过氧化氢酶
实验步骤
(1)温度对酶活性的影响
(2)pH对酶活性的影响
3、酶的作用条件较温和
通过实验可以看出,溶液的温度和pH都对酶活性有影响。与无机催化剂相比,酶所催化的化学反应一般是在比较温和的条件下进行的。在最适宜的温度和pH条件下,酶的活性最高。
一般来说,动物体内的酶最适温度在35~40℃;植物体内的酶最适温度在40~50℃;细菌和真菌体内的酶最适温度差别较大,有的酶最适温度可高达70℃。动物体内的酶最适pH大多在6.5~8.0,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶最适pH大多为4.5~6.5。
拓展 与酶有关的曲线
a、b曲线相比较才可说明酶催化作用的高效性;a、c曲线只能说明酶具有催化作用
每一种酶只能催化一种或一类化学反应。
温度低于最适温度时
酶活性随着温度的升高而上升
温度高于最适温度时
酶活性随着温度的升高而下降
最适温度时:
酶活性最高
高温能使酶的空间结构受到破坏而使酶失活,低温虽降低酶活性,但未破坏酶的空间结构,适宜低温下可恢复活性
过氧化氢酶
在过酸过碱的条件下,都会使酶的空间结构遭到破坏而失去活性。
在最适合的pH下,酶的活性最高
酶的浓度:反应速率随酶浓度的升高而加快。
底物浓度:在一定浓度范围内,反应速率随浓度的升高而加快,但达到一定浓度,反应速率不再变化。
课堂总结
降低化学反应的活化能
细胞代谢
酶在细胞代谢中的作用
酶的本质
酶的特性
酶的作用和本质
作用条件较温和
专一性
高效性
第1节 降低化学反应活化能的酶
第五章 细胞的能量供应和利用
1773年,意大利科学家斯帕兰扎尼做了一个巧妙的实验:将肉块放入小巧的金属笼内,然后让鹰把小笼子吞下去。过一段时间后,他把小笼子取出来,发现笼内的肉块消失了。
讨论
1、为什么要将肉块放在金属笼内?
便于取出实验材料,排除物理性消化对肉块的影响,确定其是否发生了化学性消化
2、是什么物质使肉块消失了?
胃内的化学物质
3、怎样才能证明你的推测?
(收集胃内的化学物质,看看这些物质在体外是否也能将肉块分解)
一、细胞代谢
从斯帕兰扎尼的实验中可知:胃液具有化学性消化的作用。然而体内不仅仅消化是化学反应,各种生命活动的进行都离不开化学反应。细胞中每时每刻都进行着许多化学反应,这统称为细胞代谢。细胞代谢离不开酶。
思考:细胞代谢的意义是什么?
细胞代谢是细胞生命活动的基础
二、酶在细胞代谢中的作用
细胞代谢是细胞生命活动的基础,但细胞代谢中也会产生代谢废物,甚至会产生对细胞有害的物质,如过氧化氢。幸而细胞中含有另一种物质,能降过氧化氢及时分解为氧气和水,这种物质就是过氧化氢酶。除了过氧化氢酶,加热、FeCl3溶液也能使过氧化氢分解,但他们之间的效率一样吗?
探究1
比较过氧化氢在不同条件下的分解
实验原理
实验目的
通过比较H2O2过氧化氢在不同条件下分解的快慢,了解酶的作用和意义。
2 H2O2 2 H2O + O2
加热或Fe3+或过氧化氢酶
实验材料
新配制的体积分数为3%的H2O2溶液
新鲜的质量分数为20%的肝脏研磨液
质量分数为3.5%的FeCl3溶液
卫生香等
【经计算,质量分数为3.5%的FeCl3溶液和质量分数为20%的肝脏研磨液相比,每滴FeCl3溶液中的Fe3+数,大约是每滴肝脏研磨液中过氧化氢酶分子数的25万倍】
注意:
(1)要用新鲜肝脏研磨液,过氧化氢酶是一种蛋白质,不新鲜的肝脏研磨液中过氧化氢酶的活性较低或失活
(2)肝脏要磨碎,使肝脏细胞中的过氧化氢酶释放出来,可充分与过氧化氢接触,发挥作用
(3)过氧化氢溶液也要现用现配,因为过氧化氢不稳定
实验步骤
试管 编号 过氧化 氢溶液 处理 方式 结果 气泡多少 点燃的卫生香
1 2mL 不做处理
2 90℃左右水浴加热
3 滴入2滴FeCl3溶液
4 滴入2滴肝脏研磨液
基本无气泡
少量
较多
大量
—
—
复燃不明显
复燃明显
讨论
(1)2号管现象与1号管不同,说明了什么?
2号试管放出的气泡多。这一现象说明加热能促进过氧化氢的分解,提高反应速率
(2)3号和4号管并未加热,也有大量气泡产生,说明什么?
说明FeCl3中的Fe3+和新鲜肝脏中的过氧化氢酶都能加快过氧化氢分解的速率。
(3)4号比3号相比,哪支试管的反应速率快说明什么?体现了酶的什么特点?为什么说酶对于细胞内化学反应的顺利进行至关重要?
3号。说明过氧化氢酶比Fe3+的催化效率高得多。体现了酶的高效性。细胞内每时每刻都在进行着成千上万种化学反应,这些化学反应需要在常温、常压下高效率地进行,只有酶能够满足这样的要求,所以说酶对于细胞内化学反应的顺利进行至关重要。
实验结论
(1)加热、FeCl3、过氧化氢酶都能加快过氧化氢分解的速率
(2)与无机催化剂FeCl3相比,过氧化氢酶的催化效率要高得多
实验过程中的注意事项
(1)滴加肝脏研磨液和FeCl3溶液时不能共用一支滴管,原因是少量酶混入FeCl3溶液中也会影响实验的准确性。
(2)气泡产生量越多,说明氧气产生量越多,卫生香燃烧越猛烈。
(3)加入催化剂后要振荡混匀,使催化剂和反应物(底物)充分接触。
(4)H2O2有轻度腐蚀性,使用时要小心,不要接触皮肤,实验后要及时洗手。
自变量 在实验中人为改变的量 试管2 90℃水浴
试管3 FeCl3溶液
试管4 肝脏研磨液
因变量 随自变量变化而变化的量 过氧化氢分解的速率 无关变量 除自变量外,实验中可能对实验结果造成影响的量 过氧化氢溶液的浓度、反应时间、肝脏的新鲜程度 通过以上实验,请思考产生这种结果的原因是什么?
Fe3+和过氧化氢酶降低了过氧化氢分解反应的活化能
分子从常态转变为容易发生化学反应的活跃状态所需要的能量成为活化能
与无机催化剂相比,酶降低活化能的作用更显著,催化效率更高
正是由于酶的催化作用,细胞代谢才能在温和条件(常温、常压、生理pH)下快速有序的进行
那么酶到底是什么物质?
三、酶的本质
发酵是纯化学反应,与生命活动无关
发酵与整个细
胞的活动有关
发酵与细胞中
某些物质有关
酵母细胞中的某物质能在细胞外起作用
酶是蛋白质
巴斯德之前
巴斯德
李比希
毕希纳
萨姆纳
切赫、奥尔特曼
少数RNA也具有生物催化功能
酶是活细胞产生的具有催化作用的有机物。
绝大多数是蛋白质,少数是RNA
来源
功能
化学本质
活细胞产生的
催化剂
酶
四、酶的特性
酶的化学本质不同于无机催化剂。一般来说,酶是活细胞产生的具有催化作用的有机物,其中绝大多数酶是蛋白质。
酶的催化作用与无机催化剂有什么不同呢?酶有哪些特性?
1、酶具有高效性
大量实验数据表明,酶的催化效率一般是无机催化剂的107~1013倍。
酶高效性的曲线:
无机催化剂催化的化学反应范围比较广。例如,酸既能催化蛋白质水解,也能催化脂肪水解,还能催化淀粉水解。
酶能像无机催化剂一样,催化多种化学反应吗?
探究2
淀粉酶对淀粉和蔗糖的水解作用
实验原理
(1)淀粉和蔗糖都是非还原糖,它们在酶的催化作用下都能水解成还原糖
(2)还原糖与斐林试剂在水浴加热条件下反应生成砖红色沉淀
实验目的
探究淀粉酶是否只能催化特定的化学反应(探究酶的专一性)
实验材料
质量分数为2%的新配制的淀粉酶溶液
质量分数为3%的可溶性淀粉溶液
质量分数为3%的蔗糖溶液
斐林试剂
热水
新配制:
保证淀粉酶有较高的活性
实验步骤
序号 项目 试管1 试管2
1 注入可溶性淀粉溶液 2mL —
2 注入蔗糖溶液 — 2mL
3 注入新鲜的淀粉酶溶液 2mL 2mL
4 轻轻震荡,保温5min 60℃ 左右 60℃
左右
5 加入斐林试剂,轻轻震荡 2mL 2mL
6 水浴加热 煮沸并保持1min 7 记录实验结果
砖红色
浅蓝色
注意:
震荡试管的目的:使试管内的液体混合均匀
淀粉酶的最适温度为60℃左右,此温度下酶的活性最高,催化效率最高
思考:
在已知淀粉酶能够催化淀粉水解的情况下,本实验设置1号管还有没有必要?为什么?
有必要。排除无关变量对实验的影响
实验结论
淀粉酶只能催化淀粉水解,即每一种酶只能催化一种或一类化学反应
2、酶具有专一性
每一种酶只能催化一种或一类化学反应。
许多无机催化剂能在高温、高压、强酸或强碱条件下催化化学反应。那么酶起催化作用需要怎样的条件呢?
探究3 影响酶活性的条件
酶催化特定化学反应的能力称为酶活性
酶活性可用在一定条件下酶催化某一化学反应的速率表示
酶活性含义:
单位时间内生物的生成量
单位时间内反应物的减少量
到平衡点所用时间的长短
实验原理
(1)探究温度对酶活性的影响
温度影响酶的活性,从而影响淀粉的水解,滴加碘液后,根据是否出现蓝色及蓝色深浅来判断酶的活性。
(2)探究pH对酶活性的影响
pH影响酶的活性,从而影响O2的生成量,可用带火星的卫生香来检测O2的产生量
2 H2O2 2 H2O + O2
过氧化氢酶
实验步骤
(1)温度对酶活性的影响
(2)pH对酶活性的影响
3、酶的作用条件较温和
通过实验可以看出,溶液的温度和pH都对酶活性有影响。与无机催化剂相比,酶所催化的化学反应一般是在比较温和的条件下进行的。在最适宜的温度和pH条件下,酶的活性最高。
一般来说,动物体内的酶最适温度在35~40℃;植物体内的酶最适温度在40~50℃;细菌和真菌体内的酶最适温度差别较大,有的酶最适温度可高达70℃。动物体内的酶最适pH大多在6.5~8.0,但也有例外,如胃蛋白酶的最适pH为1.5;植物体内的酶最适pH大多为4.5~6.5。
拓展 与酶有关的曲线
a、b曲线相比较才可说明酶催化作用的高效性;a、c曲线只能说明酶具有催化作用
每一种酶只能催化一种或一类化学反应。
温度低于最适温度时
酶活性随着温度的升高而上升
温度高于最适温度时
酶活性随着温度的升高而下降
最适温度时:
酶活性最高
高温能使酶的空间结构受到破坏而使酶失活,低温虽降低酶活性,但未破坏酶的空间结构,适宜低温下可恢复活性
过氧化氢酶
在过酸过碱的条件下,都会使酶的空间结构遭到破坏而失去活性。
在最适合的pH下,酶的活性最高
酶的浓度:反应速率随酶浓度的升高而加快。
底物浓度:在一定浓度范围内,反应速率随浓度的升高而加快,但达到一定浓度,反应速率不再变化。
课堂总结
降低化学反应的活化能
细胞代谢
酶在细胞代谢中的作用
酶的本质
酶的特性
酶的作用和本质
作用条件较温和
专一性
高效性
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
