化学人教版(2019)必修第一册1.1.2分散系及其分类(共22张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.2分散系及其分类(共22张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 22.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-31 17:15:01 | ||
图片预览




文档简介
(共22张PPT)
分散系及其分类
2. 分散系及其分类
(1)分散系
溶液
乳浊液
悬浊液
2. 分散系及其分类
(1)分散系
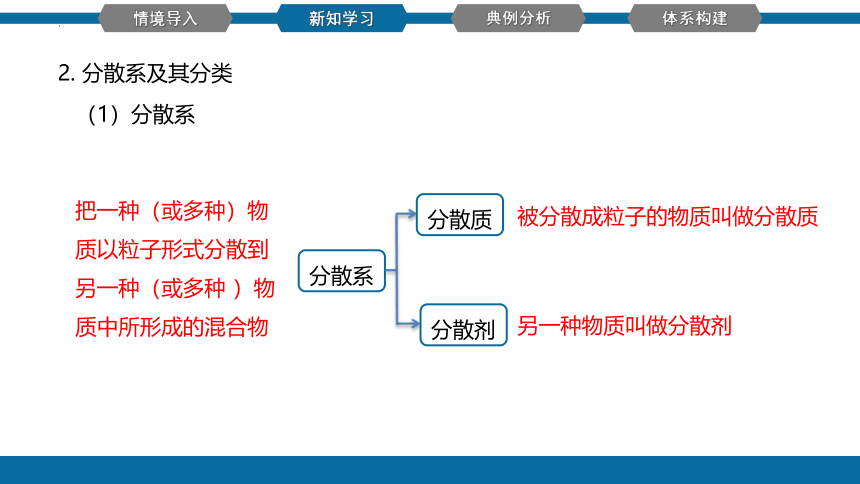
把一种(或多种)物质以粒子形式分散到另一种(或多种 )物质中所形成的混合物
分散系
分散质
分散剂
被分散成粒子的物质叫做分散质
另一种物质叫做分散剂
(1)分散系
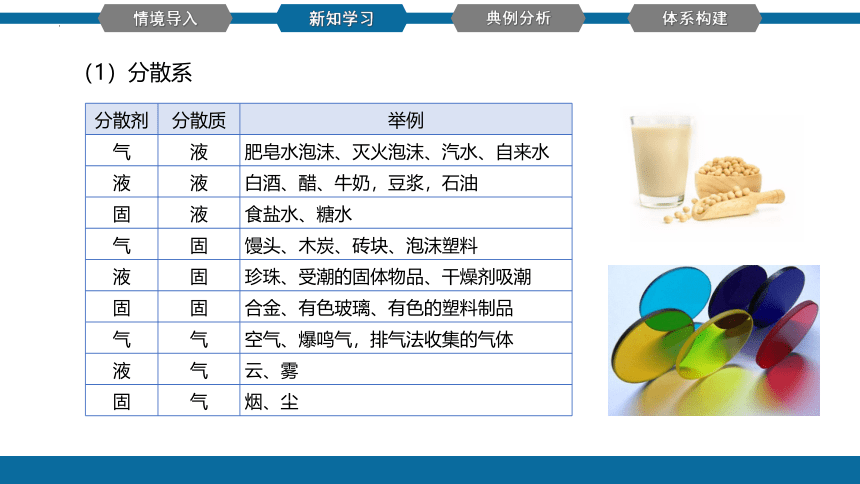
分散剂 分散质 举例
气 液 肥皂水泡沫、灭火泡沫、汽水、自来水
液 液 白酒、醋、牛奶,豆浆,石油
固 液 食盐水、糖水
气 固 馒头、木炭、砖块、泡沫塑料
液 固 珍珠、受潮的固体物品、干燥剂吸潮
固 固 合金、有色玻璃、有色的塑料制品
气 气 空气、爆鸣气,排气法收集的气体
液 气 云、雾
固 气 烟、尘
(1)分散系
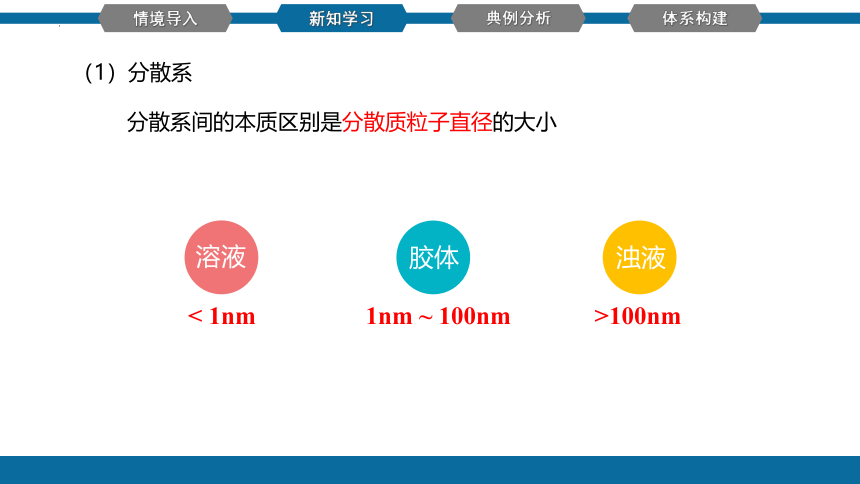
溶液
浊液
< 1nm
1nm ~ 100nm
>100nm
胶体
分散系间的本质区别是分散质粒子直径的大小
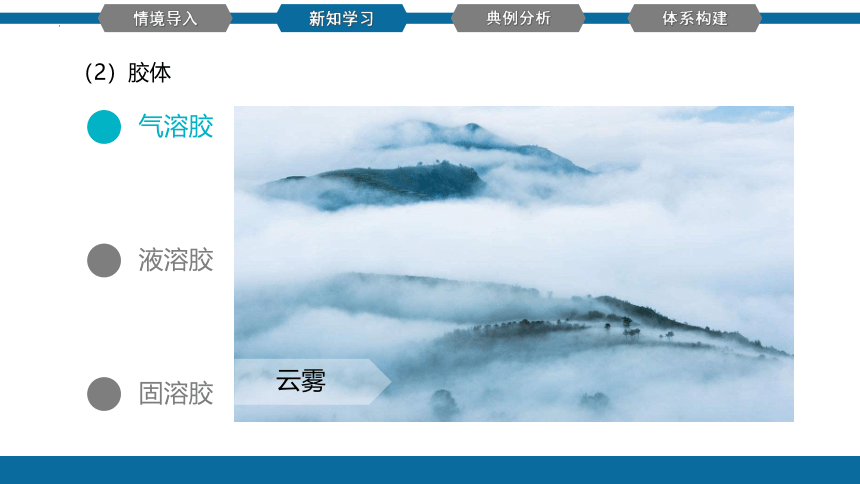
(2)胶体
气溶胶
液溶胶
固溶胶
云雾
(2)胶体
气溶胶
液溶胶
固溶胶
油漆
(2)胶体
气溶胶
液溶胶
固溶胶
土壤
(2)胶体
FeCl3 + 3H2O Fe(OH)3 (胶体)+ 3HCl
△
向小烧杯中加入40mL 蒸馏水,加热至沸腾,向沸水中逐滴加入5~6滴 FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。
制备 Fe(OH)3 胶体
(2)胶体
如何
区
分
?
Fe(OH)3 胶体
CuSO4 溶液
(2)胶体
丁达尔效应
有一条光亮的通路
无光亮的通路
胶体粒子对光线散射形成的
(2)胶体
丁达尔效应
(2)胶体
胶体的聚沉
胶粒运动加剧
碰撞增多
胶核对离子的吸附作用减弱
胶体聚沉
(2)胶体
胶体的聚沉
加入带相反电荷的胶粒
相互吸引
体积变大
胶体聚沉
电解质电离
中和胶粒所带电荷
聚集沉降
加入电解质溶液
(2)胶体
胶体的聚沉
豆腐的制作
豆浆
豆腐
加入卤水、石膏
(2)胶体
胶体的聚沉
河水
形成三角洲
汇入海水中
三角洲的形成
(2)胶体
胶体的电泳
胶体粒子在外加电场作用下做定向移动
【例题】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1) 若将FeCl3饱和溶液分别滴入下列物质中,能形成胶体的是 _____
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2) 写出制备Fe(OH)3胶体的化学方程式: 。
(3) 怎样检验制得的物质是胶体? ,
。
(4) 取少量制得的胶体加入试管中,然后加入 (NH4)2SO4 溶液,现象是 ,
这种现象称为胶体的 。
(5) Fe(OH)3胶体区别于FeCl3溶液的本质特征是______
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体可产生丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质能透过滤纸
B
FeCl3 + 3H2O == Fe(OH)3 (胶体)+ 3HCl
△
A
聚沉
产生红褐色沉淀
让一束光线通过制得的物质
若能从侧面观察到一条光亮的“通路”,则说明制得的是胶体
溶液 胶体 浊液
分散质粒子种类 分子、离子 较多分子集合体或大分子 大量分子集合体
分散质粒子直径 d<1 nm 1 nm100 nm
外部特征 均一、透明、稳定 均一、透明、较稳定 不均一、不透明、
不稳定
稳定性 稳定 介稳体系 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
鉴别方法 无丁达尔效应 有丁达尔效应 静置分层
实例 碘酒、蔗糖溶液、盐酸 豆浆、云、雾、烟 泥浆、油水混合物
谢谢观看!
分散系及其分类
2. 分散系及其分类
(1)分散系
溶液
乳浊液
悬浊液
2. 分散系及其分类
(1)分散系
把一种(或多种)物质以粒子形式分散到另一种(或多种 )物质中所形成的混合物
分散系
分散质
分散剂
被分散成粒子的物质叫做分散质
另一种物质叫做分散剂
(1)分散系
分散剂 分散质 举例
气 液 肥皂水泡沫、灭火泡沫、汽水、自来水
液 液 白酒、醋、牛奶,豆浆,石油
固 液 食盐水、糖水
气 固 馒头、木炭、砖块、泡沫塑料
液 固 珍珠、受潮的固体物品、干燥剂吸潮
固 固 合金、有色玻璃、有色的塑料制品
气 气 空气、爆鸣气,排气法收集的气体
液 气 云、雾
固 气 烟、尘
(1)分散系
溶液
浊液
< 1nm
1nm ~ 100nm
>100nm
胶体
分散系间的本质区别是分散质粒子直径的大小
(2)胶体
气溶胶
液溶胶
固溶胶
云雾
(2)胶体
气溶胶
液溶胶
固溶胶
油漆
(2)胶体
气溶胶
液溶胶
固溶胶
土壤
(2)胶体
FeCl3 + 3H2O Fe(OH)3 (胶体)+ 3HCl
△
向小烧杯中加入40mL 蒸馏水,加热至沸腾,向沸水中逐滴加入5~6滴 FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。
制备 Fe(OH)3 胶体
(2)胶体
如何
区
分
?
Fe(OH)3 胶体
CuSO4 溶液
(2)胶体
丁达尔效应
有一条光亮的通路
无光亮的通路
胶体粒子对光线散射形成的
(2)胶体
丁达尔效应
(2)胶体
胶体的聚沉
胶粒运动加剧
碰撞增多
胶核对离子的吸附作用减弱
胶体聚沉
(2)胶体
胶体的聚沉
加入带相反电荷的胶粒
相互吸引
体积变大
胶体聚沉
电解质电离
中和胶粒所带电荷
聚集沉降
加入电解质溶液
(2)胶体
胶体的聚沉
豆腐的制作
豆浆
豆腐
加入卤水、石膏
(2)胶体
胶体的聚沉
河水
形成三角洲
汇入海水中
三角洲的形成
(2)胶体
胶体的电泳
胶体粒子在外加电场作用下做定向移动
【例题】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1) 若将FeCl3饱和溶液分别滴入下列物质中,能形成胶体的是 _____
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
(2) 写出制备Fe(OH)3胶体的化学方程式: 。
(3) 怎样检验制得的物质是胶体? ,
。
(4) 取少量制得的胶体加入试管中,然后加入 (NH4)2SO4 溶液,现象是 ,
这种现象称为胶体的 。
(5) Fe(OH)3胶体区别于FeCl3溶液的本质特征是______
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体可产生丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质能透过滤纸
B
FeCl3 + 3H2O == Fe(OH)3 (胶体)+ 3HCl
△
A
聚沉
产生红褐色沉淀
让一束光线通过制得的物质
若能从侧面观察到一条光亮的“通路”,则说明制得的是胶体
溶液 胶体 浊液
分散质粒子种类 分子、离子 较多分子集合体或大分子 大量分子集合体
分散质粒子直径 d<1 nm 1 nm
外部特征 均一、透明、稳定 均一、透明、较稳定 不均一、不透明、
不稳定
稳定性 稳定 介稳体系 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
鉴别方法 无丁达尔效应 有丁达尔效应 静置分层
实例 碘酒、蔗糖溶液、盐酸 豆浆、云、雾、烟 泥浆、油水混合物
谢谢观看!
