10.2.2 溶液酸碱度的表示法——pH(课件17页)
文档属性
| 名称 | 10.2.2 溶液酸碱度的表示法——pH(课件17页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 80.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-03 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第十单元 酸和碱
课题2 酸和碱的中和反应
第二课时 溶液酸碱度的表示法—pH
人教版九年级下册
新课引入
山茶花花姿丰盈,端庄高雅,为中国传统十大名花之一,也是世界名花之一。常用弱酸性腐殖土来种植山茶花,但土壤的酸性过强会影响山茶花的生长。
如何来比较土壤的酸性强弱呢?
新课讲解
一、溶液的酸碱性与酸碱度
溶液的酸碱性指的是溶液呈酸性、碱性还是中性,常用酸碱指示剂测定;
溶液的酸碱度是表示酸碱性的强弱程度。稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
新课讲解
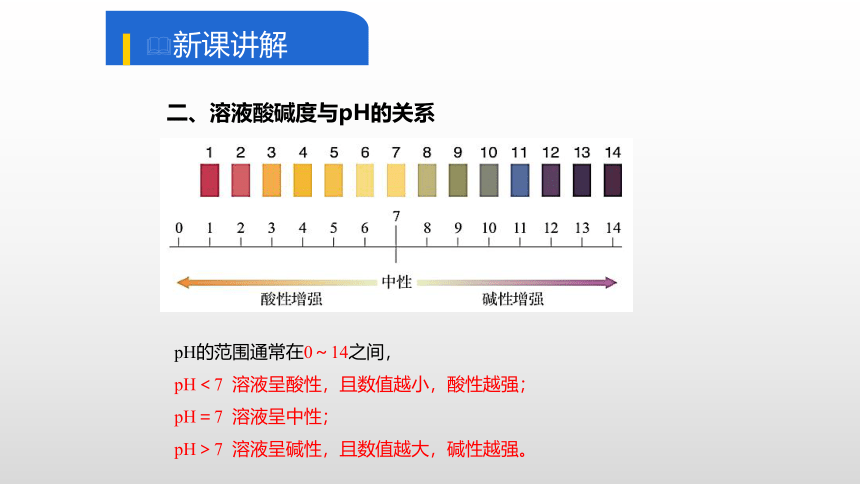
二、溶液酸碱度与pH的关系
pH的范围通常在0~14之间,
pH<7 溶液呈酸性,且数值越小,酸性越强;
pH=7 溶液呈中性;
pH>7 溶液呈碱性,且数值越大,碱性越强。
新课讲解
三、溶液酸碱度的测定
新课讲解
测定方法:
取一块pH试纸放在玻璃片上,用玻璃棒蘸取少量待测溶液,滴在pH试纸上,把试纸显示的颜色跟标准比色卡对照,便可粗略知道溶液的pH。
新课讲解
【注意事项】
1、不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂;
2、pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后溶液的酸碱度,导致测定结果不准确。
新课讲解
四、溶液酸碱度对生产、生活及人类生命活动的意义
生活中常见物质的pH
新课讲解
化工生产中许多反应必须在一定pH的溶液中才能进行。
1
农作物一般适宜在pH接近于7或等于7的土壤中生长。
2
测定雨水的pH,可了解空气的污染状况
3
测定体液或排出物的pH,可了解人体的健康状况。
4
(酸雨是指pH<5.6的雨水)
新课讲解
【知识拓展】
向氢氧化钠溶液中逐滴滴加盐酸,溶液的pH随盐酸滴入量的图像如下:
(1)V表示盐酸与氢氧化钠完全反应时,盐酸的体积。
(2)图像不是直线,而是平滑的曲线。
开始加入盐酸时,曲线变化缓慢,随着盐酸的加入,曲线陡降,当完全反应时,pH=7;继续加盐酸,pH<7,曲线逐渐趋于平缓,逐渐接近所加盐酸的pH。
归纳小结
1、利用pH来表示溶液酸碱性的强弱;利用数轴来理解pH的定义,并比较溶液的酸碱性强弱;
2、pH试纸可以粗略测定溶液的酸碱度;掌握正确测定溶液酸碱度的方法。
1、下列物质呈碱性的是( )
A.血液,pH为7.35~7.45 B.胃液,pH为0.9~1.5
C.牛奶,pH为6.3~6.6 D.苹果汁,pH为2.9~3.3
强化训练
A
【解析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性。
A、血液,pH为7.35~7.45,大于7,呈碱性;
B、胃液,pH为0.9~1.5,小于7,呈酸性;
C、牛奶,pH为6.3~6.6,小于7,呈酸性;
D、苹果汁,pH为2.9~3.3,小于7,呈酸性。
强化训练
2、下列是人体内一些体液的正常pH值范围,其中酸性最强的体液是
( )
A.唾液 B.胃液 C.胆汁 D.胰液
B
【解析】当pH<7时,呈酸性,当pH>7时,呈碱性,当溶液的pH小于7时,随着pH的减小,酸性逐渐增强。A、唾液的pH为6.6~7.1,接近中性;
B、胃液的pH为0.9~1.5,呈强酸性;C、胆汁的pH为7.1~7.3,呈弱碱性;
D、胰液的pH为7.5~8.0,呈弱碱性。
液体 唾液 胃液 胆汁 胰液
pH 6.6~7.1 0.9~1.5 7.1~7.3 7.5~8.0
强化训练
3、一些食物pH 的近似值范围如下:橘子汁3.0~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0。下列说法中,不正确的是( )
A.鸡蛋清显碱性
B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红
D.牛奶比橘子汁的酸性强
D
【解析】
A、鸡蛋清的pH为7.6~8.0,呈弱碱性,故A正确;
B、泡菜的pH为3.2~3.6,呈酸性,胃酸过多的人不宜多吃,故B正确;
C、橘子汁呈酸性,石蕊试液在酸性溶液中变红,故C正确;
D、牛奶和橘子汁的pH都小于7,显酸性,牛奶的pH比橘子汁的pH大,酸性比橘子汁弱,故D错误。
布置作业
某小型造纸厂向河水中非法排放了大量碱性废液。请你根据所学的知识,谈一下如何检测受污染河水的pH。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
第十单元 酸和碱
课题2 酸和碱的中和反应
第二课时 溶液酸碱度的表示法—pH
人教版九年级下册
新课引入
山茶花花姿丰盈,端庄高雅,为中国传统十大名花之一,也是世界名花之一。常用弱酸性腐殖土来种植山茶花,但土壤的酸性过强会影响山茶花的生长。
如何来比较土壤的酸性强弱呢?
新课讲解
一、溶液的酸碱性与酸碱度
溶液的酸碱性指的是溶液呈酸性、碱性还是中性,常用酸碱指示剂测定;
溶液的酸碱度是表示酸碱性的强弱程度。稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
新课讲解
二、溶液酸碱度与pH的关系
pH的范围通常在0~14之间,
pH<7 溶液呈酸性,且数值越小,酸性越强;
pH=7 溶液呈中性;
pH>7 溶液呈碱性,且数值越大,碱性越强。
新课讲解
三、溶液酸碱度的测定
新课讲解
测定方法:
取一块pH试纸放在玻璃片上,用玻璃棒蘸取少量待测溶液,滴在pH试纸上,把试纸显示的颜色跟标准比色卡对照,便可粗略知道溶液的pH。
新课讲解
【注意事项】
1、不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂;
2、pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后溶液的酸碱度,导致测定结果不准确。
新课讲解
四、溶液酸碱度对生产、生活及人类生命活动的意义
生活中常见物质的pH
新课讲解
化工生产中许多反应必须在一定pH的溶液中才能进行。
1
农作物一般适宜在pH接近于7或等于7的土壤中生长。
2
测定雨水的pH,可了解空气的污染状况
3
测定体液或排出物的pH,可了解人体的健康状况。
4
(酸雨是指pH<5.6的雨水)
新课讲解
【知识拓展】
向氢氧化钠溶液中逐滴滴加盐酸,溶液的pH随盐酸滴入量的图像如下:
(1)V表示盐酸与氢氧化钠完全反应时,盐酸的体积。
(2)图像不是直线,而是平滑的曲线。
开始加入盐酸时,曲线变化缓慢,随着盐酸的加入,曲线陡降,当完全反应时,pH=7;继续加盐酸,pH<7,曲线逐渐趋于平缓,逐渐接近所加盐酸的pH。
归纳小结
1、利用pH来表示溶液酸碱性的强弱;利用数轴来理解pH的定义,并比较溶液的酸碱性强弱;
2、pH试纸可以粗略测定溶液的酸碱度;掌握正确测定溶液酸碱度的方法。
1、下列物质呈碱性的是( )
A.血液,pH为7.35~7.45 B.胃液,pH为0.9~1.5
C.牛奶,pH为6.3~6.6 D.苹果汁,pH为2.9~3.3
强化训练
A
【解析】当溶液的pH等于7时,呈中性;当溶液的pH大于7时,呈碱性;当溶液的pH小于7时,呈酸性。
A、血液,pH为7.35~7.45,大于7,呈碱性;
B、胃液,pH为0.9~1.5,小于7,呈酸性;
C、牛奶,pH为6.3~6.6,小于7,呈酸性;
D、苹果汁,pH为2.9~3.3,小于7,呈酸性。
强化训练
2、下列是人体内一些体液的正常pH值范围,其中酸性最强的体液是
( )
A.唾液 B.胃液 C.胆汁 D.胰液
B
【解析】当pH<7时,呈酸性,当pH>7时,呈碱性,当溶液的pH小于7时,随着pH的减小,酸性逐渐增强。A、唾液的pH为6.6~7.1,接近中性;
B、胃液的pH为0.9~1.5,呈强酸性;C、胆汁的pH为7.1~7.3,呈弱碱性;
D、胰液的pH为7.5~8.0,呈弱碱性。
液体 唾液 胃液 胆汁 胰液
pH 6.6~7.1 0.9~1.5 7.1~7.3 7.5~8.0
强化训练
3、一些食物pH 的近似值范围如下:橘子汁3.0~4.0;泡菜3.2~3.6;牛奶6.3~6.6;鸡蛋清7.6~8.0。下列说法中,不正确的是( )
A.鸡蛋清显碱性
B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红
D.牛奶比橘子汁的酸性强
D
【解析】
A、鸡蛋清的pH为7.6~8.0,呈弱碱性,故A正确;
B、泡菜的pH为3.2~3.6,呈酸性,胃酸过多的人不宜多吃,故B正确;
C、橘子汁呈酸性,石蕊试液在酸性溶液中变红,故C正确;
D、牛奶和橘子汁的pH都小于7,显酸性,牛奶的pH比橘子汁的pH大,酸性比橘子汁弱,故D错误。
布置作业
某小型造纸厂向河水中非法排放了大量碱性废液。请你根据所学的知识,谈一下如何检测受污染河水的pH。
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
