第六章 微专题四 解答化学反应速率图像题的思路 学案(含答案)
文档属性
| 名称 | 第六章 微专题四 解答化学反应速率图像题的思路 学案(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 173.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-01-31 00:00:00 | ||
图片预览


文档简介
微专题四 解答化学反应速率图像题的思路
化学反应速率问题常以图像题的形式出现,在相关图像的平面直角坐标系中,可能出现的物理量有物质的量、浓度、时间等。解题时,重点是理解图像的意义和特点。
1.关注图像中的“点、线、面”
(1)关注“面”——明确研究对象
理解各坐标轴所代表量的意义及曲线所表示的是哪些量之间的关系。弄清楚是物质的量,还是浓度随时间的变化。
(2)关注“线”
①弄清曲线的走向,是增大还是减小,确定反应物和生成物,浓度减小的是反应物,浓度增大的是生成物。
②分清突变和渐变;理解曲线“平”与“陡”即斜率大小的意义。
(3)关注“点”
解题时要特别关注特殊点,如坐标轴的交点、几条曲线的交叉点、极值点、转折点等。深刻理解这些特殊点的意义。
2.联系规律
如各物质的转化量之比与化学计量数之比的关系,各物质的化学反应速率之比与化学计量数之比的关系,外界条件的改变对化学反应速率的影响规律等。
3.正确判断
根据题干和题目要求,结合图像信息,正确利用相关规律做出正确的判断。
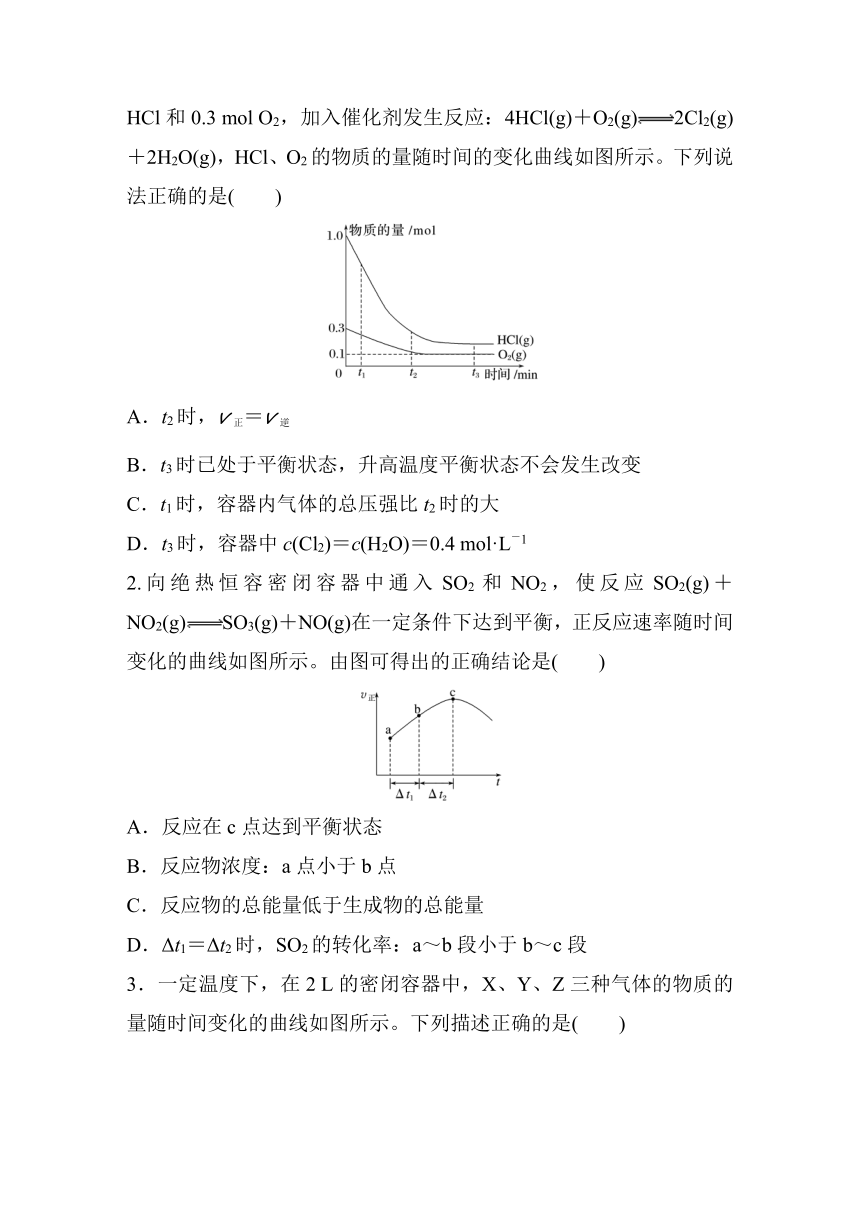
1.(2022·徐州高一阶段检测)在2.0 L恒温恒容密闭容器中充入1.0 mol HCl和0.3 mol O2,加入催化剂发生反应:4HCl(g)+O2(g)2Cl2(g)+2H2O(g),HCl、O2的物质的量随时间的变化曲线如图所示。下列说法正确的是( )
A.t2时,v正=v逆
B.t3时已处于平衡状态,升高温度平衡状态不会发生改变
C.t1时,容器内气体的总压强比t2时的大
D.t3时,容器中c(Cl2)=c(H2O)=0.4 mol·L-1
2.向绝热恒容密闭容器中通入SO2和NO2,使反应SO2(g)+NO2(g)SO3(g)+NO(g)在一定条件下达到平衡,正反应速率随时间变化的曲线如图所示。由图可得出的正确结论是( )
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
3.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是( )
A.t min时该反应达到化学平衡状态
B.反应开始到10 min,用X表示的反应速率为0.079 mol·L-1·min-1
C.反应开始到10 min时,Y的转化率为79%
D.反应的化学方程式为X(g)+2Y(g)3Z(g)
4.氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO+3HSO===3SO+Cl-+3H+。已知该反应的速率随c(H+)的增大而加快。如图为用ClO在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法不正确的是( )
A.图中阴影部分的面积表示t1~t2时间内ClO的物质的量的减少量
B.纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C.反应开始时速率增大可能是c(H+)所致
D.后期反应速率下降的主要原因是反应物浓度减小
5.(2022·河北保定高一期中)恒温下在2 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
(1)该反应的化学方程式为_________________________________________________________
_______________________________________________________________________________。
(2)从开始至5 min,Y的平均反应速率为____________;X的转化率为____________________。
(3)反应达平衡时体系的压强是开始时的____________倍。
(4)下列描述中能表明反应已达到平衡状态的是____________(填序号)。
①容器内温度不变
②混合气体的密度不变
③混合气体的压强不变
④混合气体的平均相对分子质量不变
⑤Z(g)的物质的量浓度不变
⑥容器内X、Y、Z三种气体的浓度之比为3∶1∶2
⑦某时刻v(X)=3v(Y)且不等于零
⑧单位时间内生成2n mol Z,同时生成3n mol X
(5)在某一时刻采取下列措施能加快反应速率的是________(填字母)。
A.加催化剂
B.降低温度
C.体积不变,充入X
D.体积不变,从容器中分离出Y
微专题四 解答化学反应速率图像题的思路
跟踪训练
1.C
2.D [化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,且保持不变,c点对应的正反应速率显然还在改变,故一定未达平衡,A错误;a点到b点正反应速率增加,反应物浓度不断减小,B错误;随着反应的进行,反应物浓度减小,但正反应速率增大,说明体系温度升高,正反应是放热反应,即反应物的总能量高于生成物的总能量,C错误;因为反应一直正向进行,且a~c段正反应速率一直在增大,故SO2的转化率:a~b段小于b~c段,D正确。]
3.C
4.A [图像为ClO在单位时间内物质的量浓度变化表示的该反应v-t图,则阴影部分的面积表示t1~t2时间内ClO的物质的量浓度的减少量,故A错误;化学方程式为ClO+3HSO===3SO+Cl-+3H+,v(ClO)∶v(Cl-)=1∶1,纵坐标为v(Cl-)的v-t曲线与图中曲线重合,故B正确;由化学方程式可知,反应开始时随着反应的进行,c(H+)不断增大,反应的速率加快,由题目信息可知反应的速率随c(H+)的增大而加快,故C正确;随着反应的进行,反应物的浓度减小,反应速率减小,所以后期反应速率下降的主要原因是反应物浓度减小,故D正确。]
5.(1)3X(g)+Y(g)2Z(g)
(2)0.02 mol·L-1·min-1 60%
(3)
(4)③④⑤⑧
(5)AC
化学反应速率问题常以图像题的形式出现,在相关图像的平面直角坐标系中,可能出现的物理量有物质的量、浓度、时间等。解题时,重点是理解图像的意义和特点。
1.关注图像中的“点、线、面”
(1)关注“面”——明确研究对象
理解各坐标轴所代表量的意义及曲线所表示的是哪些量之间的关系。弄清楚是物质的量,还是浓度随时间的变化。
(2)关注“线”
①弄清曲线的走向,是增大还是减小,确定反应物和生成物,浓度减小的是反应物,浓度增大的是生成物。
②分清突变和渐变;理解曲线“平”与“陡”即斜率大小的意义。
(3)关注“点”
解题时要特别关注特殊点,如坐标轴的交点、几条曲线的交叉点、极值点、转折点等。深刻理解这些特殊点的意义。
2.联系规律
如各物质的转化量之比与化学计量数之比的关系,各物质的化学反应速率之比与化学计量数之比的关系,外界条件的改变对化学反应速率的影响规律等。
3.正确判断
根据题干和题目要求,结合图像信息,正确利用相关规律做出正确的判断。
1.(2022·徐州高一阶段检测)在2.0 L恒温恒容密闭容器中充入1.0 mol HCl和0.3 mol O2,加入催化剂发生反应:4HCl(g)+O2(g)2Cl2(g)+2H2O(g),HCl、O2的物质的量随时间的变化曲线如图所示。下列说法正确的是( )
A.t2时,v正=v逆
B.t3时已处于平衡状态,升高温度平衡状态不会发生改变
C.t1时,容器内气体的总压强比t2时的大
D.t3时,容器中c(Cl2)=c(H2O)=0.4 mol·L-1
2.向绝热恒容密闭容器中通入SO2和NO2,使反应SO2(g)+NO2(g)SO3(g)+NO(g)在一定条件下达到平衡,正反应速率随时间变化的曲线如图所示。由图可得出的正确结论是( )
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量低于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
3.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是( )
A.t min时该反应达到化学平衡状态
B.反应开始到10 min,用X表示的反应速率为0.079 mol·L-1·min-1
C.反应开始到10 min时,Y的转化率为79%
D.反应的化学方程式为X(g)+2Y(g)3Z(g)
4.氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO+3HSO===3SO+Cl-+3H+。已知该反应的速率随c(H+)的增大而加快。如图为用ClO在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法不正确的是( )
A.图中阴影部分的面积表示t1~t2时间内ClO的物质的量的减少量
B.纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C.反应开始时速率增大可能是c(H+)所致
D.后期反应速率下降的主要原因是反应物浓度减小
5.(2022·河北保定高一期中)恒温下在2 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
(1)该反应的化学方程式为_________________________________________________________
_______________________________________________________________________________。
(2)从开始至5 min,Y的平均反应速率为____________;X的转化率为____________________。
(3)反应达平衡时体系的压强是开始时的____________倍。
(4)下列描述中能表明反应已达到平衡状态的是____________(填序号)。
①容器内温度不变
②混合气体的密度不变
③混合气体的压强不变
④混合气体的平均相对分子质量不变
⑤Z(g)的物质的量浓度不变
⑥容器内X、Y、Z三种气体的浓度之比为3∶1∶2
⑦某时刻v(X)=3v(Y)且不等于零
⑧单位时间内生成2n mol Z,同时生成3n mol X
(5)在某一时刻采取下列措施能加快反应速率的是________(填字母)。
A.加催化剂
B.降低温度
C.体积不变,充入X
D.体积不变,从容器中分离出Y
微专题四 解答化学反应速率图像题的思路
跟踪训练
1.C
2.D [化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,且保持不变,c点对应的正反应速率显然还在改变,故一定未达平衡,A错误;a点到b点正反应速率增加,反应物浓度不断减小,B错误;随着反应的进行,反应物浓度减小,但正反应速率增大,说明体系温度升高,正反应是放热反应,即反应物的总能量高于生成物的总能量,C错误;因为反应一直正向进行,且a~c段正反应速率一直在增大,故SO2的转化率:a~b段小于b~c段,D正确。]
3.C
4.A [图像为ClO在单位时间内物质的量浓度变化表示的该反应v-t图,则阴影部分的面积表示t1~t2时间内ClO的物质的量浓度的减少量,故A错误;化学方程式为ClO+3HSO===3SO+Cl-+3H+,v(ClO)∶v(Cl-)=1∶1,纵坐标为v(Cl-)的v-t曲线与图中曲线重合,故B正确;由化学方程式可知,反应开始时随着反应的进行,c(H+)不断增大,反应的速率加快,由题目信息可知反应的速率随c(H+)的增大而加快,故C正确;随着反应的进行,反应物的浓度减小,反应速率减小,所以后期反应速率下降的主要原因是反应物浓度减小,故D正确。]
5.(1)3X(g)+Y(g)2Z(g)
(2)0.02 mol·L-1·min-1 60%
(3)
(4)③④⑤⑧
(5)AC
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
