化学人教版(2019)高中化学必修第一册1.1 物质的分类及转化(共26张ppt)
文档属性
| 名称 | 化学人教版(2019)高中化学必修第一册1.1 物质的分类及转化(共26张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-01 00:00:00 | ||
图片预览




文档简介
(共26张PPT)
物质的分类
图书馆分类陈列的图书
智能机器人对快递进行分拣
一、物质的分类
1. 根据物质的组成和性质分类
金刚石
石墨
C60
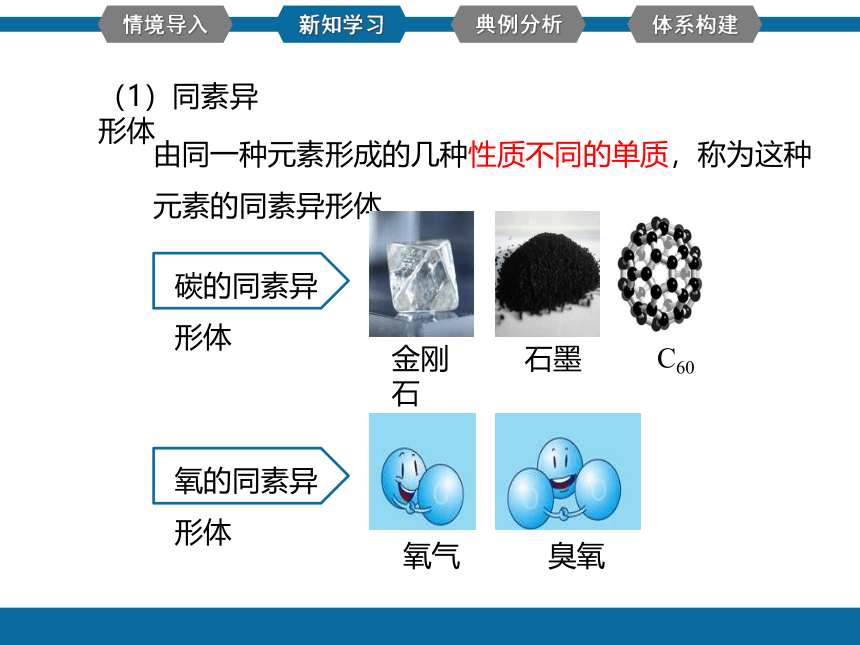
(1)同素异形体
由同一种元素形成的几种性质不同的单质,称为这种元素的同素异形体
金刚石
石墨
C60
(1)同素异形体
碳的同素异形体
氧的同素异形体
氧气
臭氧
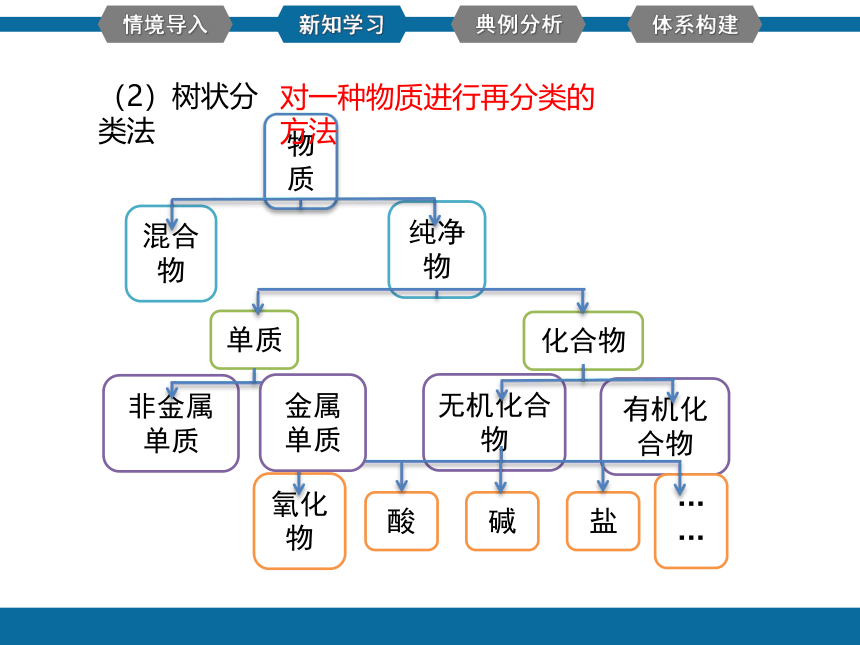
(2)树状分类法
物质
混合物
纯净物
单质
化合物
非金属单质
氧化物
酸
碱
盐
无机化合物
有机化合物
……
金属单质
对一种物质进行再分类的方法
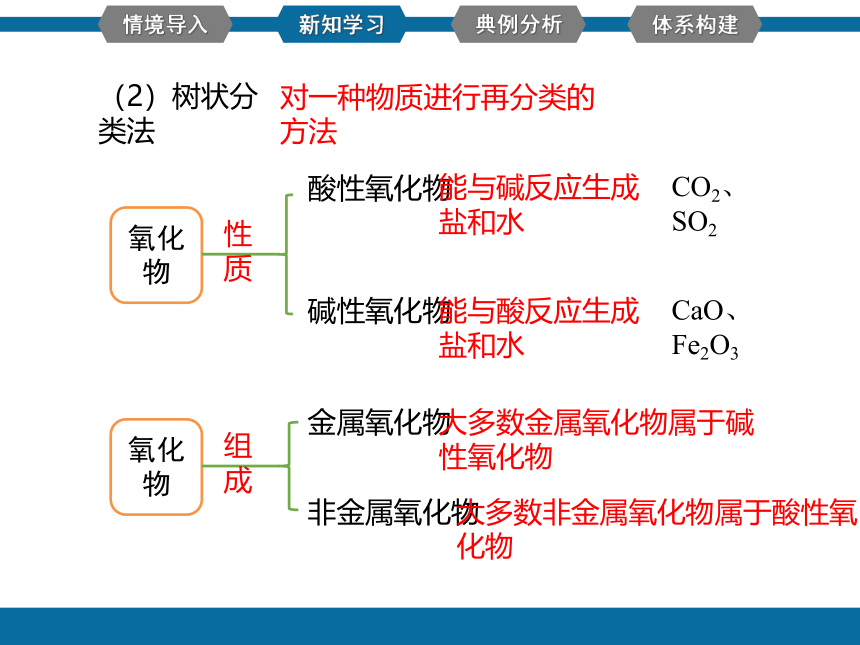
(2)树状分类法
氧化物
对一种物质进行再分类的方法
酸性氧化物
碱性氧化物
性质
氧化物
金属氧化物
非金属氧化物
组成
能与碱反应生成盐和水
能与酸反应生成盐和水
CO2、SO2
CaO、Fe2O3
大多数金属氧化物属于碱性氧化物
大多数非金属氧化物属于酸性氧化物
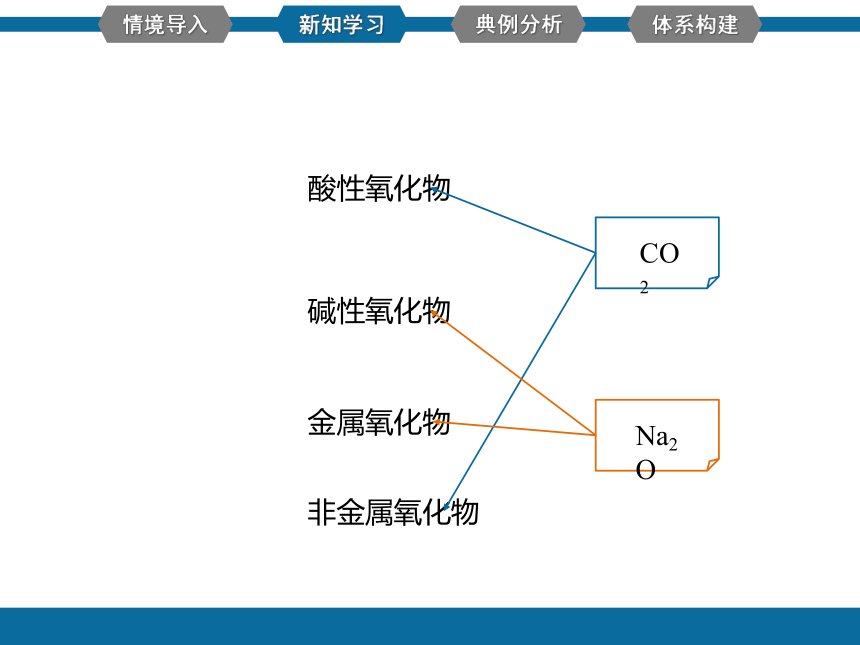
酸性氧化物
碱性氧化物
金属氧化物
非金属氧化物
CO2
Na2O
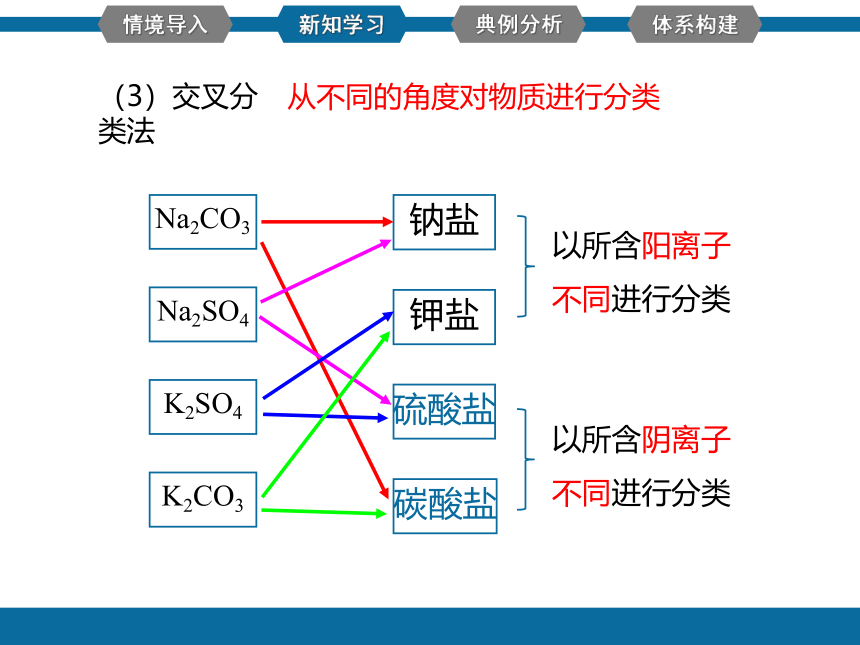
(3)交叉分类法
从不同的角度对物质进行分类
钾盐
钠盐
硫酸盐
碳酸盐
Na2CO3
K2SO4
Na2SO4
K2CO3
以所含阳离子不同进行分类
以所含阴离子不同进行分类
【例题】阅读下列科普短文并填空。
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,氢氧燃料电池在工作时,从负极连续通入①H2,从正极连续通入②O2,二者在电池内部(含有③H2SO4或④KOH等物质的溶液)发生反应生成⑤H2O,同时产生电能。除了H2,⑥CH4,⑦C2H5OH等也可以作为燃料电池的燃料。目前已研制成功⑧A1-⑨空气燃料电池,它可以代替汽油为汽车提供动力,也可以用作照明电源等。
(1)在上述短文标有序号的物质中,属于混合物的是: ;属于氧化物的是: ;属于酸的是 ;属于碱的是 ;属于有机物的是 ;
(2)从物质的类别来看,H2、O2和Al都属于 ;请写出与O2互为同素异形体的物质的化学式: 。
⑨
⑤
③
④
⑥⑦
单质
O3
物质的分类
根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法
科学的分类能够反映事物的本质特征
有利于人们分门别类地进行深入研究
分类有一定的标准,根据不同的标准,人们对研究对象进行不同的分类
树状分类法
交叉分类法
垃圾分类
快递分类
图书馆分类
信息分类
分类思想
物质的转化
年 级:高一年级 学 科:化学(人教版)
主讲人:赵迪 学 校:咸阳市实验中学
工业上制取 NaOH 一般选择什么方法?
二、物质的转化
1. 酸、碱、盐的性质
酸
碱
盐
(1)酸的性质
酸的主要化学性质 实例(化学反应方程式)
与指示剂反应
酸与活泼金属的反应
酸与碱性氧化物的反应
酸与碱的反应
酸与某些盐的反应
使紫色石蕊试液变红
不同的酸具有相似的化学性质,因为不同酸溶液中都含有 H+
Fe + 2HCl = FeCl2 + H2↑
CaO + 2HCl = CaCl2 + H2O
NaOH + HCl = NaCl + H2O
AgNO3 + HCl = AgCl↓ + HNO3
(2)碱的性质
碱的主要化学性质 实例(化学反应方程式)
与指示剂反应
碱与酸性氧化物的反应
碱与酸的反应
碱与某些盐的反应
使紫色石蕊试液变蓝;使无色酚酞变红
不同的碱具有相似的化学性质,因为不同碱溶液中都含有 OH-
2NaOH + CO2 = Na2CO3 + H2O
NaOH + HCl = NaCl + H2O
2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)盐的性质
碱的主要化学性质 实例(化学反应方程式)
与金属反应
盐与碱的反应
盐与酸的反应
盐与某些盐的反应
具有相似性质的盐类具有相同的离子
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl
Fe + CuSO4 = FeSO4 + Cu
酸与金属的反应
盐与金属的反应
置换反应
酸与碱的反应
盐与酸的反应
复分解反应
盐与碱的反应
盐与盐的反应
物质的组成和性质
物质间的转化
化学反应
元素不变
2. 物质的转化
2Ca + O2 ═ 2CaO
Ca(OH)2+ H2SO4 ═ CaSO4 + 2H2O
CaO + H2O ═ Ca(OH)2
Ca
CaO
Ca(OH)2
CaSO4
2. 物质的转化
H2CO3 + Ca(OH)2 ═ CaCO3↓+ 2 H2O
CO2 + H2O ═ H2CO3
C
CO2
H2CO3
CaCO3
C + O2 == CO2
点燃
2. 物质的转化
Ca
CaO
Ca(OH)2
CaSO4
碱性氧化物
金属单质
碱
盐
酸或 酸性氧化物
O2
H2O
C
CO2
H2CO3
CaCO3
酸性氧化物
非金属单质
酸
盐
碱或 碱性氧化物
O2
H2O
方案一:氧化物与水反应
方案二:盐和另一种碱反应
工业上制取 NaOH 一般选择什么方法?
原料来源
成本高低
设备要求
电解饱和食盐水
2NaCl(饱和) + 2H2O === 2NaOH + H2↑+ Cl2↑
通电
【例题】许多食品包装袋中常有一个小纸袋,内盛白色固体物质,标有“干燥剂”字样,其主要成分为生石灰。
(1)写出生石灰的化学式: ;
生石灰属于哪一类别的物质? 。
(2)生石灰为什么可用作干燥剂?用化学方程式表示为: 。
(3)生石灰可以与哪些类别的物质发生化学反应?
请列举两例,并写出反应的化学方程式。
(4)在你学过的物质中,还有哪些物质可用作干燥剂?
CaO + H2O = Ca(OH)2
CaO
浓硫酸、五氧化二磷、硅胶、无水氯化钙
碱性氧化物
酸、酸性氧化物、水
CaO + 2HCl = CaCl2 + H2O
CaO + SiO2 === CaSiO3
高温
物质的转化
氯化镁的制备
方法一:Mg + 2HCl = MgCl2 + H2 ↑
方法二:MgO + 2HCl = MgCl2 + H2O
方法三:Mg(OH)2 + 2HCl = MgCl2 + 2H2O
金属铜的冶炼
方法一:CuO + H2SO4 = CuSO4 + H2O Fe + CuSO4 = FeSO4 + Cu
方法二:Fe + H2SO4 = FeSO4 + H2 ↑ CuO + H2 == Cu + H2O
谢谢观看!
物质的分类
图书馆分类陈列的图书
智能机器人对快递进行分拣
一、物质的分类
1. 根据物质的组成和性质分类
金刚石
石墨
C60
(1)同素异形体
由同一种元素形成的几种性质不同的单质,称为这种元素的同素异形体
金刚石
石墨
C60
(1)同素异形体
碳的同素异形体
氧的同素异形体
氧气
臭氧
(2)树状分类法
物质
混合物
纯净物
单质
化合物
非金属单质
氧化物
酸
碱
盐
无机化合物
有机化合物
……
金属单质
对一种物质进行再分类的方法
(2)树状分类法
氧化物
对一种物质进行再分类的方法
酸性氧化物
碱性氧化物
性质
氧化物
金属氧化物
非金属氧化物
组成
能与碱反应生成盐和水
能与酸反应生成盐和水
CO2、SO2
CaO、Fe2O3
大多数金属氧化物属于碱性氧化物
大多数非金属氧化物属于酸性氧化物
酸性氧化物
碱性氧化物
金属氧化物
非金属氧化物
CO2
Na2O
(3)交叉分类法
从不同的角度对物质进行分类
钾盐
钠盐
硫酸盐
碳酸盐
Na2CO3
K2SO4
Na2SO4
K2CO3
以所含阳离子不同进行分类
以所含阴离子不同进行分类
【例题】阅读下列科普短文并填空。
燃料电池是一种化学电池,具有能量转化率高、对环境友好等优点。例如,氢氧燃料电池在工作时,从负极连续通入①H2,从正极连续通入②O2,二者在电池内部(含有③H2SO4或④KOH等物质的溶液)发生反应生成⑤H2O,同时产生电能。除了H2,⑥CH4,⑦C2H5OH等也可以作为燃料电池的燃料。目前已研制成功⑧A1-⑨空气燃料电池,它可以代替汽油为汽车提供动力,也可以用作照明电源等。
(1)在上述短文标有序号的物质中,属于混合物的是: ;属于氧化物的是: ;属于酸的是 ;属于碱的是 ;属于有机物的是 ;
(2)从物质的类别来看,H2、O2和Al都属于 ;请写出与O2互为同素异形体的物质的化学式: 。
⑨
⑤
③
④
⑥⑦
单质
O3
物质的分类
根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法
科学的分类能够反映事物的本质特征
有利于人们分门别类地进行深入研究
分类有一定的标准,根据不同的标准,人们对研究对象进行不同的分类
树状分类法
交叉分类法
垃圾分类
快递分类
图书馆分类
信息分类
分类思想
物质的转化
年 级:高一年级 学 科:化学(人教版)
主讲人:赵迪 学 校:咸阳市实验中学
工业上制取 NaOH 一般选择什么方法?
二、物质的转化
1. 酸、碱、盐的性质
酸
碱
盐
(1)酸的性质
酸的主要化学性质 实例(化学反应方程式)
与指示剂反应
酸与活泼金属的反应
酸与碱性氧化物的反应
酸与碱的反应
酸与某些盐的反应
使紫色石蕊试液变红
不同的酸具有相似的化学性质,因为不同酸溶液中都含有 H+
Fe + 2HCl = FeCl2 + H2↑
CaO + 2HCl = CaCl2 + H2O
NaOH + HCl = NaCl + H2O
AgNO3 + HCl = AgCl↓ + HNO3
(2)碱的性质
碱的主要化学性质 实例(化学反应方程式)
与指示剂反应
碱与酸性氧化物的反应
碱与酸的反应
碱与某些盐的反应
使紫色石蕊试液变蓝;使无色酚酞变红
不同的碱具有相似的化学性质,因为不同碱溶液中都含有 OH-
2NaOH + CO2 = Na2CO3 + H2O
NaOH + HCl = NaCl + H2O
2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)盐的性质
碱的主要化学性质 实例(化学反应方程式)
与金属反应
盐与碱的反应
盐与酸的反应
盐与某些盐的反应
具有相似性质的盐类具有相同的离子
2NaOH + CuSO4 = Cu(OH)2↓ + Na2SO4
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl
Fe + CuSO4 = FeSO4 + Cu
酸与金属的反应
盐与金属的反应
置换反应
酸与碱的反应
盐与酸的反应
复分解反应
盐与碱的反应
盐与盐的反应
物质的组成和性质
物质间的转化
化学反应
元素不变
2. 物质的转化
2Ca + O2 ═ 2CaO
Ca(OH)2+ H2SO4 ═ CaSO4 + 2H2O
CaO + H2O ═ Ca(OH)2
Ca
CaO
Ca(OH)2
CaSO4
2. 物质的转化
H2CO3 + Ca(OH)2 ═ CaCO3↓+ 2 H2O
CO2 + H2O ═ H2CO3
C
CO2
H2CO3
CaCO3
C + O2 == CO2
点燃
2. 物质的转化
Ca
CaO
Ca(OH)2
CaSO4
碱性氧化物
金属单质
碱
盐
酸或 酸性氧化物
O2
H2O
C
CO2
H2CO3
CaCO3
酸性氧化物
非金属单质
酸
盐
碱或 碱性氧化物
O2
H2O
方案一:氧化物与水反应
方案二:盐和另一种碱反应
工业上制取 NaOH 一般选择什么方法?
原料来源
成本高低
设备要求
电解饱和食盐水
2NaCl(饱和) + 2H2O === 2NaOH + H2↑+ Cl2↑
通电
【例题】许多食品包装袋中常有一个小纸袋,内盛白色固体物质,标有“干燥剂”字样,其主要成分为生石灰。
(1)写出生石灰的化学式: ;
生石灰属于哪一类别的物质? 。
(2)生石灰为什么可用作干燥剂?用化学方程式表示为: 。
(3)生石灰可以与哪些类别的物质发生化学反应?
请列举两例,并写出反应的化学方程式。
(4)在你学过的物质中,还有哪些物质可用作干燥剂?
CaO + H2O = Ca(OH)2
CaO
浓硫酸、五氧化二磷、硅胶、无水氯化钙
碱性氧化物
酸、酸性氧化物、水
CaO + 2HCl = CaCl2 + H2O
CaO + SiO2 === CaSiO3
高温
物质的转化
氯化镁的制备
方法一:Mg + 2HCl = MgCl2 + H2 ↑
方法二:MgO + 2HCl = MgCl2 + H2O
方法三:Mg(OH)2 + 2HCl = MgCl2 + 2H2O
金属铜的冶炼
方法一:CuO + H2SO4 = CuSO4 + H2O Fe + CuSO4 = FeSO4 + Cu
方法二:Fe + H2SO4 = FeSO4 + H2 ↑ CuO + H2 == Cu + H2O
谢谢观看!
