化学人教版(2019)必修第一册3.1.2 铁及其重要化合物(共22张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册3.1.2 铁及其重要化合物(共22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 45.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-01 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
2018年10月23日,习近平主席出席仪式并宣布港珠澳大桥正式开通。此桥用钢铁量42万吨,是世界最长的跨海大桥。
中国,再次向世界彰显着民族的力量和智慧。
江西南昌县刘家村的井水有着令人不解的奇特现象,这里的村民甚至把它称作怪水。据村民介绍,这些水刚压上来的时候看着很清亮,可是只要放得时间稍微一长,或者是烧开之后,它就会变得又黄又浑。当人们把普通的茶水倒进刚刚从井里压上来的生水中时,水的颜色则会发生更加令人难以置信的变化,茶水会立刻变黑。30多年来,江西刘家村的村民一直在恐惧与猜测中度过。怪水之中究竟隐含了怎样的秘密?
【奇闻趣事】
井水稍微放置就变黄
普通茶水倒入井水中会立即变黑
用戶至上 用心服务 Customer First Service Foremost
铁及其化合物
第二课时 铁的重要化合物
【教学目标】
1.通过实验探究铁的氢氧化物、铁盐和亚铁盐的化学性质,并能用化学方程式或离子方程式正确表示。体会实验对认识和研究物质性质的重要作用,形成证据意识;
2.通过学习铁及其化合物,学会从物质类别和元素价态的视角认识具有变价元素物质间的转化关系,并建立认识模型,丰富研究物质的思路和方法;
3.结合应用实例,将铁及其化合物性质的知识运用于解决生产、生活中简单的化学问题,强化性质决定用途的观念。
【教学重点难点】
重点:铁盐与亚铁盐的转化、Fe3+的检验。
难点:制备Fe(OH)2的实验设计;Fe、Fe2+、Fe3+转化关系模型的构建。
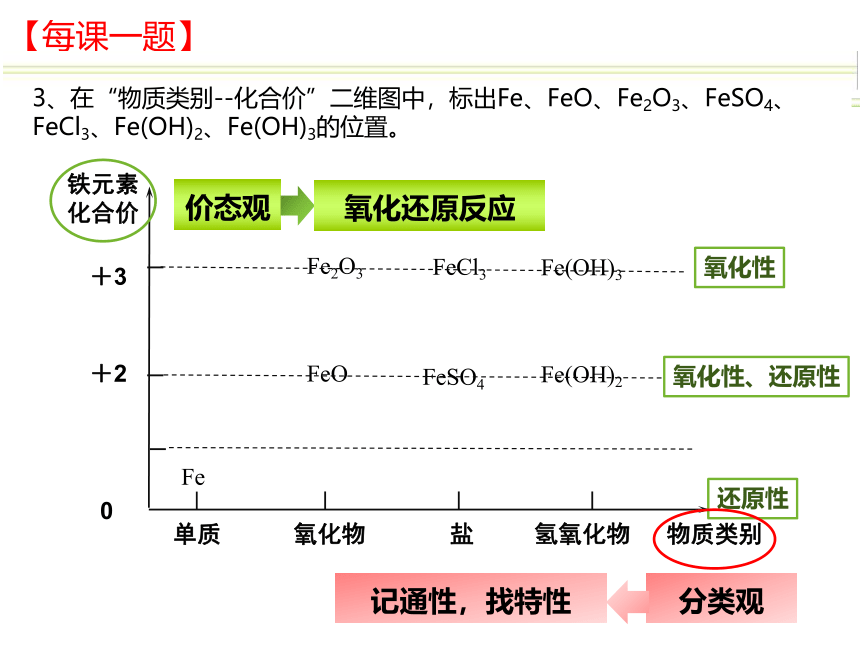
【每课一题】
1、以下反应属于离子反应的写出离子方程式,其它的写出化学方程式。
① 铁与稀硫酸:_______________________________________________。
②铁与硫酸铜溶液:____________________________________________。
③铝与氯化亚铁溶液:__________________________________________。
④铁与氯气反应:______________________________________________。
⑤氧化铁与一氧化碳反应:______________________________________。
2、从氧化还原的角度,亚铁盐转化为铁盐应该加入__________,铁盐转化为亚铁盐应该加入__________。(填“氧化剂”或“还原剂”)。
Fe2O3+ 3CO == 2Fe + 3CO2
高温
Fe + 2H+ == Fe2+ + H2↑
Fe + Cu2+ == Fe2+ + Cu
2Al + 3Fe2+ == 2Al3+ + 3Fe
2Fe + 3Cl2 == 2FeCl3
点燃
氧化剂
还原剂
Fe
FeO
Fe2O3
Fe(OH)2
Fe(OH)3
FeSO4
FeCl3
单质 氧化物 盐 氢氧化物 物质类别
铁元素
化合价
+3
+2
0
分类观
氧化性
氧化性、还原性
还原性
价态观
氧化还原反应
记通性,找特性
【每课一题】
3、在“物质类别--化合价”二维图中,标出Fe、FeO、Fe2O3、FeSO4、FeCl3、Fe(OH)2、Fe(OH)3的位置。
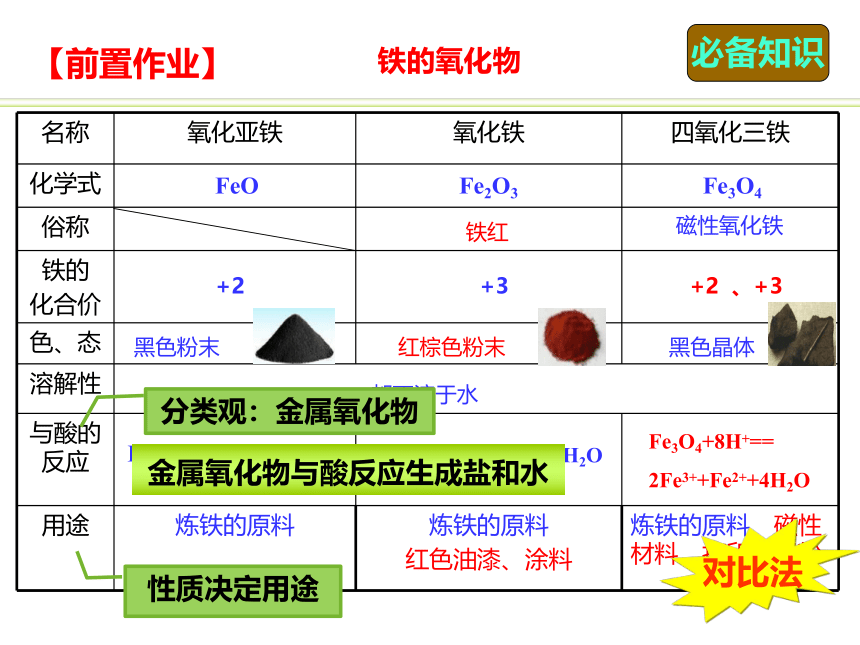
【前置作业】
名称 氧化亚铁 氧化铁 四氧化三铁
化学式
俗称
铁的 化合价
色、态
溶解性
与酸的反应
用途 炼铁的原料 炼铁的原料 红色油漆、涂料 炼铁的原料、磁性材料、打印机墨粉
+2
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
铁红
磁性氧化铁
都不溶于水
Fe2O3+6H+=2Fe3++3H2O
+3
+2 、+3
分类观:金属氧化物
FeO+2H+=Fe2++H2O
性质决定用途
铁的氧化物
对比法
必备知识
Fe3O4+8H+==
2Fe3++Fe2++4H2O
金属氧化物与酸反应生成盐和水
主题一:铁的氢氧化物
【问题1】已知Fe(OH)2和Fe(OH)3均不溶于水,请根据复分解反应的规律设计出制备这两种物质的方案:
分别用可溶性亚铁盐、铁盐与碱溶液反应
主题一:铁的氢氧化物
【实验3-1】分组实验
在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴加NaOH溶液。观察并描述发生的现象。
实验 FeCl3溶液+NaOH溶液 FeSO4溶液+NaOH溶液
现象
离子方程式
生成红褐色沉淀
Fe3++3OH- =Fe(OH)3↓
Fe2++2OH- =Fe(OH)2↓
4Fe(OH)2+O2+2H2O =4Fe(OH)3
生成白色絮状沉淀,迅速变为灰绿色,最终变为红褐色。
主题一:铁的氢氧化物
【问题2】由实验3-1可知,白色的Fe(OH)2会被溶解在溶液中的氧气氧化。那么,在实验室里,如何得到Fe(OH)2呢?
长胶头滴管伸入液面以下
油封
将NaOH溶液煮沸以排除溶解的氧气,溶液现制现用。
隔绝氧气
主题一:铁的氢氧化物
比较氢氧化亚铁、氢氧化铁的性质
必备知识
名称 氢氧化亚铁 氢氧化铁
化学式 Fe(OH)2 Fe(OH)3
颜色状态 白色固体 红褐色固体
溶解性 均不溶于水
与酸的反应 (离子方程式)
稳定性
Fe(OH)2 + 2H+ = Fe2++ 2H2O
Fe(OH)3 + 3H+ = Fe3++3H2O
4Fe(OH)2+O2+2H2O =4Fe(OH)3
△
2Fe(OH)3 == Fe2O3+3H2O
对比法
易氧化
受热易分解
高中生小明最近出现头昏、乏力,面色苍白,食欲不振的现象,经医生诊断是缺铁性贫血。小明妈妈听说食用菠菜可以补铁,但是她半信半疑。那么菠菜中含有铁元素吗?请你结合资料卡片,设计实验加以证明。
资料卡片:
Fe3+可以与KSCN(硫氰化钾)溶液反应形成红色物质。常用此现象检验Fe3+的存在。
实验方案:
①取新鲜的菠菜10g,将菠菜剪碎后放在研钵中研磨,然后倒入烧杯中,倒入30ml蒸馏水,搅拌。将上述浊液过滤,得到的滤液作为试验样品。
②取少量试验样品到倒入试管中,然后加入少量稀硝酸,再滴加加几滴KSCN溶液,振荡,观察现象。
【问题3】
主题二:Fe3+的检验
【实验3-2】分组实验
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴加几滴KSCN溶液。观察并记录现象。
滴入KSCN溶液
FeCl3溶液
FeCl2溶液
溶液变红色
溶液不变红
Fe3+的检验方法:_____________________________
_____________________________。
取少量溶液于试管中,滴加KSCN溶液,
如果溶液变红色,证明存在Fe3+
必备知识
概括归理
离子检验答题规范:取样→加试剂→现象→结论
物质的检验利用性质的差异,抓特性
小明去医院看病时,医生建议小明服用琥珀酸亚铁片治疗缺铁性贫血。小明通过阅读说明书,产生了几个疑问。
①该药片为什么为薄膜衣片?
②为什么建议该药与维生素C同时使用时,效果会更好呢?
防止Fe2+被氧化为Fe3+
维生素C具有还原性,将Fe3+还原为Fe2+
资料卡片:
①Fe2+是人体所吸收的主要形式;Fe3+人体不好吸收,
②维生素C又叫L- 抗坏血酸,是一种水溶性维生素。具有较强的还原性。
概括归理
Fe3+
加入还原剂
加入氧化剂
Fe2+
价态观
【问题4】
主题三:Fe2+与Fe3+的转化
【问题5】根据氧化还原反应规律,从铁粉、新制氯水、FeCl2溶液、FeCl3溶液中,选择合适的药品,实现Fe3+与Fe2+的相互转化?
实验 试剂
Fe3+转化为Fe2+
Fe2+转化为Fe3+
FeCl3溶液、铁粉
FeCl2溶液、新制氯水
主题三:Fe2+与Fe3+的转化
【实验3-3】分组实验
实验 现象 离子方程式
在盛有2mlFeCl3溶液试管中,加入少量铁粉,振荡,充分反应后,滴入几滴KSCN溶液
在盛有2mlFeCl2溶液试管中,滴入几滴KSCN溶液,再滴入几滴氯水。
加铁粉后溶液由黄色变为浅绿色,滴加几滴KSCN溶液后,无明显现象
加KSCN溶液后不变色,加氯水后变红色
取少量溶液于试管中,滴加KSCN溶液,无明显现象,再滴加新制氯水,如果溶液变红色,证明存在Fe2+
必备知识
Fe2+的检验方法:_______________________________________
____________________________________________________。
2FeCl3+Fe = 3FeCl2
2Fe3++Fe = 3Fe2+
2FeCl2+Cl2 = 2FeCl3
2Fe2++Cl2=2Fe3++2Cl-
宏观辨识与微观探析
【问题6】
在电子工业中常用覆铜板为基础材料制作印刷电路板,印刷电路板广泛用于电视机、计算机、手机等电子产品中。用覆铜板制作印刷电路板原理是,利用FeCl3溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀。根据工业上制作印刷电路板的原理,可以利用覆铜板制作所需要的图案。试着写出这个过程的离子方程式,并思考如何处理使用后的“腐蚀液”。
处理方法:铁的还原性置换并回收废液中的铜,更环保。利用氯水等氧化剂氧化废液中的Fe2+,实现腐蚀液的循环利用。
主题三:Fe2+与Fe3+的转化
Cu+2FeCl3==CuCl2+2FeCl2
Cu+2Fe3+==Cu2++2Fe2+
科学态度与社会责任
绿色化学
“铁三角”的转化关系模型
必备知识
Fe2+ Fe3+
Fe
只有还原性
既有氧化性又有还原性
只有氧化性
H+、Cu2+等较弱氧化剂
Cl2等较强氧化剂
Zn、Al等还原剂
CO等还原剂
Cl2、O2等较强氧化剂
Fe、Cu、维生素C等还原剂
证据推理与模型认知
【揭秘怪水村之谜】
井水稍微放置就变黄
普通茶水倒入井水中会立即变黑
化学的神奇
被维生素C还原
Fe3+
Fe2+
被空气氧化
21世纪的化学是无限的,是至关重要的,它将帮助我们解决21世纪所面临的一系列问题,化学将迎来它的黄金时代!
白春礼(1953.9~)
名 人 名 言
用戶至上 用心服务 Customer First Service Foremost
同学们,再见!
2018年10月23日,习近平主席出席仪式并宣布港珠澳大桥正式开通。此桥用钢铁量42万吨,是世界最长的跨海大桥。
中国,再次向世界彰显着民族的力量和智慧。
江西南昌县刘家村的井水有着令人不解的奇特现象,这里的村民甚至把它称作怪水。据村民介绍,这些水刚压上来的时候看着很清亮,可是只要放得时间稍微一长,或者是烧开之后,它就会变得又黄又浑。当人们把普通的茶水倒进刚刚从井里压上来的生水中时,水的颜色则会发生更加令人难以置信的变化,茶水会立刻变黑。30多年来,江西刘家村的村民一直在恐惧与猜测中度过。怪水之中究竟隐含了怎样的秘密?
【奇闻趣事】
井水稍微放置就变黄
普通茶水倒入井水中会立即变黑
用戶至上 用心服务 Customer First Service Foremost
铁及其化合物
第二课时 铁的重要化合物
【教学目标】
1.通过实验探究铁的氢氧化物、铁盐和亚铁盐的化学性质,并能用化学方程式或离子方程式正确表示。体会实验对认识和研究物质性质的重要作用,形成证据意识;
2.通过学习铁及其化合物,学会从物质类别和元素价态的视角认识具有变价元素物质间的转化关系,并建立认识模型,丰富研究物质的思路和方法;
3.结合应用实例,将铁及其化合物性质的知识运用于解决生产、生活中简单的化学问题,强化性质决定用途的观念。
【教学重点难点】
重点:铁盐与亚铁盐的转化、Fe3+的检验。
难点:制备Fe(OH)2的实验设计;Fe、Fe2+、Fe3+转化关系模型的构建。
【每课一题】
1、以下反应属于离子反应的写出离子方程式,其它的写出化学方程式。
① 铁与稀硫酸:_______________________________________________。
②铁与硫酸铜溶液:____________________________________________。
③铝与氯化亚铁溶液:__________________________________________。
④铁与氯气反应:______________________________________________。
⑤氧化铁与一氧化碳反应:______________________________________。
2、从氧化还原的角度,亚铁盐转化为铁盐应该加入__________,铁盐转化为亚铁盐应该加入__________。(填“氧化剂”或“还原剂”)。
Fe2O3+ 3CO == 2Fe + 3CO2
高温
Fe + 2H+ == Fe2+ + H2↑
Fe + Cu2+ == Fe2+ + Cu
2Al + 3Fe2+ == 2Al3+ + 3Fe
2Fe + 3Cl2 == 2FeCl3
点燃
氧化剂
还原剂
Fe
FeO
Fe2O3
Fe(OH)2
Fe(OH)3
FeSO4
FeCl3
单质 氧化物 盐 氢氧化物 物质类别
铁元素
化合价
+3
+2
0
分类观
氧化性
氧化性、还原性
还原性
价态观
氧化还原反应
记通性,找特性
【每课一题】
3、在“物质类别--化合价”二维图中,标出Fe、FeO、Fe2O3、FeSO4、FeCl3、Fe(OH)2、Fe(OH)3的位置。
【前置作业】
名称 氧化亚铁 氧化铁 四氧化三铁
化学式
俗称
铁的 化合价
色、态
溶解性
与酸的反应
用途 炼铁的原料 炼铁的原料 红色油漆、涂料 炼铁的原料、磁性材料、打印机墨粉
+2
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
铁红
磁性氧化铁
都不溶于水
Fe2O3+6H+=2Fe3++3H2O
+3
+2 、+3
分类观:金属氧化物
FeO+2H+=Fe2++H2O
性质决定用途
铁的氧化物
对比法
必备知识
Fe3O4+8H+==
2Fe3++Fe2++4H2O
金属氧化物与酸反应生成盐和水
主题一:铁的氢氧化物
【问题1】已知Fe(OH)2和Fe(OH)3均不溶于水,请根据复分解反应的规律设计出制备这两种物质的方案:
分别用可溶性亚铁盐、铁盐与碱溶液反应
主题一:铁的氢氧化物
【实验3-1】分组实验
在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴加NaOH溶液。观察并描述发生的现象。
实验 FeCl3溶液+NaOH溶液 FeSO4溶液+NaOH溶液
现象
离子方程式
生成红褐色沉淀
Fe3++3OH- =Fe(OH)3↓
Fe2++2OH- =Fe(OH)2↓
4Fe(OH)2+O2+2H2O =4Fe(OH)3
生成白色絮状沉淀,迅速变为灰绿色,最终变为红褐色。
主题一:铁的氢氧化物
【问题2】由实验3-1可知,白色的Fe(OH)2会被溶解在溶液中的氧气氧化。那么,在实验室里,如何得到Fe(OH)2呢?
长胶头滴管伸入液面以下
油封
将NaOH溶液煮沸以排除溶解的氧气,溶液现制现用。
隔绝氧气
主题一:铁的氢氧化物
比较氢氧化亚铁、氢氧化铁的性质
必备知识
名称 氢氧化亚铁 氢氧化铁
化学式 Fe(OH)2 Fe(OH)3
颜色状态 白色固体 红褐色固体
溶解性 均不溶于水
与酸的反应 (离子方程式)
稳定性
Fe(OH)2 + 2H+ = Fe2++ 2H2O
Fe(OH)3 + 3H+ = Fe3++3H2O
4Fe(OH)2+O2+2H2O =4Fe(OH)3
△
2Fe(OH)3 == Fe2O3+3H2O
对比法
易氧化
受热易分解
高中生小明最近出现头昏、乏力,面色苍白,食欲不振的现象,经医生诊断是缺铁性贫血。小明妈妈听说食用菠菜可以补铁,但是她半信半疑。那么菠菜中含有铁元素吗?请你结合资料卡片,设计实验加以证明。
资料卡片:
Fe3+可以与KSCN(硫氰化钾)溶液反应形成红色物质。常用此现象检验Fe3+的存在。
实验方案:
①取新鲜的菠菜10g,将菠菜剪碎后放在研钵中研磨,然后倒入烧杯中,倒入30ml蒸馏水,搅拌。将上述浊液过滤,得到的滤液作为试验样品。
②取少量试验样品到倒入试管中,然后加入少量稀硝酸,再滴加加几滴KSCN溶液,振荡,观察现象。
【问题3】
主题二:Fe3+的检验
【实验3-2】分组实验
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴加几滴KSCN溶液。观察并记录现象。
滴入KSCN溶液
FeCl3溶液
FeCl2溶液
溶液变红色
溶液不变红
Fe3+的检验方法:_____________________________
_____________________________。
取少量溶液于试管中,滴加KSCN溶液,
如果溶液变红色,证明存在Fe3+
必备知识
概括归理
离子检验答题规范:取样→加试剂→现象→结论
物质的检验利用性质的差异,抓特性
小明去医院看病时,医生建议小明服用琥珀酸亚铁片治疗缺铁性贫血。小明通过阅读说明书,产生了几个疑问。
①该药片为什么为薄膜衣片?
②为什么建议该药与维生素C同时使用时,效果会更好呢?
防止Fe2+被氧化为Fe3+
维生素C具有还原性,将Fe3+还原为Fe2+
资料卡片:
①Fe2+是人体所吸收的主要形式;Fe3+人体不好吸收,
②维生素C又叫L- 抗坏血酸,是一种水溶性维生素。具有较强的还原性。
概括归理
Fe3+
加入还原剂
加入氧化剂
Fe2+
价态观
【问题4】
主题三:Fe2+与Fe3+的转化
【问题5】根据氧化还原反应规律,从铁粉、新制氯水、FeCl2溶液、FeCl3溶液中,选择合适的药品,实现Fe3+与Fe2+的相互转化?
实验 试剂
Fe3+转化为Fe2+
Fe2+转化为Fe3+
FeCl3溶液、铁粉
FeCl2溶液、新制氯水
主题三:Fe2+与Fe3+的转化
【实验3-3】分组实验
实验 现象 离子方程式
在盛有2mlFeCl3溶液试管中,加入少量铁粉,振荡,充分反应后,滴入几滴KSCN溶液
在盛有2mlFeCl2溶液试管中,滴入几滴KSCN溶液,再滴入几滴氯水。
加铁粉后溶液由黄色变为浅绿色,滴加几滴KSCN溶液后,无明显现象
加KSCN溶液后不变色,加氯水后变红色
取少量溶液于试管中,滴加KSCN溶液,无明显现象,再滴加新制氯水,如果溶液变红色,证明存在Fe2+
必备知识
Fe2+的检验方法:_______________________________________
____________________________________________________。
2FeCl3+Fe = 3FeCl2
2Fe3++Fe = 3Fe2+
2FeCl2+Cl2 = 2FeCl3
2Fe2++Cl2=2Fe3++2Cl-
宏观辨识与微观探析
【问题6】
在电子工业中常用覆铜板为基础材料制作印刷电路板,印刷电路板广泛用于电视机、计算机、手机等电子产品中。用覆铜板制作印刷电路板原理是,利用FeCl3溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀。根据工业上制作印刷电路板的原理,可以利用覆铜板制作所需要的图案。试着写出这个过程的离子方程式,并思考如何处理使用后的“腐蚀液”。
处理方法:铁的还原性置换并回收废液中的铜,更环保。利用氯水等氧化剂氧化废液中的Fe2+,实现腐蚀液的循环利用。
主题三:Fe2+与Fe3+的转化
Cu+2FeCl3==CuCl2+2FeCl2
Cu+2Fe3+==Cu2++2Fe2+
科学态度与社会责任
绿色化学
“铁三角”的转化关系模型
必备知识
Fe2+ Fe3+
Fe
只有还原性
既有氧化性又有还原性
只有氧化性
H+、Cu2+等较弱氧化剂
Cl2等较强氧化剂
Zn、Al等还原剂
CO等还原剂
Cl2、O2等较强氧化剂
Fe、Cu、维生素C等还原剂
证据推理与模型认知
【揭秘怪水村之谜】
井水稍微放置就变黄
普通茶水倒入井水中会立即变黑
化学的神奇
被维生素C还原
Fe3+
Fe2+
被空气氧化
21世纪的化学是无限的,是至关重要的,它将帮助我们解决21世纪所面临的一系列问题,化学将迎来它的黄金时代!
白春礼(1953.9~)
名 人 名 言
用戶至上 用心服务 Customer First Service Foremost
同学们,再见!
