化学人教版(2019)选择性必修3 3.2.2 酚的结构与性质(共31张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.2.2 酚的结构与性质(共31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 101.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-02 00:00:00 | ||
图片预览






文档简介
(共31张PPT)
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第二节 醇 酚
在19世纪初,医院的设备很差,那时缺少麻醉药和消毒剂,许多病人死于手术后的伤口感染中。在英国的爱丁堡有一家医院,一名叫李斯特的的外科医生,发现在化工厂附近的污水沟里,沟水清澈,浮在水面上的草根很少腐烂。原来,就是从化工厂流出的石炭酸(苯酚)混杂在沟水里,石炭酸是化工厂提炼煤焦油时排出的“废弃物”。李斯特用石炭酸对手术器械、纱布等一系列用品进行了消毒,病人手术后伤口化脓、感染的现象立即减少了,死亡率大大下降。由此,爱丁堡医院手术伤口感染率一度成为全世界外科医院中最低的。这一发现使苯酚成为一种强有力的外科消毒剂,李斯特也因此被誉为“外科消毒之父”。同时使苯酚首次声名远扬。
是谁使苯酚声名远扬?
外科消毒之父
———利斯特
利用苯酚外科消毒
学习
目标
第2课时
酚的结构与性质
PART
01
PART
02
通过认识酚的结构,了解苯酚的主要性质,能理解羟基和苯环的相互影响,形成物质结构决定性质的核心理念
通过酚及其酚类性质的学习,列举事实说明有机分子中基团之间存在相互影响
HO
OH
OH
OH
OCH3
CH2
葡萄酚
丁香酚
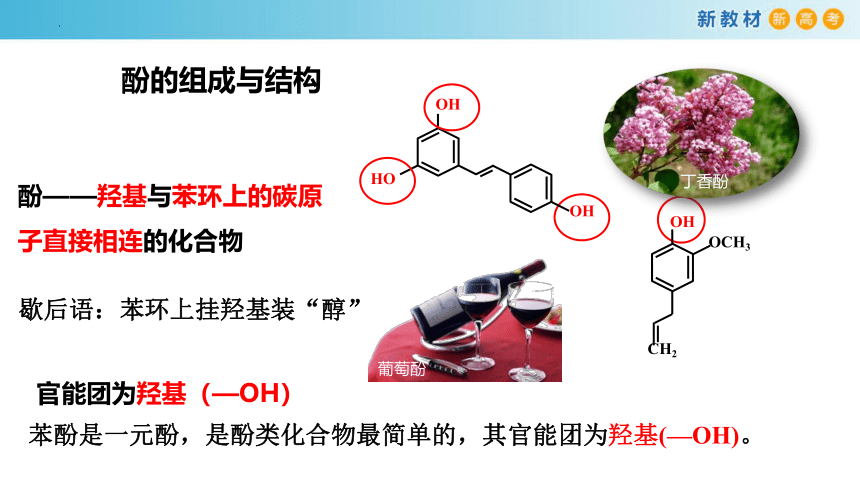
酚——羟基与苯环上的碳原子直接相连的化合物
官能团为羟基(—OH)
歇后语:苯环上挂羟基装“醇”
苯酚是一元酚,是酚类化合物最简单的,其官能团为羟基(—OH)。
酚的组成与结构
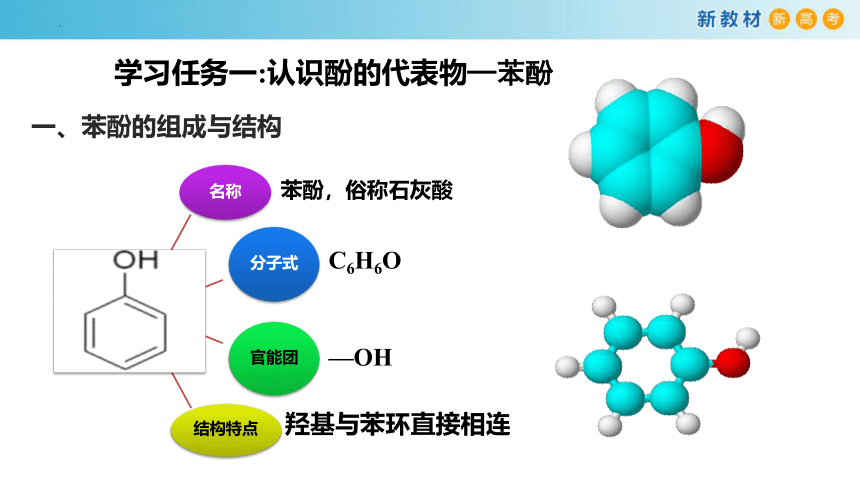
一、苯酚的组成与结构
名称
苯酚,俗称石灰酸
分子式
C6H6O
官能团
—OH
结构特点
羟基与苯环直接相连
学习任务一:认识酚的代表物─苯酚
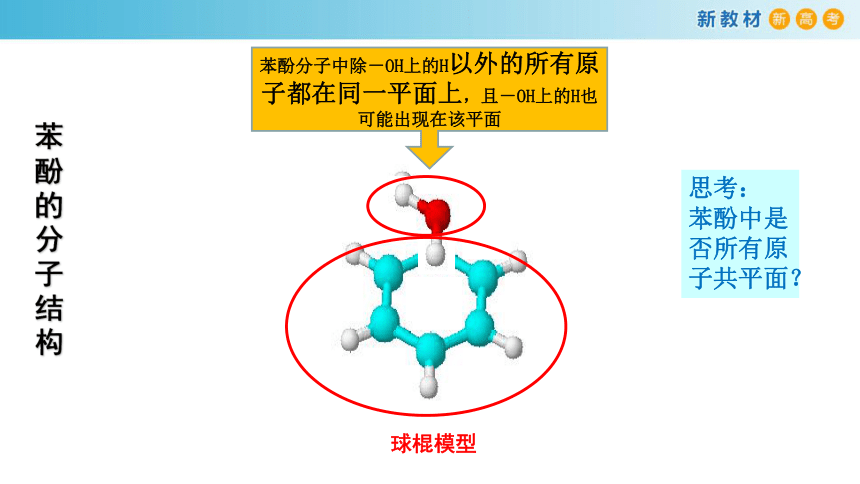
球棍模型
思考:
苯酚中是否所有原子共平面?
苯酚分子中除-OH上的H以外的所有原子都在同一平面上,且-OH上的H也可能出现在该平面
苯酚的分子结构
【实验探究1】
认识苯酚的溶解性
常温下将苯酚溶于水,会有什么现象?加热苯酚和水的混合物,会发生什么现象?再冷却该混合物至室温,会发生什么现象?
苯酚乳浊液
加热
溶解度增大
苯酚澄清溶液
冷却
溶解度下降
苯酚乳浊液
观察分析
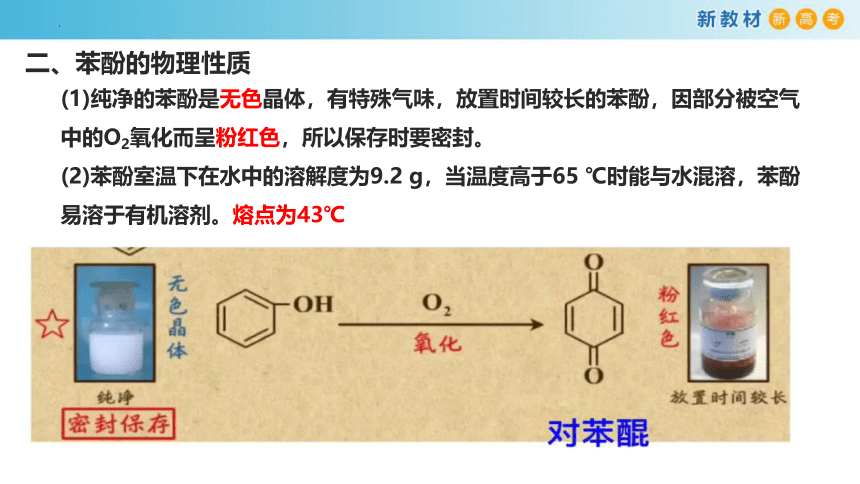
二、苯酚的物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,放置时间较长的苯酚,因部分被空气中的O2氧化而呈粉红色,所以保存时要密封。
(2)苯酚室温下在水中的溶解度为9.2 g,当温度高于65 ℃时能与水混溶,苯酚易溶于有机溶剂。熔点为43℃
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗。
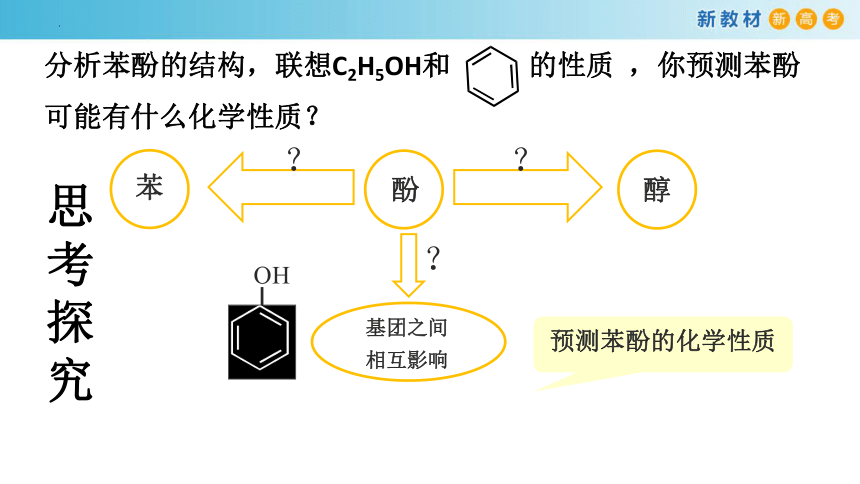
酚
苯
基团之间相互影响
醇
?
?
?
OH
预测苯酚的化学性质
思考探究
分析苯酚的结构,联想C2H5OH和 的性质 ,你预测苯酚可能有什么化学性质?
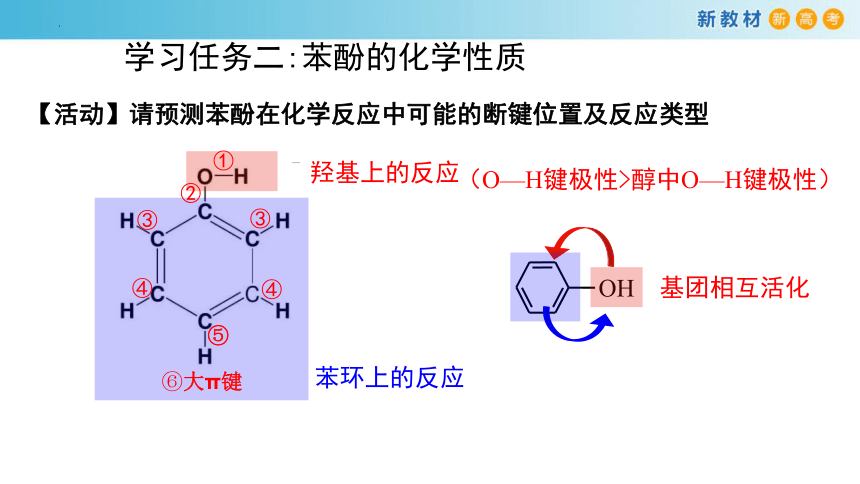
羟基上的反应
苯环上的反应
①
④
②
③
⑤
③
④
⑥大π键
学习任务二:苯酚的化学性质
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
OH
基团相互活化
(O—H键极性>醇中O—H键极性)
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
断裂①
取代反应(酯化反应)
置换反应
ONa
断裂①等
氧化反应
OH
电离出H+,显酸性,石炭酸
羟基上的反应
①
④
②
③
⑤
③
④
⑥大π键
(O—H键极性增强)
三、苯酚的化学性质
结论:苯环对—OH的影响导致酚羟基中的氧氢键易断,呈弱酸性,且酸性极弱,不能使石蕊试剂变色。
苯酚又名石炭酸
苯氧离子
苯酚溶液电离方程式:
1.弱酸性
与NaOH溶液反应
+H2O
OH
ONa
+NaOH
苯酚钠
苯酚钠与盐酸反应生成苯酚
澄清
浑浊
思考:苯酚酸性与H2CO3酸性如何设计实验较?
CO2
苯酚的弱酸性
将二氧化碳气体通入适量苯酚钠溶液中,观察现象。
CO2
苯酚的弱酸性
ONa
OH+
+CO2+H2O
现象:溶液变浑浊
NaHCO3?
Na2CO3?
酸性强弱:H2CO3 > C6H5OH
思考:苯酚酸性与H2CO3酸性如何设计实验较?
+Na2CO3
—OH
—ONa
+NaHCO3
饱和Na2CO3溶液
苯酚固体
NaHCO3溶液
苯酚固体
现象:
固体溶解
现象:
固体不溶解
酸性强弱:C6H5OH > HCO3-
苯酚的弱酸性
思考:苯酚酸性与H2CO3酸性如何设计实验较?
电离平衡常数( 25℃ )
Ka Ka
苯酚(C6H5OH) 1.2×10 10 ——
碳酸(H2CO3) 4.4×10 7 4.7×10 11
1
2
+NaHCO3
ONa
OH
+CO2+H2O
+NaHCO3
OH
ONa
+ Na2CO3
酸性:H2CO3 > 苯酚 > HCO3-
数据分析
思考:苯酚酸性与H2CO3酸性如何设计实验较?
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
苯环上的反应
断裂③⑤
OH
Br
Br
Br
取代反应
断大π键
OH
加成反应
①
④
②
③
⑤
③
④
⑥大π键
OH
活动:探究羟基对苯环的影响
实验 澄清的苯酚溶液+浓溴水
现象
结论
方程式
苯酚和浓溴水反应生成了三溴苯酚,三溴苯酚是难溶于水但易溶于有机溶剂的白色固体
产生白色沉淀
活化
+ 3Br2
OH
-
+ 3HBr
Br
OH
-
Br
Br
-
↓
2.苯酚的取代反应
总结:酚羟基的两种检验方法:
1.苯酚和浓溴水反应,生成白色的2,4,6-三溴苯酚沉淀;
2.苯酚和FeCl3溶液反应,溶液变紫色。
实验方案 实验现象
向苯酚溶液中滴入几滴FeCl3溶液,观察现象
溶液变成紫色
FeCl3
3.苯酚的显色反应
——检验酚羟基
a. 苯酚可以燃烧
b.苯酚在空气中被O2氧化呈粉红色
4.氧化反应
新开封的苯酚
无色晶体
久置于空气中的苯酚
粉红色晶体
O2
c. 苯酚能使酸性KMnO4溶液褪色
结论:苯酚结构上有羟基,表现还原性。
课堂小结
OH
苯环活化羟基
羟基的性质:
弱酸性
还原性
羟基活化苯环
苯环的性质:
取代反应(三取代)
加成反应
特征反应: 显色反应
官能团
基团之间相互影响改变
键的极性
合成纤维
染料
合成香料
含酚类物质的废水对生物具有毒害作用,会对水体造成严重污染。化工厂和炼焦厂的废水中常含有酚类物质,在排放前必须经过处理。
医药方面
防腐剂
四、苯酚的应用
酚醛树脂
消毒剂
练一练
1、只用一种试剂把下列四种无色溶液鉴别开:
苯酚、乙醇、NaOH、KSCN,现象分别怎样?
物质 苯酚 乙醇 NaOH KSCN
现象
紫色液溶
无明显现象
红褐色沉淀
血红色溶液
FeCl3溶液
2、如何检验一份溶液中含有苯酚?
取少量样品 浓溴水——产生白色沉淀,说明含有苯酚。
取少量样品 氯化铁溶液——溶液显紫色,说明含有苯酚。
3.乙烯雌酚是人工合成的激素药物,能改善体内激素的平衡状态,其结构如图。下列有关叙述错误的是
A.乙烯雌酚能发生取代、加成、氧化反应
B.乙烯雌酚可分别与NaOH、NaHCO3溶液反应
C.每1 mol该有机物最多可以与含5 mol Br2的溴水反应
D.该有机物分子中最多有18个碳原子共平面
B
4.A、B、C三种物质的分子式都是C7H8O,若滴入FeCl3溶液,只有C呈紫色。若投入金属钠,只有B没有变化。
(1)写出A、B的结构简式:A________、B________。
(2)C有多种同分异构体,请写出苯环上一溴代物最少的结构简式________。
【解析】C7H8O含苯环的同分异构体有:
找同分异构体时注意从类别上分析,醇类与醚类属于同分异构体,芳香醇与酚类属于同分异构体。
根据C能与FeCl3溶液发生显色反应判断,C应属酚类;A不和FeCl3溶液发生显色反应,但能和金属钠反应,且分子中只含一个氧原子,应属醇类;同理可分析得出B中不含羟基。结合三种物质的分子式,可推得三种物
练一练
5、怎样分离苯酚和苯的混合物
苯酚和苯的混合物
加入NaOH溶液
苯酚钠和苯的混合物
分液
苯
苯酚钠
或通入CO2
加盐酸
苯
酚
分液
苯酚的浑浊液静置后,没有晶体析出,这是什么原因呢?
[资料卡片]
苯酚的熔点很低(常压下为43℃),含水的苯酚熔点更低,当苯酚含10%以上水时,在常温下则呈液态。所以,我们实验中得到的浑浊液,实际上是液态苯酚和苯酚水溶液的混合液。由于温度低于70℃,因此液态苯酚与水不能完全互溶而呈浑浊状。又因为在这种浑浊状的混合液中没有固态苯酚小颗粒,所以久置后也不会有晶体析出,而是呈油状液,属于乳浊液。静置后,分层,下层为苯酚(密度比水大),上层为苯酚的稀溶液。
有机化学思维构建
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第二节 醇 酚
在19世纪初,医院的设备很差,那时缺少麻醉药和消毒剂,许多病人死于手术后的伤口感染中。在英国的爱丁堡有一家医院,一名叫李斯特的的外科医生,发现在化工厂附近的污水沟里,沟水清澈,浮在水面上的草根很少腐烂。原来,就是从化工厂流出的石炭酸(苯酚)混杂在沟水里,石炭酸是化工厂提炼煤焦油时排出的“废弃物”。李斯特用石炭酸对手术器械、纱布等一系列用品进行了消毒,病人手术后伤口化脓、感染的现象立即减少了,死亡率大大下降。由此,爱丁堡医院手术伤口感染率一度成为全世界外科医院中最低的。这一发现使苯酚成为一种强有力的外科消毒剂,李斯特也因此被誉为“外科消毒之父”。同时使苯酚首次声名远扬。
是谁使苯酚声名远扬?
外科消毒之父
———利斯特
利用苯酚外科消毒
学习
目标
第2课时
酚的结构与性质
PART
01
PART
02
通过认识酚的结构,了解苯酚的主要性质,能理解羟基和苯环的相互影响,形成物质结构决定性质的核心理念
通过酚及其酚类性质的学习,列举事实说明有机分子中基团之间存在相互影响
HO
OH
OH
OH
OCH3
CH2
葡萄酚
丁香酚
酚——羟基与苯环上的碳原子直接相连的化合物
官能团为羟基(—OH)
歇后语:苯环上挂羟基装“醇”
苯酚是一元酚,是酚类化合物最简单的,其官能团为羟基(—OH)。
酚的组成与结构
一、苯酚的组成与结构
名称
苯酚,俗称石灰酸
分子式
C6H6O
官能团
—OH
结构特点
羟基与苯环直接相连
学习任务一:认识酚的代表物─苯酚
球棍模型
思考:
苯酚中是否所有原子共平面?
苯酚分子中除-OH上的H以外的所有原子都在同一平面上,且-OH上的H也可能出现在该平面
苯酚的分子结构
【实验探究1】
认识苯酚的溶解性
常温下将苯酚溶于水,会有什么现象?加热苯酚和水的混合物,会发生什么现象?再冷却该混合物至室温,会发生什么现象?
苯酚乳浊液
加热
溶解度增大
苯酚澄清溶液
冷却
溶解度下降
苯酚乳浊液
观察分析
二、苯酚的物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,放置时间较长的苯酚,因部分被空气中的O2氧化而呈粉红色,所以保存时要密封。
(2)苯酚室温下在水中的溶解度为9.2 g,当温度高于65 ℃时能与水混溶,苯酚易溶于有机溶剂。熔点为43℃
医院常用的“来苏水”消毒剂便是苯酚钠盐的稀溶液。
苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗。
酚
苯
基团之间相互影响
醇
?
?
?
OH
预测苯酚的化学性质
思考探究
分析苯酚的结构,联想C2H5OH和 的性质 ,你预测苯酚可能有什么化学性质?
羟基上的反应
苯环上的反应
①
④
②
③
⑤
③
④
⑥大π键
学习任务二:苯酚的化学性质
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
OH
基团相互活化
(O—H键极性>醇中O—H键极性)
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
断裂①
取代反应(酯化反应)
置换反应
ONa
断裂①等
氧化反应
OH
电离出H+,显酸性,石炭酸
羟基上的反应
①
④
②
③
⑤
③
④
⑥大π键
(O—H键极性增强)
三、苯酚的化学性质
结论:苯环对—OH的影响导致酚羟基中的氧氢键易断,呈弱酸性,且酸性极弱,不能使石蕊试剂变色。
苯酚又名石炭酸
苯氧离子
苯酚溶液电离方程式:
1.弱酸性
与NaOH溶液反应
+H2O
OH
ONa
+NaOH
苯酚钠
苯酚钠与盐酸反应生成苯酚
澄清
浑浊
思考:苯酚酸性与H2CO3酸性如何设计实验较?
CO2
苯酚的弱酸性
将二氧化碳气体通入适量苯酚钠溶液中,观察现象。
CO2
苯酚的弱酸性
ONa
OH+
+CO2+H2O
现象:溶液变浑浊
NaHCO3?
Na2CO3?
酸性强弱:H2CO3 > C6H5OH
思考:苯酚酸性与H2CO3酸性如何设计实验较?
+Na2CO3
—OH
—ONa
+NaHCO3
饱和Na2CO3溶液
苯酚固体
NaHCO3溶液
苯酚固体
现象:
固体溶解
现象:
固体不溶解
酸性强弱:C6H5OH > HCO3-
苯酚的弱酸性
思考:苯酚酸性与H2CO3酸性如何设计实验较?
电离平衡常数( 25℃ )
Ka Ka
苯酚(C6H5OH) 1.2×10 10 ——
碳酸(H2CO3) 4.4×10 7 4.7×10 11
1
2
+NaHCO3
ONa
OH
+CO2+H2O
+NaHCO3
OH
ONa
+ Na2CO3
酸性:H2CO3 > 苯酚 > HCO3-
数据分析
思考:苯酚酸性与H2CO3酸性如何设计实验较?
【活动】请预测苯酚在化学反应中可能的断键位置及反应类型
苯环上的反应
断裂③⑤
OH
Br
Br
Br
取代反应
断大π键
OH
加成反应
①
④
②
③
⑤
③
④
⑥大π键
OH
活动:探究羟基对苯环的影响
实验 澄清的苯酚溶液+浓溴水
现象
结论
方程式
苯酚和浓溴水反应生成了三溴苯酚,三溴苯酚是难溶于水但易溶于有机溶剂的白色固体
产生白色沉淀
活化
+ 3Br2
OH
-
+ 3HBr
Br
OH
-
Br
Br
-
↓
2.苯酚的取代反应
总结:酚羟基的两种检验方法:
1.苯酚和浓溴水反应,生成白色的2,4,6-三溴苯酚沉淀;
2.苯酚和FeCl3溶液反应,溶液变紫色。
实验方案 实验现象
向苯酚溶液中滴入几滴FeCl3溶液,观察现象
溶液变成紫色
FeCl3
3.苯酚的显色反应
——检验酚羟基
a. 苯酚可以燃烧
b.苯酚在空气中被O2氧化呈粉红色
4.氧化反应
新开封的苯酚
无色晶体
久置于空气中的苯酚
粉红色晶体
O2
c. 苯酚能使酸性KMnO4溶液褪色
结论:苯酚结构上有羟基,表现还原性。
课堂小结
OH
苯环活化羟基
羟基的性质:
弱酸性
还原性
羟基活化苯环
苯环的性质:
取代反应(三取代)
加成反应
特征反应: 显色反应
官能团
基团之间相互影响改变
键的极性
合成纤维
染料
合成香料
含酚类物质的废水对生物具有毒害作用,会对水体造成严重污染。化工厂和炼焦厂的废水中常含有酚类物质,在排放前必须经过处理。
医药方面
防腐剂
四、苯酚的应用
酚醛树脂
消毒剂
练一练
1、只用一种试剂把下列四种无色溶液鉴别开:
苯酚、乙醇、NaOH、KSCN,现象分别怎样?
物质 苯酚 乙醇 NaOH KSCN
现象
紫色液溶
无明显现象
红褐色沉淀
血红色溶液
FeCl3溶液
2、如何检验一份溶液中含有苯酚?
取少量样品 浓溴水——产生白色沉淀,说明含有苯酚。
取少量样品 氯化铁溶液——溶液显紫色,说明含有苯酚。
3.乙烯雌酚是人工合成的激素药物,能改善体内激素的平衡状态,其结构如图。下列有关叙述错误的是
A.乙烯雌酚能发生取代、加成、氧化反应
B.乙烯雌酚可分别与NaOH、NaHCO3溶液反应
C.每1 mol该有机物最多可以与含5 mol Br2的溴水反应
D.该有机物分子中最多有18个碳原子共平面
B
4.A、B、C三种物质的分子式都是C7H8O,若滴入FeCl3溶液,只有C呈紫色。若投入金属钠,只有B没有变化。
(1)写出A、B的结构简式:A________、B________。
(2)C有多种同分异构体,请写出苯环上一溴代物最少的结构简式________。
【解析】C7H8O含苯环的同分异构体有:
找同分异构体时注意从类别上分析,醇类与醚类属于同分异构体,芳香醇与酚类属于同分异构体。
根据C能与FeCl3溶液发生显色反应判断,C应属酚类;A不和FeCl3溶液发生显色反应,但能和金属钠反应,且分子中只含一个氧原子,应属醇类;同理可分析得出B中不含羟基。结合三种物质的分子式,可推得三种物
练一练
5、怎样分离苯酚和苯的混合物
苯酚和苯的混合物
加入NaOH溶液
苯酚钠和苯的混合物
分液
苯
苯酚钠
或通入CO2
加盐酸
苯
酚
分液
苯酚的浑浊液静置后,没有晶体析出,这是什么原因呢?
[资料卡片]
苯酚的熔点很低(常压下为43℃),含水的苯酚熔点更低,当苯酚含10%以上水时,在常温下则呈液态。所以,我们实验中得到的浑浊液,实际上是液态苯酚和苯酚水溶液的混合液。由于温度低于70℃,因此液态苯酚与水不能完全互溶而呈浑浊状。又因为在这种浑浊状的混合液中没有固态苯酚小颗粒,所以久置后也不会有晶体析出,而是呈油状液,属于乳浊液。静置后,分层,下层为苯酚(密度比水大),上层为苯酚的稀溶液。
有机化学思维构建
