化学人教版(2019)选择性必修2 3.1.1 晶体与非晶体(共55张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修2 3.1.1 晶体与非晶体(共55张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 13.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-02 00:00:00 | ||
图片预览








文档简介
(共55张PPT)
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
第1课时 物质的聚集状态、晶体与非晶体
学习目标
CONTENT
1. 物质的聚集状态
2. 晶体、非晶体的概念
3. 晶体、非晶体的性质
【知识回顾】
1.由分子构成的物质,保持其化学性质不变的最小微粒: 。
分子
2.由分子构成的物质在固、液、气三态变化过程中,分子本身保持 。只是分子之间的 发生了变化。
距 离
固态
液态
气态
不变
固态
液态
气态
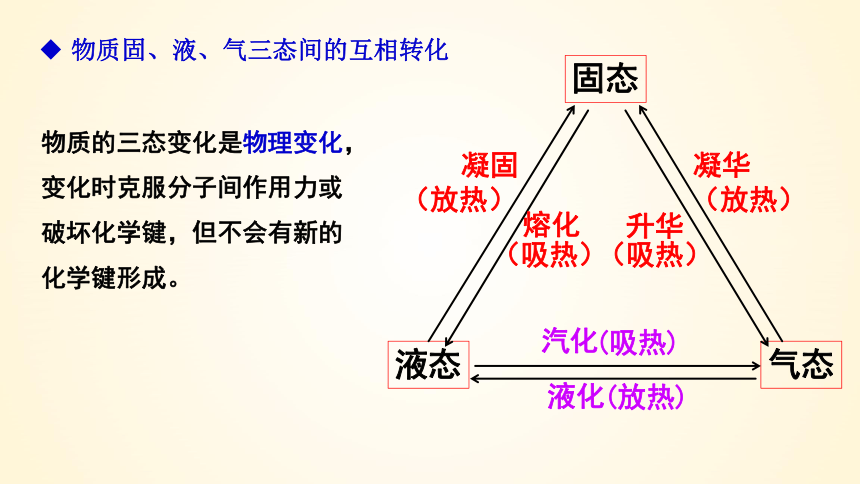
凝固
凝华
熔化
升华
(放热)
(放热)
(吸热)
(吸热)
汽化
液化
(放热)
(吸热)
物质固、液、气三态间的互相转化
物质的三态变化是物理变化,变化时克服分子间作用力或破坏化学键,但不会有新的化学键形成。
→20世纪初,通过X射线衍射等实验手段,发现许多常见的晶体中并无分子。气态和液态物质也不一定是由分子构成。
→20世纪前,人们认为物质的三态变化只是分子间距离发生了变化。
石墨
氯化钠
金刚石
金属
许多晶体中没有分子
→NaCl等离子化合物是由阳离子和阴离子组成的;
→石墨、SiO2、金刚石等由非金属原子构成的物质;
→各种金属及合金等由金属阳离子和自由电子组成。
极光
雷电
思考:那么雷电和极光里的物质又是什么状态的呢?
等离子体
物
质
的
聚
集
状
态
晶态
塑晶态
液晶态
非晶态
等离子体
液晶
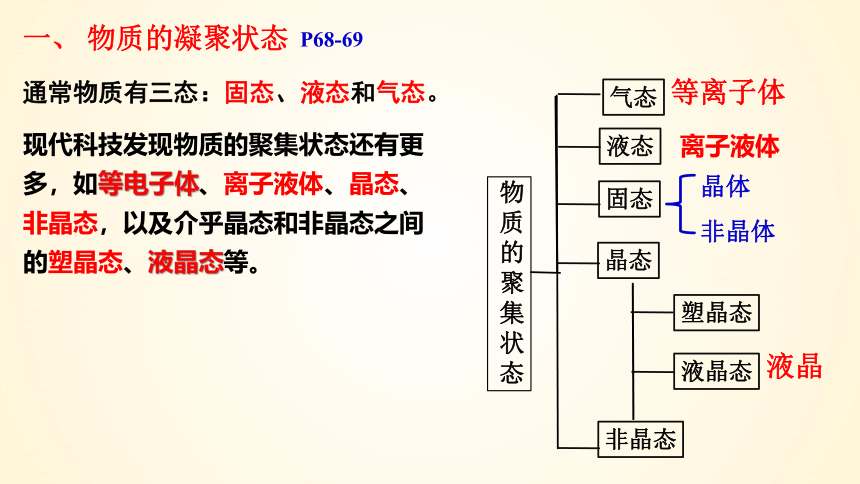
一、 物质的凝聚状态
P68-69
气态
固态
液态
通常物质有三态:固态、液态和气态。
现代科技发现物质的聚集状态还有更多,如等电子体、离子液体、晶态、非晶态,以及介乎晶态和非晶态之间的塑晶态、液晶态等。
离子液体
晶体
非晶体
→等离子体:
1.概念:是由电子、阳离子和电中性粒子(分子或原子)组成的整体上呈电中性的气态物质。
→是除去固、液、气外,物质存在的第四态。
2.形成:气态物质在高温或者在外加电场激发下,分子发生分解,产生电子和阳离子等。
3.特点:是离子化的气体状物质,具有良好的导电性、流动性。
P68
例如,在日光灯和霓虹灯的灯管里,在蜡烛的火焰里,在极光和雷电里,都能找到等离子体。
4.用途:制造等离子体显示器;进行化学合成;核聚变等。
→离子液体:
是熔点不高的全部由离子组成的液体。
如高温下的KCl,KOH呈液体状态,此时它们就是离子液体。
在室温或室温附近温度下呈液态的由离子构成的物质,称为室温离子液体,也称为低温熔融盐。
(低温熔融盐)一般由有机阳离子和无机或有机阴离子构成,常见的阳离子有季铵盐离子、季鏻盐离子、咪唑盐离子和吡咯盐离子等(如下图所示),阴离子有卤素离子、四氟硼酸根离子、六氟磷酸根离子等。
N
N
+
Y-
Y
N
C
Ag
C
N
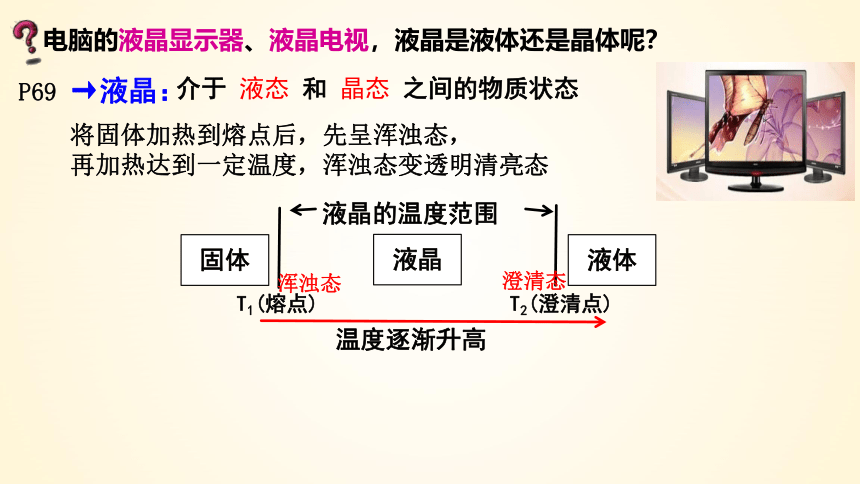
→液晶:
介于 液态 和 晶态 之间的物质状态
固体
液体
液晶的温度范围
液晶
T1(熔点)
T2(澄清点)
温度逐渐升高
P69
电脑的液晶显示器、液晶电视,液晶是液体还是晶体呢?
将固体加热到熔点后,先呈浑浊态,
再加热达到一定温度,浑浊态变透明清亮态
浑浊态
澄清态
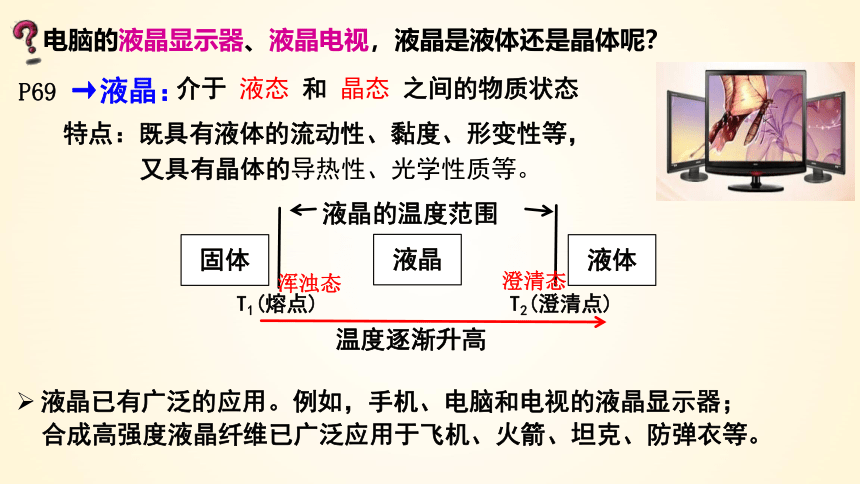
→液晶:
介于 液态 和 晶态 之间的物质状态
特点:既具有液体的流动性、黏度、形变性等,
固体
液体
液晶的温度范围
液晶
T1(熔点)
T2(澄清点)
温度逐渐升高
又具有晶体的导热性、光学性质等。
P69
电脑的液晶显示器、液晶电视,液晶是液体还是晶体呢?
液晶已有广泛的应用。例如,手机、电脑和电视的液晶显示器;
合成高强度液晶纤维已广泛应用于飞机、火箭、坦克、防弹衣等。
浑浊态
澄清态
热致液晶: 指由单一化合物或由少数化合物的均匀混合物形成的液晶。通常在一定温度范围内才显现液晶相的物质。
溶致液晶:是一种包含溶剂化合物在内的两种或多种化合物形成的液晶。是在溶液中溶质分子浓度处于一定范围内时出现液晶相,即胶束等。
实用液晶在常温下十分稳定。已经获得实际应用的热致液晶均为刚性棒状强极性(或易于极化的)分子,其分子有取向序,分子的长轴取向一致,但无位置序,分子可滑动。此外,还有平板状、盘状、叶状分子等液晶。
→准晶
准晶具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性。准晶体具有独特的属性,其坚硬又有弹性、非常平滑,而且,与大多数金属不同的是,其导电、导热性很差,在日常生活中可用来制造不粘锅、发光二极管、热电转化设备等。
准晶体亦称为准晶或拟晶,是一种介于晶体和非晶体之间的固体。
下列关于等离子体的叙述正确的是( )
A.物质一般有固态、液态和气态三种常见状态,等离子体却被认为是物质存在的第四状态
B.为了使气体变成等离子体,必须使其通电
C.等离子体通过电场时,所有粒子的运动方向都发生改变
D.等离子体性质稳定,不易发生化学反应
【同步练习】
A
高温加热、激光照射也可以使气体转变为等离子体
等离子体中也存在电中性微粒,
电中性微粒在电场中运动方向不发生改变
等离子体性质活泼,可发生在一般条件下无法进行的化学反应
碳酸钙
二、晶体与非晶体
蜡状的白磷(P4)
黄色的硫黄(S8)
紫黑色的碘(I2)
蓝色的硫酸铜
(CuSO4·5H2O)
高锰酸钾
从饱和硫酸铜溶液中析出的CuSO4.5H2O
绝大多数常见的固体是晶体
晶体
玻璃
炭黑
非晶体
思考:
二、晶体与非晶体
如何判断固体物质是晶体还是非晶体?晶体与非晶体有什么本质差异呢?
如玻璃、炭黑之类的物质属于非晶体
又称玻璃体
又称无定形体
二、晶体与非晶体
1、晶体:
是由内部微粒(原子、离子或分子)在三维空间里呈周期性重复排列而构成的具有规则几何外形的固体。
①概念:
→晶体中粒子排列的周期性是指一定方向上每隔一定距离就重复出现的排列。
氯化钠
金刚石
粒子排列的周期性导致晶体呈现规则的几何外形。
NaCl
晶体的特点
铜晶体结构
氯化钠晶体结构
→晶体外形和内部质点排列高度有序性
明矾
K2Cr2O7
干冰
NaCl
金刚石
自然铜
二、晶体与非晶体
1、晶体:
②分类:
根据组成晶体的微粒和微粒间的相互作用,可分为
离子晶体
共价晶体
分子晶体
金属晶体
是由内部微粒(原子、离子或分子)在三维空间里呈周期性重复排列而构成的具有规则几何外形的固体。
①概念:
(后面章节将讲解)
2.非晶体
→玻璃体是典型的非晶体,所以非晶态又称为玻璃态。
①概念:
组成物质的微粒(分子、原子、离子)在三维空间里呈相对无序排列而构成的不具有规则几何外形的固体。
② 玻璃、橡胶、石蜡、沥青、塑料等都是非晶体!
二、晶体与非晶体
固体 自范性 微观结构
晶体 有(能自发呈现多面体外形) 原子在三维空间里呈
周期性有序排列
非晶体 没有(不能自发呈现多面体外形) 原子排列相对无序
3. 晶体与非晶体的本质差异
P70
表3-1
→自范性:
晶体在适当条件下能自发地呈现多面体外形的性质
→晶体呈现自范性的条件之一是晶体生长的速率适当。
原因:晶体内部粒子排列的有序性;非晶体粒子的排列则相对无序,无自范性。
→晶体生长速率适当是保持自范性的条件之一。
→阅读课本P70,【思考】岩浆中的SiO2侵入地壳的空洞冷却后形成的水晶球,其外层是非晶态的玛瑙,内部是呈现晶体外形的水晶。原因是什么?
图3-4 天然水晶球里的玛瑙和水晶
说明:玛瑙中含有细小的晶体,但又不纯粹是晶体,要依具体情况而定
玛瑙
水晶
外层冷却快,内层冷却慢
水晶
如果凝固速率过快,常得到粉末或没有规则几何外形的块状物。
→本质上,晶体的自范性是晶体中粒子在微观空间里呈现周期性有序排列的宏观表象。
→非晶体粒子的排列则相对无序,无自范性。
晶体的自范性
晶体SiO2和非晶体SiO2的投影示意图
某同学在网站上找到一张玻璃的结构示意图,如下图,这张图说明玻璃是不是晶体?为什么?
【思考与讨论】
→硅、氧原子在空间排列上并没有周期性有序排列,呈现无序状态,因此,玻璃是非晶体。
晶体的特点并不仅限于外形和内部质点排列的高度有序性,它们的许多物理性质,如强度、导热性、光学性质等,常常表现出各向异性。
→各向异性
:晶体在不同方向上具有不同的物理性质。
(包括晶体的强度、导电性、导热性、光学性质等)
水 晶
[实验]
在水晶和玻璃表面涂一层蜡,用一根红热的铁针刺中凝固的石蜡,观察蜡熔化的形状。
椭圆形
圆形
说明水晶在不同方向的传热能力不同,呈现各向异性。
而非晶体玻璃则呈现各向同性。
玻 璃
这说明了什么呢?
石墨中,与层平行方向上的导电率比与层垂直方向上的导电率大一万倍。
→再比如:石墨的导电性
晶体的特点并不仅限于外形和内部质点排列的高度有序性,它们的许多物理性质,如强度、导热性、光学性质等,常常表现出各向异性。
原因:同一晶体在不同方向上质点排列一般是不一样的, 因此,晶体的物理性质常常随方向的不同而有所差异。
→各向异性
:晶体在不同方向上具有不同的物理性质。
(包括晶体的强度、导电性、导热性、光学性质等)
非晶体则不具有物理性质各向异性的特点,表现为“各向同性”
为什么晶体具有各向异性呢?
——具有固定的熔点
→反映在步冷曲线上出现平台,
而非晶体没有固定的熔点, 反映在步冷曲线上不会出现平台。
晶体的另一特点
晶体步冷曲线
非晶体步冷曲线
→玻璃没有固定的熔点,在一定温度范围内软化
总结:晶体和非晶体
固体 外观 微观结构 自范性 各向异性 熔点
晶体
非晶体
本质区别
具有规则的几何外形
不具有规则的几何外形
有
没有
粒子在三维空间周期性有序排列
粒子排列相对无序
各向异性
各向同性
固定
不固定
微观粒子在三维空间是否呈现周期性有序排列
晶体与非晶体之间在一定条件下可以相互转化。
实验步骤 实验现象
(1)用研钵把硫黄粉末研细,放入蒸发皿中,放在三脚架的铁圈上,用酒精灯加热至熔融态,自然冷却结晶后,观察实验现象。
(2)在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,并在表面皿上加少量冷水。把小烧杯放在石棉网上小火加热,观察实验现象。
(3)在250 mL烧杯中加入半杯饱和氯化钠溶液,用滴管滴入浓盐酸,观察实验现象。
P71 实验3-1
4.晶体形成的途径
实验步骤 实验现象
(1)用研钵把硫黄粉末研细,放入蒸发皿中,放在三脚架的铁圈上,用酒精灯加热至熔融态,自然冷却结晶后,观察实验现象。
(2)在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,并在表面皿上加少量冷水。把小烧杯放在石棉网上小火加热,观察实验现象。
(3)在250 mL烧杯中加入半杯饱和氯化钠溶液,用滴管滴入浓盐酸,观察实验现象。
硫加热融化,自然冷却结晶后,得到黄色晶体。
固体直接变成紫色蒸气,蒸气遇冷又重新凝聚成紫黑色的固体。
有白色细小晶体析出。
P71 实验3-1
4.晶体形成的途径
4.晶体形成的途径
①熔融态物质凝固;
③溶质从溶液中析出。
②气态物质冷却不经液态直接凝固(凝华)
凝华得到的碘晶体
从饱和CuSO4溶液中析出的CuSO4·5H2O晶体
从熔融态结晶出来的硫晶体
饱和氯化钠溶液中滴入浓盐酸
,析出白色细小晶体。
→我们发现,常见的晶体大多是具有光泽的块状或颗粒状固体,那么粉末状的还是晶体吗?
想一想1
碳酸钙晶体粉末和电子显微镜下的碳酸钙晶体
可能是晶体,只是颗粒太小。
如何鉴别水晶的和玻璃的镜片?
想一想2
→区分晶体和非晶体的方法有哪些?
组成
结构
性质
鉴别
方法
自范性
各向异性
有固定熔点
√
晶体
√
5.区别晶体与非晶体
①测熔点。
晶体有固定熔点,非晶体没有固定熔点
②最可靠的科学方法是对固体进行X射线衍射实验。
X射线衍射原理:单一波长的X射线通过晶体时,X射线和晶体中的电子相互作用,会在记录仪上产生分立的斑点或明锐的衍射峰。
衍射
散射效应
→晶体物质能使X-射线产生衍射,非晶体只有散射效应。
松香
橡胶
水晶SiO2
石蜡
判断下列物质是晶体还是非晶体:
非晶体
晶体
观察对称性、刻划玻璃、加热、X—射线衍射
P72思考与讨论:
(2) 根据晶体物理性质的各向异性的特点,能鉴别用玻璃仿造的假宝石。请你能列举一些可能有效的方法鉴别假宝石。
不一定。晶体规则的几何外形是自发形成的。在人力作用下形成的有规则几何外形的固体不是晶体,如玻璃、塑料等相关制品。
不一定。同一种物质既可以有晶体状态也可以有非晶体状态。
思考与讨论2:
(2)某种晶体的物质呈现的状态一定是晶体吗?
(1)具有规则几何外形的固体, 一定是晶体吗?
(3)在一定温度下,将一不规则的NaCl固体,放入饱和NaCl溶液中,经过一段时间,会发生什么变化?为什么?
NaCl固体会变为规则的立方体。因为溶解和结晶是可逆过程。根据晶体的自范性可知,在溶解和结晶的过程中,离子会自发地规则排列,形成规则的立方体。
③晶体也不一定都有规则的几何外形,如玛瑙。
①同一物质可以是晶体,也可以是非晶体,
如晶体SiO2和非晶体SiO2。
②有着规则几何外形或者美观、对称外形的固体,不一定是晶体。例如,玻璃制品可以塑造出规则的几何外形,也可以具有美观对称的外观。
④具有固定组成的物质也不一定是晶体,
如某些无定形体也有固定的组成。
【归纳小结】
提示 宝石是晶体,具有固定的熔点和各向异性,
玻璃仿造的假宝石是非晶体没有固定的熔点和各向异性,
思考与交流
(1)如何鉴别宝石和用玻璃仿造的假宝石?
常用鉴别方法:
①测试硬度,宝石可在玻璃上刻划出痕迹;
②利用宝石的折光率鉴别;
③进行X射线衍射实验鉴别。
提示 晶体内部的粒子一定按一定规律呈周期性的排列,
而非晶体中的粒子排列是无规则的。
思考与交流
(2)液晶内部沿分子长轴方向呈有序排列,因此液晶也属晶体吗?
提示 液晶内部是沿分子长轴方向呈有序排列,
但晶体是三维有序,因此液晶不属于晶体。
(3)晶体内部的微粒一定按一定规律呈周期性的排列吗?
提示 能。
NaCl从溶液中析出,可使缺角的NaCl晶体形成完美的NaCl晶体。
(4)缺角的NaCl晶体在饱和NaCl溶液中能否慢慢变为完美的立方体块?
1.普通玻璃和水晶的根本区别在于( )
A.外形不一样
B.普通玻璃的基本构成粒子无规则性地排列,水晶的基本构成粒子按一定规律做周期性重复排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
B
2.要得到较大颗粒的明矾晶体,在结晶时可采取的操作是
A.配制比室温高10~20 ℃的明矾饱和溶液,然后浸入悬挂的明矾小晶核,
室温下静置
B.在沸水中配制明矾饱和溶液,然后急速冷却结晶
C.室温下,在明矾饱和溶液中投入明矾小晶核,静置
D.快速蒸发明矾饱和溶液至大量晶体析出
A
3.下列关于晶体性质的叙述不正确的是
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
B
4.如图所示是芒硝和玻璃的熔化曲线,下列说法中正确的是( )
A
A.a是芒硝,属于晶体 B.a是玻璃,属于非晶体
C.b是玻璃,属于晶体 D.b是芒硝,属于非晶体
芒硝
玻璃
解析:芒硝是晶体,玻璃是非晶体。晶体有固定的熔点
5.下列有关晶体的特征及结构的叙述不正确的是( )
A.晶体一般都有各向异性
B.宝石在不同方向上硬度不一定相同
C.有规则几何外形的固体不一定都是晶体
D.冰和碘晶体中微粒间的作用力完全相同
D
解析:冰中水分子间除了含有范德华力外还含有氢键,而碘晶体中碘分子之间只含有范德华力
6.晶体是一类非常重要的材料,在很多领域都有广泛的应用。我国现已能够拉制出直径为300毫米,重量达81千克的大直径硅单晶,晶体硅大量用于电子产业。下列对晶体硅的叙述正确的是( )
A.晶体硅没有固定的熔、沸点
B.形成晶体硅的速率越快越好
C.可用X射线衍射实验来鉴别晶体硅和玻璃
D.晶体硅的形成与晶体的自范性有关,形成的晶体无各向异性
C
7.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述中正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.X射线通过玻璃态水时,能产生谱线
解析 玻璃态水无固定形状,不存在晶体结构,故玻璃态水不是晶体,X射线通过玻璃态水时不能产生谱线,因密度与普通水相同,故水由液态变为玻璃态时体积不变
C
8.下列过程中不能得到晶体的是( )
A.对NaCl饱和溶液降温所得到的固体
B.气态水直接冷却成固态水
C.熔融的KNO3冷却后所得到的固体
D.液态的玻璃冷却后所得到的固体
D
解析 得到晶体的三条途径:①溶质从溶液中析出;②气态物质凝华;③熔融态物质凝固。A选项符合①,B选项符合②,C选项符合③。由于玻璃属于非晶体,熔融后再冷却所得到的固体仍为非晶体。
9.下列可用于判断某物质为晶体的方法是( )
A.质谱法 B.红外光谱法
C.核磁共振法 D.X射线衍射法
D
10.用烧热的钢针接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡呈椭圆形,这是因为( )
A.云母是热的不良导体,传热不均匀
B.石蜡是热的不良导体,传热不均匀
C.石蜡具有各向异性,不同方向导热性能不同
D.云母具有各向异性,不同方向导热性能不同
D
11.如图为一块密度、厚度均匀的矩形样品,长为宽的两倍,若用多用电表沿两对称轴测其电阻均为R,则这块样品一定是( )
A.金属 B.半导体 C.非晶体 D.晶体
解析 由于AB=2CD,而AB、CD间的电阻却相等,说明样品横向(AB)与纵向(CD)的导电性不同,具有各向异性,而晶体的特征之一是各向异性,非晶体则具有各向同性,故该样品为晶体。
D
12.(1)在下列物质中, (填序号,下同)是晶体,
是非晶体。
①塑料 ②明矾 ③松香 ④玻璃 ⑤CuSO4·5H2O
⑥冰糖 ⑦石蜡 ⑧单晶硅 ⑨铝块 ⑩橡胶
②⑤⑥⑧⑨
①③④⑦⑩
(2)判断物质是晶体还是非晶体,比较正确的方法是 (填序号)。
①从外形上来判断 ②从各向异性或各向同性上来判断
③从导电性能来判断 ④从有无固定熔点来判断
②④
晶体 非晶体
微观结构特征 粒子周期性有序排列 粒子排列相对无序
性质 特征 自范性 有 无
各向异性 有 无
熔点 固定 不固定
鉴别 方法 间接方法 看是否具有固定的熔点或根据某些物理性质的各向异性
科学方法 对固体进行X-射线衍射实验
举例 NaCl、I2、SiO2、Na晶体等 玻璃、橡胶等
【课堂小结】
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
第1课时 物质的聚集状态、晶体与非晶体
学习目标
CONTENT
1. 物质的聚集状态
2. 晶体、非晶体的概念
3. 晶体、非晶体的性质
【知识回顾】
1.由分子构成的物质,保持其化学性质不变的最小微粒: 。
分子
2.由分子构成的物质在固、液、气三态变化过程中,分子本身保持 。只是分子之间的 发生了变化。
距 离
固态
液态
气态
不变
固态
液态
气态
凝固
凝华
熔化
升华
(放热)
(放热)
(吸热)
(吸热)
汽化
液化
(放热)
(吸热)
物质固、液、气三态间的互相转化
物质的三态变化是物理变化,变化时克服分子间作用力或破坏化学键,但不会有新的化学键形成。
→20世纪初,通过X射线衍射等实验手段,发现许多常见的晶体中并无分子。气态和液态物质也不一定是由分子构成。
→20世纪前,人们认为物质的三态变化只是分子间距离发生了变化。
石墨
氯化钠
金刚石
金属
许多晶体中没有分子
→NaCl等离子化合物是由阳离子和阴离子组成的;
→石墨、SiO2、金刚石等由非金属原子构成的物质;
→各种金属及合金等由金属阳离子和自由电子组成。
极光
雷电
思考:那么雷电和极光里的物质又是什么状态的呢?
等离子体
物
质
的
聚
集
状
态
晶态
塑晶态
液晶态
非晶态
等离子体
液晶
一、 物质的凝聚状态
P68-69
气态
固态
液态
通常物质有三态:固态、液态和气态。
现代科技发现物质的聚集状态还有更多,如等电子体、离子液体、晶态、非晶态,以及介乎晶态和非晶态之间的塑晶态、液晶态等。
离子液体
晶体
非晶体
→等离子体:
1.概念:是由电子、阳离子和电中性粒子(分子或原子)组成的整体上呈电中性的气态物质。
→是除去固、液、气外,物质存在的第四态。
2.形成:气态物质在高温或者在外加电场激发下,分子发生分解,产生电子和阳离子等。
3.特点:是离子化的气体状物质,具有良好的导电性、流动性。
P68
例如,在日光灯和霓虹灯的灯管里,在蜡烛的火焰里,在极光和雷电里,都能找到等离子体。
4.用途:制造等离子体显示器;进行化学合成;核聚变等。
→离子液体:
是熔点不高的全部由离子组成的液体。
如高温下的KCl,KOH呈液体状态,此时它们就是离子液体。
在室温或室温附近温度下呈液态的由离子构成的物质,称为室温离子液体,也称为低温熔融盐。
(低温熔融盐)一般由有机阳离子和无机或有机阴离子构成,常见的阳离子有季铵盐离子、季鏻盐离子、咪唑盐离子和吡咯盐离子等(如下图所示),阴离子有卤素离子、四氟硼酸根离子、六氟磷酸根离子等。
N
N
+
Y-
Y
N
C
Ag
C
N
→液晶:
介于 液态 和 晶态 之间的物质状态
固体
液体
液晶的温度范围
液晶
T1(熔点)
T2(澄清点)
温度逐渐升高
P69
电脑的液晶显示器、液晶电视,液晶是液体还是晶体呢?
将固体加热到熔点后,先呈浑浊态,
再加热达到一定温度,浑浊态变透明清亮态
浑浊态
澄清态
→液晶:
介于 液态 和 晶态 之间的物质状态
特点:既具有液体的流动性、黏度、形变性等,
固体
液体
液晶的温度范围
液晶
T1(熔点)
T2(澄清点)
温度逐渐升高
又具有晶体的导热性、光学性质等。
P69
电脑的液晶显示器、液晶电视,液晶是液体还是晶体呢?
液晶已有广泛的应用。例如,手机、电脑和电视的液晶显示器;
合成高强度液晶纤维已广泛应用于飞机、火箭、坦克、防弹衣等。
浑浊态
澄清态
热致液晶: 指由单一化合物或由少数化合物的均匀混合物形成的液晶。通常在一定温度范围内才显现液晶相的物质。
溶致液晶:是一种包含溶剂化合物在内的两种或多种化合物形成的液晶。是在溶液中溶质分子浓度处于一定范围内时出现液晶相,即胶束等。
实用液晶在常温下十分稳定。已经获得实际应用的热致液晶均为刚性棒状强极性(或易于极化的)分子,其分子有取向序,分子的长轴取向一致,但无位置序,分子可滑动。此外,还有平板状、盘状、叶状分子等液晶。
→准晶
准晶具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性。准晶体具有独特的属性,其坚硬又有弹性、非常平滑,而且,与大多数金属不同的是,其导电、导热性很差,在日常生活中可用来制造不粘锅、发光二极管、热电转化设备等。
准晶体亦称为准晶或拟晶,是一种介于晶体和非晶体之间的固体。
下列关于等离子体的叙述正确的是( )
A.物质一般有固态、液态和气态三种常见状态,等离子体却被认为是物质存在的第四状态
B.为了使气体变成等离子体,必须使其通电
C.等离子体通过电场时,所有粒子的运动方向都发生改变
D.等离子体性质稳定,不易发生化学反应
【同步练习】
A
高温加热、激光照射也可以使气体转变为等离子体
等离子体中也存在电中性微粒,
电中性微粒在电场中运动方向不发生改变
等离子体性质活泼,可发生在一般条件下无法进行的化学反应
碳酸钙
二、晶体与非晶体
蜡状的白磷(P4)
黄色的硫黄(S8)
紫黑色的碘(I2)
蓝色的硫酸铜
(CuSO4·5H2O)
高锰酸钾
从饱和硫酸铜溶液中析出的CuSO4.5H2O
绝大多数常见的固体是晶体
晶体
玻璃
炭黑
非晶体
思考:
二、晶体与非晶体
如何判断固体物质是晶体还是非晶体?晶体与非晶体有什么本质差异呢?
如玻璃、炭黑之类的物质属于非晶体
又称玻璃体
又称无定形体
二、晶体与非晶体
1、晶体:
是由内部微粒(原子、离子或分子)在三维空间里呈周期性重复排列而构成的具有规则几何外形的固体。
①概念:
→晶体中粒子排列的周期性是指一定方向上每隔一定距离就重复出现的排列。
氯化钠
金刚石
粒子排列的周期性导致晶体呈现规则的几何外形。
NaCl
晶体的特点
铜晶体结构
氯化钠晶体结构
→晶体外形和内部质点排列高度有序性
明矾
K2Cr2O7
干冰
NaCl
金刚石
自然铜
二、晶体与非晶体
1、晶体:
②分类:
根据组成晶体的微粒和微粒间的相互作用,可分为
离子晶体
共价晶体
分子晶体
金属晶体
是由内部微粒(原子、离子或分子)在三维空间里呈周期性重复排列而构成的具有规则几何外形的固体。
①概念:
(后面章节将讲解)
2.非晶体
→玻璃体是典型的非晶体,所以非晶态又称为玻璃态。
①概念:
组成物质的微粒(分子、原子、离子)在三维空间里呈相对无序排列而构成的不具有规则几何外形的固体。
② 玻璃、橡胶、石蜡、沥青、塑料等都是非晶体!
二、晶体与非晶体
固体 自范性 微观结构
晶体 有(能自发呈现多面体外形) 原子在三维空间里呈
周期性有序排列
非晶体 没有(不能自发呈现多面体外形) 原子排列相对无序
3. 晶体与非晶体的本质差异
P70
表3-1
→自范性:
晶体在适当条件下能自发地呈现多面体外形的性质
→晶体呈现自范性的条件之一是晶体生长的速率适当。
原因:晶体内部粒子排列的有序性;非晶体粒子的排列则相对无序,无自范性。
→晶体生长速率适当是保持自范性的条件之一。
→阅读课本P70,【思考】岩浆中的SiO2侵入地壳的空洞冷却后形成的水晶球,其外层是非晶态的玛瑙,内部是呈现晶体外形的水晶。原因是什么?
图3-4 天然水晶球里的玛瑙和水晶
说明:玛瑙中含有细小的晶体,但又不纯粹是晶体,要依具体情况而定
玛瑙
水晶
外层冷却快,内层冷却慢
水晶
如果凝固速率过快,常得到粉末或没有规则几何外形的块状物。
→本质上,晶体的自范性是晶体中粒子在微观空间里呈现周期性有序排列的宏观表象。
→非晶体粒子的排列则相对无序,无自范性。
晶体的自范性
晶体SiO2和非晶体SiO2的投影示意图
某同学在网站上找到一张玻璃的结构示意图,如下图,这张图说明玻璃是不是晶体?为什么?
【思考与讨论】
→硅、氧原子在空间排列上并没有周期性有序排列,呈现无序状态,因此,玻璃是非晶体。
晶体的特点并不仅限于外形和内部质点排列的高度有序性,它们的许多物理性质,如强度、导热性、光学性质等,常常表现出各向异性。
→各向异性
:晶体在不同方向上具有不同的物理性质。
(包括晶体的强度、导电性、导热性、光学性质等)
水 晶
[实验]
在水晶和玻璃表面涂一层蜡,用一根红热的铁针刺中凝固的石蜡,观察蜡熔化的形状。
椭圆形
圆形
说明水晶在不同方向的传热能力不同,呈现各向异性。
而非晶体玻璃则呈现各向同性。
玻 璃
这说明了什么呢?
石墨中,与层平行方向上的导电率比与层垂直方向上的导电率大一万倍。
→再比如:石墨的导电性
晶体的特点并不仅限于外形和内部质点排列的高度有序性,它们的许多物理性质,如强度、导热性、光学性质等,常常表现出各向异性。
原因:同一晶体在不同方向上质点排列一般是不一样的, 因此,晶体的物理性质常常随方向的不同而有所差异。
→各向异性
:晶体在不同方向上具有不同的物理性质。
(包括晶体的强度、导电性、导热性、光学性质等)
非晶体则不具有物理性质各向异性的特点,表现为“各向同性”
为什么晶体具有各向异性呢?
——具有固定的熔点
→反映在步冷曲线上出现平台,
而非晶体没有固定的熔点, 反映在步冷曲线上不会出现平台。
晶体的另一特点
晶体步冷曲线
非晶体步冷曲线
→玻璃没有固定的熔点,在一定温度范围内软化
总结:晶体和非晶体
固体 外观 微观结构 自范性 各向异性 熔点
晶体
非晶体
本质区别
具有规则的几何外形
不具有规则的几何外形
有
没有
粒子在三维空间周期性有序排列
粒子排列相对无序
各向异性
各向同性
固定
不固定
微观粒子在三维空间是否呈现周期性有序排列
晶体与非晶体之间在一定条件下可以相互转化。
实验步骤 实验现象
(1)用研钵把硫黄粉末研细,放入蒸发皿中,放在三脚架的铁圈上,用酒精灯加热至熔融态,自然冷却结晶后,观察实验现象。
(2)在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,并在表面皿上加少量冷水。把小烧杯放在石棉网上小火加热,观察实验现象。
(3)在250 mL烧杯中加入半杯饱和氯化钠溶液,用滴管滴入浓盐酸,观察实验现象。
P71 实验3-1
4.晶体形成的途径
实验步骤 实验现象
(1)用研钵把硫黄粉末研细,放入蒸发皿中,放在三脚架的铁圈上,用酒精灯加热至熔融态,自然冷却结晶后,观察实验现象。
(2)在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,并在表面皿上加少量冷水。把小烧杯放在石棉网上小火加热,观察实验现象。
(3)在250 mL烧杯中加入半杯饱和氯化钠溶液,用滴管滴入浓盐酸,观察实验现象。
硫加热融化,自然冷却结晶后,得到黄色晶体。
固体直接变成紫色蒸气,蒸气遇冷又重新凝聚成紫黑色的固体。
有白色细小晶体析出。
P71 实验3-1
4.晶体形成的途径
4.晶体形成的途径
①熔融态物质凝固;
③溶质从溶液中析出。
②气态物质冷却不经液态直接凝固(凝华)
凝华得到的碘晶体
从饱和CuSO4溶液中析出的CuSO4·5H2O晶体
从熔融态结晶出来的硫晶体
饱和氯化钠溶液中滴入浓盐酸
,析出白色细小晶体。
→我们发现,常见的晶体大多是具有光泽的块状或颗粒状固体,那么粉末状的还是晶体吗?
想一想1
碳酸钙晶体粉末和电子显微镜下的碳酸钙晶体
可能是晶体,只是颗粒太小。
如何鉴别水晶的和玻璃的镜片?
想一想2
→区分晶体和非晶体的方法有哪些?
组成
结构
性质
鉴别
方法
自范性
各向异性
有固定熔点
√
晶体
√
5.区别晶体与非晶体
①测熔点。
晶体有固定熔点,非晶体没有固定熔点
②最可靠的科学方法是对固体进行X射线衍射实验。
X射线衍射原理:单一波长的X射线通过晶体时,X射线和晶体中的电子相互作用,会在记录仪上产生分立的斑点或明锐的衍射峰。
衍射
散射效应
→晶体物质能使X-射线产生衍射,非晶体只有散射效应。
松香
橡胶
水晶SiO2
石蜡
判断下列物质是晶体还是非晶体:
非晶体
晶体
观察对称性、刻划玻璃、加热、X—射线衍射
P72思考与讨论:
(2) 根据晶体物理性质的各向异性的特点,能鉴别用玻璃仿造的假宝石。请你能列举一些可能有效的方法鉴别假宝石。
不一定。晶体规则的几何外形是自发形成的。在人力作用下形成的有规则几何外形的固体不是晶体,如玻璃、塑料等相关制品。
不一定。同一种物质既可以有晶体状态也可以有非晶体状态。
思考与讨论2:
(2)某种晶体的物质呈现的状态一定是晶体吗?
(1)具有规则几何外形的固体, 一定是晶体吗?
(3)在一定温度下,将一不规则的NaCl固体,放入饱和NaCl溶液中,经过一段时间,会发生什么变化?为什么?
NaCl固体会变为规则的立方体。因为溶解和结晶是可逆过程。根据晶体的自范性可知,在溶解和结晶的过程中,离子会自发地规则排列,形成规则的立方体。
③晶体也不一定都有规则的几何外形,如玛瑙。
①同一物质可以是晶体,也可以是非晶体,
如晶体SiO2和非晶体SiO2。
②有着规则几何外形或者美观、对称外形的固体,不一定是晶体。例如,玻璃制品可以塑造出规则的几何外形,也可以具有美观对称的外观。
④具有固定组成的物质也不一定是晶体,
如某些无定形体也有固定的组成。
【归纳小结】
提示 宝石是晶体,具有固定的熔点和各向异性,
玻璃仿造的假宝石是非晶体没有固定的熔点和各向异性,
思考与交流
(1)如何鉴别宝石和用玻璃仿造的假宝石?
常用鉴别方法:
①测试硬度,宝石可在玻璃上刻划出痕迹;
②利用宝石的折光率鉴别;
③进行X射线衍射实验鉴别。
提示 晶体内部的粒子一定按一定规律呈周期性的排列,
而非晶体中的粒子排列是无规则的。
思考与交流
(2)液晶内部沿分子长轴方向呈有序排列,因此液晶也属晶体吗?
提示 液晶内部是沿分子长轴方向呈有序排列,
但晶体是三维有序,因此液晶不属于晶体。
(3)晶体内部的微粒一定按一定规律呈周期性的排列吗?
提示 能。
NaCl从溶液中析出,可使缺角的NaCl晶体形成完美的NaCl晶体。
(4)缺角的NaCl晶体在饱和NaCl溶液中能否慢慢变为完美的立方体块?
1.普通玻璃和水晶的根本区别在于( )
A.外形不一样
B.普通玻璃的基本构成粒子无规则性地排列,水晶的基本构成粒子按一定规律做周期性重复排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
B
2.要得到较大颗粒的明矾晶体,在结晶时可采取的操作是
A.配制比室温高10~20 ℃的明矾饱和溶液,然后浸入悬挂的明矾小晶核,
室温下静置
B.在沸水中配制明矾饱和溶液,然后急速冷却结晶
C.室温下,在明矾饱和溶液中投入明矾小晶核,静置
D.快速蒸发明矾饱和溶液至大量晶体析出
A
3.下列关于晶体性质的叙述不正确的是
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
B
4.如图所示是芒硝和玻璃的熔化曲线,下列说法中正确的是( )
A
A.a是芒硝,属于晶体 B.a是玻璃,属于非晶体
C.b是玻璃,属于晶体 D.b是芒硝,属于非晶体
芒硝
玻璃
解析:芒硝是晶体,玻璃是非晶体。晶体有固定的熔点
5.下列有关晶体的特征及结构的叙述不正确的是( )
A.晶体一般都有各向异性
B.宝石在不同方向上硬度不一定相同
C.有规则几何外形的固体不一定都是晶体
D.冰和碘晶体中微粒间的作用力完全相同
D
解析:冰中水分子间除了含有范德华力外还含有氢键,而碘晶体中碘分子之间只含有范德华力
6.晶体是一类非常重要的材料,在很多领域都有广泛的应用。我国现已能够拉制出直径为300毫米,重量达81千克的大直径硅单晶,晶体硅大量用于电子产业。下列对晶体硅的叙述正确的是( )
A.晶体硅没有固定的熔、沸点
B.形成晶体硅的速率越快越好
C.可用X射线衍射实验来鉴别晶体硅和玻璃
D.晶体硅的形成与晶体的自范性有关,形成的晶体无各向异性
C
7.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述中正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.X射线通过玻璃态水时,能产生谱线
解析 玻璃态水无固定形状,不存在晶体结构,故玻璃态水不是晶体,X射线通过玻璃态水时不能产生谱线,因密度与普通水相同,故水由液态变为玻璃态时体积不变
C
8.下列过程中不能得到晶体的是( )
A.对NaCl饱和溶液降温所得到的固体
B.气态水直接冷却成固态水
C.熔融的KNO3冷却后所得到的固体
D.液态的玻璃冷却后所得到的固体
D
解析 得到晶体的三条途径:①溶质从溶液中析出;②气态物质凝华;③熔融态物质凝固。A选项符合①,B选项符合②,C选项符合③。由于玻璃属于非晶体,熔融后再冷却所得到的固体仍为非晶体。
9.下列可用于判断某物质为晶体的方法是( )
A.质谱法 B.红外光谱法
C.核磁共振法 D.X射线衍射法
D
10.用烧热的钢针接触涂有薄薄一层石蜡的云母片的反面,熔化了的石蜡呈椭圆形,这是因为( )
A.云母是热的不良导体,传热不均匀
B.石蜡是热的不良导体,传热不均匀
C.石蜡具有各向异性,不同方向导热性能不同
D.云母具有各向异性,不同方向导热性能不同
D
11.如图为一块密度、厚度均匀的矩形样品,长为宽的两倍,若用多用电表沿两对称轴测其电阻均为R,则这块样品一定是( )
A.金属 B.半导体 C.非晶体 D.晶体
解析 由于AB=2CD,而AB、CD间的电阻却相等,说明样品横向(AB)与纵向(CD)的导电性不同,具有各向异性,而晶体的特征之一是各向异性,非晶体则具有各向同性,故该样品为晶体。
D
12.(1)在下列物质中, (填序号,下同)是晶体,
是非晶体。
①塑料 ②明矾 ③松香 ④玻璃 ⑤CuSO4·5H2O
⑥冰糖 ⑦石蜡 ⑧单晶硅 ⑨铝块 ⑩橡胶
②⑤⑥⑧⑨
①③④⑦⑩
(2)判断物质是晶体还是非晶体,比较正确的方法是 (填序号)。
①从外形上来判断 ②从各向异性或各向同性上来判断
③从导电性能来判断 ④从有无固定熔点来判断
②④
晶体 非晶体
微观结构特征 粒子周期性有序排列 粒子排列相对无序
性质 特征 自范性 有 无
各向异性 有 无
熔点 固定 不固定
鉴别 方法 间接方法 看是否具有固定的熔点或根据某些物理性质的各向异性
科学方法 对固体进行X-射线衍射实验
举例 NaCl、I2、SiO2、Na晶体等 玻璃、橡胶等
【课堂小结】
