氨气的实验室制法导学案(无答案)
文档属性
| 名称 | 氨气的实验室制法导学案(无答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 432.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-02 00:00:00 | ||
图片预览

文档简介
(
(北京)股份有限公司
)
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
第2课时 氨气的实验室制法
一、课标与教材分析
1.本节课选自人教版高中必修二第五章第二节第二课时氨和铵盐。在这之前,学生已经学过硫及其化合物知识。氨、铵盐与我们的生活息息相关,可以让学生体会化学学习的价值。
2.设计氨气的制备实验以,实现氨的转化与生成,增强科学探究与创新意识。
二、自主学习
1.氨气的实验室制法
(1)原理:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O。
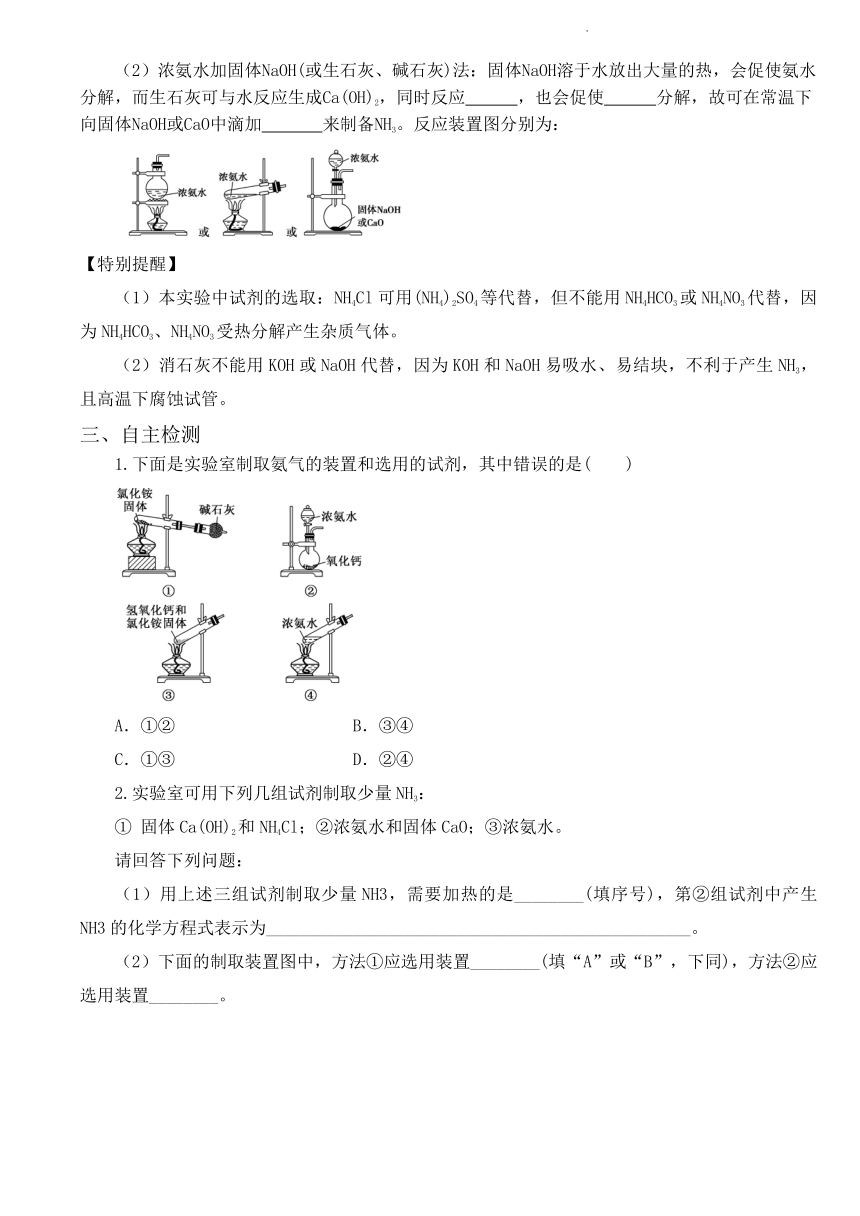
(2)装置:
① 发生装置:固体+固体气体,与实验室利用 和 加热制取氧气的装置相同。
② 净化装置:通常用 干燥氨气,不能用五氧化二磷、 和无水氯化钙干燥。
(3)收集方法: 排空气法收集,试管口塞一团疏松的棉花团,目的是防止 与空气形成对流,以收集到较纯净的氨气。
(4)验满方法
① 方法一:用镊子夹住一片湿润的 试纸放在试管口,若试纸变 ,说明已经收集满。
② 方法二:用蘸取 的玻璃棒靠近试管口,若有 生成,说明已经收集满。
(5)尾气处理:多余的氨气要吸收掉(可在导管口放一团用水或 浸润的棉花球)以避免污染空气。在吸收时要防止 ,常采用的装置如图所示:
2.实验室快速制氨气的方法
(1)加热浓氨水法:NH3·H2O不稳定,受 易分解生成NH3:NH3·H2ONH3↑+H2O,故可直接加 制备NH3。
(2)浓氨水加固体NaOH(或生石灰、碱石灰)法:固体NaOH溶于水放出大量的热,会促使氨水分解,而生石灰可与水反应生成Ca(OH)2,同时反应 ,也会促使 分解,故可在常温下向固体NaOH或CaO中滴加 来制备NH3。反应装置图分别为:
【特别提醒】
(1)本实验中试剂的选取:NH4Cl可用(NH4)2SO4等代替,但不能用NH4HCO3或NH4NO3代替,因为NH4HCO3、NH4NO3受热分解产生杂质气体。
(2)消石灰不能用KOH或NaOH代替,因为KOH和NaOH易吸水、易结块,不利于产生NH3,且高温下腐蚀试管。
自主检测
1.下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A.①② B.③④
C.①③ D.②④
2.实验室可用下列几组试剂制取少量NH3:
① 固体Ca(OH)2和NH4Cl;②浓氨水和固体CaO;③浓氨水。
请回答下列问题:
(1)用上述三组试剂制取少量NH3,需要加热的是________(填序号),第②组试剂中产生NH3的化学方程式表示为_________________________________________________。
(2)下面的制取装置图中,方法①应选用装置________(填“A”或“B”,下同),方法②应选用装置________。
(3)在制取后,如果要干燥氨气,应选用的干燥剂是________。
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷
D.碱石灰 E.固体CaO F.无水CaCl2
(4)检验集气瓶中是否收集满氨气的方法是___________________________________。
(5)为防止环境污染,以下装置 (盛放的液体为水)可用于吸收多余NH3的是________(填序号)。
例题精讲
1.下列有关制取少量干燥的氨气的叙述正确的是( )
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
2.下列方法中,不能用于实验室里制取氨气的是( )
A.在试管中将熟石灰和氯化铵混合后加热
B.加热试管中的氯化铵固体
C.将烧瓶中的浓氨水加热
D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
应用体验
1.已知氨气极易溶于水,难溶于有机溶剂CCl4。下列不适合作氨气的尾气吸收装置的是( )
2.氮元素的单质和常见的化合物在工农业生产中用途广泛。
Ⅰ.(1)常用作食品袋中填充气的是 ;常用作制冷剂的化合物是 ,该物质在空气中与HCl相遇有白烟生成,产生该现象的反应的化学方程式是 。
(2)铵盐大多在农业上用作化肥。工业制备氨气的化学方程式为 。
Ⅱ.某同学用下列装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究。回答下列问题:
(1)若用装置①制取并收集干燥的NH3,其反应的化学方程式为 。若要测定生成的NH3的体积,则必须选择的装置是 (填序号),装置中所盛试剂具有的性质是 。
(2)若用装置②制取并收集干燥的NH3,烧瓶内的试剂是 ,分液漏斗中的试剂是 ,收集装置应选择 (填序号)。
(3)已知氨气极易溶于水,而难溶于有机溶剂。下列装置中不适用于氨气的尾气吸收的是
(填序号)。
作业检测
1.某同学利用如图所示的装置,验证氨气的喷泉实验。回答下列问题:
(1)仪器A的名称是___________。
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:___________。
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向___________填“上”或“下”)排空气法收集氨气。
②下列物质可用于干燥氨气的是___________(填序号)。
A. 浓硫酸 B. 碱石灰 C. 浓硝酸
(4)引发喷泉实验的操作是___________。
2.某化学学习小组设计实验制取氨气并探究氨气的有关性质:
(1)已知NH3难溶于有机溶剂CCl4,该小组成员设计实验制备氨气并探究氨气的还原性及产物,提供实验装置如图:
①装置C中发生反应的化学方程式为______
②根据上述提供的装置正确的连接顺序为______ (用各接口序号表示)
③该装置在设计上有一定的缺陷,你对该装置的改进措施是___________。
(2)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式______
(3)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。请你设计一个简单的实验检验该红色物质中是否含有Cu2O___________。(已知:Cu2O+2H+=Cu+Cu2+ +H2O)
(4)按下图装置进行NH3性质实验。
①先打开旋塞1,现象是___________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________ 。
(北京)股份有限公司
)
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
第2课时 氨气的实验室制法
一、课标与教材分析
1.本节课选自人教版高中必修二第五章第二节第二课时氨和铵盐。在这之前,学生已经学过硫及其化合物知识。氨、铵盐与我们的生活息息相关,可以让学生体会化学学习的价值。
2.设计氨气的制备实验以,实现氨的转化与生成,增强科学探究与创新意识。
二、自主学习
1.氨气的实验室制法
(1)原理:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O。
(2)装置:
① 发生装置:固体+固体气体,与实验室利用 和 加热制取氧气的装置相同。
② 净化装置:通常用 干燥氨气,不能用五氧化二磷、 和无水氯化钙干燥。
(3)收集方法: 排空气法收集,试管口塞一团疏松的棉花团,目的是防止 与空气形成对流,以收集到较纯净的氨气。
(4)验满方法
① 方法一:用镊子夹住一片湿润的 试纸放在试管口,若试纸变 ,说明已经收集满。
② 方法二:用蘸取 的玻璃棒靠近试管口,若有 生成,说明已经收集满。
(5)尾气处理:多余的氨气要吸收掉(可在导管口放一团用水或 浸润的棉花球)以避免污染空气。在吸收时要防止 ,常采用的装置如图所示:
2.实验室快速制氨气的方法
(1)加热浓氨水法:NH3·H2O不稳定,受 易分解生成NH3:NH3·H2ONH3↑+H2O,故可直接加 制备NH3。
(2)浓氨水加固体NaOH(或生石灰、碱石灰)法:固体NaOH溶于水放出大量的热,会促使氨水分解,而生石灰可与水反应生成Ca(OH)2,同时反应 ,也会促使 分解,故可在常温下向固体NaOH或CaO中滴加 来制备NH3。反应装置图分别为:
【特别提醒】
(1)本实验中试剂的选取:NH4Cl可用(NH4)2SO4等代替,但不能用NH4HCO3或NH4NO3代替,因为NH4HCO3、NH4NO3受热分解产生杂质气体。
(2)消石灰不能用KOH或NaOH代替,因为KOH和NaOH易吸水、易结块,不利于产生NH3,且高温下腐蚀试管。
自主检测
1.下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
A.①② B.③④
C.①③ D.②④
2.实验室可用下列几组试剂制取少量NH3:
① 固体Ca(OH)2和NH4Cl;②浓氨水和固体CaO;③浓氨水。
请回答下列问题:
(1)用上述三组试剂制取少量NH3,需要加热的是________(填序号),第②组试剂中产生NH3的化学方程式表示为_________________________________________________。
(2)下面的制取装置图中,方法①应选用装置________(填“A”或“B”,下同),方法②应选用装置________。
(3)在制取后,如果要干燥氨气,应选用的干燥剂是________。
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷
D.碱石灰 E.固体CaO F.无水CaCl2
(4)检验集气瓶中是否收集满氨气的方法是___________________________________。
(5)为防止环境污染,以下装置 (盛放的液体为水)可用于吸收多余NH3的是________(填序号)。
例题精讲
1.下列有关制取少量干燥的氨气的叙述正确的是( )
A.①是氨气发生装置 B.②是氨气吸收装置
C.③是氨气发生装置 D.④是氨气收集、检验装置
2.下列方法中,不能用于实验室里制取氨气的是( )
A.在试管中将熟石灰和氯化铵混合后加热
B.加热试管中的氯化铵固体
C.将烧瓶中的浓氨水加热
D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
应用体验
1.已知氨气极易溶于水,难溶于有机溶剂CCl4。下列不适合作氨气的尾气吸收装置的是( )
2.氮元素的单质和常见的化合物在工农业生产中用途广泛。
Ⅰ.(1)常用作食品袋中填充气的是 ;常用作制冷剂的化合物是 ,该物质在空气中与HCl相遇有白烟生成,产生该现象的反应的化学方程式是 。
(2)铵盐大多在农业上用作化肥。工业制备氨气的化学方程式为 。
Ⅱ.某同学用下列装置(固定、加热仪器和橡胶管略)进行有关氨气制取的实验探究。回答下列问题:
(1)若用装置①制取并收集干燥的NH3,其反应的化学方程式为 。若要测定生成的NH3的体积,则必须选择的装置是 (填序号),装置中所盛试剂具有的性质是 。
(2)若用装置②制取并收集干燥的NH3,烧瓶内的试剂是 ,分液漏斗中的试剂是 ,收集装置应选择 (填序号)。
(3)已知氨气极易溶于水,而难溶于有机溶剂。下列装置中不适用于氨气的尾气吸收的是
(填序号)。
作业检测
1.某同学利用如图所示的装置,验证氨气的喷泉实验。回答下列问题:
(1)仪器A的名称是___________。
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:___________。
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向___________填“上”或“下”)排空气法收集氨气。
②下列物质可用于干燥氨气的是___________(填序号)。
A. 浓硫酸 B. 碱石灰 C. 浓硝酸
(4)引发喷泉实验的操作是___________。
2.某化学学习小组设计实验制取氨气并探究氨气的有关性质:
(1)已知NH3难溶于有机溶剂CCl4,该小组成员设计实验制备氨气并探究氨气的还原性及产物,提供实验装置如图:
①装置C中发生反应的化学方程式为______
②根据上述提供的装置正确的连接顺序为______ (用各接口序号表示)
③该装置在设计上有一定的缺陷,你对该装置的改进措施是___________。
(2)利用改进后的装置进行实验,观察到CuO全部变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式______
(3)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。请你设计一个简单的实验检验该红色物质中是否含有Cu2O___________。(已知:Cu2O+2H+=Cu+Cu2+ +H2O)
(4)按下图装置进行NH3性质实验。
①先打开旋塞1,现象是___________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是___________ 。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
