人教版九下10.2 酸和碱的中和反应(第2课时) 课件(共24张PPT内嵌视频)
文档属性
| 名称 | 人教版九下10.2 酸和碱的中和反应(第2课时) 课件(共24张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 28.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-03 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
10.2 酸和碱的中和反应(第2课时)
日常生活中,在我们吃食醋、橘子、葡萄等水果时,会感到它们酸的程度是不一样的,那么,如何表示物质酸性的强弱呢
学习目标
1. 会用PH试纸测定溶液的酸碱度,了解溶液的酸碱度在实际中的意义。
2. 会用分析、归纳的方法对有关信息加工处理。
溶液的酸碱性与酸碱度
溶液的酸碱性: 指的是溶液呈酸性、碱性还是中性,常用酸碱指 示剂测定;
酸性溶液:
能使紫色石蕊试液变红
碱性溶液:
能使紫色石蕊试液变蓝,使无色酚酞试液变红
中性溶液:
不能使石蕊及酚酞试液变色
溶液的酸碱度是表示酸碱性的强弱程度。
稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
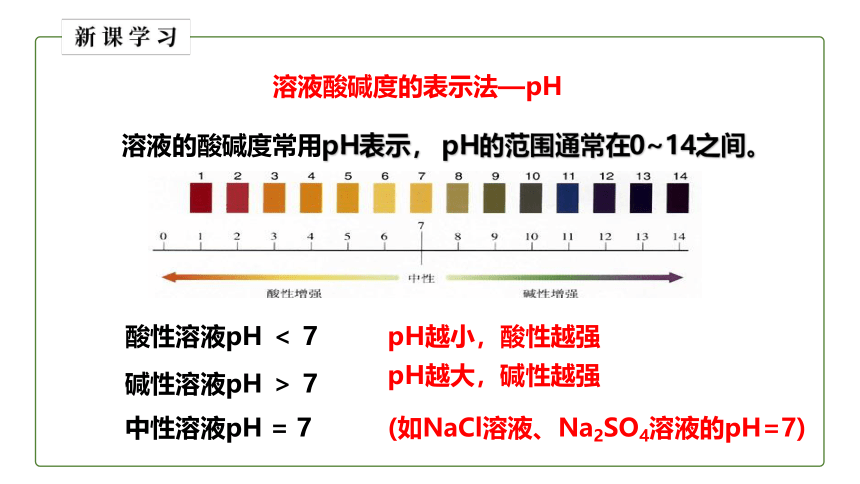
溶液酸碱度的表示法—pH
溶液的酸碱度常用pH表示, pH的范围通常在0~14之间。
酸性溶液pH < 7
碱性溶液pH > 7
中性溶液pH = 7
pH越小,酸性越强
pH越大,碱性越强
(如NaCl溶液、Na2SO4溶液的pH=7)
①pH表示溶液酸碱性的强弱程度,但不确定是酸的溶液或碱的溶液。
②注意酸(碱)、酸性(碱性)和酸碱度的区别和联系。
③pH是溶液中所含H+的浓度或OH-浓度大小的一种表示方法,溶液中H+浓度越大,酸性越强,pH越小;OH-的浓度越大,则碱性越强,pH越大;当溶液中H+和OH-浓度相等时,则溶液的pH=7,呈中性。
④碱性溶液中一定含OH-,但不一定是碱的溶液;酸性溶液中一定含H+,但不一定是酸的溶液。
注意:
1. pH的测定——用pH试纸测定(最简便的方法)
测定方法:在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出被测液的pH 。
【注意事项】
1. 不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂;
2. pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后的溶液酸碱度,导致测定结果不准确;
3. 读数只能整数;
4. 检验气体酸性碱性润湿再用。
原溶液为酸性,会使pH变大;
原溶液为碱性,会使pH变小;
原溶液为中性,对pH无影响;
更精确的pH测试仪器——pH计
用pH试纸测定一些液体的酸碱性
酸溶液的pH<7,碱溶液的pH>7。即:酸溶液显酸性,碱溶液显碱性。
1. 酸溶液都是酸性溶液,但酸性溶液不一定是酸溶液,例如NH4NO3溶液是酸性溶液,但不是酸溶液, NH4NO3是一种盐。
总之,酸性溶液包含酸溶液。
2. 碱溶液都是碱性溶液,但碱性溶液不一定是碱溶液,例如Na2CO3溶液是碱性溶液,但不是碱溶液, Na2CO3是一种盐。
总之,碱性溶液包含碱溶液。
酸溶液
酸性溶液
碱溶液
碱性溶液
溶液的浓度与pH的关系
浓度越小,酸性越弱,pH越大;
浓度越小,碱性越弱,pH越小;
浓度越大,酸性越强,pH越小。
浓度越大,碱性越强,pH越大。
问:NaCl 的水溶液呢?浓度对pH有什么影响?
氯化钠溶液是中性的, pH =7,所以不管溶液的浓度高低,溶液的pH都是7,因此无影响。
酸溶液
碱溶液
测定生活中一些物质的pH,说明它们的酸碱性。
实验10-10
身边一些物质的pH
测生活中一些物质的PH
(1)化工生产中许多反应必须在一定的pH溶液里才能进行;
(2)农业生产中农作物一般适宜在pH为7或者接近7的土壤中生长;
了解溶液酸碱性的意义
西瓜6.0~7.0
苹果树6.0~8.0
小麦6.0~7.0
3. 测定人体内或排出的液体的pH,可以了解人体的健康状况。
人体中几种重要体液的正常pH范围
体液 血液 唾液 胃液 乳汁 尿液
pH 7.35-7.45 6.6-7.1 0.9-1.5 6.6-7.6 4.7-8.4
人的体液的pH必须维持在一定范围内,如果超越正常范围,会导致生理功能失调或发生疾病,甚至出现酸中毒或碱中毒。
4. 测定雨水的pH,可以了解空气的污染情况
雨水一般呈弱酸性(由于空气中的二氧化碳溶解在雨水中),人们一般把pH小于5.6 的雨水称为酸雨。
酸雨的危害
洗发剂和护发剂酸碱性
溶液酸碱度对头发的影响
讨论:溶液的酸碱度对头发有什么影响?对你选择洗发液有什么启示?
答:碱性物质对头发有损坏作用。所以洗发液应选
pH=1 pH=4 pH=7 pH=10 pH=13
观察头发光泽
拉断的难易程度
接近中性的,不要选碱性大的洗发液。然后再用微酸性的护发素来保护头发。
光泽好
较好
正常
不好
很不好
难
较难
易
很易
正常
课堂练习
1.下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
2.人体内一些液体的正常pH范围如下,下列说法中不正确的是( )
A.胆汁和胰液显碱性
B.胃液比唾液酸性弱
C.胰液比胆汁碱性强
D.服用含氢氧化铝[Al(OH3)]的药物可以治疗胃酸过多症
C
B
液体 胃液 唾液 胆汁 胰液
pH 0.9﹣1.5 6.6﹣7.1 7.1﹣7.3 7.5﹣8.0
课堂练习
3.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性 B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨 D.酸溶液的pH越小酸性越强
4.下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A. 用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B. 先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C. 用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D. 用pH试纸测得该氢氧化钠溶液的pH=12.6
C
C
课堂小结
溶液酸碱度与pH的关系
溶液酸碱度表示
了解溶液的酸碱度在实际生活中有重要的意义
pH<7 溶液呈酸性
pH>7 溶液呈碱性
pH=7 溶液呈中性
测定pH最简便的方法
使用pH试纸
布置作业
完成配套课后练习。
10.2 酸和碱的中和反应(第2课时)
日常生活中,在我们吃食醋、橘子、葡萄等水果时,会感到它们酸的程度是不一样的,那么,如何表示物质酸性的强弱呢
学习目标
1. 会用PH试纸测定溶液的酸碱度,了解溶液的酸碱度在实际中的意义。
2. 会用分析、归纳的方法对有关信息加工处理。
溶液的酸碱性与酸碱度
溶液的酸碱性: 指的是溶液呈酸性、碱性还是中性,常用酸碱指 示剂测定;
酸性溶液:
能使紫色石蕊试液变红
碱性溶液:
能使紫色石蕊试液变蓝,使无色酚酞试液变红
中性溶液:
不能使石蕊及酚酞试液变色
溶液的酸碱度是表示酸碱性的强弱程度。
稀溶液的酸碱度可用pH表示,用pH试纸测定。
pH试纸
溶液酸碱度的表示法—pH
溶液的酸碱度常用pH表示, pH的范围通常在0~14之间。
酸性溶液pH < 7
碱性溶液pH > 7
中性溶液pH = 7
pH越小,酸性越强
pH越大,碱性越强
(如NaCl溶液、Na2SO4溶液的pH=7)
①pH表示溶液酸碱性的强弱程度,但不确定是酸的溶液或碱的溶液。
②注意酸(碱)、酸性(碱性)和酸碱度的区别和联系。
③pH是溶液中所含H+的浓度或OH-浓度大小的一种表示方法,溶液中H+浓度越大,酸性越强,pH越小;OH-的浓度越大,则碱性越强,pH越大;当溶液中H+和OH-浓度相等时,则溶液的pH=7,呈中性。
④碱性溶液中一定含OH-,但不一定是碱的溶液;酸性溶液中一定含H+,但不一定是酸的溶液。
注意:
1. pH的测定——用pH试纸测定(最简便的方法)
测定方法:在白瓷板或玻璃片上放一小片pH 试纸,用干净的玻璃棒蘸取被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出被测液的pH 。
【注意事项】
1. 不能把pH试纸放到待测溶液中测pH,以免带入杂质,污染试剂;
2. pH试纸不能用蒸馏水润湿后再测定,否则测定的是稀释后的溶液酸碱度,导致测定结果不准确;
3. 读数只能整数;
4. 检验气体酸性碱性润湿再用。
原溶液为酸性,会使pH变大;
原溶液为碱性,会使pH变小;
原溶液为中性,对pH无影响;
更精确的pH测试仪器——pH计
用pH试纸测定一些液体的酸碱性
酸溶液的pH<7,碱溶液的pH>7。即:酸溶液显酸性,碱溶液显碱性。
1. 酸溶液都是酸性溶液,但酸性溶液不一定是酸溶液,例如NH4NO3溶液是酸性溶液,但不是酸溶液, NH4NO3是一种盐。
总之,酸性溶液包含酸溶液。
2. 碱溶液都是碱性溶液,但碱性溶液不一定是碱溶液,例如Na2CO3溶液是碱性溶液,但不是碱溶液, Na2CO3是一种盐。
总之,碱性溶液包含碱溶液。
酸溶液
酸性溶液
碱溶液
碱性溶液
溶液的浓度与pH的关系
浓度越小,酸性越弱,pH越大;
浓度越小,碱性越弱,pH越小;
浓度越大,酸性越强,pH越小。
浓度越大,碱性越强,pH越大。
问:NaCl 的水溶液呢?浓度对pH有什么影响?
氯化钠溶液是中性的, pH =7,所以不管溶液的浓度高低,溶液的pH都是7,因此无影响。
酸溶液
碱溶液
测定生活中一些物质的pH,说明它们的酸碱性。
实验10-10
身边一些物质的pH
测生活中一些物质的PH
(1)化工生产中许多反应必须在一定的pH溶液里才能进行;
(2)农业生产中农作物一般适宜在pH为7或者接近7的土壤中生长;
了解溶液酸碱性的意义
西瓜6.0~7.0
苹果树6.0~8.0
小麦6.0~7.0
3. 测定人体内或排出的液体的pH,可以了解人体的健康状况。
人体中几种重要体液的正常pH范围
体液 血液 唾液 胃液 乳汁 尿液
pH 7.35-7.45 6.6-7.1 0.9-1.5 6.6-7.6 4.7-8.4
人的体液的pH必须维持在一定范围内,如果超越正常范围,会导致生理功能失调或发生疾病,甚至出现酸中毒或碱中毒。
4. 测定雨水的pH,可以了解空气的污染情况
雨水一般呈弱酸性(由于空气中的二氧化碳溶解在雨水中),人们一般把pH小于5.6 的雨水称为酸雨。
酸雨的危害
洗发剂和护发剂酸碱性
溶液酸碱度对头发的影响
讨论:溶液的酸碱度对头发有什么影响?对你选择洗发液有什么启示?
答:碱性物质对头发有损坏作用。所以洗发液应选
pH=1 pH=4 pH=7 pH=10 pH=13
观察头发光泽
拉断的难易程度
接近中性的,不要选碱性大的洗发液。然后再用微酸性的护发素来保护头发。
光泽好
较好
正常
不好
很不好
难
较难
易
很易
正常
课堂练习
1.下列溶液显碱性的是( )
A.酸雨 B.食醋 C.NaOH溶液 D.盐酸
2.人体内一些液体的正常pH范围如下,下列说法中不正确的是( )
A.胆汁和胰液显碱性
B.胃液比唾液酸性弱
C.胰液比胆汁碱性强
D.服用含氢氧化铝[Al(OH3)]的药物可以治疗胃酸过多症
C
B
液体 胃液 唾液 胆汁 胰液
pH 0.9﹣1.5 6.6﹣7.1 7.1﹣7.3 7.5﹣8.0
课堂练习
3.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性 B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨 D.酸溶液的pH越小酸性越强
4.下列有关测定氢氧化钠溶液pH的实验操作或描述,你认为正确的是( )
A. 用镊子夹取pH试纸直接伸入氢氧化钠溶液中测量
B. 先用蒸馏水将pH试纸润湿,再用滴管吸取氢氧化钠溶液滴到pH试纸上测量
C. 用洁净干燥的玻璃棒蘸取氢氧化钠溶液滴到pH试纸上,再与标准比色卡对照
D. 用pH试纸测得该氢氧化钠溶液的pH=12.6
C
C
课堂小结
溶液酸碱度与pH的关系
溶液酸碱度表示
了解溶液的酸碱度在实际生活中有重要的意义
pH<7 溶液呈酸性
pH>7 溶液呈碱性
pH=7 溶液呈中性
测定pH最简便的方法
使用pH试纸
布置作业
完成配套课后练习。
同课章节目录
