人教版九下10.1 常见的酸和碱(第3课时) 作业(含解析)
文档属性
| 名称 | 人教版九下10.1 常见的酸和碱(第3课时) 作业(含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 187.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-03 00:00:00 | ||
图片预览



文档简介
10.1 常见的酸和碱(第3课时)
一、选择题
1.【2021湖南邵阳】下列关于氢氧化钠的描述中错误的是( )
A.对皮肤有强烈的腐蚀作用 B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂 D.易溶于水,溶解时放出热量
2.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( )
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
3.下列物质间能够发生反应,但没有出现明显现象的是( )
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
4.某同学总结的Ca(OH)2的化学性质如图。下列说法错误的是( )
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.NaOH可用于造纸和印染工业,NaOH属于( )
A.单质 B.酸 C.碱 D.盐
6.碱石灰是用氢氧化钠和生石灰按一定比例混合而成的,在实验室中常用于干燥气体。下列气体不能用碱石灰干燥的是( )
A.H2 B.O2 C.CO D.CO2
7.若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
8.物质的性质决定它的用途还决定了它的保存方法。固体氢氧化钠具有以下性质:①白色片状固体②有强腐蚀性③易吸收水分而潮解④易溶于水,且溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
二、综合题
9. 实验室有一瓶敞口放置的氢氧化钠固体样品,为探究样品中的成分,小科进行如下实验:
(1)操作①是加水充分溶解,操作②的名称是 。
(2)沉淀B的化学式是 。
(3)小科根据实验现象认为样品中一定含有氢氧化钠,请你评价小科的判断是否正确,并说明理由 。
10.某化学兴趣小组开展的氢氧化钠性质系列探究活动如下图所示。
回答下列问题:
(1)实验①观察到氢氧化钠表面变______。
(2)实验②观察到紫色石蕊溶液变成______色,实验③观察到无色酚酞溶液变成____色。
(3)实验④: I.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有 (填化学式)。
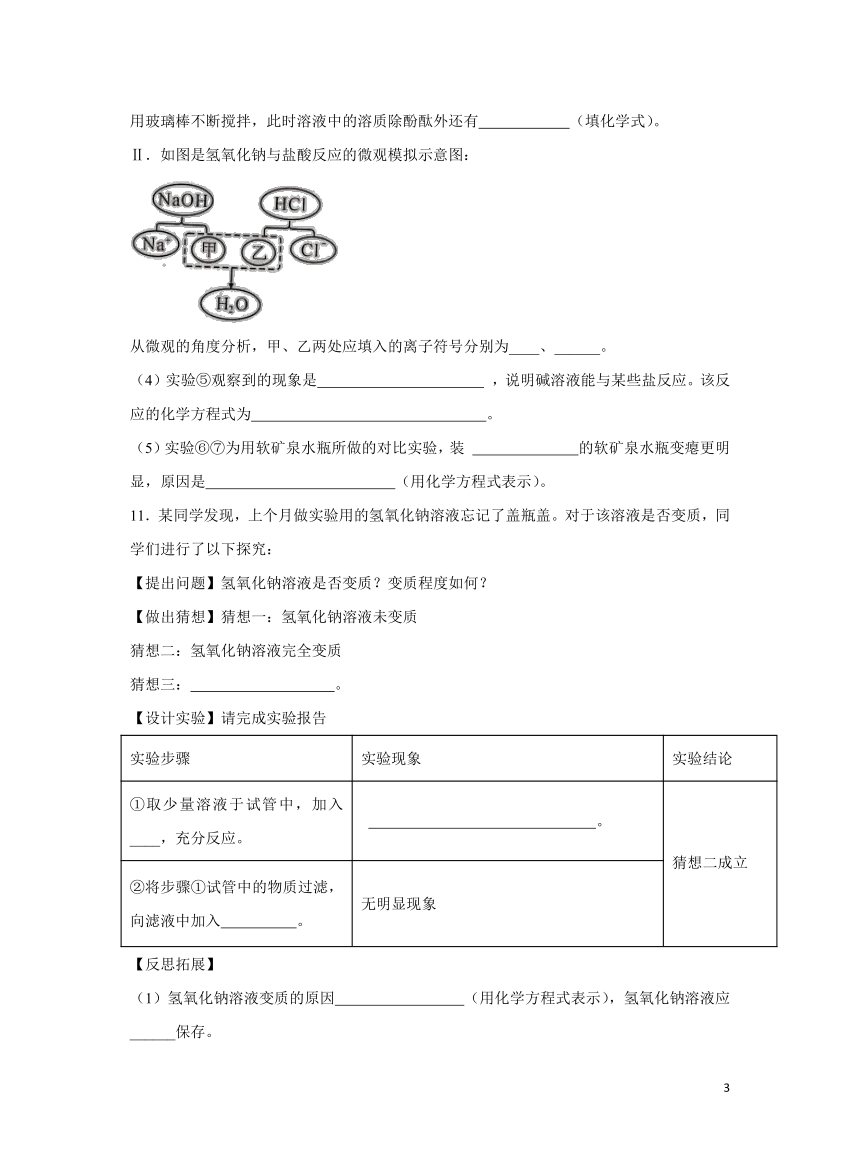
Ⅱ.如图是氢氧化钠与盐酸反应的微观模拟示意图:
从微观的角度分析,甲、乙两处应填入的离子符号分别为____、______。
(4)实验⑤观察到的现象是 ,说明碱溶液能与某些盐反应。该反应的化学方程式为 。
(5)实验⑥⑦为用软矿泉水瓶所做的对比实验,装 的软矿泉水瓶变瘪更明显,原因是 (用化学方程式表示)。
11.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们进行了以下探究:
【提出问题】氢氧化钠溶液是否变质?变质程度如何?
【做出猜想】猜想一:氢氧化钠溶液未变质
猜想二:氢氧化钠溶液完全变质
猜想三: 。
【设计实验】请完成实验报告
实验步骤 实验现象 实验结论
①取少量溶液于试管中,加入____,充分反应。 。 猜想二成立
②将步骤①试管中的物质过滤,向滤液中加入 。 无明显现象
【反思拓展】
(1)氢氧化钠溶液变质的原因 (用化学方程式表示),氢氧化钠溶液应______保存。
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有 。
参考答案与解析
一、选择题
1.【答案】B
【解析】解:A.氢氧化钠具有强烈的腐蚀性,对皮肤有强烈的腐蚀作用,故选项说法正确;
B.氢氧化钠的水溶液显碱性,其水溶液能使石蕊溶液变蓝,故选项说法错误;
C.氢氧化钠能与油脂反应,能去除油污,可作炉具清洁剂,故选项说法正确;
D.氢氧化钠易溶于水,溶解时放出热量,故选项说法正确。
2.【答案】C
【解析】A.HCl与氢氧化钠溶液、氢氧化钙溶液均能发生中和反应,分别生成氯化钠和水、氯化钙和水,但均无明显变化,不能鉴别,故选项错误;
B.KNO3与氢氧化钠溶液、氢氧化钙溶液均不反应,不能鉴别,故选项错误;
C.Na2CO3与氢氧化钙溶液反应生成碳酸钙白色沉淀,与氢氧化钠溶液不反应,可以鉴别,故选项正确;
D.氯化铁与氢氧化钠溶液、氢氧化钙溶液均能发生反应,均生成氢氧化铁沉淀,不能鉴别,故选项错误。
3.【答案】B
【解析】A.将稀盐酸滴入盛石灰石的试管中,有气泡产生,有明显的现象,不符合题意;
B.将CO2通入NaOH溶液中生成碳酸钠和水,没有明显的现象,符合题意;
C.将碳酸钠溶液滴入澄清石灰水中生成碳酸钙,石灰水变浑浊,有明显的现象,不符合题意;
D.将稀硫酸滴入NaCl溶液中不能发生反应,不符合题意。
4.【答案】A
【解析】A.甲不一定是碳酸盐,也可能是硫酸铜等盐,氢氧化钙能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故选项说法错误;
B.反应②是酸和碱的反应,属于中和反应,为放热反应,故选项说法正确;
C.反应③是非金属氧化物与氢氧化钙反应生成盐和水,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,反应③可用于检验某种温室气体,故选项说法正确;
D.澄清石灰水显碱性,向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色,故选项说法正确。
5.【答案】C
【解析】NaOH是由金属阳离子和氢氧根离子构成的,属于碱。
6.【答案】D
【解析】二氧化碳能与氢氧化钠反应生成碳酸钠,不可以用碱石灰干燥。故选D。
7.【答案】C
【解析】A.氢氧化镁能与稀盐酸反应生成氯化镁和水,氢氧化镁与碳酸钠不反应,可以根据是否溶解,鉴别稀盐酸和Na2CO3溶液,不符合题意;
B.氢氧化钠溶于水放出大量的热,氯化钠溶于水温度变化不大,可以根据温度是否明显升高,鉴别氢氧化钠固体和氯化钠固体,不符合题意;
C.氢氧化钡能与氯化镁反应生成氢氧化镁和氯化钡,氢氧化钡能与硫酸钠反应生成硫酸钡和氢氧化钠,均有白色沉淀产生,无法根据是否产生沉淀,鉴别MgCl2溶液和Na2SO4溶液,符合题意;
D.熟石灰能与硫酸铵反应生成氨气,熟石灰与硫酸钾不反应,故根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体,不符合题意。故选C。
8.【答案】D
【解析】氢氧化钠固体易吸收水分而潮解,也能与空气中的二氧化碳反应,这些性质决定了氢氧化钠固体必须密封保存。
二、综合题
9.【答案】(1)过滤;(2)CaCO3;(3)不正确,是因为碳酸钠和氢氧化钙反应生成了氢氧化钠,与氯化铁反应的氢氧化钠也可能全部是碳酸钠和氢氧化钙反应生成的氢氧化钠。
【解析】解:(1)操作①是加水充分溶解,操作②的名称是过滤。
(2)沉淀B是碳酸钠和氢氧化钙反应生成的碳酸钙,碳酸钙的化学式是CaCO3。
(3)小科的判断不正确,是因为碳酸钠和氢氧化钙反应生成了氢氧化钠,与氯化铁反应的氢氧化钠也可能全部是碳酸钠和氢氧化钙反应生成的氢氧化钠。
10. 【答案】(1)潮湿;(2)蓝;红; (3)无;NaCl、HCl ;OH-;H+;(4)产生蓝色沉淀;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;(5)氢氧化钠溶液;2NaOH + CO2= Na2CO3+ H2O
【解析】
(1)氢氧化钠在空气中易吸收水蒸气而潮解,实验①观察到氢氧化钠表面变潮湿。
(2)氢氧化钠溶液呈碱性,能使紫色的石蕊溶液变蓝色,无色的酚酞变红色。实验②观察到紫色石蕊溶液变成蓝色,实验③观察到无色酚酞溶液变成红色。由此得出:碱溶液能使指示剂变色。
(3)I.氢氧化钠与盐酸反应生成氯化钠和水,氯化钠溶液呈中性,酚酞遇中性溶液呈无色。当滴加稀盐酸至溶液呈中性时,溶液显无色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有氯化钠和氯化氢,化学式分别为:NaCl、HCl;
Ⅱ.氢氧化钠与盐酸的实质是氢氧化钠中氢氧根离子与盐酸中的氢离子结合生成水,从微观的角度分析,甲、乙两处应填入的离子符号分别为OH-、H+;
(4)氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠。实验⑤观察到的现象是产生蓝色沉淀,说明碱溶液能与某些盐反应。该反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(5)氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钠溶液能吸收二氧化碳气体,使软矿泉水瓶中的气压降低。实验⑥⑦为用软矿泉水瓶所做的对比实验,装氢氧化钠溶液的软矿泉水瓶变瘪更明显,原因是2NaOH + CO2= Na2CO3+ H2O。
11.【答案】(1)氢氧化钠溶液部分变质;(2)加入足量(或过量)的氯化钙溶液(或可溶性钙盐、钡盐溶液)(合理即可); (3)产生白色沉淀(或产生白色浑浊);(4)酚酞溶液(或可溶性铜盐、铁盐、镁盐溶液、石蕊溶液)(合理即可);
(5);(6)密封;(7)氯化钠氯化钙(或NaCl、CaC12)
【解析】氢氧化钠露置在空气的情况是未变质、部分变质或全部变质,故填:氢氧化钠溶液部分变质;
①猜想二时氢氧化钠溶液完全变质,即氢氧化钠与二氧化碳完全反应生成碳酸钠。因此向溶液的样品中滴加氯化钙溶液,利用氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,若观察到有白色沉淀出现可判断氢氧化钠溶液变质生成了碳酸钠;
②在反应后的溶液中滴入酚酞,由于氢氧化钠能使酚酞变红,而溶液无明显现象;因此说明溶液中不含氢氧化钠,因此氢氧化钠完全变质。
反思拓展:
(1)因为氢氧化钠吸收二氧化碳生成碳酸钠和水而变质,故反应的方程式为:,氢氧化钠溶液可以与空气中的二氧化碳气体反应变质,因此需要密封保存。
(2)两份完全变质的氢氧化钠溶液样品即碳酸钠溶液于试管中,向其中一份加入盐酸有气泡产生,同时生成氯化钠,另一份加入氢氧化钙溶液有碳酸钙白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,说明白色沉淀的碳酸钙与剩余的盐酸反应生成了氯化钙,因此所得溶液中溶质一定有氯化钠、氯化钙。
1
一、选择题
1.【2021湖南邵阳】下列关于氢氧化钠的描述中错误的是( )
A.对皮肤有强烈的腐蚀作用 B.其水溶液能使石蕊溶液变红
C.能去除油污,可作炉具清洁剂 D.易溶于水,溶解时放出热量
2.能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( )
A.HCl B.KNO3 C.Na2CO3 D.FeCl3
3.下列物质间能够发生反应,但没有出现明显现象的是( )
A.将稀盐酸滴入盛石灰石的试管中
B.将CO2通入NaOH溶液中
C.将碳酸钠溶液滴入澄清石灰水中
D.将稀硫酸滴入NaCl溶液中
4.某同学总结的Ca(OH)2的化学性质如图。下列说法错误的是( )
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
5.NaOH可用于造纸和印染工业,NaOH属于( )
A.单质 B.酸 C.碱 D.盐
6.碱石灰是用氢氧化钠和生石灰按一定比例混合而成的,在实验室中常用于干燥气体。下列气体不能用碱石灰干燥的是( )
A.H2 B.O2 C.CO D.CO2
7.若利用碱的性质进行下列实验,不能达到相应目的的是( )
A.分别加入少量Mg(OH)2固体,根据是否溶解,可鉴别稀盐酸和Na2CO3溶液
B.分别加入适量水溶解,根据温度是否明显升高,可鉴别NaOH固体和NaCl固体
C.分别加入Ba(OH)2溶液,根据是否产生沉淀,可鉴别MgCl2溶液和Na2SO4溶液
D.分别加入熟石灰粉末研磨,根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体
8.物质的性质决定它的用途还决定了它的保存方法。固体氢氧化钠具有以下性质:①白色片状固体②有强腐蚀性③易吸收水分而潮解④易溶于水,且溶解放热⑤能与空气中的二氧化碳反应。实验室中必须将它密封保存的主要原因是( )
A.①② B.①②③ C.②③④ D.③⑤
二、综合题
9. 实验室有一瓶敞口放置的氢氧化钠固体样品,为探究样品中的成分,小科进行如下实验:
(1)操作①是加水充分溶解,操作②的名称是 。
(2)沉淀B的化学式是 。
(3)小科根据实验现象认为样品中一定含有氢氧化钠,请你评价小科的判断是否正确,并说明理由 。
10.某化学兴趣小组开展的氢氧化钠性质系列探究活动如下图所示。
回答下列问题:
(1)实验①观察到氢氧化钠表面变______。
(2)实验②观察到紫色石蕊溶液变成______色,实验③观察到无色酚酞溶液变成____色。
(3)实验④: I.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有 (填化学式)。
Ⅱ.如图是氢氧化钠与盐酸反应的微观模拟示意图:
从微观的角度分析,甲、乙两处应填入的离子符号分别为____、______。
(4)实验⑤观察到的现象是 ,说明碱溶液能与某些盐反应。该反应的化学方程式为 。
(5)实验⑥⑦为用软矿泉水瓶所做的对比实验,装 的软矿泉水瓶变瘪更明显,原因是 (用化学方程式表示)。
11.某同学发现,上个月做实验用的氢氧化钠溶液忘记了盖瓶盖。对于该溶液是否变质,同学们进行了以下探究:
【提出问题】氢氧化钠溶液是否变质?变质程度如何?
【做出猜想】猜想一:氢氧化钠溶液未变质
猜想二:氢氧化钠溶液完全变质
猜想三: 。
【设计实验】请完成实验报告
实验步骤 实验现象 实验结论
①取少量溶液于试管中,加入____,充分反应。 。 猜想二成立
②将步骤①试管中的物质过滤,向滤液中加入 。 无明显现象
【反思拓展】
(1)氢氧化钠溶液变质的原因 (用化学方程式表示),氢氧化钠溶液应______保存。
(2)分别取两份完全变质的氢氧化钠溶液样品于试管中,向其中一份加入盐酸有气泡产生,另一份加入氢氧化钙溶液有白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,所得溶液中溶质一定有 。
参考答案与解析
一、选择题
1.【答案】B
【解析】解:A.氢氧化钠具有强烈的腐蚀性,对皮肤有强烈的腐蚀作用,故选项说法正确;
B.氢氧化钠的水溶液显碱性,其水溶液能使石蕊溶液变蓝,故选项说法错误;
C.氢氧化钠能与油脂反应,能去除油污,可作炉具清洁剂,故选项说法正确;
D.氢氧化钠易溶于水,溶解时放出热量,故选项说法正确。
2.【答案】C
【解析】A.HCl与氢氧化钠溶液、氢氧化钙溶液均能发生中和反应,分别生成氯化钠和水、氯化钙和水,但均无明显变化,不能鉴别,故选项错误;
B.KNO3与氢氧化钠溶液、氢氧化钙溶液均不反应,不能鉴别,故选项错误;
C.Na2CO3与氢氧化钙溶液反应生成碳酸钙白色沉淀,与氢氧化钠溶液不反应,可以鉴别,故选项正确;
D.氯化铁与氢氧化钠溶液、氢氧化钙溶液均能发生反应,均生成氢氧化铁沉淀,不能鉴别,故选项错误。
3.【答案】B
【解析】A.将稀盐酸滴入盛石灰石的试管中,有气泡产生,有明显的现象,不符合题意;
B.将CO2通入NaOH溶液中生成碳酸钠和水,没有明显的现象,符合题意;
C.将碳酸钠溶液滴入澄清石灰水中生成碳酸钙,石灰水变浑浊,有明显的现象,不符合题意;
D.将稀硫酸滴入NaCl溶液中不能发生反应,不符合题意。
4.【答案】A
【解析】A.甲不一定是碳酸盐,也可能是硫酸铜等盐,氢氧化钙能与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,故选项说法错误;
B.反应②是酸和碱的反应,属于中和反应,为放热反应,故选项说法正确;
C.反应③是非金属氧化物与氢氧化钙反应生成盐和水,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,反应③可用于检验某种温室气体,故选项说法正确;
D.澄清石灰水显碱性,向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色,故选项说法正确。
5.【答案】C
【解析】NaOH是由金属阳离子和氢氧根离子构成的,属于碱。
6.【答案】D
【解析】二氧化碳能与氢氧化钠反应生成碳酸钠,不可以用碱石灰干燥。故选D。
7.【答案】C
【解析】A.氢氧化镁能与稀盐酸反应生成氯化镁和水,氢氧化镁与碳酸钠不反应,可以根据是否溶解,鉴别稀盐酸和Na2CO3溶液,不符合题意;
B.氢氧化钠溶于水放出大量的热,氯化钠溶于水温度变化不大,可以根据温度是否明显升高,鉴别氢氧化钠固体和氯化钠固体,不符合题意;
C.氢氧化钡能与氯化镁反应生成氢氧化镁和氯化钡,氢氧化钡能与硫酸钠反应生成硫酸钡和氢氧化钠,均有白色沉淀产生,无法根据是否产生沉淀,鉴别MgCl2溶液和Na2SO4溶液,符合题意;
D.熟石灰能与硫酸铵反应生成氨气,熟石灰与硫酸钾不反应,故根据是否产生氨味,可鉴别(NH4)2SO4固体和K2SO4固体,不符合题意。故选C。
8.【答案】D
【解析】氢氧化钠固体易吸收水分而潮解,也能与空气中的二氧化碳反应,这些性质决定了氢氧化钠固体必须密封保存。
二、综合题
9.【答案】(1)过滤;(2)CaCO3;(3)不正确,是因为碳酸钠和氢氧化钙反应生成了氢氧化钠,与氯化铁反应的氢氧化钠也可能全部是碳酸钠和氢氧化钙反应生成的氢氧化钠。
【解析】解:(1)操作①是加水充分溶解,操作②的名称是过滤。
(2)沉淀B是碳酸钠和氢氧化钙反应生成的碳酸钙,碳酸钙的化学式是CaCO3。
(3)小科的判断不正确,是因为碳酸钠和氢氧化钙反应生成了氢氧化钠,与氯化铁反应的氢氧化钠也可能全部是碳酸钠和氢氧化钙反应生成的氢氧化钠。
10. 【答案】(1)潮湿;(2)蓝;红; (3)无;NaCl、HCl ;OH-;H+;(4)产生蓝色沉淀;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;(5)氢氧化钠溶液;2NaOH + CO2= Na2CO3+ H2O
【解析】
(1)氢氧化钠在空气中易吸收水蒸气而潮解,实验①观察到氢氧化钠表面变潮湿。
(2)氢氧化钠溶液呈碱性,能使紫色的石蕊溶液变蓝色,无色的酚酞变红色。实验②观察到紫色石蕊溶液变成蓝色,实验③观察到无色酚酞溶液变成红色。由此得出:碱溶液能使指示剂变色。
(3)I.氢氧化钠与盐酸反应生成氯化钠和水,氯化钠溶液呈中性,酚酞遇中性溶液呈无色。当滴加稀盐酸至溶液呈中性时,溶液显无色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有氯化钠和氯化氢,化学式分别为:NaCl、HCl;
Ⅱ.氢氧化钠与盐酸的实质是氢氧化钠中氢氧根离子与盐酸中的氢离子结合生成水,从微观的角度分析,甲、乙两处应填入的离子符号分别为OH-、H+;
(4)氢氧化钠与硫酸铜反应生成氢氧化铜和硫酸钠。实验⑤观察到的现象是产生蓝色沉淀,说明碱溶液能与某些盐反应。该反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(5)氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钠溶液能吸收二氧化碳气体,使软矿泉水瓶中的气压降低。实验⑥⑦为用软矿泉水瓶所做的对比实验,装氢氧化钠溶液的软矿泉水瓶变瘪更明显,原因是2NaOH + CO2= Na2CO3+ H2O。
11.【答案】(1)氢氧化钠溶液部分变质;(2)加入足量(或过量)的氯化钙溶液(或可溶性钙盐、钡盐溶液)(合理即可); (3)产生白色沉淀(或产生白色浑浊);(4)酚酞溶液(或可溶性铜盐、铁盐、镁盐溶液、石蕊溶液)(合理即可);
(5);(6)密封;(7)氯化钠氯化钙(或NaCl、CaC12)
【解析】氢氧化钠露置在空气的情况是未变质、部分变质或全部变质,故填:氢氧化钠溶液部分变质;
①猜想二时氢氧化钠溶液完全变质,即氢氧化钠与二氧化碳完全反应生成碳酸钠。因此向溶液的样品中滴加氯化钙溶液,利用氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,若观察到有白色沉淀出现可判断氢氧化钠溶液变质生成了碳酸钠;
②在反应后的溶液中滴入酚酞,由于氢氧化钠能使酚酞变红,而溶液无明显现象;因此说明溶液中不含氢氧化钠,因此氢氧化钠完全变质。
反思拓展:
(1)因为氢氧化钠吸收二氧化碳生成碳酸钠和水而变质,故反应的方程式为:,氢氧化钠溶液可以与空气中的二氧化碳气体反应变质,因此需要密封保存。
(2)两份完全变质的氢氧化钠溶液样品即碳酸钠溶液于试管中,向其中一份加入盐酸有气泡产生,同时生成氯化钠,另一份加入氢氧化钙溶液有碳酸钙白色沉淀产生,然后将两支试管中所有物质一起倒入废液缸中,得到无色澄清溶液,说明白色沉淀的碳酸钙与剩余的盐酸反应生成了氯化钙,因此所得溶液中溶质一定有氯化钠、氯化钙。
1
同课章节目录
