人教版九下10.2 酸和碱的中和反应(第1课时) 作业(含答案)
文档属性
| 名称 | 人教版九下10.2 酸和碱的中和反应(第1课时) 作业(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 193.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-03 00:00:00 | ||
图片预览


文档简介
10.2 酸和碱的中和反应(第1课时)
一、选择题
1.下列生活经验没有应用酸碱中和反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
2.下列有关中和反应的说法,不正确的是( )
A.中和反应一定是酸和碱的反应
B.凡是生成盐和水的化学反应都是中和反应
C.中和反应的实质是H+和OH-结合生成水
D.中和反应一定生成盐和水
3.能与稀盐酸发生中和反应的是( )
A.铁锈 B.石灰石 C.石灰水 D.锌粒
4.下列做法利用了中和反应原理的是( )
A.用食醋腌木瓜放入食盐进行调味
B.用稀盐酸除去铁钉上的铁锈
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松
D.被蚊虫叮咬后,涂含碱性物质的药水减轻痛痒
5.下列反应中属于中和反应的是( )
A.Na2CO3+2HCl=2NaCl+H2O+CO2↑ B.2NaOH+H2SO4=Na2SO4+2H2O
C.SO2+2NaOH=Na2SO3+H2O D.Zn+CuSO4=ZnSO4+Cu
二、综合题
6.(2021·河南)氢氧化钠溶液与盐酸反应的化学方程式为_______________。下图是该反应的微观示意图,则该反应前后没有发生变化的离子有______;从微观角度看,该化学反应的实质是_______。
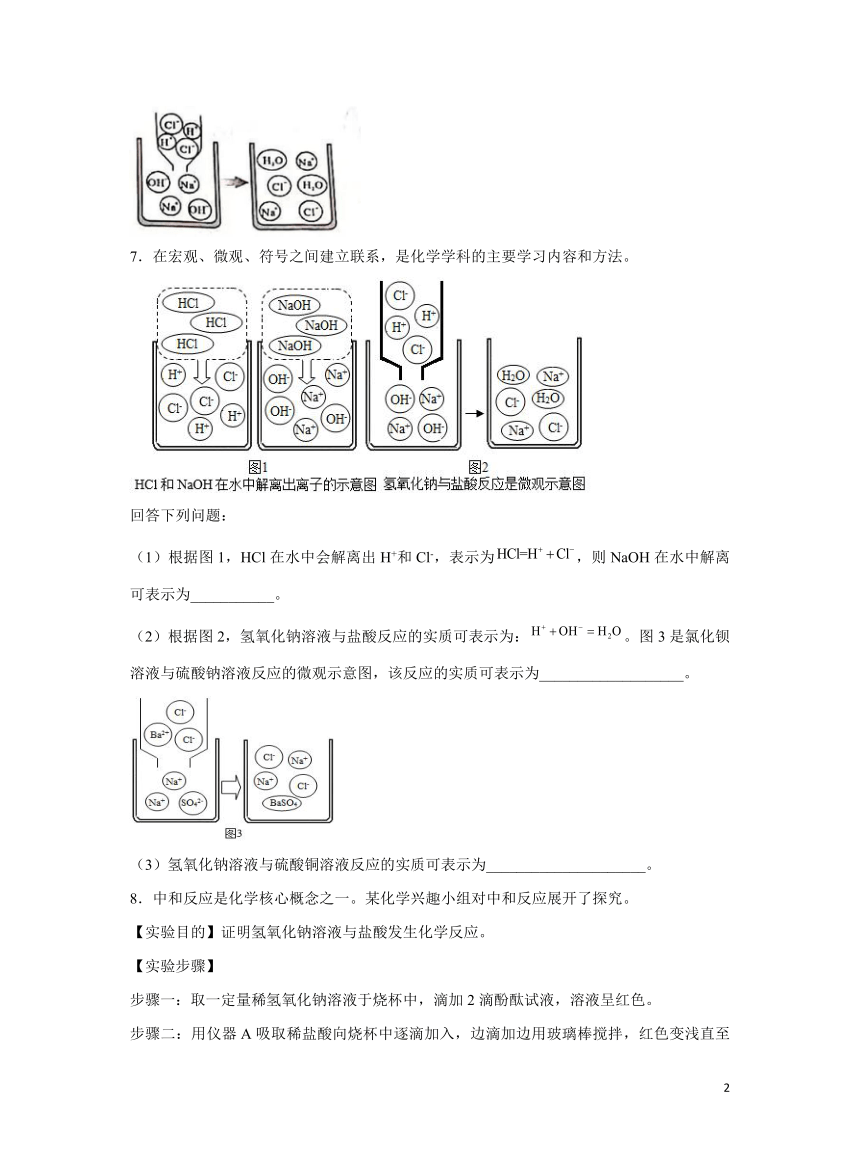
7.在宏观、微观、符号之间建立联系,是化学学科的主要学习内容和方法。
回答下列问题:
(1)根据图1,HCl在水中会解离出H+和Cl-,表示为,则NaOH在水中解离可表示为___________。
(2)根据图2,氢氧化钠溶液与盐酸反应的实质可表示为:。图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质可表示为___________________。
(3)氢氧化钠溶液与硫酸铜溶液反应的实质可表示为_____________________。
8.中和反应是化学核心概念之一。某化学兴趣小组对中和反应展开了探究。
【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞试液,溶液呈红色。
步骤二:用仪器A吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至失。
步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。
【思考拓展】
(1)从下列仪器中选择步骤二中的“仪器A”,名称是_________。
(2)兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。
查阅资料:(i)酚酞试液在不同的pH时变化情况如下:
pH 0~8.2 8.2~10.0 10.0~14.0
颜色 无色 粉红色 红色
(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。
兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加CuSO4溶液,振荡,静置 ①无___色沉淀生成 白色固体不是NaOH。
向另一份滴加AgNO3溶液,振荡,静置 出现白色沉淀 ②白色固体是NaCl,反应的化学方程式为 。
【继续探究】
(4)如图是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是 。
(5)兴趣小组认为上述实验对反应实质缺少直观的验证。
査阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。
兴趣小组据此设计了如图实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。
①U型管内液面左低右高说明该反应 热量(填写“放出”或“吸收”)。
②无水醋酸由CH3COO-和H+构成。变色硅胶由蓝色变成红色的原因是 (用化学方程式表示)。
参考答案与解析
1.【答案】D
【解析】A.用熟石灰改良酸性土壤,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误;
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸,该反应的反应物是酸和碱,属于中和反应,应用了酸碱反应原理,故选项错误;
C.用氢氧化铝治疗胃酸过多,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误;
D.用生石灰作干燥剂,该反应的反应物是金属氧化物和水,不是酸与碱的反应,不属于中和反应,没有应用酸碱反应原理,故选项正确。
2.【答案】B
【解析】A.中和反应是酸与碱作用生成盐和水的反应,中和反应一定是酸和碱的反应,故选项说法正确。
B.凡是生成盐和水的化学反应不一定都是中和反应,如CO2+2NaOH=Na2CO3+H2O,故选项说法错误。
C.中和反应是酸与碱作用生成盐和水的反应,反应的实质是H+和OH-结合生成水,故选项说法正确。
D.中和反应是酸与碱作用生成盐和水的反应,中和反应一定生成盐和水,故选项说法正确。3.【答案】C
4.【答案】D
【解析】A.用食醋腌木瓜放入食盐进行调味,没有发生酸与碱生成盐和水的反应,没有运用中和反应原理,故选项错误;
B.铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,是利用了酸能与金属氧化物反应生成盐和水,没有运用中和反应原理,故选项错误;
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松,主要是利用了碳酸氢钠受热生成碳酸钠.水和二氧化碳,没有运用中和反应原理,故选项错误;
D.人被蚊虫叮咬后,会在人的皮肤分泌出蚁酸,如果涂一些含碱性物质的溶液,可减轻痛痒,是利用了蚁酸能与碱性物质发生中和反应,故选项正确。
故选D。
5.【答案】B
【解析】A.碳酸钠是盐不是碱,盐酸是酸,虽然会反应,但不是酸和碱的反应,故A错误;
B.氢氧化钠是碱,硫酸是酸,两者反应生成了盐硫酸钠和水,符合定义,故B正确;
C.二氧化硫是酸性氧化物,不是酸,氢氧化钠是碱,虽然生成了盐和水,但不符合定义,故C错误;
D.锌属于金属单质,硫酸铜属于盐,反应物不符合中和反应的定义,故D错误。
二、综合题
6.【答案】HCl+NaOH=NaCl+H2O Na +、Cl- H ++OH-= H2O(或 H+与 OH-反应生成 H2O)
7.【答案】(1)NaOH= Na++OH-;(2);(3)
【解析】(1)分析图1知道,HCl在水中会解离出H+和Cl-,表示为,NaOH在水中会解离出Na+和OH-,则NaOH在水中解离可表示为NaOH= Na++OH-;
(2)根据图2,氢氧化钠溶液与盐酸反应的实质可表示为:,Cl-和Na+是旁观者,并没有参加反应;所以分析图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质是Ba2+和SO42-反应,结合生成BaSO4沉淀,而Cl-和Na+则是旁观者,并没有参加反应,可表示为;
(3)NaOH在水中会解离出Na+和OH-,硫酸铜在水中会解离出Cu2+和SO42-,反应的实质可表示OH-和Cu2+反应,结合生成Cu(OH)2沉淀,而SO42-和Na+则是旁观者,并没有参加反应,可表示为。
8.【答案】 (1)胶头滴管;(2)用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响;(3)蓝;NaCl+AgNO3=AgCl↓+NaNO3;(4)H+和OH-结合生成H2O;
(5)放出;CH3COOH+NaOH=CH3COONa+H2O
【解析】(1)步骤二中,用仪器A吸取稀盐酸向烧杯中逐滴加入,所以A是胶头滴管。
(2)稀盐酸中含有水,水对实验有影响,根据控制变量法设计实验,该对比实验方案是用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响。
(3)①氢氧化钠与硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠,因此无蓝色沉淀可说明白色固体不是NaOH;
②根据题意氯化钠与硝酸银反应生成氯化银和硝酸钠,反应的化学方程式为 。
(4)氢氧化钠溶液是碱,盐酸溶液是酸,氢氧化钠和盐酸反应就是酸碱中和的实质即H+和OH-结合生成H2O。
(5)①反应放热使得空气膨胀,从而使该反应U型管内液面左低右高,因此是放出热量;
②变色硅胶遇水由蓝色变成红色是因为醋酸和氢氧化钠反应生成醋酸钠和水,无水醋酸由CH3COO-和H+构成与碱发生中和反应方程式为。
1
一、选择题
1.下列生活经验没有应用酸碱中和反应原理的是( )
A.用熟石灰改良酸性土壤
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸
C.用氢氧化铝治疗胃酸过多
D.用生石灰作干燥剂
2.下列有关中和反应的说法,不正确的是( )
A.中和反应一定是酸和碱的反应
B.凡是生成盐和水的化学反应都是中和反应
C.中和反应的实质是H+和OH-结合生成水
D.中和反应一定生成盐和水
3.能与稀盐酸发生中和反应的是( )
A.铁锈 B.石灰石 C.石灰水 D.锌粒
4.下列做法利用了中和反应原理的是( )
A.用食醋腌木瓜放入食盐进行调味
B.用稀盐酸除去铁钉上的铁锈
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松
D.被蚊虫叮咬后,涂含碱性物质的药水减轻痛痒
5.下列反应中属于中和反应的是( )
A.Na2CO3+2HCl=2NaCl+H2O+CO2↑ B.2NaOH+H2SO4=Na2SO4+2H2O
C.SO2+2NaOH=Na2SO3+H2O D.Zn+CuSO4=ZnSO4+Cu
二、综合题
6.(2021·河南)氢氧化钠溶液与盐酸反应的化学方程式为_______________。下图是该反应的微观示意图,则该反应前后没有发生变化的离子有______;从微观角度看,该化学反应的实质是_______。
7.在宏观、微观、符号之间建立联系,是化学学科的主要学习内容和方法。
回答下列问题:
(1)根据图1,HCl在水中会解离出H+和Cl-,表示为,则NaOH在水中解离可表示为___________。
(2)根据图2,氢氧化钠溶液与盐酸反应的实质可表示为:。图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质可表示为___________________。
(3)氢氧化钠溶液与硫酸铜溶液反应的实质可表示为_____________________。
8.中和反应是化学核心概念之一。某化学兴趣小组对中和反应展开了探究。
【实验目的】证明氢氧化钠溶液与盐酸发生化学反应。
【实验步骤】
步骤一:取一定量稀氢氧化钠溶液于烧杯中,滴加2滴酚酞试液,溶液呈红色。
步骤二:用仪器A吸取稀盐酸向烧杯中逐滴加入,边滴加边用玻璃棒搅拌,红色变浅直至失。
步骤三:向溶液中继续滴加稀盐酸至溶液呈酸性,用玻璃棒蘸取其中溶液,在酒精灯上加热至蒸干,有白色固体产生。
【思考拓展】
(1)从下列仪器中选择步骤二中的“仪器A”,名称是_________。
(2)兴趣小组认为仅从上述步骤二的现象,难以证明盐酸与氢氧化钠发生了反应。
查阅资料:(i)酚酞试液在不同的pH时变化情况如下:
pH 0~8.2 8.2~10.0 10.0~14.0
颜色 无色 粉红色 红色
(ⅱ)氢氧化钠溶液的pH随浓度的降低而减小。
兴趣小组据此形成了对比实验方案以排除干扰,该对比实验方案是
(3)为确认步骤三中的白色固体是氯化钠而不是氢氧化钠,进行如下实验:
步骤 现象 结论
将白色固体溶于水形成溶液,均分成两等份 向其中一份滴加CuSO4溶液,振荡,静置 ①无___色沉淀生成 白色固体不是NaOH。
向另一份滴加AgNO3溶液,振荡,静置 出现白色沉淀 ②白色固体是NaCl,反应的化学方程式为 。
【继续探究】
(4)如图是氢氧化钠与盐酸反应的微观示意图。从微观角度分析,氢氧化钠溶液和盐酸反应的实质是 。
(5)兴趣小组认为上述实验对反应实质缺少直观的验证。
査阅资料:(ⅲ)变色硅胶为蓝色,吸水后呈红色。(ⅳ)变色硅胶与NaOH固体充分混合,无明显现象;变色硅胶与无水醋酸(CH3COOH)充分混合,无明显现象。
兴趣小组据此设计了如图实验,验证中和反应有水生成:将无水醋酸迅速倒入装有NaOH固体和变色硅胶的试管中,并用玻璃棒在试管中不断搅拌,观察到变色硅胶由蓝色逐渐变为红色,U型管内液面左低右高。
①U型管内液面左低右高说明该反应 热量(填写“放出”或“吸收”)。
②无水醋酸由CH3COO-和H+构成。变色硅胶由蓝色变成红色的原因是 (用化学方程式表示)。
参考答案与解析
1.【答案】D
【解析】A.用熟石灰改良酸性土壤,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误;
B.用氢氧化钠溶液洗涤石油产品中的残留硫酸,该反应的反应物是酸和碱,属于中和反应,应用了酸碱反应原理,故选项错误;
C.用氢氧化铝治疗胃酸过多,该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,应用了酸碱反应原理,故选项错误;
D.用生石灰作干燥剂,该反应的反应物是金属氧化物和水,不是酸与碱的反应,不属于中和反应,没有应用酸碱反应原理,故选项正确。
2.【答案】B
【解析】A.中和反应是酸与碱作用生成盐和水的反应,中和反应一定是酸和碱的反应,故选项说法正确。
B.凡是生成盐和水的化学反应不一定都是中和反应,如CO2+2NaOH=Na2CO3+H2O,故选项说法错误。
C.中和反应是酸与碱作用生成盐和水的反应,反应的实质是H+和OH-结合生成水,故选项说法正确。
D.中和反应是酸与碱作用生成盐和水的反应,中和反应一定生成盐和水,故选项说法正确。3.【答案】C
4.【答案】D
【解析】A.用食醋腌木瓜放入食盐进行调味,没有发生酸与碱生成盐和水的反应,没有运用中和反应原理,故选项错误;
B.铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,是利用了酸能与金属氧化物反应生成盐和水,没有运用中和反应原理,故选项错误;
C.焙制蛋糕时加入碳酸氢钠使蛋糕膨松,主要是利用了碳酸氢钠受热生成碳酸钠.水和二氧化碳,没有运用中和反应原理,故选项错误;
D.人被蚊虫叮咬后,会在人的皮肤分泌出蚁酸,如果涂一些含碱性物质的溶液,可减轻痛痒,是利用了蚁酸能与碱性物质发生中和反应,故选项正确。
故选D。
5.【答案】B
【解析】A.碳酸钠是盐不是碱,盐酸是酸,虽然会反应,但不是酸和碱的反应,故A错误;
B.氢氧化钠是碱,硫酸是酸,两者反应生成了盐硫酸钠和水,符合定义,故B正确;
C.二氧化硫是酸性氧化物,不是酸,氢氧化钠是碱,虽然生成了盐和水,但不符合定义,故C错误;
D.锌属于金属单质,硫酸铜属于盐,反应物不符合中和反应的定义,故D错误。
二、综合题
6.【答案】HCl+NaOH=NaCl+H2O Na +、Cl- H ++OH-= H2O(或 H+与 OH-反应生成 H2O)
7.【答案】(1)NaOH= Na++OH-;(2);(3)
【解析】(1)分析图1知道,HCl在水中会解离出H+和Cl-,表示为,NaOH在水中会解离出Na+和OH-,则NaOH在水中解离可表示为NaOH= Na++OH-;
(2)根据图2,氢氧化钠溶液与盐酸反应的实质可表示为:,Cl-和Na+是旁观者,并没有参加反应;所以分析图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该反应的实质是Ba2+和SO42-反应,结合生成BaSO4沉淀,而Cl-和Na+则是旁观者,并没有参加反应,可表示为;
(3)NaOH在水中会解离出Na+和OH-,硫酸铜在水中会解离出Cu2+和SO42-,反应的实质可表示OH-和Cu2+反应,结合生成Cu(OH)2沉淀,而SO42-和Na+则是旁观者,并没有参加反应,可表示为。
8.【答案】 (1)胶头滴管;(2)用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响;(3)蓝;NaCl+AgNO3=AgCl↓+NaNO3;(4)H+和OH-结合生成H2O;
(5)放出;CH3COOH+NaOH=CH3COONa+H2O
【解析】(1)步骤二中,用仪器A吸取稀盐酸向烧杯中逐滴加入,所以A是胶头滴管。
(2)稀盐酸中含有水,水对实验有影响,根据控制变量法设计实验,该对比实验方案是用相同量的蒸馏水代替稀盐酸进行步骤二实验,如红色不消失,则可排除水的影响。
(3)①氢氧化钠与硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠,因此无蓝色沉淀可说明白色固体不是NaOH;
②根据题意氯化钠与硝酸银反应生成氯化银和硝酸钠,反应的化学方程式为 。
(4)氢氧化钠溶液是碱,盐酸溶液是酸,氢氧化钠和盐酸反应就是酸碱中和的实质即H+和OH-结合生成H2O。
(5)①反应放热使得空气膨胀,从而使该反应U型管内液面左低右高,因此是放出热量;
②变色硅胶遇水由蓝色变成红色是因为醋酸和氢氧化钠反应生成醋酸钠和水,无水醋酸由CH3COO-和H+构成与碱发生中和反应方程式为。
1
同课章节目录
