人教版九下8.3 金属资源的利用和保护(第2课时)作业(含解析)
文档属性
| 名称 | 人教版九下8.3 金属资源的利用和保护(第2课时)作业(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 61.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-03 00:00:00 | ||
图片预览


文档简介
8.3 金属资源的利用和保护(第2课时)
一、选择题
1.空气中含①N2 ②O2 ③稀有气体 ④水蒸气等成分,其中与钢铁生锈有关的是( )
A.①③ B.②④ C.③④ D.①④
2.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是( )
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
3.金属是一类重要的材料。下列有关金属的说法正确的是( )
A.不锈钢是绝对不会生锈的铁合金
B.武德合金的熔点比其成分金属高
C.日常生活中,钢铁表面刷油漆可以防止生锈
D.“曾青得铁则化为铜”的原理是用铜置换出铁
4.关于废旧金属回收的意义,下列叙述错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废弃金属对环境的污染
D.可以节约宝贵的金属资源
5.下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
6.除铁锈的试剂是( )
A.氯化钠溶液 B.稀盐酸 C.氢氧化钠溶液 D.水
7.将垃圾分类回收利用,既节约资源,又防止污染,符合可持续发展的要求。例如:破铁锅、坏车架、废弃易拉罐、旧电线和铝材下脚料等可归为一类回收,它们属于( )
A.金属材料 B.氧化物 C.单质 D.非金属
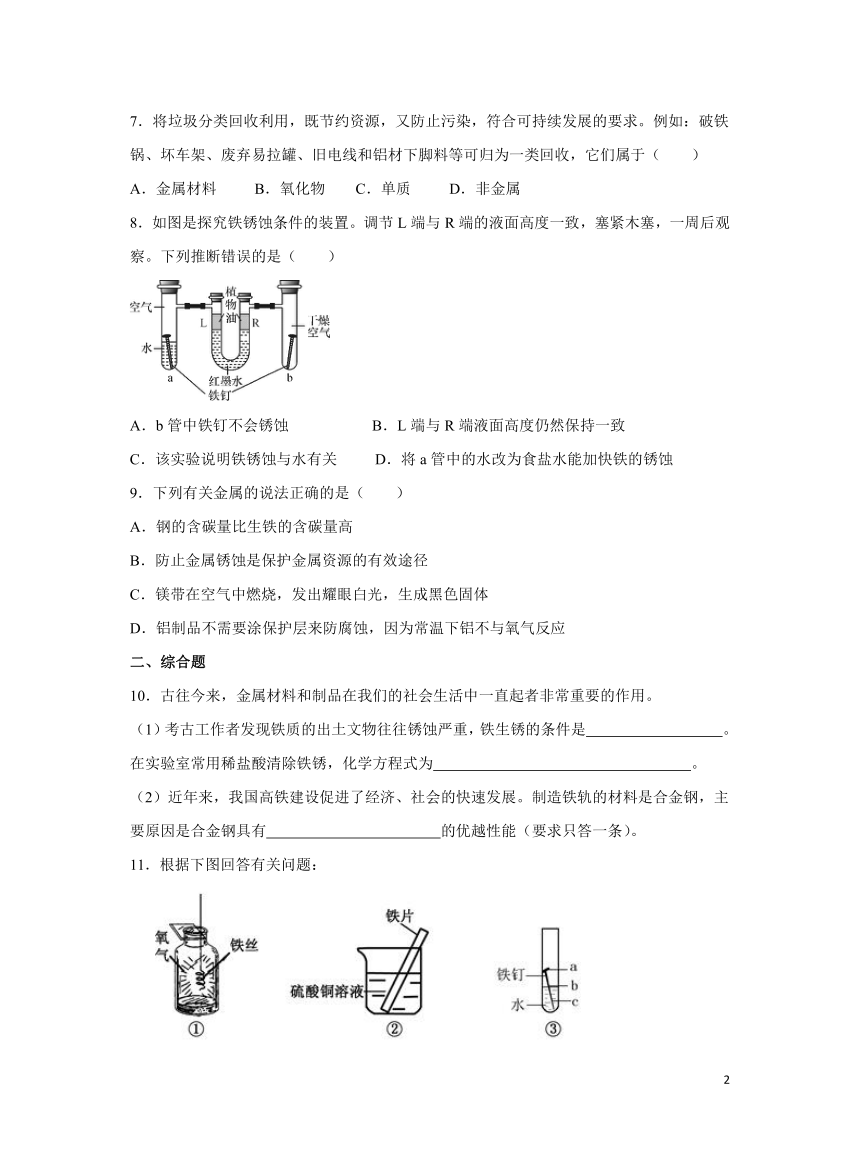
8.如图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断错误的是( )
A.b管中铁钉不会锈蚀 B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与水有关 D.将a管中的水改为食盐水能加快铁的锈蚀
9.下列有关金属的说法正确的是( )
A.钢的含碳量比生铁的含碳量高
B.防止金属锈蚀是保护金属资源的有效途径
C.镁带在空气中燃烧,发出耀眼白光,生成黑色固体
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
二、综合题
10.古往今来,金属材料和制品在我们的社会生活中一直起者非常重要的作用。
(1)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是 。在实验室常用稀盐酸清除铁锈,化学方程式为 。
(2)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,主要原因是合金钢具有 的优越性能(要求只答一条)。
11.根据下图回答有关问题:
(1)写出实验①中反应的化学方程式 。
(2)实验②中可观察到铁片的表面 ,说明铁的金属活动性比铜 。(填“强”或“弱”)
(3)实验③中可观察到试管中铁钉最先生锈的是 处。(填“a”或“b”或“c”)。
(4)你认为防止铁架台生锈的方法有 。(写一点)
12.金属防腐是科学研究中的重大课题。某校学习小组以铁的腐蚀为项目进行如下研究。
【认识铁的腐蚀】
(1)下列环境中的铁制品最容易生锈的是 (填字母序号)。
A.未擦干的铁锅 B.涂油漆的栏杆 C.盛水的不锈钢水杯
(2)铁锈的主要成分是Fe2O3 xH2O,其中铁元素的化合价是 。
【探究铁的腐蚀】
(3)该小组用如图甲装置进行实验,起始时量筒内水面处于50 mL刻度处,之后水面缓慢上升。几天后水面最终处于约 (填“40”或“10”)mL刻度处,原因是 。
【拓展探究】
(4)小强同学进行如下实验:取铁钉用砂纸打磨,称其质量,按如图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
温度/℃ 10 20 30 40 50 60 70
铁钉质量增加/g 0.02 0.04 0.08 0.16 0.18 0.18 0.18
小强同学的实验是探究 因素对铁钉腐蚀快慢的影响,结论是 。
(5)有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因 ;改进实验方案证明你的分析 。
参考答案与解析
一、选择题
1.【答案】B
【解析】铁生锈的原因是和空气中的水和氧气接触反应而生锈,所以正确答案选B。
2.【答案】D
【解析】A.在金属制品表面镀保护层,使金属和空气或水隔绝,防止金属生锈,正确,不符合题意;
B.合金往往具有良好的抗腐蚀性,制成合金后使用,能防止生锈,正确,不符合题意;
C.在金属表面刷漆或是涂油使金属和空气或水隔绝,能防止金属生锈,正确,不符合题意;
D.用稀盐酸定期清洗金属制品,稀盐酸是酸性物质,会加速铁的锈蚀,符合题意。故选D。
3.【答案】C
【解析】A.不锈钢并不是绝对不会生锈的铁合金,而是比较难生锈的铁合金,A不正确;
B.合金的特征是熔点低、硬度大,故武德合金的熔点比其成分金属低,B不正确;
C.日常生活中,钢铁表面刷油漆,可以防止铁与氧气和水接触,防止铁生锈,C正确;
D.“曾青得铁则化为铜”的原理是用铁置换出铜,D不正确。
4.【答案】A
【解析】A.回收废旧金属,可以节约金属资源,虽然耗费大量人力物力,但可以节约金属资源,故选项说法错误;
B.回收废旧金属,是保护金属资源的重要途径,故选项说法正确;
C.回收废旧金属,可以减少对环境的污染,故选项说法正确;
D.回收废旧金属,可以节约宝贵的金属资源,故选项说法正确。
5.【答案】B
【解析】A.钢管存放在干燥的地方,能防止铁与水分接触,能防止铁锈蚀,故选项防锈措施正确;
B.用盐水清洗菜刀,盐水能加快铁锈蚀的速率,故选项防锈措施错误;
C.铁锈很疏松,及时清除铁制品表面的锈渍,能防止铁锈蚀,故选项防锈措施正确;
D.在铁管表面镀上一层不易锈蚀的金属,能防止铁锈蚀,故选项防锈措施正确。
6.【答案】B
【解析】A.铁锈的主要成分是氧化铁,氯化钠能加快铁锈蚀的速率,不能用作除铁锈的试剂,故选项错误;
B.铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁和水,能用作除铁锈的试剂,故选项正确;
C.铁锈的主要成分是氧化铁,不与氢氧化钠溶液反应,不能用作除铁锈的试剂,故选项错误;
D.铁锈的主要成分是氧化铁,难溶于水,水不能用作除铁锈的试剂,故选项错误。
7.【答案】A
【解析】破铁锅、坏车架、废弃易拉罐、旧电线和铝材下脚料都属于金属材料。
8.【答案】B
【解析】A.b管中缺少水,铁钉不会锈蚀。故选项正确;
B.因为a中的氧气减少,压强也减小,从而导致L端比R端液面高。故选项错误;
C.a试管中铁钉生锈,b试管中铁钉没有生锈,说明铁锈蚀与空气、水有关。故选项正确;
D.铁在有盐和酸存在时锈蚀速度会加快,所以将a管中的水改为食盐水能加快铁的锈蚀。故选项正确。
9.【答案】B
【解析】A.钢的含碳量为0.03%~2%之间,而生铁的含碳量在2%~4.3%之间,故错误;
B.防止金属锈蚀是保护金属资源的有效途径,故正确;
C.镁带在空气中燃烧,发出耀眼白光,生成白色固体,故错误;
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝能与氧气反应生成致密的氧化铝保护膜,故错误。
二、综合题
10.【答案】(1)铁与氧气、水同时接触;Fe2O3+6HCl═2FeCl3+3H2O;
(2)硬度大(或机械强度好、或韧性好等);
【解析】(1)铁在与氧气、水共存时会发生锈蚀;铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;故填:铁与氧气、水同时接触;Fe2O3+6HCl═2FeCl3+3H2O;
(2)合金钢的主要成分是铁、锰、碳,其韧性好,硬度大,纯铁硬度小且脆;所以铁轨用合金钢;故填:硬度大(或机械强度好、或韧性好等);
11.【答案】(1) 3Fe+2O2==Fe3O4 (2)铁片表面有红色物质附着;强(3)b(4)刷油漆
【解析】略。
12.【答案】(1)A;(2)+3价;(3)40;铁锈蚀消耗氧气,且氧气约占空气总体积的1/5;(4)温度;在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快;(5)试管内的氧气已耗尽,剩余的铁不能继续锈蚀; 向乙装置的试管中充入氧气,并在50℃的环境中放置3天;若铁钉增加的质量大于0.18 g,则分析成立。
【解析】(1)因为铁生锈的条件是与氧气和水同时接触,A.未擦干的铁锅中铁与水和氧气同时接触易生锈;B.涂油漆的栏杆隔绝氧气和水不易生锈;C.盛水的不锈钢水杯,由于不锈钢也不易生锈。故填:A;
(2)依据在化合物中正负化合价的代数和为零,根据铁锈的化学式Fe2O3 xH2O,设铁元素化合价为a,2a+3×(﹣2)+x[(+1)×2+(﹣2)]=0 a=+3,故填:+3价;
(3)因为铁丝绒生锈消耗试管内的氧气,又知空气中的氧气约占空气体积的1/5,可知量筒水面刻度上升到40 mL处,故填:40;铁锈蚀消耗氧气,且氧气约占空气总体积的1/5;
(4)分析表格中的数据可推知实验探究的因素为温度,其实验结论为在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快,故填:温度;在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快;
(5)因为铁钉生锈后,量筒水面刻度上升到40 mL处,说明试管内的氧气全部耗尽,所以50℃后铁钉的质量不再增加,向试管内通入氧气,铁钉会继续生锈,铁锈的质量继续增加,故填:试管内的氧气已耗尽,剩余的铁不能继续锈蚀; 向乙装置的试管中充入氧气,并在50℃的环境中放置3天;若铁钉增加的质量大于0.18 g,则分析成立。
1
一、选择题
1.空气中含①N2 ②O2 ③稀有气体 ④水蒸气等成分,其中与钢铁生锈有关的是( )
A.①③ B.②④ C.③④ D.①④
2.港珠澳大桥的桥、岛、隧以及“雪龙2号”的船身等主要由金属材料制成。下列金属防护措施不正确的是( )
A.在金属制品表面镀保护层
B.改变金属结构制成合金使用
C.在金属制品表面涂油漆
D.用稀盐酸定期清洗金属制品
3.金属是一类重要的材料。下列有关金属的说法正确的是( )
A.不锈钢是绝对不会生锈的铁合金
B.武德合金的熔点比其成分金属高
C.日常生活中,钢铁表面刷油漆可以防止生锈
D.“曾青得铁则化为铜”的原理是用铜置换出铁
4.关于废旧金属回收的意义,下列叙述错误的是( )
A.耗费大量人力物力,得不偿失
B.是保护金属资源的重要途径
C.可以减少废弃金属对环境的污染
D.可以节约宝贵的金属资源
5.下列防锈措施不合理的是( )
A.钢管存放在干燥的地方
B.用盐水清洗菜刀
C.及时清除铁制品表面的锈渍
D.在铁管表面镀上一层不易锈蚀的金属
6.除铁锈的试剂是( )
A.氯化钠溶液 B.稀盐酸 C.氢氧化钠溶液 D.水
7.将垃圾分类回收利用,既节约资源,又防止污染,符合可持续发展的要求。例如:破铁锅、坏车架、废弃易拉罐、旧电线和铝材下脚料等可归为一类回收,它们属于( )
A.金属材料 B.氧化物 C.单质 D.非金属
8.如图是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧木塞,一周后观察。下列推断错误的是( )
A.b管中铁钉不会锈蚀 B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与水有关 D.将a管中的水改为食盐水能加快铁的锈蚀
9.下列有关金属的说法正确的是( )
A.钢的含碳量比生铁的含碳量高
B.防止金属锈蚀是保护金属资源的有效途径
C.镁带在空气中燃烧,发出耀眼白光,生成黑色固体
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝不与氧气反应
二、综合题
10.古往今来,金属材料和制品在我们的社会生活中一直起者非常重要的作用。
(1)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是 。在实验室常用稀盐酸清除铁锈,化学方程式为 。
(2)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,主要原因是合金钢具有 的优越性能(要求只答一条)。
11.根据下图回答有关问题:
(1)写出实验①中反应的化学方程式 。
(2)实验②中可观察到铁片的表面 ,说明铁的金属活动性比铜 。(填“强”或“弱”)
(3)实验③中可观察到试管中铁钉最先生锈的是 处。(填“a”或“b”或“c”)。
(4)你认为防止铁架台生锈的方法有 。(写一点)
12.金属防腐是科学研究中的重大课题。某校学习小组以铁的腐蚀为项目进行如下研究。
【认识铁的腐蚀】
(1)下列环境中的铁制品最容易生锈的是 (填字母序号)。
A.未擦干的铁锅 B.涂油漆的栏杆 C.盛水的不锈钢水杯
(2)铁锈的主要成分是Fe2O3 xH2O,其中铁元素的化合价是 。
【探究铁的腐蚀】
(3)该小组用如图甲装置进行实验,起始时量筒内水面处于50 mL刻度处,之后水面缓慢上升。几天后水面最终处于约 (填“40”或“10”)mL刻度处,原因是 。
【拓展探究】
(4)小强同学进行如下实验:取铁钉用砂纸打磨,称其质量,按如图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。
温度/℃ 10 20 30 40 50 60 70
铁钉质量增加/g 0.02 0.04 0.08 0.16 0.18 0.18 0.18
小强同学的实验是探究 因素对铁钉腐蚀快慢的影响,结论是 。
(5)有同学认为小强的实验未能真实反映50℃以后铁钉腐蚀的快慢,理由是50℃以后铁钉质量没有变化。请分析铁钉质量没有变化的原因 ;改进实验方案证明你的分析 。
参考答案与解析
一、选择题
1.【答案】B
【解析】铁生锈的原因是和空气中的水和氧气接触反应而生锈,所以正确答案选B。
2.【答案】D
【解析】A.在金属制品表面镀保护层,使金属和空气或水隔绝,防止金属生锈,正确,不符合题意;
B.合金往往具有良好的抗腐蚀性,制成合金后使用,能防止生锈,正确,不符合题意;
C.在金属表面刷漆或是涂油使金属和空气或水隔绝,能防止金属生锈,正确,不符合题意;
D.用稀盐酸定期清洗金属制品,稀盐酸是酸性物质,会加速铁的锈蚀,符合题意。故选D。
3.【答案】C
【解析】A.不锈钢并不是绝对不会生锈的铁合金,而是比较难生锈的铁合金,A不正确;
B.合金的特征是熔点低、硬度大,故武德合金的熔点比其成分金属低,B不正确;
C.日常生活中,钢铁表面刷油漆,可以防止铁与氧气和水接触,防止铁生锈,C正确;
D.“曾青得铁则化为铜”的原理是用铁置换出铜,D不正确。
4.【答案】A
【解析】A.回收废旧金属,可以节约金属资源,虽然耗费大量人力物力,但可以节约金属资源,故选项说法错误;
B.回收废旧金属,是保护金属资源的重要途径,故选项说法正确;
C.回收废旧金属,可以减少对环境的污染,故选项说法正确;
D.回收废旧金属,可以节约宝贵的金属资源,故选项说法正确。
5.【答案】B
【解析】A.钢管存放在干燥的地方,能防止铁与水分接触,能防止铁锈蚀,故选项防锈措施正确;
B.用盐水清洗菜刀,盐水能加快铁锈蚀的速率,故选项防锈措施错误;
C.铁锈很疏松,及时清除铁制品表面的锈渍,能防止铁锈蚀,故选项防锈措施正确;
D.在铁管表面镀上一层不易锈蚀的金属,能防止铁锈蚀,故选项防锈措施正确。
6.【答案】B
【解析】A.铁锈的主要成分是氧化铁,氯化钠能加快铁锈蚀的速率,不能用作除铁锈的试剂,故选项错误;
B.铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁和水,能用作除铁锈的试剂,故选项正确;
C.铁锈的主要成分是氧化铁,不与氢氧化钠溶液反应,不能用作除铁锈的试剂,故选项错误;
D.铁锈的主要成分是氧化铁,难溶于水,水不能用作除铁锈的试剂,故选项错误。
7.【答案】A
【解析】破铁锅、坏车架、废弃易拉罐、旧电线和铝材下脚料都属于金属材料。
8.【答案】B
【解析】A.b管中缺少水,铁钉不会锈蚀。故选项正确;
B.因为a中的氧气减少,压强也减小,从而导致L端比R端液面高。故选项错误;
C.a试管中铁钉生锈,b试管中铁钉没有生锈,说明铁锈蚀与空气、水有关。故选项正确;
D.铁在有盐和酸存在时锈蚀速度会加快,所以将a管中的水改为食盐水能加快铁的锈蚀。故选项正确。
9.【答案】B
【解析】A.钢的含碳量为0.03%~2%之间,而生铁的含碳量在2%~4.3%之间,故错误;
B.防止金属锈蚀是保护金属资源的有效途径,故正确;
C.镁带在空气中燃烧,发出耀眼白光,生成白色固体,故错误;
D.铝制品不需要涂保护层来防腐蚀,因为常温下铝能与氧气反应生成致密的氧化铝保护膜,故错误。
二、综合题
10.【答案】(1)铁与氧气、水同时接触;Fe2O3+6HCl═2FeCl3+3H2O;
(2)硬度大(或机械强度好、或韧性好等);
【解析】(1)铁在与氧气、水共存时会发生锈蚀;铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;故填:铁与氧气、水同时接触;Fe2O3+6HCl═2FeCl3+3H2O;
(2)合金钢的主要成分是铁、锰、碳,其韧性好,硬度大,纯铁硬度小且脆;所以铁轨用合金钢;故填:硬度大(或机械强度好、或韧性好等);
11.【答案】(1) 3Fe+2O2==Fe3O4 (2)铁片表面有红色物质附着;强(3)b(4)刷油漆
【解析】略。
12.【答案】(1)A;(2)+3价;(3)40;铁锈蚀消耗氧气,且氧气约占空气总体积的1/5;(4)温度;在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快;(5)试管内的氧气已耗尽,剩余的铁不能继续锈蚀; 向乙装置的试管中充入氧气,并在50℃的环境中放置3天;若铁钉增加的质量大于0.18 g,则分析成立。
【解析】(1)因为铁生锈的条件是与氧气和水同时接触,A.未擦干的铁锅中铁与水和氧气同时接触易生锈;B.涂油漆的栏杆隔绝氧气和水不易生锈;C.盛水的不锈钢水杯,由于不锈钢也不易生锈。故填:A;
(2)依据在化合物中正负化合价的代数和为零,根据铁锈的化学式Fe2O3 xH2O,设铁元素化合价为a,2a+3×(﹣2)+x[(+1)×2+(﹣2)]=0 a=+3,故填:+3价;
(3)因为铁丝绒生锈消耗试管内的氧气,又知空气中的氧气约占空气体积的1/5,可知量筒水面刻度上升到40 mL处,故填:40;铁锈蚀消耗氧气,且氧气约占空气总体积的1/5;
(4)分析表格中的数据可推知实验探究的因素为温度,其实验结论为在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快,故填:温度;在其它条件相同时,温度在10~50℃的范围内,温度越高,铁钉腐蚀的速度越快;
(5)因为铁钉生锈后,量筒水面刻度上升到40 mL处,说明试管内的氧气全部耗尽,所以50℃后铁钉的质量不再增加,向试管内通入氧气,铁钉会继续生锈,铁锈的质量继续增加,故填:试管内的氧气已耗尽,剩余的铁不能继续锈蚀; 向乙装置的试管中充入氧气,并在50℃的环境中放置3天;若铁钉增加的质量大于0.18 g,则分析成立。
1
同课章节目录
