课题3 溶液的浓度
图片预览
文档简介
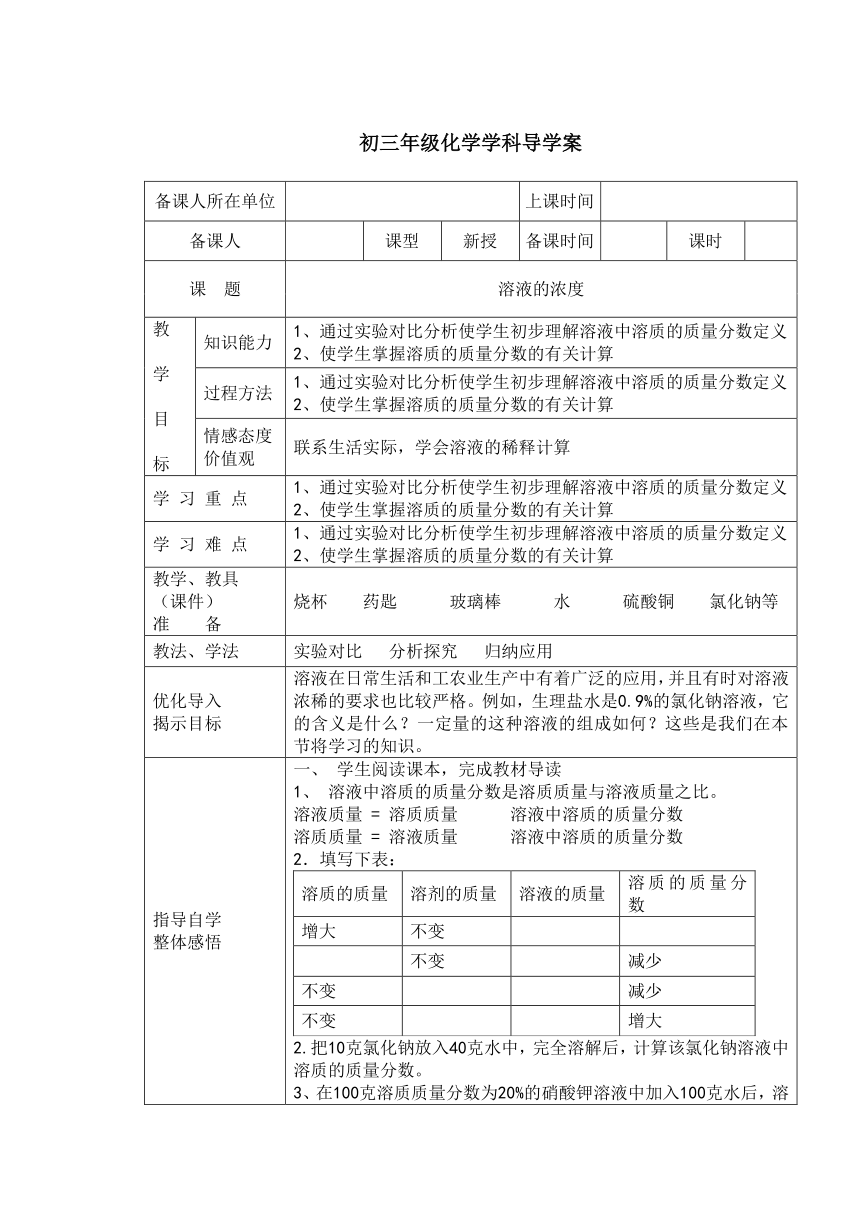
初三年级化学学科导学案
备课人所在单位 上课时间
备课人 课型 新授 备课时间 课时
课 题 溶液的浓度
教
学
目
标 知识能力 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
过程方法 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
情感态度价值观 联系生活实际,学会溶液的稀释计算
学 习 重 点 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
学 习 难 点 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
教学、教具
(课件)
准 备 烧杯 药匙 玻璃棒 水 硫酸铜 氯化钠等
教法、学法 实验对比 分析探究 归纳应用
优化导入揭示目标 溶液在日常生活和工农业生产中有着广泛的应用,并且有时对溶液浓稀的要求也比较严格。例如,生理盐水是0.9%的氯化钠溶液,它的含义是什么?一定量的这种溶液的组成如何?这些是我们在本节将学习的知识。
指导自学整体感悟 一、 学生阅读课本,完成教材导读1、 溶液中溶质的质量分数是溶质质量与溶液质量之比。溶液质量 = 溶质质量 溶液中溶质的质量分数溶质质量 = 溶液质量 溶液中溶质的质量分数2.填写下表:溶质的质量溶剂的质量溶液的质量溶质的质量分数增大不变 不变 减少不变 减少不变 增大2.把10克氯化钠放入40克水中,完全溶解后,计算该氯化钠溶液中溶质的质量分数。3、在100克溶质质量分数为20%的硝酸钾溶液中加入100克水后,溶液的溶质质量分数变为 。4、要把100克10%的硝酸钾溶液稀释为5%的硝酸钾溶液,需加水质量为 。二、小组交流,讨论解决
互动互研解疑释难 探究一:通过观察有色溶液的颜色,确定溶液的浓稀。1、在3个小烧杯里分别加入0.1克、0.5克、2克无水硫酸铜,振荡。使硫酸铜全部溶解,比较三种溶液的颜色: 个烧杯中的颜色最深,该溶液的浓度最 , 个烧杯中的颜色最浅,该溶液的浓度最 。可见,对于有色溶液,浓度越大,颜色越 ,浓度越小,颜色越 。2、溶液中溶质、溶剂量的多少对溶液浓度的影响:溶液质量一定时,含溶质较多的硫酸铜溶液的浓度较 ;在硫酸铜溶液中加水后,溶液颜色 ,即溶液的浓度变 ,说明含溶质相对多的硫酸铜溶液浓度较 。探究二:比较溶液的组成,计算出这两种溶质的质量分数。1.根据表格中的数据,计算出这两种溶液中溶质的质量分数。溶质质量溶剂质量溶液质量溶质质量分数1090 2080 溶液质量一定时,溶质质量小,溶剂质量大,溶液中溶质的质量分数较 溶液质量一定时,溶质质量大,溶剂质量小,溶液中溶质的质量分数较 2.溶液的稀释问题讨论课本例题2,可知向50克98%的浓硫酸中加入水后,溶液的质量 溶剂的质量 ,溶质的质量 ,溶液中溶质的质量分数 所以解决稀释问题的依据是
精点巧拨归纳生成 1.溶液中溶质的质量分数是溶质质量与溶液质量之比。溶液质量 = 溶质质量 溶液中溶质的质量分数溶质质量 = 溶液质量 溶液中溶质的质量分数2.溶液质量一定时,溶质质量小,溶剂质量大,溶液中溶质的质量分数较 溶液质量一定时,溶质质量大,溶剂质量小,溶液中溶质的质量分数较 3.解决稀释问题的依据是
分层设练拓展延伸 1.从1000克1%的氯化钠溶液中取出100克,则这100克溶液中溶质的质量分数是( )A.1% B.0.1% C.10% D.无法判断2.20克溶质完全溶解在80克溶剂中,该溶液中溶质的质量分数为 ( )A.25% B.25克 C.20% D.20克3.在20℃时,硝酸钾的溶解度是31.6克,20℃时硝酸钾饱和溶液中的硝酸钾的质量分数是多少4.把100克98%的硫酸稀释成10%的稀硫酸需加水多少克? 5.把50克质量分数为20%的氯化钠溶液加水稀释到200克,此溶液中氯化钠的质量分数为多少?
板书设计 溶液的浓度1.溶液的浓度2.浓溶液和稀溶液3.溶液浓度的表示方法4.溶质的质量分数概念、影响因素、公式计算5.溶液的稀释计算
课后反思
备课人所在单位 上课时间
备课人 课型 新授 备课时间 课时
课 题 溶液的浓度
教
学
目
标 知识能力 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
过程方法 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
情感态度价值观 联系生活实际,学会溶液的稀释计算
学 习 重 点 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
学 习 难 点 1、通过实验对比分析使学生初步理解溶液中溶质的质量分数定义 2、使学生掌握溶质的质量分数的有关计算
教学、教具
(课件)
准 备 烧杯 药匙 玻璃棒 水 硫酸铜 氯化钠等
教法、学法 实验对比 分析探究 归纳应用
优化导入揭示目标 溶液在日常生活和工农业生产中有着广泛的应用,并且有时对溶液浓稀的要求也比较严格。例如,生理盐水是0.9%的氯化钠溶液,它的含义是什么?一定量的这种溶液的组成如何?这些是我们在本节将学习的知识。
指导自学整体感悟 一、 学生阅读课本,完成教材导读1、 溶液中溶质的质量分数是溶质质量与溶液质量之比。溶液质量 = 溶质质量 溶液中溶质的质量分数溶质质量 = 溶液质量 溶液中溶质的质量分数2.填写下表:溶质的质量溶剂的质量溶液的质量溶质的质量分数增大不变 不变 减少不变 减少不变 增大2.把10克氯化钠放入40克水中,完全溶解后,计算该氯化钠溶液中溶质的质量分数。3、在100克溶质质量分数为20%的硝酸钾溶液中加入100克水后,溶液的溶质质量分数变为 。4、要把100克10%的硝酸钾溶液稀释为5%的硝酸钾溶液,需加水质量为 。二、小组交流,讨论解决
互动互研解疑释难 探究一:通过观察有色溶液的颜色,确定溶液的浓稀。1、在3个小烧杯里分别加入0.1克、0.5克、2克无水硫酸铜,振荡。使硫酸铜全部溶解,比较三种溶液的颜色: 个烧杯中的颜色最深,该溶液的浓度最 , 个烧杯中的颜色最浅,该溶液的浓度最 。可见,对于有色溶液,浓度越大,颜色越 ,浓度越小,颜色越 。2、溶液中溶质、溶剂量的多少对溶液浓度的影响:溶液质量一定时,含溶质较多的硫酸铜溶液的浓度较 ;在硫酸铜溶液中加水后,溶液颜色 ,即溶液的浓度变 ,说明含溶质相对多的硫酸铜溶液浓度较 。探究二:比较溶液的组成,计算出这两种溶质的质量分数。1.根据表格中的数据,计算出这两种溶液中溶质的质量分数。溶质质量溶剂质量溶液质量溶质质量分数1090 2080 溶液质量一定时,溶质质量小,溶剂质量大,溶液中溶质的质量分数较 溶液质量一定时,溶质质量大,溶剂质量小,溶液中溶质的质量分数较 2.溶液的稀释问题讨论课本例题2,可知向50克98%的浓硫酸中加入水后,溶液的质量 溶剂的质量 ,溶质的质量 ,溶液中溶质的质量分数 所以解决稀释问题的依据是
精点巧拨归纳生成 1.溶液中溶质的质量分数是溶质质量与溶液质量之比。溶液质量 = 溶质质量 溶液中溶质的质量分数溶质质量 = 溶液质量 溶液中溶质的质量分数2.溶液质量一定时,溶质质量小,溶剂质量大,溶液中溶质的质量分数较 溶液质量一定时,溶质质量大,溶剂质量小,溶液中溶质的质量分数较 3.解决稀释问题的依据是
分层设练拓展延伸 1.从1000克1%的氯化钠溶液中取出100克,则这100克溶液中溶质的质量分数是( )A.1% B.0.1% C.10% D.无法判断2.20克溶质完全溶解在80克溶剂中,该溶液中溶质的质量分数为 ( )A.25% B.25克 C.20% D.20克3.在20℃时,硝酸钾的溶解度是31.6克,20℃时硝酸钾饱和溶液中的硝酸钾的质量分数是多少4.把100克98%的硫酸稀释成10%的稀硫酸需加水多少克? 5.把50克质量分数为20%的氯化钠溶液加水稀释到200克,此溶液中氯化钠的质量分数为多少?
板书设计 溶液的浓度1.溶液的浓度2.浓溶液和稀溶液3.溶液浓度的表示方法4.溶质的质量分数概念、影响因素、公式计算5.溶液的稀释计算
课后反思
同课章节目录
