6.1.2 化学反应与电能 课件(共53张PPT)
文档属性
| 名称 | 6.1.2 化学反应与电能 课件(共53张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 72.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-04 00:00:00 | ||
图片预览









文档简介
(共53张PPT)
第六章 化学反应与能量
第一节 化学反应与能量变化
第2课时 化学反应与电能
各式各样的电器
新课导入
一次能源
二次能源
水能
风能
电能
蒸气能
我们的生活很难离开电力
电是从哪里来的?
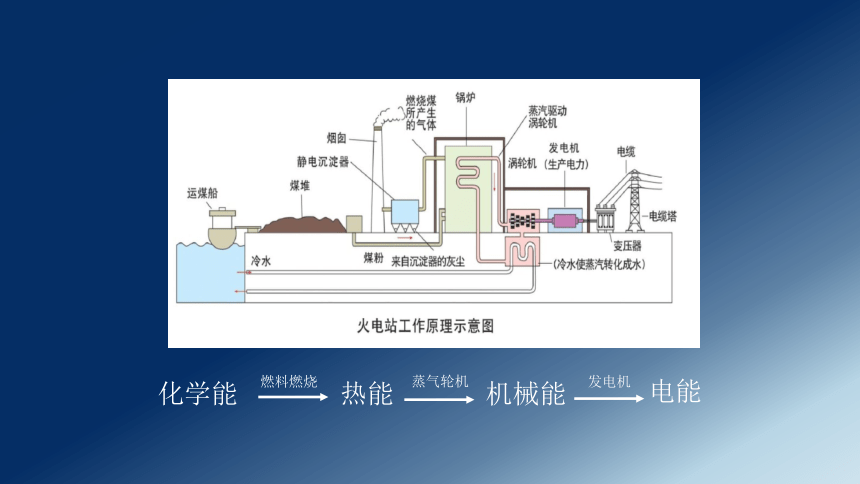
火力发电
核电站
水力发电
风力发电
一、化学能与电能
我们日常使用的电能主要来自火力发电。
2015年我国发电总量构成图
知识梳理
在化学反应中,物质中的化学能的变化通常表现为热量的变化,即化学能转变为热能。
问题:
物质中的化学能在什么条件下能转化为电能?
化学能如何转化为电能?
化学能
热能
机械能
电能
燃料燃烧
蒸气轮机
发电机
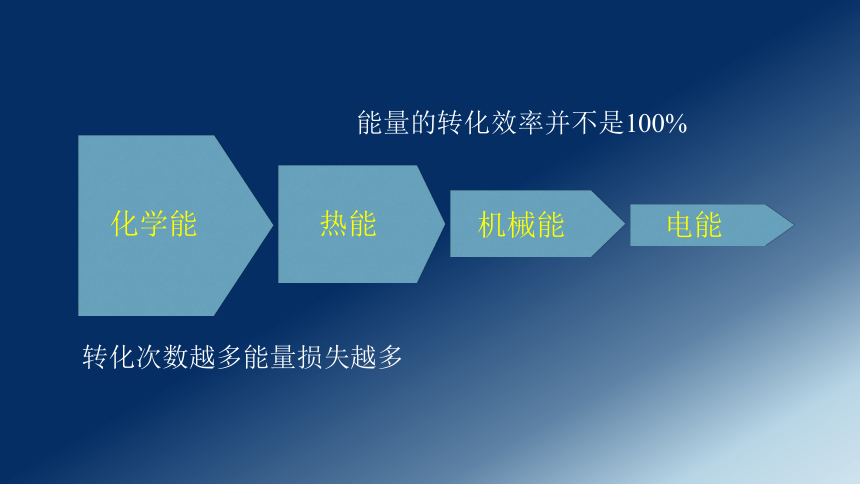
能量的转化效率并不是100%
化学能
热能
机械能
电能
转化次数越多能量损失越多
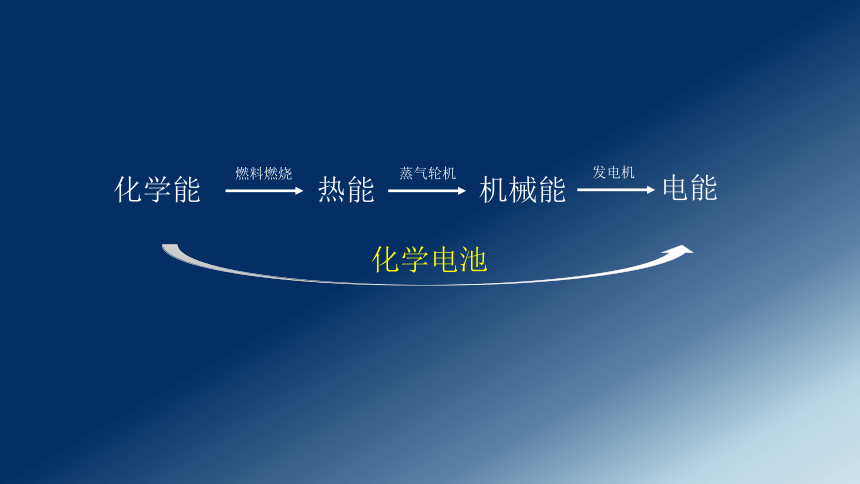
化学能
热能
机械能
电能
燃料燃烧
蒸气轮机
发电机
化学电池
1799年意大利物理学家伏特发明了世界上第一个发电器,也就是电池组,伏特电堆开创了电学发展的新时代。
伏特电堆
二、原电池
19世纪,英国化学家尼克尔森和卡莱尔利用伏特电池成功的电解了水,证明了水是由氢和氧两种元素组成的化合物。
英国化学家戴维,利用串联起来的伏特电池组,通过电解法发现了几种活泼的金属元素。比如金属钠和金属钾。
电能是如何产生的?
资料
Zn
H2
1.将锌片放入稀硫酸中
Zn
H2
H+
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
SO4
2-
1.将锌片放入稀硫酸中
氧化反应:Zn – 2e- Zn2+
还原反应:2H+ + 2e- H2↑
Zn
H2
H+
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
SO4
2-
1.将锌片放入稀硫酸中
氧化反应:Zn – 2e- Zn2+
还原反应:2H+ + 2e- H2↑
总反应:Zn + 2H+ Zn2+ + H2↑
2.将锌片和铜片同时放入稀硫酸中
Cu
Zn
H2
H+
Zn2+
SO4
2-
3.将稀硫酸中的锌片和铜片用导线和电流计连接
Cu
Zn
H2
H+
Zn2+
SO4
2-
H2
Cu
H+
A
Zn
SO4
2-
铜片上的氢气是如何产生的?
问题:
H2
Cu
H+
A
Zn
SO4
2-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
这种把化学能转化为电能的装置叫原电池
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn – 2e- Zn2+
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn – 2e- Zn2+
2H+ + 2e- H2↑
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
原电池装置小结
正极 得到电子 发生还原反应
负极 失去电子 发生氧化反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
—
+
原电池装置小结
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
电子流动方向:
负极 导线 正极
—
+
原电池装置小结
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
—
+
原电池装置小结
e-
e-
Cu
A
Zn
Zn2+
H+
SO4
2-
离子运动方向:
阳离子 正极
阴离子 负极
三、原电池的构成要素
1.在原电池当中,稀硫酸的作用是什么?
2.制作原电池的过程中,对电极材料的选择是否有要求?
3.在原电池的制作中,电池有哪些不可或缺的部分?
Zn
酒精
Cu
A
Zn
稀硫酸
Cu
A
Zn
酒精
Cu
A
Zn
稀硫酸
Cu
A
Zn
酒精
Zn
A
Zn
稀硫酸
C
A
Zn
稀硫酸
玻璃
A
Zn
酒精
Zn
A
Zn
稀硫酸
C
A
Zn
稀硫酸
玻璃
A
1.电极材料
2.自发进行的电极反应
3.电子导体和离子导体
三、原电池的构成要素
例1.判断下列原电池的正极和负极
Zn
稀硫酸
Al
A
Zn
稀硫酸
Cu
A
Fe
稀硫酸
C
A
四、典型例题
—
+
+
—
—
+
例1.判断下列原电池的正极和负极
Zn
稀硫酸
Al
A
Zn
稀硫酸
Cu
A
Fe
稀硫酸
C
A
四、典型例题
例2.下列关于右图所示装置的叙述,错误的是( )
A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原,产生气泡
C.电流从锌片经过导线流向铜片
D.电子从锌片经过导线流向铜片
Zn
稀硫酸
Cu
A
例2.下列关于右图所示装置的叙述,错误的是( )
A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原,产生气泡
C.电流从锌片经过导线流向铜片
D.电子从锌片经过导线流向铜片
Zn
稀硫酸
Cu
A
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡逸出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>c
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>c
d>b
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
答案:a>c>d>b
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
c>d
a>c
d>b
—
+
e-
e-
Cu
A
Zn
Zn2+
H+
SO4
2-
本节内容结束
第六章 化学反应与能量
第一节 化学反应与能量变化
第2课时 化学反应与电能
各式各样的电器
新课导入
一次能源
二次能源
水能
风能
电能
蒸气能
我们的生活很难离开电力
电是从哪里来的?
火力发电
核电站
水力发电
风力发电
一、化学能与电能
我们日常使用的电能主要来自火力发电。
2015年我国发电总量构成图
知识梳理
在化学反应中,物质中的化学能的变化通常表现为热量的变化,即化学能转变为热能。
问题:
物质中的化学能在什么条件下能转化为电能?
化学能如何转化为电能?
化学能
热能
机械能
电能
燃料燃烧
蒸气轮机
发电机
能量的转化效率并不是100%
化学能
热能
机械能
电能
转化次数越多能量损失越多
化学能
热能
机械能
电能
燃料燃烧
蒸气轮机
发电机
化学电池
1799年意大利物理学家伏特发明了世界上第一个发电器,也就是电池组,伏特电堆开创了电学发展的新时代。
伏特电堆
二、原电池
19世纪,英国化学家尼克尔森和卡莱尔利用伏特电池成功的电解了水,证明了水是由氢和氧两种元素组成的化合物。
英国化学家戴维,利用串联起来的伏特电池组,通过电解法发现了几种活泼的金属元素。比如金属钠和金属钾。
电能是如何产生的?
资料
Zn
H2
1.将锌片放入稀硫酸中
Zn
H2
H+
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
SO4
2-
1.将锌片放入稀硫酸中
氧化反应:Zn – 2e- Zn2+
还原反应:2H+ + 2e- H2↑
Zn
H2
H+
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
SO4
2-
1.将锌片放入稀硫酸中
氧化反应:Zn – 2e- Zn2+
还原反应:2H+ + 2e- H2↑
总反应:Zn + 2H+ Zn2+ + H2↑
2.将锌片和铜片同时放入稀硫酸中
Cu
Zn
H2
H+
Zn2+
SO4
2-
3.将稀硫酸中的锌片和铜片用导线和电流计连接
Cu
Zn
H2
H+
Zn2+
SO4
2-
H2
Cu
H+
A
Zn
SO4
2-
铜片上的氢气是如何产生的?
问题:
H2
Cu
H+
A
Zn
SO4
2-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
总反应:Zn + 2H+ Zn2+ + H2↑
这种把化学能转化为电能的装置叫原电池
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
还原反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
氧化反应
Zn2+
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn – 2e- Zn2+
Zn2+
Zn
H2
Cu
H+
Zn2+
H2
Cu
H+
A
Zn
Zn2+
e-
e-
SO4
2-
SO4
2-
还原反应
氧化反应
Zn – 2e- Zn2+
2H+ + 2e- H2↑
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
原电池装置小结
正极 得到电子 发生还原反应
负极 失去电子 发生氧化反应
2H+ + 2e- H2↑
铜片:
Zn – 2e- Zn2+
锌片:
—
+
原电池装置小结
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
电子流动方向:
负极 导线 正极
—
+
原电池装置小结
e-
e-
H2
Cu
H+
A
Zn
SO4
2-
Zn2+
—
+
原电池装置小结
e-
e-
Cu
A
Zn
Zn2+
H+
SO4
2-
离子运动方向:
阳离子 正极
阴离子 负极
三、原电池的构成要素
1.在原电池当中,稀硫酸的作用是什么?
2.制作原电池的过程中,对电极材料的选择是否有要求?
3.在原电池的制作中,电池有哪些不可或缺的部分?
Zn
酒精
Cu
A
Zn
稀硫酸
Cu
A
Zn
酒精
Cu
A
Zn
稀硫酸
Cu
A
Zn
酒精
Zn
A
Zn
稀硫酸
C
A
Zn
稀硫酸
玻璃
A
Zn
酒精
Zn
A
Zn
稀硫酸
C
A
Zn
稀硫酸
玻璃
A
1.电极材料
2.自发进行的电极反应
3.电子导体和离子导体
三、原电池的构成要素
例1.判断下列原电池的正极和负极
Zn
稀硫酸
Al
A
Zn
稀硫酸
Cu
A
Fe
稀硫酸
C
A
四、典型例题
—
+
+
—
—
+
例1.判断下列原电池的正极和负极
Zn
稀硫酸
Al
A
Zn
稀硫酸
Cu
A
Fe
稀硫酸
C
A
四、典型例题
例2.下列关于右图所示装置的叙述,错误的是( )
A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原,产生气泡
C.电流从锌片经过导线流向铜片
D.电子从锌片经过导线流向铜片
Zn
稀硫酸
Cu
A
例2.下列关于右图所示装置的叙述,错误的是( )
A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原,产生气泡
C.电流从锌片经过导线流向铜片
D.电子从锌片经过导线流向铜片
Zn
稀硫酸
Cu
A
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡逸出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>c
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
c>d
a>c
d>b
例3.把a、b、c、d 4种金属浸入到稀硫酸中,用导线两两相连可以组成各种原电池,请根据下列信息,判断四种金属的活动性顺序。
答案:a>c>d>b
a>b
(1)若a、b相连,a为负极。
(2)若c、d相连,d上有气泡溢出。
(3)若a、c相连,a的质量减少。
(4)若b、d相连,b为正极。
c>d
a>c
d>b
—
+
e-
e-
Cu
A
Zn
Zn2+
H+
SO4
2-
本节内容结束
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
