人教版化学九下:8.2.2 金属活动性顺序 探究课件(共25张PPT)
文档属性
| 名称 | 人教版化学九下:8.2.2 金属活动性顺序 探究课件(共25张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-02-06 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
R·九年级化学下册
第八单元 金属和金属材料
课题2 金属的化学性质
第2课时 金属活动性顺序
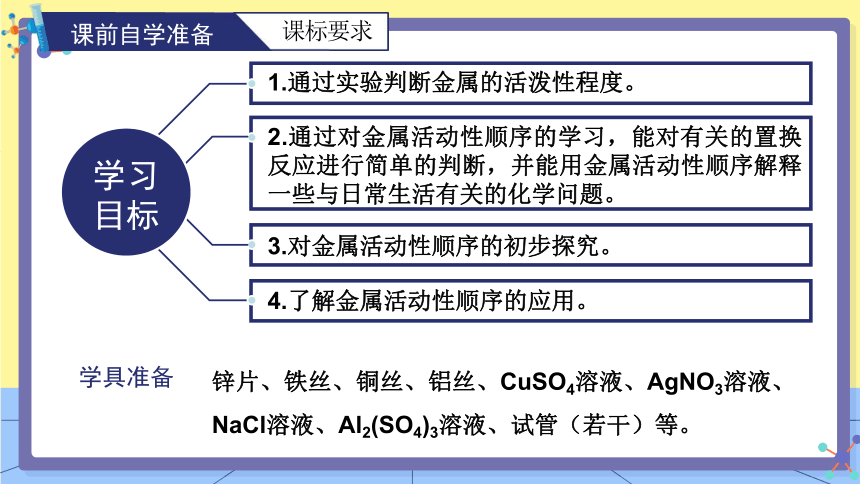
锌片、铁丝、铜丝、铝丝、CuSO4溶液、AgNO3溶液、NaCl溶液、Al2(SO4)3溶液、试管(若干)等。
课前自学准备
课标要求
1.通过实验判断金属的活泼性程度。
2.通过对金属活动性顺序的学习,能对有关的置换反应进行简单的判断,并能用金属活动性顺序解释一些与日常生活有关的化学问题。
3.对金属活动性顺序的初步探究。
4.了解金属活动性顺序的应用。
学习
目标
学具准备
金属与金属化合物溶液的反应:铁钉放在硫酸铜溶液中时,铁钉表面有 物质析出,溶液由蓝色变为 色,反应的化学方程式为
。若铝丝具有和铁钉相似的性质,则铝丝放在硫酸铜溶液中反应的化学方程式为 ,以上反应的反应类型是 。
红色
浅绿
置换反应
课前自学准备
预习检测
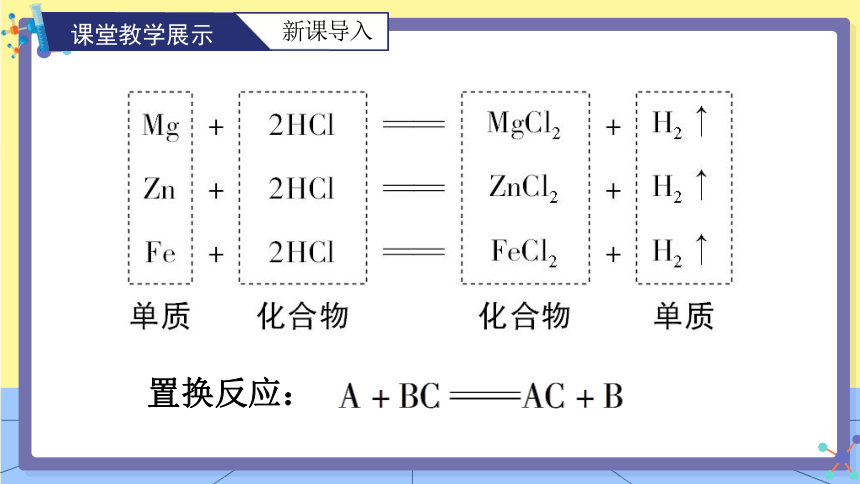
置换反应:
课堂教学展示
新课导入
把铁钉放在硫酸铜溶液中,铁钉上会有紫红色的铜生成。
Fe+CuSO4=FeSO4+Cu
说明铁的金属活动性比铜的强。
知识点1 金属与金属化合物溶液的反应
课堂教学展示
课堂探究
把一根用砂纸打磨过的的铝丝浸入硫酸铜溶液中,过一会儿取出,观察,有什么现象发生?
把一根洁净的铜丝浸入硝酸银溶液中,过一会儿取出,观察,有什么现象发生?
把另一根洁净的铜丝浸入硫酸铝溶液中,过一会儿取出,观察,有什么现象发生?
探究
实验 现象 反应的化学方程式
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
浸入溶液的铝丝表面覆盖一层紫红色的物质,溶液由蓝色逐渐变为无色。
浸入溶液的铜丝表面覆盖一层银白色的物质,溶液由无色逐渐变为蓝色。
无明显现象
Cu+2AgNO3=Cu(NO3)2+2Ag
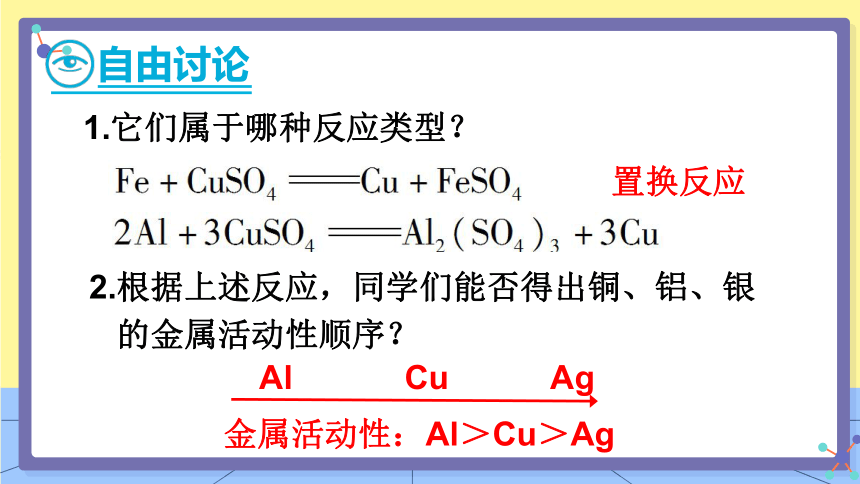
自由讨论
1.它们属于哪种反应类型?
2.根据上述反应,同学们能否得出铜、铝、银
的金属活动性顺序?
Al Cu Ag
置换反应
金属活动性:Al>Cu>Ag
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
排在氢前的金属能置换出盐酸或稀硫酸中的氢,生成氢气,而排在氢后的金属不能置换出盐酸或稀硫酸中的氢(即不反应)。
知识点2 常见金属活动性顺序
课堂教学展示
课堂探究
1.金属的位置越靠前,它的活动性就越强。
2.位于氢前的金属能置换出盐酸、稀硫酸中的氢。
3.位于前面的金属能把位于后面的金属从它们的
盐溶液中置换出来(除K、Ca、Na外)。
归纳
金属活动性顺序的应用:
1.如何验证Zn、Cu、Ag三种金属的活动性?
自由讨论
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
方法1:取活动性居中的金属为单质,例如取Cu丝,而Cu两边的金属取其溶液,如ZnCl2溶液和AgNO3溶液,然后将Cu丝分别伸入两溶液中,通过是否有金属被置换出来而确定金属的活动性。即中间的金属,两端的溶液的方法。
方法2:取金属活动性居中的金属盐溶液,例如取CuSO4溶液,而Cu两边的金属取其单质,如Zn片和Ag片,然后分别将Zn片和Ag片放入CuSO4溶液中,根据是否有紫红色的铜被置换出来,确定金属的活动性。即中间的溶液,两端的金属的方法。
2. 如何验证Mg、Zn、Cu、Ag的活动性?
自由讨论
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
氢前
氢后
一般情况下金属可分成两类:一类氢前金属,一类氢后金属。所以通常先取四种金属的单质和一种稀酸(如稀盐酸)反应,根据是否有气泡产生,来确定Mg、Zn比Cu、Ag活泼,同时又可根据产生气泡速率的快慢来确定Mg比Zn活泼。氢后金属,可根据金属单质与金属盐溶液的反应来确定Cu比Ag活泼(例如将Cu丝放入AgNO3溶液中)。
归纳
利用金属与金属化合物溶液的反应。依据反应能否发生判断:能反应说明置换的金属比被置换金属活动性强。
常用的探究金属活动性顺序的方法:
方法1:
利用金属与盐酸、稀硫酸的反应。依据现象判断:放出气体速率越快,其金属活动性越强。没有气体产生的,其金属活动性位于金属活动性顺序中氢的后面。
方法2:
3.黄金饰品中的假货常常鱼目混珠,社会上有些
不法分子时常以黄铜冒充黄金进行欺诈活动。
黄铜(铜锌合金)与黄金的外观很相似,我们
可用什么办法来鉴别它们呢?
自由讨论
黄铜
黄金
方法1:能与稀盐酸、稀硫酸反应的为黄铜、不
反应的为黄金。
方法2:能与AgNO3溶液反应的为黄铜、不反应
的为黄金。
方法3:黄金与黄铜的密度不同,测一下它们的
密度即可区别。
方法4:黄金与黄铜的硬度不同,把它们互相刻
画,硬度大的为黄铜,小的为黄金。
例 向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。
②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag。
④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3。
以上说法正确的个数为 ( )
A.0个 B.1个 C.2个 D.3个
×
×
√
×
B
课堂教学展示
典例剖析
第2课时 金属活动性顺序
一、金属与金属化合物溶液反应
2Al+3CuSO4=3Cu+Al2(SO4)3
Cu+2AgNO3=2Ag+Cu(NO3)2
Cu和Al2(SO4)3不反应
结论:金属活动性 Al>Cu>Ag
二、金属活动性顺序的应用
1.金属的位置越靠前,它的活动性越强。
2.位于氢前的金属能置换出盐酸和稀硫酸中的氢。
课堂教学展示
课堂小结
3.位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(除K、Ca、Na外)。
三、探究金属活动性常用的两种方法
1.利用金属和金属化合物溶液反应探究(验证Zn、Ag、Cu三种金属活动性)。
(1)“中间的金属,两端的溶液”的方法(Cu丝、ZnCl2溶液、AgNO3溶液)。
(2)“中间的溶液,两端的金属”的方法(Zn片、Ag片、CuSO4溶液)。
2.利用金属和盐酸、稀硫酸反应探究(验证Mg、Zn、Cu、Ag的活动性)。
练习与应用(P13)
2. 波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。为什么不能用铁制容器来配制波尔多液?
若用铁制容器来配制波尔多液,则容器会被腐
蚀,硫酸铜也会变质,发生如下反应:
Fe+CuSO4=FeSO4+Cu
课后反馈总结
课本习题
5. 下列物质能否发生反应?写出能发生反应的化
学方程式。
(1)银与稀盐酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)铝与硝酸银溶液
不能
能,
不能
能,
6. 填写下列表格(“混合物”栏中括号内为杂质)。
混合物 除去杂质的化学方程式 主要操作步骤
铜粉
(Fe)
FeCl2溶液(CuCl2)
加适量稀盐酸至无气泡产生,过滤、洗涤、干燥
加适量无锈铁钉或铁粉,过滤
7. 现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y和Z的金属活动性顺序。
解:金属活动性由强至弱依次为X、Y、Z。
R·九年级化学下册
第八单元 金属和金属材料
课题2 金属的化学性质
第2课时 金属活动性顺序
锌片、铁丝、铜丝、铝丝、CuSO4溶液、AgNO3溶液、NaCl溶液、Al2(SO4)3溶液、试管(若干)等。
课前自学准备
课标要求
1.通过实验判断金属的活泼性程度。
2.通过对金属活动性顺序的学习,能对有关的置换反应进行简单的判断,并能用金属活动性顺序解释一些与日常生活有关的化学问题。
3.对金属活动性顺序的初步探究。
4.了解金属活动性顺序的应用。
学习
目标
学具准备
金属与金属化合物溶液的反应:铁钉放在硫酸铜溶液中时,铁钉表面有 物质析出,溶液由蓝色变为 色,反应的化学方程式为
。若铝丝具有和铁钉相似的性质,则铝丝放在硫酸铜溶液中反应的化学方程式为 ,以上反应的反应类型是 。
红色
浅绿
置换反应
课前自学准备
预习检测
置换反应:
课堂教学展示
新课导入
把铁钉放在硫酸铜溶液中,铁钉上会有紫红色的铜生成。
Fe+CuSO4=FeSO4+Cu
说明铁的金属活动性比铜的强。
知识点1 金属与金属化合物溶液的反应
课堂教学展示
课堂探究
把一根用砂纸打磨过的的铝丝浸入硫酸铜溶液中,过一会儿取出,观察,有什么现象发生?
把一根洁净的铜丝浸入硝酸银溶液中,过一会儿取出,观察,有什么现象发生?
把另一根洁净的铜丝浸入硫酸铝溶液中,过一会儿取出,观察,有什么现象发生?
探究
实验 现象 反应的化学方程式
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
浸入溶液的铝丝表面覆盖一层紫红色的物质,溶液由蓝色逐渐变为无色。
浸入溶液的铜丝表面覆盖一层银白色的物质,溶液由无色逐渐变为蓝色。
无明显现象
Cu+2AgNO3=Cu(NO3)2+2Ag
自由讨论
1.它们属于哪种反应类型?
2.根据上述反应,同学们能否得出铜、铝、银
的金属活动性顺序?
Al Cu Ag
置换反应
金属活动性:Al>Cu>Ag
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
排在氢前的金属能置换出盐酸或稀硫酸中的氢,生成氢气,而排在氢后的金属不能置换出盐酸或稀硫酸中的氢(即不反应)。
知识点2 常见金属活动性顺序
课堂教学展示
课堂探究
1.金属的位置越靠前,它的活动性就越强。
2.位于氢前的金属能置换出盐酸、稀硫酸中的氢。
3.位于前面的金属能把位于后面的金属从它们的
盐溶液中置换出来(除K、Ca、Na外)。
归纳
金属活动性顺序的应用:
1.如何验证Zn、Cu、Ag三种金属的活动性?
自由讨论
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
方法1:取活动性居中的金属为单质,例如取Cu丝,而Cu两边的金属取其溶液,如ZnCl2溶液和AgNO3溶液,然后将Cu丝分别伸入两溶液中,通过是否有金属被置换出来而确定金属的活动性。即中间的金属,两端的溶液的方法。
方法2:取金属活动性居中的金属盐溶液,例如取CuSO4溶液,而Cu两边的金属取其单质,如Zn片和Ag片,然后分别将Zn片和Ag片放入CuSO4溶液中,根据是否有紫红色的铜被置换出来,确定金属的活动性。即中间的溶液,两端的金属的方法。
2. 如何验证Mg、Zn、Cu、Ag的活动性?
自由讨论
K Ca Na Mg Al Zn Fe Sn Pb〔H〕Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
氢前
氢后
一般情况下金属可分成两类:一类氢前金属,一类氢后金属。所以通常先取四种金属的单质和一种稀酸(如稀盐酸)反应,根据是否有气泡产生,来确定Mg、Zn比Cu、Ag活泼,同时又可根据产生气泡速率的快慢来确定Mg比Zn活泼。氢后金属,可根据金属单质与金属盐溶液的反应来确定Cu比Ag活泼(例如将Cu丝放入AgNO3溶液中)。
归纳
利用金属与金属化合物溶液的反应。依据反应能否发生判断:能反应说明置换的金属比被置换金属活动性强。
常用的探究金属活动性顺序的方法:
方法1:
利用金属与盐酸、稀硫酸的反应。依据现象判断:放出气体速率越快,其金属活动性越强。没有气体产生的,其金属活动性位于金属活动性顺序中氢的后面。
方法2:
3.黄金饰品中的假货常常鱼目混珠,社会上有些
不法分子时常以黄铜冒充黄金进行欺诈活动。
黄铜(铜锌合金)与黄金的外观很相似,我们
可用什么办法来鉴别它们呢?
自由讨论
黄铜
黄金
方法1:能与稀盐酸、稀硫酸反应的为黄铜、不
反应的为黄金。
方法2:能与AgNO3溶液反应的为黄铜、不反应
的为黄金。
方法3:黄金与黄铜的密度不同,测一下它们的
密度即可区别。
方法4:黄金与黄铜的硬度不同,把它们互相刻
画,硬度大的为黄铜,小的为黄金。
例 向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法:
①向滤渣中加入稀盐酸,一定有气泡产生。
②向滤液中加入稀盐酸,一定有沉淀产生。
③滤渣中一定含有Ag。
④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3。
以上说法正确的个数为 ( )
A.0个 B.1个 C.2个 D.3个
×
×
√
×
B
课堂教学展示
典例剖析
第2课时 金属活动性顺序
一、金属与金属化合物溶液反应
2Al+3CuSO4=3Cu+Al2(SO4)3
Cu+2AgNO3=2Ag+Cu(NO3)2
Cu和Al2(SO4)3不反应
结论:金属活动性 Al>Cu>Ag
二、金属活动性顺序的应用
1.金属的位置越靠前,它的活动性越强。
2.位于氢前的金属能置换出盐酸和稀硫酸中的氢。
课堂教学展示
课堂小结
3.位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(除K、Ca、Na外)。
三、探究金属活动性常用的两种方法
1.利用金属和金属化合物溶液反应探究(验证Zn、Ag、Cu三种金属活动性)。
(1)“中间的金属,两端的溶液”的方法(Cu丝、ZnCl2溶液、AgNO3溶液)。
(2)“中间的溶液,两端的金属”的方法(Zn片、Ag片、CuSO4溶液)。
2.利用金属和盐酸、稀硫酸反应探究(验证Mg、Zn、Cu、Ag的活动性)。
练习与应用(P13)
2. 波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。为什么不能用铁制容器来配制波尔多液?
若用铁制容器来配制波尔多液,则容器会被腐
蚀,硫酸铜也会变质,发生如下反应:
Fe+CuSO4=FeSO4+Cu
课后反馈总结
课本习题
5. 下列物质能否发生反应?写出能发生反应的化
学方程式。
(1)银与稀盐酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)铝与硝酸银溶液
不能
能,
不能
能,
6. 填写下列表格(“混合物”栏中括号内为杂质)。
混合物 除去杂质的化学方程式 主要操作步骤
铜粉
(Fe)
FeCl2溶液(CuCl2)
加适量稀盐酸至无气泡产生,过滤、洗涤、干燥
加适量无锈铁钉或铁粉,过滤
7. 现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y和Z的金属活动性顺序。
解:金属活动性由强至弱依次为X、Y、Z。
同课章节目录
